Nova Técnica
|
|
| Aplicação da radiação ultravioleta como forma de contribuição para a Química Verde e construção de um reator fotoquímico alternativo e de baixo custo, para pré-tratamento de amostras Application of ultraviolet radiation as a contribution to green chemistry and construction of an alternative and low-cost photochemical reactor for pre-treatment of samples |
|
Marcos M. Gouvêa; Glayce S. Lima; Adalberto A. Silva Neto; Annibal D. Pereira Netto; Flávia F. de C. Marques*
Departamento de Química Analítica, Instituto de Química, Universidade Federal Fluminense, 24020-141 Niterói - RJ, Brasil Recebido em 16/04/2013 *e-mail: flaviamarques@vm.uff.br Ultraviolet radiation corresponds to a fraction of electromagnetic radiation, covering wavelengths between 1 and 400 nm. Methods based on UV irradiation have become popular because it is possible to treat samples simply by applying energy, avoiding procedures that require the use of toxic substances, thus contributing to the development of Green Chemistry. This study aimed to assess the main applications of UV radiation reported in the literature and thoroughly described the construction of an alternative and low-cost photochemical reactor to be used for the pretreatment of samples in the laboratory. The use of this new photochemical reactor in the clean-up of milk samples for spectrofluorimetric measurements was also reported. INTRODUÇAO No início do século XX, Albert Einstein elucidou o efeito fotoelétrico verificado em 1887 por Heinrich Hertz. Desde entao, as teorias modernas passaram a descrever a radiaçao eletromagnética por um comportamento dual, ou seja, como ondas e também como partículas. As propriedades ondulatórias como refraçao, reflexao, interferência e difraçao puderam ser mais facilmente explicadas, enquanto os fenômenos associados com a absorçao e a emissao da energia radiante também possibilitaram comprovar o comportamento da radiaçao como partículas contendo quantidades discretas de energia, chamadas de fótons.1 A radiaçao eletromagnética é comumente classificada através da frequência da onda característica de cada energia. A classificaçao da radiaçao eletromagnética em funçao de seu efeito físico leva à construçao de um espectro eletromagnético que abrange desde raios gama até as ondas de rádio.2 Dentre estas, destaca-se a radiaçao ultravioleta (UV) por apresentar importantes aplicaçoes no campo científico. A descoberta dessa radiaçao ocorreu durante a observaçao do escurecimento dos sais de prata quando expostos à luz do sol. Em 1801, o cientista alemao Johan Ritter percebeu que os raios de sol, logo após o limite superior do espectro visível, ou seja, raios invisíveis eram capazes de oxidar haletos de prata. Estes foram chamados de raios desoxidantes (para destacar sua reatividade química) e, posteriormente, denominados de luz ultravioleta no fim do século XIX.3 O fenômeno da interaçao da matéria com essa forma de radiaçao é utilizado na espectroscopia para caracterizaçao molecular e quantificaçao de diversas substâncias e espécies químicas. A absorçao da radiaçao UV é capaz de promover a transiçao eletrônica dos elétrons de valência a níveis mais energéticos. A energia absorvida pode ser liberada na forma de fótons, através dos fenômenos de fluorescência e fosforescência, ou pode ocorrer simplesmente uma relaxaçao nao radiativa, que pode ser explicada pelos fenômenos de conversao interna e relaxaçao vibracional (devido a colisoes moleculares que desativam o estado excitado da molécula) e, ainda, pelo cruzamento intersistemas (no qual acontecem transiçoes entre os estados singleto e tripleto, ou seja, a multiplicidade do estado eletrônico excitado é alterada) (Figura 1).4 Tanto a absorçao molecular quanto a emissao radiativa sao fenômenos úteis em Química Analítica, pois podem ser medidos e podem ser proporcionais à concentraçao da substância na amostra.
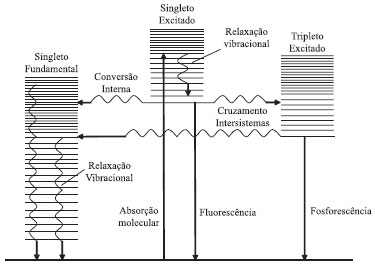 Figura 1. Diagrama de níveis de energia mostrando os processos físicos que podem ocorrer após cada molécula absorver um fóton no ultravioleta ou visível40
A faixa do espectro eletromagnético correspondente à radiaçao UV (Figura 2) abrange comprimentos de onda de 1 a 400 nm e pode ser subdividida em ultravioleta de vácuo - UVV (1 - 200 nm), ultravioleta distante (200 - 300 nm) e ultravioleta próximo (300 - 400 nm). De modo geral, fótons nestas faixas de comprimento de onda têm efeitos diferentes sobre a matéria. Outra subclassificaçao usual divide a radiaçao UV em radiaçao UV-C (100 - 280 nm), UV-B (280 - 315 nm) e UV-A (315 - 400 nm). A radiaçao UV-A é o principal tipo de radiaçao UV que atinge a biosfera a partir da emissao solar. A maior fraçao dos outros componentes do espectro de UV é refletida ou absorvida pela camada de ozônio, presente na estratosfera.5,6
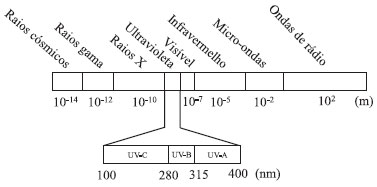 Figura 2. Espectro eletromagnético, relacionando os comprimentos de onda às respectivas classificaçoes da radiaçao eletromagnética, com destaque para as subclassificaçoes da radiaçao UV
O uso da irradiaçao por UV tem sido cada vez maior em Química Analítica na etapa de pré-tratamento da amostra, que é um conjunto de procedimentos necessários para converter o analito a uma forma mais adequada para posterior quantificaçao e determinaçao.7 Assim, a irradiaçao por UV pode ser utilizada, por exemplo, para gerar fotoderivados de elevado rendimento quântico de luminescência que melhoram a detectabilidade da espécie de interesse. Tal procedimento também pode ser utilizado para gerar derivados nao luminescentes, suprimindo a luminescência de espécies químicas que sejam potenciais interferentes quando misturas complexas sao analisadas. Vale ressaltar que este é um artifício simples e limpo para pré-tratamento de amostras, uma vez que é capaz de provocar quebra de ligaçoes químicas e gerar derivados fotoquímicos sem o uso de solventes ou reagentes, que poderiam produzir rejeitos tóxicos. Desse modo, sao respeitados os princípios da Química Verde, conceito introduzido pela Agência de Proteçao Ambiental Americana (US-EPA) a partir da década de 1990 e que, atualmente, é definido pela IUPAC como: "A invençao, desenvolvimento e aplicaçao de produtos e processos químicos para reduzir ou eliminar o uso e a geraçao de substâncias perigosas".8 Assim, este trabalho teve como objetivo avaliar as atuais aplicaçoes da radiaçao UV, o seu potencial como ferramenta na área de Química e descrever a montagem e o funcionamento de um equipamento simples e construído com material de baixo custo, para ser utilizado como reator fotoquímico. Mecanismo de foto-oxidaçao mediada por irradiaçao por UV A foto-oxidaçao de substâncias orgânicas ocorre preferencialmente através de mecanismo radicalar e nao através da interaçao direta entre a radiaçao ultravioleta e a matriz de interesse. Assim, a geraçao de radicais HO·, que têm vida curta e alto poder oxidante, é a responsável pela oxidaçao e degradaçao de moléculas orgânicas. Entretanto, matrizes que apresentam conteúdo de matéria orgânica muito elevado, como alimentos, requerem uma quantidade maior de HO· e, nestes casos, a associaçao do tratamento radiativo com a adiçao de um agente auxiliar (que atua como agente oxidante forte), método conhecido como Processo Avançado de Oxidaçao (PAO), pode ser uma excelente alternativa para melhorar a eficiência do procedimento foto-oxidativo.9 O PAO mais empregado é o tratamento baseado na combinaçao da radiaçao UV com a adiçao de H2O2.10-14 A irradiaçao por UV é capaz de provocar a quebra homolítica das moléculas de H2O2 e, assim, gerar os radicais hidroxila necessários para a foto-oxidaçao da amostra (Equaçao1).

Outros PAO já desenvolvidos envolvem a combinaçao da radiaçao UV com gás O3 (Equaçoes 2a e 2b), TiO2 e reagente de Fenton (Equaçao 3).15
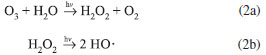
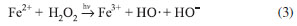
Utilizando a radiaçao UV para formar radicais hidroxila a partir do ozônio (Equaçoes 2a e 2b), observa-se um potencial maior para a degradaçao completa de compostos orgânicos poluentes, como os organoclorados. No entanto, vale ressaltar que o ozônio também pode atuar como oxidante enérgico para degradaçao de alguns compostos orgânicos, reagindo diretamente, através de reaçao eletrofílica ou por cicloadiçao (Equaçao 4); e indiretamente, através do radical hidroxila formado através da sua decomposiçao (Equaçao 5). E nestes casos, nao é necessário o uso da irradiaçao UV.15
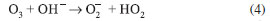
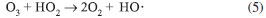
Como pode ser visto na Equaçao 1, a produçao de radicais hidroxila a partir do peróxido de hidrogênio nao precisa necessariamente partir do processo mostrado nas Equaçoes 2a e 2b, ou seja, o peróxido de hidrogênio pode ser utilizado diretamente. Devido à eficiência dos procedimentos, além da digestao de amostras que contêm alto teor de matéria orgânica, os PAO também sao utilizados para diversas outras finalidades, como a derivatizaçao fotoquímica de substâncias destinadas à determinaçao analítica16-19 e a degradaçao de contaminantes presentes em diferentes matrizes.11-14,20-23 Os processos mostrados acima sao as diversas alternativas para o tratamento de compostos orgânicos através dos PAO baseados na geraçao do radical hidroxila. E as vantagens, desvantagens, a eficácia e a utilidade de cada um deles vai depender do grupo de compostos contaminantes presentes nas diferentes matrizes.
APLICAÇOES DA IRRADIAÇAO DE AMOSTRAS POR UV Tratamento de efluentes Os poluentes orgânicos representam uma importante fonte de contaminaçao dos cursos d'água e, dentre eles, destacam-se os efluentes farmacêuticos. Algumas substâncias sao resistentes ao tratamento tradicional empregado para a purificaçao da água e acabam se acumulando no meio ambiente. Tratamentos baseados no uso de processos avançados de oxidaçao, como a irradiaçao UV, vêm sendo desenvolvidos como alternativa para a despoluiçao de águas contaminadas com estas substâncias. Kim e colaboradores (2012) estudaram a degradaçao e a toxicidade de dois antibióticos, sulfametoxazol (SMX) e clortetraciclina (CTCN), após a aplicaçao de diferentes PAO (ozônio e UV).24 A aplicaçao de ozônio foi eficiente para a degradaçao dos antibióticos após 90 min de tratamento, porém apenas a CTCN apresentou reduçao completa da toxicidade, enquanto o SMX apresentou um pequeno aumento. Neste caso, o tratamento por UV foi capaz de provocar a completa degradaçao do SMX, que ocorreu após 30 min de exposiçao. Entretanto, a toxicidade das substâncias geradas aumentou significativamente em relaçao à substância inicial. A CTCN apresentou uma moderada taxa de degradaçao e a sua toxicidade nao foi alterada pela radiaçao UV. Keen e colaboradores (2012) estudaram a decomposiçao da carbamazepina (CBZ), um fármaco utilizado para o tratamento da epilepsia, que é amplamente encontrado em águas residuais ao redor do mundo e apresenta resistência ao tratamento de efluentes.10 A literatura relata que a biodegradaçao da CBZ em sua forma original é ineficiente e que o tratamento da CBZ com UV/H2O2 gera, como um dos subprodutos, a acridina, que é uma substância carcinogênica.25,26 Com o intuito de favorecer a açao microbiana sobre a CBZ, os autores submeteram esta substância ao ataque dos radicais OH· (favorecendo a inserçao de grupamentos hidroxila na molécula), mas uma fraçao da CBZ permaneceu inalterada. Apesar disso, submetendo as substâncias geradas, principalmente a acridina, a um processo de biodegradaçao, seguido de um procedimento de oxidaçao avançada (PAO) UV/H2O2, estes subprodutos gerados foram eficientemente degradados. Desta forma, os resultados obtidos indicaram que o procedimento de oxidaçao avançada combinado com a biodegradaçao apresenta potencial para ser adotado como alternativa para o tratamento de água contaminada com substâncias semelhantes à carbamazepina.10 A degradaçao de diversas outras substâncias através de processos oxidativos foi estudada como possibilidade para tratamento de efluentes. Guimaraes e colaboradores (2012) verificaram que a fotólise exclusivamente nao é eficiente para a remoçao de formaldeído de águas residuais, entretanto a associaçao da irradiaçao UV com H2O2 foi o procedimento mais eficiente para esta finalidade.11 Nagel-Hassemer e colaboradores (2012) observaram que a aplicaçao da radiaçao UV combinada com soluçao aquosa de H2O2 250 mg L-1, durante 60 min, foi o procedimento mais bem-sucedido para a degradaçao de corantes presentes em efluentes têxteis, que haviam sido previamente tratados por procedimentos biológicos.12 Barrera e colaboradores (2011) estudaram seis diferentes combinaçoes de processos radiativos, envolvendo radiaçao UVV (1-200 nm) e UV-C (100-280 nm), para o tratamento de efluentes sintéticos de abatedouros. Foi observado que a combinaçao da irradiaçao UV-C seguida do procedimento UVV foi o tratamento mais eficiente para a reduçao da quantidade total de carbono orgânico na amostra. Também se observou que os procedimentos em que foi utilizado H2O2 proporcionaram uma taxa de degradaçao mais acentuada em comparaçao com os mesmos procedimentos realizados na ausência deste aditivo.13 Os processos avançados de oxidaçao podem apresentar elevado custo financeiro para aplicaçao no tratamento de efluentes, devido à necessidade de implantaçao de instalaçoes de grande porte nas redes de tratamento de água e ao enorme gasto de energia demandado pela maior parte dos procedimentos. Entretanto, tendo em vista que quantidades significativas de substâncias nao podem ser degradadas pelos procedimentos usuais de tratamento de água e que a conservaçao do meio ambiente representa uma das maiores preocupaçoes da sociedade contemporânea, essas técnicas alternativas adquiriram considerável importância como estratégia para diminuiçao da poluiçao ambiental, uma vez que diversos trabalhos indicaram que podem ser muito eficientes para a degradaçao de algumas substâncias recalcitrantes. Tratamento de alimentos através da irradiaçao por UV A irradiaçao ultravioleta como forma de tratamento de amostras é cada vez mais utilizada pela indústria de alimentos, pois o procedimento é simples e evita o risco de contaminaçao. Este tratamento é usado para o controle de deterioraçao de alimentos, uma vez que a irradiaçao atua como germicida, resultando na descontaminaçao dos produtos alimentícios, por meio da destruiçao parcial ou total dos micro-organismos. Isso acontece devido à penetraçao da radiaçao na célula microbiana e a sua absorçao pelo material genético, levando à formaçao de dímeros de bases pirimídicas, principalmente de timina. A formaçao de uma considerável quantidade de dímeros impossibilita a replicaçao do DNA, compromete a síntese proteica e, consequentemente, dificulta o crescimento microbiano.27 Outro importante resultado após o procedimento é a obtençao de alimentos mais frescos e com melhores características sensoriais, preservando suas propriedades originais e aumentando o seu tempo de vida nas prateleiras.28 No estudo de Campos e colaboradores (2009), a irradiaçao por UV foi utilizada para a desinfecçao superficial do tomate "Pitenza", pois tratamentos pós-colheita com produtos químicos causam problemas ambientais e sao nocivos aos consumidores. Também foi observado que houve um aumento da concentraçao de carotenoides totais com o aumento da irradiaçao das amostras por UV.29 Bertagnolli e colaboradores (2007) estudaram o potencial da irradiaçao UV para o aumento da concentraçao de trans-resveratrol em casca de uva.30 Este polifenol apresenta atividade anti-inflamatória e anticoagulante e, por isso, auxilia na proteçao contra a aterosclerose e doenças coronarianas.31,32 Segundo os autores do trabalho, as cascas das uvas irradiadas apresentaram maior concentraçao de trans-resveratrol. Coutinho e colaboradores (2003) avaliaram a influência e a eficiência da radiaçao UV-C no controle de podridoes do pêssego cultivar Jade. Devido à rápida desidrataçao, perda da firmeza da polpa e presença de fungos que causam podridoes na pós-colheita do pêssego, os pesquisadores estudaram o uso da radiaçao UV como possibilidade para conservaçao do fruto. Verificou-se que a aplicaçao de luz UV por 30 min controla em 100% as podridoes de pêssegos cultivar Jade, após 4 e 8 dias de armazenamento. Em relaçao à firmeza da polpa após irradiaçao, valores menores foram obtidos quando comparados com a amostra nao irradiada, entre 4 e 8 dias de armazenamento.33 Armas e colaboradores (2004) avaliaram a eficácia da radiaçao UV na reduçao dos níveis de micro-organismos superficiais, presentes em amostras de carne suína fatiada e embalada devido ao manuseio incorreto do produto, que sao comercializadas na cidade de Pelotas, Rio Grande do Sul. De acordo com os resultados obtidos, observou-se que a exposiçao durante 15 min foi eficiente para descontaminaçao superficial de lombos de porco embalados. Outro efeito positivo foi a reduçao em 90% de bactérias mesófilas aeróbias nas superfícies dos filmes de polietileno de baixa densidade após irradiaçao a 137 µ W cm-2 através de lâmpada bactericida de 15 W e 254 nm.34 Bartnicki e colaboradores (2010) propuseram um novo tratamento, utilizando a radiaçao UV, para controle de conídios (esporo assexual existente em fungos) associados à água de lavagem das maças. Os tratamentos tradicionais sugerem a utilizaçao de produtos com formulaçoes contendo compostos orgânicos e inorgânicos liberadores de cloro ativo para o controle dos conídios. Todavia, este tratamento com cloro, embora seja eficiente, acarreta corrosao do maquinário e geraçao de resíduos. Os resultados do trabalho indicaram que a irradiaçao foi eficiente no controle dos conídios (C. perennans) presentes na epiderme das maças, obtendo-se um controle de 94 a 98% em relaçao às amostras nao irradiadas.35 Enfim, conforme visto nos trabalhos mencionados acima, o controle microbiológico de alimentos através da irradiaçao UV, que atua como germicida se aplicada com intensidade e tempo suficiente, é uma tecnologia cada vez mais utilizada por ser segura, econômica e nao gerar subprodutos que alteram o sabor, coloraçao e odor dos alimentos. Derivatizaçao fotoquímica através da irradiaçao por UV O preparo da amostra é uma das primeiras etapas requeridas para a obtençao das substâncias de interesse em uma forma adequada para análise. Alguns dos métodos tradicionais empregados para esta finalidade, como a digestao úmida e a extraçao líquido-líquido, demandam a utilizaçao de grandes quantidades de solventes para extraçao dos analitos e reduçao das interferências da matriz. Estes métodos apresentam diversas desvantagens, como o alto custo devido ao grande consumo de solventes, alto risco de contaminaçao e possibilidade de perda do analito. O uso da irradiaçao por UV é uma alternativa simples e limpa para o preparo de muitas amostras. A derivatizaçao fotoquímica é utilizada para converter os analitos de interesse em substâncias ou espécies químicas que possam apresentar uma resposta analítica mais eficiente para a técnica instrumental adotada. O procedimento também pode ser efetivo para converter as substâncias que compoem a matriz em outras com menor sinal analítico ou diferente comportamento; deste modo, o efeito dos interferentes é reduzido ou eliminado e torna-se possível a determinaçao das substâncias de interesse. Com o objetivo de permitir a determinaçao seletiva de camptotecina (CPT) em formulaçoes farmacêuticas de irinotecana (CPT-11) ou de topotecana (TPT), utilizadas como quimioterápicos no tratamento contra o câncer, Marques e colaboradores (2010) propuseram a aplicaçao de um tratamento fotoquímico através do qual foi possível eliminar completamente as interferências no sinal do CPT e, nas condiçoes otimizadas (meio fortemente básico e exposiçao das soluçoes à radiaçao UV durante 30 min), o método permitiu a determinaçao de CPT em misturas contendo até 50 vezes mais TPT ou contendo até 10 vezes mais CPT-11. O limite de detecçao (LD) foi de 10-10 mol L-1.16 Pacheco e colaboradores (2008) aplicaram a irradiaçao UV para derivatizaçao fotoquímica do ciclofenil, um fármaco utilizado no tratamento contra os sintomas da menopausa. Foi observado que a intensidade de sinal fluorescente do ciclofenil é significativamente elevada após a irradiaçao UV, além do ajuste de pH e da proporçao dos solventes na soluçao. Após a otimizaçao do método, limite de quantificaçao de 3,7 x 10-7 mol L-1 foi alcançado.17 Liu e colaboradores (2010) propuseram o desenvolvimento de um método espectrométrico de fluorescência atômica para determinaçao de ultratraços de níquel sem a necessidade de etapas prévias de pré-concentraçao.18 A introduçao da amostra em espectrometria atômica baseia-se na formaçao de um aerossol líquido, por meio de nebulizadores pneumáticos. Entretanto, uma quantidade significativa da soluçao introduzida nao é transformada em aerossol útil. A alternativa usualmente adotada é a conversao do analito de interesse em uma espécie química mais volátil. Para a determinaçao de níquel, por exemplo, é necessária a conversao do metal em níquel tetracarbonilo (Ni(CO)4), que pode ser mais facilmente vaporizado.36 A metodologia proposta por Liu e colaboradores consistiu na geraçao de vapor fotoquímico através do tratamento da amostra com formaldeído e irradiaçao UV. A radiaçao UV promove a decomposiçao do formaldeído, gerando CO, que prontamente reage com o níquel em soluçao e produz Ni(CO)4. O maior sinal analítico foi obtido em 120 s de exposiçao à radiaçao UV e limite de detecçao de 10 ng L-1 foi alcançado. Gil e colaboradores (2007) propuseram a combinaçao do PAO UV/H2O2 e da irradiaçao ultrassônica como alternativa para determinaçao de tiomersal, uma substância organomercurial muito utilizada para a conservaçao de produtos farmacêuticos, como cosméticos, vacinas e preparaçoes oftálmicas, por espectrometria de absorçao atômica em amostras comerciais de colírio.14 No final do século passado, sugeriu-se que esta substância (tiomersal) poderia estar relacionada ao desenvolvimento de doenças comportamentais em crianças, entretanto evidências atuais refutam essa observaçao.37,38 A espectrometria de absorçao atômica com geraçao de vapor frio é o método mais utilizado para a determinaçao de ultratraços de mercúrio, porém é necessária uma etapa prévia para a degradaçao do organomercúrio a Hg(II), na qual usualmente sao empregados ácidos fortes e agentes oxidantes em altas temperaturas. A geraçao de vapor frio, por sua vez, requer a utilizaçao de agentes redutores, como NaBH4 e SnCl2, para a conversao do Hg(II) em Hg(0).39 No procedimento usado, os autores utilizaram ácido fórmico (0,9 mol L-1) e tratamento ultrassônico. O ultrassom provoca a decomposiçao do ácido fórmico, produzindo gases e radicais redutores, que induzem a formaçao do vapor frio. Os parâmetros otimizados do método proposto indicaram que a adiçao de 100 µL de H2O2 a uma soluçao 0,5 % de colírio e a exposiçao à radiaçao UV por um período de 5 a 15 minutos, seguida pelo tratamento ultrassônico, proporcionaram o maior valor de absorvância para a amostra. Das 8 amostras comerciais de colírio estudadas, apenas 2 apresentaram concentraçao de tiomersal inferior ao limite de detecçao do método (0,04 µg mL-1), resultado condizente com as informaçoes concedidas pelos produtores, que indicavam a ausência de tiomersal na formulaçao. As outras amostras apresentaram uma variaçao de 0,30 ± 0,02 µg mL-1 até 110 ± 4 µg mL-1.14 Woldemichael e colaboradores (2012) propuseram uma metodologia fotoquímica para determinaçao voltamétrica de urânio em amostras de água provenientes do rio Warnow (Rostock, Alemanha).19 Os autores basearam seu trabalho no desenvolvimento de um procedimento foto-oxidativo alternativo, utilizando a radiaçao UV-A proveniente da radiaçao solar para a digestao das amostras. As amostras foram discriminadas em três diferentes categorias: sem qualquer tipo de tratamento; após irradiaçao em reator fotoquímico comercial (lâmpada ultravioleta, 30 W, 254 nm); e após submeter à radiaçao UV-A solar. As amostras irradiadas foram submetidas ao procedimento por seis ou doze horas em recipientes de politereftalato de etileno (PET) transparentes à radiaçao UV-A ou em recipientes de quartzo, no caso do tratamento em reator fotoquímico. Os testes de recuperaçao em nível de fortificaçao de 1,00 µg L-1 mostraram que a amostra que nao foi submetida aos tratamentos fotoquímicos nao apresentou qualquer sinal analítico na técnica adotada. As amostras irradiadas por radiaçao solar e em fotorreator apresentaram, respectivamente, recuperaçoes de 93 e 94 %, após 6 h, e 94 e 95 %, após 12 h de tratamento. Com os resultados obtidos, foi possível concluir que a aplicaçao de radiaçao UV proveniente da radiaçao solar pode ser um excelente método verde alternativo para pré-tratamento de amostras em locais ou situaçoes em que a utilizaçao de reatores fotoquímicos nao é a opçao mais vantajosa, uma vez que o procedimento é simples, eficiente e apresenta custo operacional bastante reduzido. Diversos trabalhos comprovaram que a irradiaçao ultravioleta é um método muito promissor para digestao de amostras e derivatizaçao fotoquímica com o objetivo de pré-tratamento para a determinaçao analítica. Além de ser um método verde, também apresenta baixo custo, já que os fotorreatores apenas necessitam de lâmpadas de ultravioleta para funcionarem e sua manutençao é muito simples. Os recursos destinados a pesquisas científicas nem sempre sao abundantes, entao procedimentos menos dispendiosos sempre devem ser considerados no planejamento de um projeto de pesquisa. Funcionamento de diferentes reatores fotoquímicos Reatores fotoquímicos sao utilizados em muitos trabalhos devido às vantagens citadas anteriormente. A seguir é descrito o funcionamento de fotorreatores utilizados por diferentes pesquisadores em seus trabalhos e, na sequência, a construçao do equipamento realizado pelo grupo de pesquisa, autores deste artigo. Kammradt e colaboradores (2004) estudaram o potencial do processo oxidativo UV/H2O2 na degradaçao de corantes vermelho e amarelo em efluentes de tinturarias industriais.20 Para isso, os pesquisadores utilizaram três diferentes reatores fotoquímicos: - Reator compacto Umex UV-ELr, com 12 mL de capacidade, e ativado por micro-ondas, 750 W. Neste reator, estimou-se o tempo de reaçao de três minutos utilizando 10 mL de efluente. Ao final do estudo preliminar, observou-se que utilizando concentraçoes de H2O2 entre 3330 e 9990 mg L-1 obteve-se maior reduçao de descoloraçao do efluente vermelho. Porém, para o efluente amarelo, concentraçoes mais elevadas na faixa entre 6660 e 16650 mg L-1 conduziram a melhores resultados. - Reator fotoquímico convencional com 180 mL de capacidade, sistema de refrigeraçao com água, agitaçao magnética e lâmpada de vapor de mercúrio de 125 W imersa no meio reacional, com proteçao por bulbo de quartzo. Neste caso, análises espectrofotométricas foram realizadas para observar a reduçao das cores. Durante os primeiros minutos da reaçao ocorreu descoloraçao do efluente vermelho. Já para a descoloraçao do efluente amarelo foi necessário um intervalo de tempo maior que 10 min. - Aparelho integrável de irradiaçao de luz ultravioleta UMEX UV - LAB r NS, com capacidade de 950 mL, irradiador de formato espiral, radiaçao de comprimento de onda de até 254 nm, lâmpada com 150 W, sistemas de refrigeraçao e agitaçao. Os resultados alcançados no reator cilíndrico foram inferiores em eficiência quando comparados com os reatores anteriores, uma vez que a descoloraçao do efluente vermelho ocorreu somente após 20 min de reaçao. Para o efluente amarelo, mais de 40 min de reaçao foram necessários para notar reduçao na coloraçao. Morais e colaboradores (2005) avaliaram, dentre outros métodos de pré-tratamento de amostras, a utilizaçao de processos oxidativos avançados para tratamento de chorume de aterro sanitário.21 Para isso, os pesquisadores trabalharam com um reator convencional de bancada, com 120 mL de capacidade, equipado com refrigeraçao a água, agitaçao magnética e sistema de oxidaçao, lâmpada de vapor de mercúrio de 125 W imersa na soluçao por meio de um bulbo de quartzo. Neste reator foram realizados estudos de degradaçao em amostras de chorume (pH natural e 2000 e 2200 mg L-1 de H2O2) para análise do potencial do tratamento UV/H2O2. A partir do estudo de degradaçao prolongada por 180 min, observou-se a remoçao na ordem de 70% de quantidade de grupamentos fenólicos. Outro parâmetro que diminuiu foi o teor de carbono orgânico dissolvido (COD); as determinaçoes demonstraram reduçoes entre 60 e 77% para 30 min e entre 81 e 89% para 60 min de tratamento. Stülp e colaboradores (2008) analisaram a degradaçao fotoquímica do pesticida Malation (organofosforado para controle de formigas, lagartos e pulgoes), utilizando um reator de fotodegradaçao que consistia em uma caixa de dimensoes 50 x 40 x 20 cm, lâmpada de mercúrio (125 W), célula de quartzo e filamento de lâmpada de vapor de Hg - OSRAM de 125 W.22 Soluçoes com 100 mg mL-1 do pesticida foram analisadas eletroquimicamente antes e após 30 min de irradiaçao por UV. Foi constatado que ocorre degradaçao do pesticida, visto que houve elevaçao de correntes de 1,80 para 2,43 mA cm-2 após irradiaçao UV, indicando reduçao da concentraçao. Silva e colaboradores (2008) avaliaram o processo fotoquímico para degradaçao do corante vermelho bordeaux. Para isso foi construído um reator para degradaçao fotoquímica formado por uma célula de acrílico de 6 L e dimensoes 350 mm x 160 mm x 160 mm, tubo de quartzo (no interior colocou-se filamento de uma lâmpada), bomba de recirculaçao submersa SARLOBETTER (vazao de 90 L h-1) e lâmpada de vapor de mercúrio de 250 W (Osram HQL).23 As soluçoes com corante foram irradiadas por 5 horas e, em seguida, analisadas por espectrofotometria UV-visível. Os resultados obtidos a partir do espectro de absorvância indicaram que o processo foi eficiente, pois se constatou a reduçao da absorvância durante a degradaçao, verificando-se a reduçao de 99% da coloraçao da soluçao com corante.
PROCEDIMENTO PARA MONTAGEM DA CAMARA DE UV COM MATERIAL ALTERNATIVO No contexto descrito neste trabalho, um reator fotoquímico foi construído no Laboratório de Química Analítica Fundamental e Aplicada (LaQAFA) da Universidade Federal Fluminense. Este reator pode ser utilizado como alternativa para pré-tratamento de amostras, visando evitar o consumo de agentes químicos e também a produçao de resíduos poluentes por meio da aplicaçao da radiaçao UV. Duas fotografias mostrando o reator e os detalhes do seu interior estao nas Figuras 3A e 3B, respectivamente.
 Figura 3. Reator fotoquímico construído no LAQAFA (UFF), utilizando carcaça de um forno elétrico, sendo (A) visao frontal da câmara de UV; (B) visao interna da câmara de UV, onde: (1) 6 lâmpadas de vapor de mercúrio dispostas paralelamente; (2) estrutura metálica do forno elétrico inutilizado; (3) barras de alumínio; (4) presilhas para sustentaçao das lâmpadas; (5) caixa da fonte; (6) vedaçao com tiras de borracha rígidas; (7) estante para tubos em estrutura de tela de arame
Para a montagem deste reator fotoquímico utilizou-se material alternativo já sucateado ou de baixo custo, de forma que o gasto total nao ultrapassou o valor de US$ 100. A principal despesa consistiu na aquisiçao de um conjunto de seis lâmpadas de vapor de mercúrio de 6 W (lâmpadas de esterilizaçao) que foram distribuídas dentro da estrutura metálica de um forno elétrico (240 x 175 x 130 mm - aproximadamente 5,5 L) inutilizado (Figura 3A(1) e 3A(2)). As lâmpadas de mercúrio utilizadas sao comercialmente disponíveis para esterilizaçao bacteriológica e apresentam emissao mais intensa em 253 nm e também na faixa entre 296-313 nm. As resistências do forno elétrico que estavam defeituosas foram retiradas, assim como outros materiais que nao seriam úteis para a montagem, tais como o potenciômetro que acionava o forno, o fio da alimentaçao elétrica e algumas ferragens. Após a retirada do material que nao era de interesse, foram feitos furos no fundo para fixar suportes para manter a estrutura do forno na posiçao vertical, ou seja, com a abertura da porta na parte superior. Esses suportes foram feitos com dois pedaços de uma barra de alumínio, do tipo que é usada para trilhos de cortina de decoraçao (Figura 3A(3)). Além disso, foram feitos furos nas paredes da estrutura do forno para fixar as presilhas usadas para segurar as lâmpadas (Figura 3B(4)). Para a alimentaçao das seis lâmpadas foram utilizados 3 reatores eletrônicos do tipo 2 x 9 W, sendo cada um conectado a um par de lâmpadas. Os reatores foram acomodados dentro da caixa metálica de uma fonte de alimentaçao de computador já inutilizada. Além da caixa da fonte, foram aproveitados também os cabos de saída de energia da fonte, para fazer a conexao com as lâmpadas na estrutura do forno; o conector para cabo de força; e a chave seletora de voltagem, de forma que o equipamento pudesse ser bivolt (Figura 3A(5)). Por fim, foram feitas vedaçoes da câmara para que nao houvesse vazamentos de radiaçao UV para o meio externo. A tampa de vidro do forno foi reforçada com mais uma placa de vidro com um filme. As frestas menores encontradas na estrutura foram tapadas com papel alumínio e as frestas maiores, que ficavam à mostra nas paredes laterais ao fechar a tampa de vidro, foram vedadas fixando-se duas tiras grossas de borracha rígida, do tipo usado em proteçao de portas de carro (Figura 3A(6)). Uma estrutura de tela de arame semelhante a uma estante para tubos foi construída para que as amostras fossem introduzidas na câmara. Esta é uma escolha bastante versátil, pois as aberturas das malhas da tela podem ser modificadas para acomodar tubos de diâmetros diferentes, eliminando assim a necessidade de trocar o suporte utilizado (Figura 3B(7)). Um esquema do circuito elétrico elaborado para o funcionamento do reator fotoquímico é mostrado na Figura 4. Este circuito foi montado de forma que as seis lâmpadas de vapor de mercúrio fossem distribuídas em três pares, os quais podem ser acionados por interruptores (chaves) diferentes e independentes (S1, S2 e S3), conectados a seus respectivos reatores (X1, X2 e X3), possibilitando obter diferentes potências de radiaçao dentro forno.
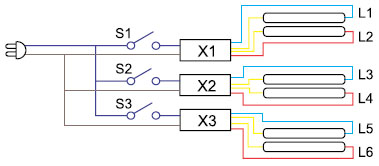 Figura 4. Esquema do circuito elétrico montado para o funcionamento do reator fotoquímico, onde S1, S2 e S3 sao as chaves; X1, X2 e X3 os respectivos reatores e L1 a L6 sao as lâmpadas de vapor de mercúrio (6 W cada)
Utilizaçao da câmara de UV montada neste trabalho no pré-tratamento de amostras complexas No Laboratório de Química Analítica Fundamental e Aplicada (LaQAFA) da Universidade Federal Fluminense, o leite é uma matriz de grande interesse e, portanto, é alvo de muitas pesquisas. No entanto, a complexidade desta matriz é um problema em todas as técnicas analíticas. Na espectrofluorimetria, por exemplo, é um desafio fazer qualquer determinaçao de contaminante no leite. Isto acontece porque o soro do leite (obtido após processos de clean up mais utilizados e mencionados na literatura) contém cerca de 20% do total das proteínas do leite (distribuídos entre beta-lactoglobulina (BLG), alfalactoalbumina (ALA), albumina do soro bovino (BSA), imunoglobulinas (Ig's) e glico-macropeptídeos (GMP)),41 de forma que esta matriz certamente terá uma determinada intensidade de sinal fluorescente que poderá interferir no sinal dos analitos. Esta fluorescência no soro do leite é decorrente do triptofano presente nas proteínas, o qual possui o grupo - NH2 que é um substituinte que doa elétrons para o sistema, induzindo um aumento do coeficiente de absorçao molar e amplificando a fluorescência.42 Por isso, pensando em minimizar ou eliminar o sinal fluorescente de amostras de leite bovino UHT integral de diversas marcas comercializadas na cidade do Rio de Janeiro e em Niterói, com o intuito de poder detectar possíveis contaminantes, foi utilizada a câmara de UV montada neste trabalho para irradiaçao das amostras. Primeiramente,50 µL de ácido acético glacial foram adicionados a 10 mL de leite bovino UHT integral. A mistura foi submetida a 10 min de centrifugaçao a 6000 rpm e o sobrenadante (soro do leite) obtido teve seu pH ajustado para 12 com NaOH 5 mol L-1. Este soro do leite em pH 12 foi irradiado por 30 min na câmara de UV (utilizando as seis lâmpadas de vapor de mercúrio de 6 W), de forma que grande parte das proteínas do soro do leite que ainda estavam solúveis se tornaram insolúveis pela açao da irradiaçao UV. Após esta precipitaçao pela açao da irradiaçao UV, foi realizada nova centrifugaçao e o sobrenadante medido em espectrômetro de luminescência da VARIAN, Cary Eclipse, utilizando banda espectral de passagem de 10 nm, velocidade de varredura de 1500 nm mm-1 e cubetas de quartzo (caminho óptico de 1 cm). Vale ressaltar que a escolha do pH 12 é proveniente de um estudo da influência do pH no sinal fluorescente de amostras de soro de leite obtidas por precipitaçao ácida conforme descrito acima, seguida do ajuste ao pH desejado com NaOH 5 mol L-1 (Figura 5).
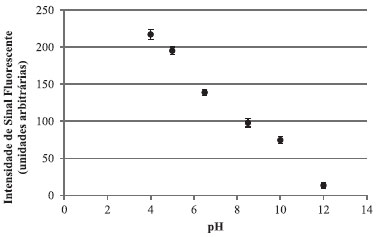 Figura 5. Estudo do efeito do pH no sinal fluorescente de amostras de soro de leite UHT integral obtidas após precipitaçao ácida de leite bovino seguida de ajuste do pH com NaOH 5 mol L-1 e 30 min de irradiaçao UV. Mediçoes realizadas em 360 nm
Assim, o estudo individual das características fluorescentes do soro do leite em diferentes meios indicou que, em soluçoes fortemente alcalinas submetidas a 30 min de irradiaçao por UV, o soro do leite tem a eliminaçao total do sinal nos comprimentos de onda de excitaçao (λexc) e emissao (λem) de 280 nm e 360 nm, respectivamente. Comparando-se com as soluçoes de soro nao irradiadas, a reduçao do sinal fluorescente foi cerca de 99% quando comparadas às mesmas soluçoes nao irradiadas (Figura 6).
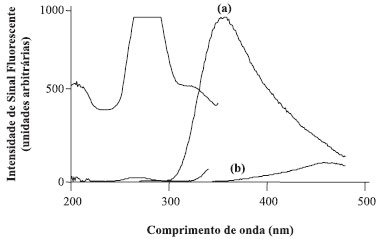 Figura 6. Espectros de excitaçao e emissao fluorescentes do soro do leite obtido após precipitaçao ácida de leite bovino UHT integral, com pH ajustado para 12 com NaOH 5 mol L-1 (a) antes e (b) após 30 min de tratamento fotoquímico com UV
Enfim, o uso da câmara de UV montada neste trabalho mostrou-se útil no tratamento de uma amostra complexa (como é o caso do leite), indicando potencial para o desenvolvimento de metodologia analítica simples e seletiva baseada na espectrofluorimetria e na irradiaçao por UV, para a determinaçao de possíveis contaminantes no leite e que nao sejam sensíveis à irradiaçao UV nas condiçoes estabelecidas.
CONCLUSAO Os métodos clássicos para pré-tratamento de amostras ainda sao os mais utilizados em laboratórios de pesquisa científica ao redor do mundo. Entretanto, a conscientizaçao acerca da preservaçao ambiental e o amadurecimento do conceito da Química Verde na última década levaram ao desenvolvimento de metodologias alternativas que visam à reduçao do consumo de produtos químicos e da geraçao de rejeitos tóxicos. As novas geraçoes de pesquisadores priorizam a adoçao desses métodos, quando estes se mostram suficientemente eficientes para a finalidade proposta. A irradiaçao por UV representa um dos principais métodos empregados com este objetivo. O uso de fotorreatores em escala laboratorial é uma maneira fácil e eficaz para o tratamento foto-oxidativo de amostras. Além disso, a sua construçao é simples e a sua manutençao requer, normalmente, apenas a troca das lâmpadas de UV, que apresentam baixo custo e sao facilmente encontradas no mercado.
REFERENCIAS 1. http://www.unicamp.br/~chibeni/textosdidaticos/fisquantica.pdf, acessada em Setembro 2013. 2. Cavalcante, M. A.; Tavolaro, C. R. C.; Cad. Cat. Ens. Fís. 2001, 18, 298. 3. Ball, D. W. Spectroscopy 2007, 3, 14. 4. http://chemkeys.com/br/2001/09/18/conceitos-fundamentais-em-espectroscopia, acessada em Setembro 2013. 5. http://www.segurancaetrabalho.com.br/download/rad-uv-seelig.pdf, acessada em Setembro 2013. 6. http://satelite.cptec.inpe.br/uv/#/imgSig.jsp, acessada em Setembro 2013. 7. Arruda, M. A. Z.; Santelli, R. E.; Quim. Nova 1997, 20, 638. 8. Tundo, P.; Anastas, P.; Black, D.; Breen, J.; Collins, T.; Memoli, S.; Miyamoto, J.; Polyakoff, M.; Tumas, W.; Pure Appl. Chem. 2000, 72, 1207. 9. Buldini, P. L.; Ricci, L.; Sharma, J. L.; J. Chromatogr. A 2002, 975, 47. 10. Keen, O. L.; Baik, S.; Linden, K. G.; Aga, D. S.; Love, N. G.; Environ. Sci. Technol. 2012, 46, 6222. 11. Guimaraes, J. R.; Farah, C. R. T.; Maniero, M. G.; Fadini, P. S.; J. Environ. Manag. 2012, 107, 96. 12. Nagel-Hassemer, M. E.; Coral, L. A.; Lapolli, F. R.; Quim. Nova 2012, 35, 900. 13. Barrera, M.; Mehrvar, M.; Gilbride, K. A.; McCarthy, L. H.; Laursen, A. E.; Bostan, V.; Pushchak, R.; Chem. Eng. Res. Des. 2012, 90, 1335. 14. Gil, S.; Lavilla, I.;Bendicho, C.; J. Anal. At. Spectrom. 2007, 22, 569. 15. Freire, R. S.; Pelegrini, R.; Kubota, L. T.; Durán, N.; Quim. Nova 2000, 4, 23. 16. Marques, F. F. C.; Cunha, A. L. M. C.; Aucélio, R. Q.; Talanta 2010, 83, 256. 17. Pacheco, W. F.; Batalha, J. L.; Oliveira, C. C.; Aucélio, R. Q.; Talanta 2008, 74, 1442. 18. Liu, L.; Deng, H.; Wu, L.; Zheng, C.; Hou, X.; Talanta 2010, 80, 1239. 19. Woldemichael, G.; Tulu, T.; Flechsig, G. U.; Microchim. Acta 2012, 179, 99. 20. Kammradt, B. P.; Dissertaçao de Mestrado, Universidade Federal do Paraná, Brasil, 2004. 21. Morais, L. J.; Tese de Doutorado, Universidade Federal do Paraná, Brasil, 2005. 22. Stülp S.; Silva C. P.; Marmitt S.; Revista Liberato 2008, 9, 7. 23. Silva, P. C.; Marmitt, S.; Haetinger, C.; Stülp, S.; Eng. Sanit. Ambient. 2008, 13, 73. 24. Kim, T. H.; Kim, S. D.; Kim, H. Y.; Lim, S. J.; Lee, M.; Yu, S.; J. Hazardous Materials 2012, 227, 237. 25. Vogna, D.; Marotta, R.; Andreozzi, R.; Napolitano, A.; d'Ischia, M.; Chemosphere 2004, 54, 497. 26. Xue, W.; Wu, C.; Xiao, K.; Huang, X.; Zhou, H.; Tsuno, H. Tanaka, H.; Water Res. 2010, 44, 5999. 27. Aguiar, A. M. S.; Fernandes Neto, M. L.; Brito, L. L. A.; Reis, A. A.; Machado, P. M. R.; Soares, A. F. S.; Vieira, M. B. M.; Libânio, M.; Eng. Sanit. Amb. 2002, 7, 37. 28. http://www.alimentosebebidas.com.br/artigos/2012/014_ed04_uv/index.htm, acessada em Setembro 2013. 29. Campos, J. A.; Vieites, L. R.; Revista Eletrônica de Agronomia 2009, 16, 20. 30. Bertagnolli, M. M. S.; Rossato, B. S., Silva, L. V.; Cervo, T.; Sautter, K. C.; Hecktheuer, H. L.; Penna, G. N.; Rev. Bras. Cienc. Farm. 2007, 43, 71. 31. Arichi, H.; Kimura, Y.; Okuda, H.; Baba, K.; Kozawa, M.; Arichi, S.; Chem. Pharm. Bull. 1982, 30, 1766. 32. Kimura, Y.; Ohminami, H.; Okuda, H.; Baba, K.; Kozawa, M.; Arichi, S.; Planta Med. 1983, 49, 51. 33. Coutinho, F. E.; Junior, S. L. J.; Haerter, A. J.; Nachtigall, R. G.; Cantillano, F. F. R.; Ciência Rural 2003, 33, 663. 34. Armas, R. D.; Bernardi, E.; Faes, A. D. R.; Ribeiro, G. A.; Resumos do XIII Congresso de Iniciaçao Científica e VI Encontro de Pós Graduaçao (ENPOS), Pelotas, Brasil, 2004. 35. Bartnicki, A. V.; Valdebenito-Sanhueza, M. R.; Amarante, T. V. C., Castro, S. A. L.; Rizzatti, R. M.; Souza, V. A. J.; Pesq. Agropec. Bras. 2010, 45, 124. 36. Takase, I.; Pereira, H. B.; Luna, A. S.; Grinberg, P.; Campos, R.C.; Quim. Nova 2002, 25, 1132. 37. Kelso, J. M.; Greenhawt, M. J.; Li, J. T.; J. Allergy Clin. Immunol. 2012, 130, 25. 38. Mrozek-Budzyn, D.; Majewska, R.; Kieltyka, A.; Augustyniak, M.; Neurotoxicol. Teratol. 2012, 34, 592. 39. Guilhen, S. N.; Pires, M. A. F.; Dantas, E. S. K.; Quim. Nova 2010, 33, 1285. 40. Marques, F. F. C.; Tese de Doutorado, Pontifícia Universidade Católica do Rio de Janeiro, Brasil, 2009. 41. Kinsella, J. E.; Whitehead, D. M.; Adv. Food Nutr. Res. 1989, 33, 343. 42. Schulman, S. G.; Molecular Luminescence Spectroscopy - Methods and Applications - Part I, John Wiley & Sons: New York, 1975. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access





