Nota Técnica
|
|
| Isolamento do verbacosídeo e validação de método analítico para padronização do extrato bruto das partes aéreas de Buddleja stachyoides Cham. & Schltdl. (Scrophulariaceae) Isolation of verbascoside and validation of method to standardize the crude extract of the aerial parts of Buddleja stachyoides Cham. & Schltdl. (Scrophulariaceae) |
|
Daniella M. S. de Oliveira*; Marilis D. Miguel; Milena Kalegari; Obdúlio G. Miguel; Thais F. Moreira
Departamento de Farmácia, Universidade Federal do Paraná, 80210-170 Curitiba - PR, Brasil Recebido em 08/05/2013 *e-mail: dani_mso@yahoo.com.br Phenylpropanoid glycoside verbascoside was isolated and identified from the ethyl acetate fraction of the aerial parts of Buddleja stachyoides Cham. & Schltdl. by 1H-NMR. A method using high-performance liquid chromatography has been developed and validated for determination of verbascoside in alcoholic crude extract of the aerial parts of B. stachyoides. Analysis was performed on a Phenomenexr Gemini-NX C18 analytical column (250 mm x 4.6 mm; 5 µm) using a mobile phase (pump A - aqueous solution containing H2SO4 (0.01 M), H3PO4 (0.4%), and (C2H5)2NH (0.4%); pump B - methanol:aqueous (95:5) solution containing H2SO4 (0.05 M), H3PO4 (2%), and (C2H5)2NH (0.2%); pump C - acetonitrile:aqueous (90:10) solution containing H2SO4 (0.05 M) and H3PO4 (2%)) and a diode array detector at 325 nm. The method was validated in accordance with ANVISA guidelines and may be applied to quality control of herbal medicine with aerial parts of B. stachyoides. INTRODUÇAO A espécie vegetal Buddleja stachyoides Cham. & Schltdl. pertence à família Scrophulariaceae.1 Conhecida no Brasil como barbasco ou verbasco,2 é utilizada na medicina caseira com base na tradiçao popular como anti-hemorroidal, béquica (acalma a tosse), analgésica, sudorífica, calmante, emoliente e anti-reumática. Cresce espontaneamente em pastagens e terrenos baldios, onde é considerada planta daninha.3 Essa espécie tem origem nativa, nao é endêmica do Brasil, tem como domínios fitogeográficos Cerrado, Mata Atlântica e Pampa. No Brasil, sua distribuiçao geográfica contempla as regioes Nordeste (Bahia, Alagoas), Centro-Oeste (Distrito Federal), Sudeste (Minas Gerais, Espírito Santo, Sao Paulo, Rio de Janeiro) e Sul (Paraná, Santa Catarina, Rio Grande do Sul).1 Atualmente, um componente foi isolado dessa espécie, o fenilpropanoide verbascosídeo [2-(3,4-dihidroxifeniletil)-1-O-α-L-ramnopiranosil-(1 → 3)-β-D-(4-O-cafeil)-glucopiranosídeo], também conhecido como acteosídeo.4 As propriedades biológicas dessa substância têm sido descritas na literatura, e possui diversas atividades, incluindo antioxidante, anti-inflamatória, fotoprotetora e quelante. A atividade anti-inflamatória do verbascosídeo foi confirmada por um ensaio in vitro realizado em culturas de células primárias de queratinócitos humano, em que o verbascosídeo foi capaz de reduzir significativamente, de forma dose-dependente, a liberaçao de quimiocinas pró-inflamatórias. Esse estudo também demonstrou que ele promove a melhora e reparaçao de inflamaçoes na pele, devido às suas atividades: seqüestradora de espécies reativas de oxigênio (ERO), antioxidante, quelante de ferro e propriedade indutora da glutationa transferase (GST). Um estudo in vivo, conduzido em inflamaçao da mucosa intestinal, demonstrou que ele é capaz de inibir a ativaçao de proteínas pró-inflamatórias e, consequentemente, a atividade enzimática da matriz metaloproteinase, esta última também envolvida nos fenômenos de envelhecimento da pele. Os resultados desse estudo sugeriram que o verbascosídeo tem a funçao de eliminar os radicais intracelulares, reduzindo os sinais microscópicos e macroscópicos de colite em rato. Assim, a administraçao de verbascosídeo pode ser benéfica para o tratamento de doença inflamatória do intestino.5 Outros estudos demonstraram que o verbascosídeo apresenta atividade antinociceptiva, sendo mais ativo que o ibuprofeno, e6 também inibe a enzima prolil oligopeptidase (POP), uma protease que hidrolisa pequenos peptídeos com prolina.4 É notável o aumento dos efeitos neuroprotetores e de melhora cognitiva com a utilizaçao de inibidores da POP. Essas substâncias sao importantes para o tratamento de condiçoes clínicas, tais como perturbaçoes neuropsiquiátricas e doenças neurodegenerativas.7 A interaçao do verbascosídeo com membranas fosfolipídicas foi avaliada por um estudo em que observou-se uma alta afinidade desta substância com as membranas carregadas negativamente dos compostos de fosfatidilglicerol (PG). Ele promoveu a separaçao de fase dos domínios lipídicos em membranas de fosfatidilcolina (PC) e formou um complexo estável com o lipídio (fosfolipídio/verbascosídeo). Apesar do seu caráter hidrofílico, a porçao cafeoil do verbascosídeo foi localizada profundamente no núcleo hidrofóbico da membrana de PC. Também alterou o comportamento de ionizaçao do grupo fosfato PG e interagiu com a superfície das vesículas. Os efeitos do verbascosídeo sobre as propriedades físicas das membranas podem contribuir para explicar algumas das suas atividades biológicas, como a antimicrobiana e a antioxidante.8 Em outros relatos o verbascosídeo inibiu a atividade enzimática da enzima conversora da angiotensina, o que pode ser benéfico contra a hipertensao arterial, inibiu a formaçao de prostaglandina E2, o fator de necrose tumoral e óxido nítrico e também suprimiu a atividade enzimática da ciclooxigenase (COX-2). Em uma série de estudos in vitro demonstrou claramente que possui atividade imunomoduladora, anti-viral e anti-metástase.9 Devido ao interesse farmacológico, torna-se importante a utilizaçao de um método analítico validado para quantificar este componente do extrato alcoólico bruto de B. stachyoides que contém o marcador verbascosídeo. Tal método poderá auxiliar na padronizaçao de um medicamento fitoterápico das partes aéreas de B. stachyoides e ser utilizado na análise de doseamento no controle de qualidade. A regulamentaçao brasileira em vigor para o registro de medicamentos fitoterápicos é a Resoluçao de Diretoria Colegiada (RDC) nº 14, de 31 de março de 2010, criada pela ANVISA (Agência Nacional de Vigilância Sanitária), que determina os aspectos essenciais ao registro, como identificaçao botânica das espécies vegetais utilizadas, padrao de qualidade e identidade e provas de eficácia e segurança que validem as indicaçoes terapêuticas propostas.10 A validaçao de método analítico para determinaçao de um marcador é outro requisito do processo de registro e, para que este método gere informaçoes confiáveis sobre a amostra, a validaçao torna-se um aspecto vital para verificar a garantia da qualidade analítica.11 Existem várias literaturas, na área de mediçoes químicas e recomendaçoes publicadas por órgaos internacionais e nacionais, que exigem a validaçao de métodos analíticos.12 Entre elas encontra-se a Resoluçao - RE nº 899, de 29 de maio de 2003, "Guia para validaçao de métodos analíticos e bioanalíticos", pertencente à ANVISA e utilizada neste estudo.13 Dada a importância deste composto, o objetivo deste estudo foi realizar o isolamento e identificaçao da substância verbascosídeo da fraçao acetato de etila e desenvolver e validar um método para quantificaçao e padronizaçao do extrato alcoólico bruto das partes aéreas de B. stachyoides.
PARTE EXPERIMENTAL Coleta O material vegetal foi coletado na Universidade Federal do Paraná, campus Jardim Botânico, Curitiba, Paraná, nos meses de maio e junho. A identificaçao botânica da espécie foi realizada no Herbário do Museu Botânico Municipal também localizado na cidade de Curitiba e comparada com a exsicata registrada sob o número 339899 B. stachyoides pelo curador Osmar do Santos Ribas. Extraçao As partes aéreas da planta seca foram rasuradas, pesadas (5970 g) e posteriormente extraídas em aparelho de Soxhlet modificado com álcool etílico hidratado de cereais 96 ºGL (Cereálcoolr), obtendo-se o extrato alcoólico bruto.14 Para obtençao das fraçoes foi utilizado o método de partiçao sistema líquido-líquido, utilizando-se solventes de diferentes polaridades seguindo esta ordem: n-hexano P.A., CHCl3 P.A., AcOEt P.A., também em equipamento de Soxhlet. Equipamentos Para purificaçao do precipitado utilizou-se o sistema de cromatografia líquida de alta eficiência da Gilsonr, com detectores DAD 171 e ELSD TMII, bomba modelo 322 e coluna cromatográfica preparativa C18 Lunar PFP com 250 mm de comprimento, 21,20 mm de d.i. e 5 µm de tamanho de partícula, e o sistema de cromatografia líquida de alta eficiência da Watersr modelo PDA 996, com detector ELSD 2420 e coluna cromatográfica analítica C18 Lunar PFP com 250 mm de comprimento, 4,6 mm de d.i. e 5 µm de tamanho de partícula. Para identificaçao da substância isolada utilizou-se o espectrometro de RMN da Brukerr modelo 600 MR, operando a 600 MHz para frequência do hidrogênio e tubo de 2 mm. Para a validaçao do método analítico utilizou-se o sistema de cromatografia líquida de alta eficiência da Merck-Hitashir, com bomba modelo L7100, degaseificador de solventes modelo L7812; injetor automático modelo L-7200; detector DAD modelo L7455; interface L7000 conectada ao sistema operacional Windows Professional e coluna cromatográfica analítica C18 Phenomenexr Gemini-NX com 250 mm de comprimento, 4,6 mm de d.i. e 5 µm de tamanho de partícula. Isolamento e identificaçao A fraçao acetato de etila foi fracionada em coluna de sílica gel 60 Merckr, para a qual 10 g da fraçao foram utilizadas. A amostra foi eluída com mistura de solventes, iniciando-se com 100% de n-hexano P.A., depois uma mistura de hexano e AcOEt P.A. na proporçao 70:30, utilizando AcOEt como gradiente de polaridade e aumentando o intervalo de 5 em 5% até 100% do mesmo. Em seguida, utilizou-se a mistura AcOEt e MeOH P.A. na proporçao 90:10, utilizando MeOH como gradiente de polaridade e aumentando o intervalo de 5 em 5% até 100% do mesmo. As fraçoes foram recolhidas (107 amostras) e secas à temperatura ambiente. Após esse procedimento, 3 fraçoes apresentaram-se cristalizadas, as quais foram reunidas e centrifugadas obtendo-se 20 mg de um precipitado. Esse precipitado foi ressuspendido em MeOH e submetido à cromatografia em cromatoplaca de sílica, utilizando como fase móvel AcOEt, H-COOH e H2O (90:0,5:0,5) e como revelador ácido difenilbórico 2- aminoetilester em EtOH. Obteve-se 10 mg de um componente, o qual foi analisado por ressonância magnética nuclear de hidrogênio, porém nao se apresentou puro. Para tanto, realizou-se uma segunda purificaçao em cromatografia preparativa por HPLC, onde 10 mg foram dissolvidos em 300 µL de DMSO e injetaram-se 300 µL no método: [Fase móvel: FA - H2O + 0,1% H3PO4, FB - ACN + 0,1% H3PO4; tempo 0-20 minutos (80-FA:20-FB), tempo 20-27 minutos (75-FA:25-FB), tempo 27 minutos (0-FA:100-FB); fluxo 24 ml/min]. Uma terceira purificaçao foi realizada com coluna analítica em HPLC. Foram dissolvidos 1,2 mg em 300 µL de metanol, com os quais fizeram-se injeçoes de 50 e 100 µL, recuperando-se manualmente o pico principal. O método utilizado foi: [Fase móvel: FA - H2O + 0,1% H3PO4, FB - ACN + 0,1% H3PO4; tempo 0-20 minutos (80-FA:20-FB), tempo 22-29 minutos (0-FA:100-FB), tempo 30 minutos (80-FA:20-FB); fluxo 1,0 mL/min]. Após essa purificaçao, foi recuperado 0,4 mg do componente com pureza de 99,93% (HPLC) e realizou-se a identificaçao por RMN-1H e técnicas mono e bidimensionais, em CD3OD e temperatura ambiente. O padrao de trabalho verbascosídeo foi isolado da fraçao acetato de etila das folhas de Duranta vestita Cham., Verbenaceae. A purificaçao desta fraçao foi realizada utilizando coluna de sílica gel 60 Merckr, para a qual foi preparada uma pastilha com 5 partes de sílica para 1 parte da fraçao. Em seguida, a amostra foi eluída com mistura de solventes, iniciando-se com 100% de n-hexano P.A., utilizando AcOEt P.A. como gradiente de polaridade e aumentando o intervalo de 10 em 10% até 100% do mesmo. Em seguida, utilizou-se a mistura AcOEt e MeOH P.A. na proporçao 90:10, utilizando MeOH como gradiente de polaridade e aumentando o intervalo de 10 em 10% até 100% do mesmo. Posteriormente foi utilizado água como gradiente, com intervalo de 50% até 100% de H2O. Os frascos 49 a 90 foram reunidos e injetados em coluna preparativa C18 (HPLC) no método: fase móvel A: H2O + 0,1% de H3PO4 e fase móvel B: MeOH; gradiente: tempo 0-7 minutos (85 a 80%-FA:15 a 20%-FB) e tempo 8-32 minutos (35%-FA:65%-FB). A substância isolada apresentou-se como um pó bege, com pureza de 99,89% (HPLC) e sua estrutura identificada por RMN de 13C e 1H.15 Desenvolvimento e validaçao do método analítico Para o desenvolvimento e validaçao do método analítico utilizou-se coluna analítica em HPLC e como fase móvel os seguintes solventes: bomba A - soluçao aquosa constituída de H2SO4 0,01 M, H3PO4 0,4% e (C2H5)2NH 0,4%; bomba B - MeOH: soluçao aquosa constituída de H2SO4 0,05 M, H3PO4 2% e (C2H5)2NH 0,2%, na proporçao de 95:5; bomba C - ACN: soluçao aquosa constituída de H2SO4 0,05 M e H3PO4 2%, na proporçao de 90:10. Os cromatogramas foram integrados no comprimento de onda 325 nm. A temperatura do forno foi 35 ºC. As amostras foram diluídas em MeOH e fase diluente (H2O + 2% de H3PO4). O volume de injeçao foi de 40 µL. O gradiente de fase móvel está descrito na Tabela 1.
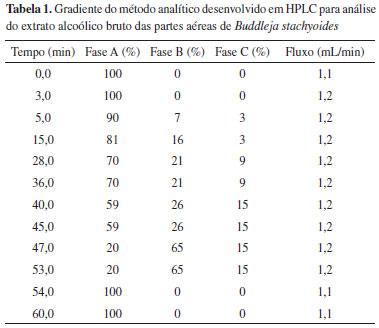
A concentraçao de verbascosídeo nas amostras foi calculada através do sistema interface L7000 conectado ao Windows Professional (equipamento Merck-Hitashi), considerando a área encontrada, a equaçao da reta e fatores reais de diluiçao [Concentraçao (mg/g) = Area x Fator de diluiçao x Equaçao da reta (escalar)]. Os parâmetros avaliados na validaçao analítica do método para doseamento de verbascosídeo foram: especificidade, linearidade, repetibilidade, precisao intermediária, exatidao e robustez, de acordo com a Resoluçao - RE nº 899, de 29 de maio de 2003, elaborada pela ANVISA.13 A curva analítica foi preparada com a soluçao padrao de verbascosídeo na concentraçao de 0,30 mg/mL em MeOH. A partir dessa soluçao foram preparadas cinco concentraçoes dissolvidas em fase diluente (0,08 mg/mL; 0,09 mg/ml; 0,10 mg/mL; 0,11 mg/mL; 0,12 mg/mL) e injetadas em triplicata. A repetibilidade foi realizada com 6 determinaçoes a 100% da concentraçao do teste para verificar a concordância entre os resultados dentro de um curto período de tempo com o mesmo analista e mesma instrumentaçao. A precisao intermediária foi também realizada com 6 determinaçoes a 100% da concentraçao do teste e serviu para verificar a concordância entre os resultados do mesmo laboratório, mas obtidos em dias e analistas diferentes. Neste ensaio as amostras sofreram uma diluiçao de 1:250 para permanecerem dentro da curva analítica. No parâmetro exatidao foi utilizado o método de adiçao de padrao, no qual adicionou-se quantidades conhecidas do padrao de trabalho (verbascosídeo) ao extrato alcoólico bruto. O estudo foi realizado em 3 concentraçoes (baixa, média e alta) no intervalo da curva analítica, em triplicata, perfazendo um total de 9 ensaios. Para obter a concentraçao 1 próxima à teórica (0,083 mg/mL) foram adicionados 125 µL da amostra extrato alcoólico bruto 1:50, 100 µL do padrao 0,30 mg/mL de verbascosídeo e 775 µL de fase diluente. Para obter a concentraçao 2 próxima à teórica (0,107 mg/mL) foram adicionados 125 µL da amostra extrato alcoólico bruto 1:50, 180 µL do padrao 0,30 mg/mL de verbascosídeo e 695 µL de fase diluente. Para obter a concentraçao 3 próxima à teórica (0,119 mg/mL) foram adicionados 125 µL da amostra extrato alcoólico bruto 1:50, 220 µL do padrao 0,30 mg/mL de verbascosídeo e 655 µL de fase diluente. A exatidao é calculada como porcentagem de recuperaçao da quantidade conhecida do analito adicionado à amostra e deve estar entre 95 e 105%.13 No parâmetro robustez realizou-se a análise de estabilidade da soluçao, a mesma amostra utilizada no parâmetro de precisao por repetibilidade foi injetada após 24 h do seu preparo. Outras formas de avaliar a robustez do método foi diluir a fase móvel A (1:2), consequentemente o pH foi alterado de 2,0 para 3,0 e também a temperatura do forno foi modificada para 40 ºC.
RESULTADOS E DISCUSSAO Identificaçao Os deslocamentos químicos e as constantes de acoplamento (J) obtidos do espectro de RMN -1H demonstraram que o componente isolado é o verbascosídeo, Figura 1.
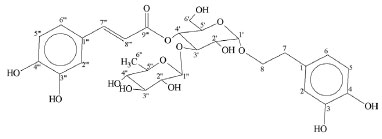 Figura 1. Estrutura do componente isolado verbascosídeo
Validaçao A curva analítica do padrao de verbascosídeo apresentou-se linear na faixa de trabalho pretendida, com um coeficiente de determinaçao (r2) de 0,9869, sendo maior que a especificaçao para fitoterápicos que é de 0,98, como mostra a Figura 2. Após obtençao da curva analítica, foi possível calcular a concentraçao de verbascosídeo presente na amostra de extrato alcoólico bruto das partes aéreas. Foram pesadas 134 mg da amostra extrato alcoólico bruto (equivalente a 1 g de droga vegetal) e diluídas para balao volumétrico de 50 mL com MeOH, depois foi diluída 1:5 em fase diluente obtendo-se uma diluiçao final de 1:250. A concentraçao encontrada foi de 21,47 mg/g de verbascosídeo, como mostra a Figura 3. A amostra foi diluída para ficar dentro da curva analítica conforme o cálculo: 21,47 mg/250 ml = 0,085 mg/ml de concentraçao final de verbascosídeo.
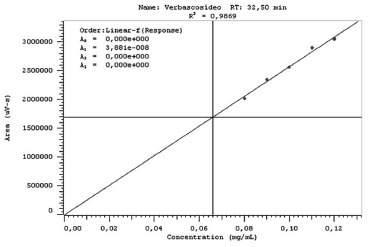 Figura 2. Curva analítica obtida com o padrao de trabalho verbascosídeo
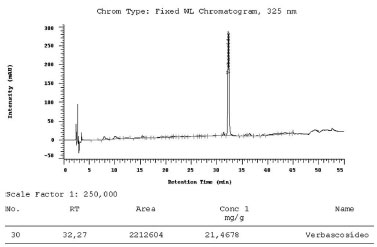 Figura 3. Concentraçao de verbascosídeo presente no extrato alcoólico bruto das partes aéreas de Buddleja stachyoides
Devido ao teor elevado de verbascosídeo quantificado no extrato alcoólico bruto das partes aéreas, escolheu-se este marcador para realizaçao de uma validaçao analítica, podendo ser utilizado para a padronizaçao no controle de qualidade de um possível medicamento fitoterápico desenvolvido com as partes aéreas de Buddleja stachyoides. No ensaio de especificidade, foi injetado o álcool etílico hidratado de cereais 96 ºGL no método desenvolvido para verificar a influência do excipiente, o qual nao apresentou nenhum pico com o mesmo tempo de retençao que o verbascosídeo ou alguma semelhança com o padrao. Dessa forma, comprovou-se que o solvente utilizado na extraçao nao possui nenhum componente que possa promover interferência na detecçao de verbascosídeo. No espectro de UV, Figura 4, com absorçao em 329,1 nm pode-se visualizar a pureza do pico de 99,88%, do extrato alcoólico bruto das partes aéreas, sendo maior que a especificaçao de 99%. Através da comparaçao espectral entre o pico de verbascosídeo presente na amostra e o padrao de verbascosídeo, obteve-se uma correlaçao espectral de 99,96%, demonstrando a existência de similaridade entre os espectros de UV e o mesmo perfil cromatográfico, como mostra a Figura 5.
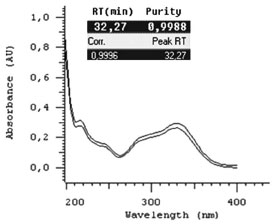 Figura 4. Espectro de UV, pureza e correlaçao espectral do pico do verbascosídeo presente no extrato alcoólico bruto das partes aéreas de Buddleja stachyoides
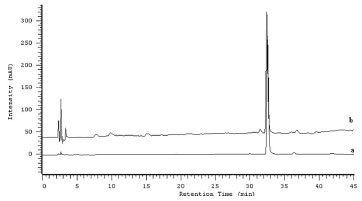 Figura 5. Perfil cromatográfico do extrato alcoólico bruto das partes aéreas de Buddleja stachyoides. a) Padrao de trabalho verbascosídeo; b) Extrato alcoólico bruto
No parâmetro repetibilidade, o desvio padrao relativo (DPR%) encontrado entre as 6 injeçoes do analista 1 foi de 0,87% com uma concentraçao média de 21,44 mg/g e para o analista 2 a concentraçao média foi de 20,57 mg/g com um desvio padrao relativo de 0,41%. Esses resultados estao dentro dos limites especificados (DPR < 5%). Na precisao intermediária a concentraçao média das análises realizadas pelos dois analistas foi de 21,01 mg/g com desvio padrao relativo de 2,26%, valor abaixo dos limites de especificaçao (DPR < 5%). Através desses resultados pode-se confirmar que o método proposto é reprodutível. As concentraçoes práticas provenientes do ensaio de exatidao foram 0,083 mg/mL, 0,105 mg/mL e 0,116 mg/mL, e ao comparar com as concentraçoes teóricas obteve-se os índices de recuperaçao de 100,72%, 98,32% e 97,81% para as concentraçoes 1, 2 e 3, respectivamente. Portanto, o método proposto apresenta exatidao, pois os índices de recuperaçao do padrao adicionado permaneceram dentro da faixa de 95% a 105%.13 No parâmetro robustez estabilidade da soluçao, após 24 horas de preparo o valor do doseamento do verbascosídeo foi de 20,92 mg/g, apresentando um desvio padrao relativo em relaçao à média da precisao por repetibilidade de 0,28%, indicando que a amostra permanece estável, alterando pouco o teor após 24 horas do seu preparo. No parâmetro pH e composiçao da fase móvel, a fase móvel A foi diluída 1:2. Dessa forma, além de ter alterado a composiçao da fase móvel, modificou o pH (que possuía um valor aproximado de 2,0 e nesta análise ficou em torno de 3,0). Obteve-se a concentraçao de verbascosídeo de 20,45 mg/g e desvio padrao relativo de 1,81%. No parâmetro robustez temperatura do forno a concentraçao encontrada foi de 20,59 mg/g com um desvio padrao relativo de 1,41%. Os três ensaios apresentaram-se robustos para o método proposto, pois em todos os desvios padrao relativo foram inferiores ao limite especificado (DPR < 5%). Os resultados obtidos para a validaçao analítica do doseamento de verbascosídeo estao apresentados na Tabela 2.
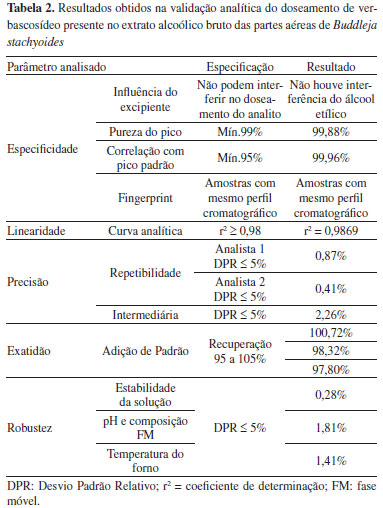
Validaçao é um processo dinâmico e constante que deve ser iniciado com o planejamento da estratégia analítica e continuar ao longo de todo o seu desenvolvimento e transferência.11 O método analítico deve ser revalidado sempre que ocorrerem modificaçoes no processo, equipamento, padronizaçao da amostra, procedimento ou quando o mesmo for usado novamente após certo período de tempo. As normas internacionais, nacionais e sistemas da qualidade destacam a importância da validaçao de métodos analíticos e a documentaçao do trabalho de validaçao para a obtençao de resultados confiáveis e adequados ao uso pretendido.12
CONCLUSAO Neste estudo foi isolado o fenilpropanoide verbascosídeo, principal componente presente nas partes aéreas de Buddleja stachyoides, o qual apresenta atividades farmacológicas importantes como antioxidante, analgésica e inibidor da POP. Além disso, foi desenvolvido e validado um método analítico para quantificaçao deste marcador e padronizaçao do extrato alcoólico bruto, o qual está de acordo com os parâmetros exigidos pela Resoluçao - RE nº. 899, de 29 de maio de 2003 da ANVISA, mostrando-se sensível, preciso, reprodutível, simples e de baixo custo. Dessa forma, apresenta grande importância na pesquisa, desenvolvimento e cadeia produtiva de medicamentos fitoterápicos e produtos farmacêuticos a base de extratos provenientes de Buddleja stachyoides, ou ainda, de qualquer outra espécie vegetal que contenha a substância verbascosídeo.
MATERIAL SUPLEMENTAR Os dados dos deslocamentos químicos e das constantes de acoplamento (J) do isolado verbascosídeo e o espectro de RMN-1H, obtidos neste trabalho, estão disponíveis em http://quimicanova.sbq.org.br, na forma de arquivo PDF, com acesso livre.
AGRADECIMENTOS Ao programa de Ciências Farmacêuticas da UFPR, ao Institut de Chimie de Substances Naturelles, à indústria As Ervas Curam, ao profº. Dr. J. C. P. de Mello da UEM e à CAPES pelo apoio financeiro.
REFERENCIAS 1. http://www.floradobrasil.jbrj.gov.br/jabot, acessada em Outubro 2013. 2. Ferreira, H. D.; Dissertaçao de Mestrado, Universidade Estadual de Campinas, Brasil, 1988. 3. Lorenzi, H.; Matos, F. J. A.; Plantas medicinais no Brasil: nativa e exóticas, 2 ed., Instituto Plantarum: Sao Paulo, 2008. 4. Gitzel Filho, A.; Morel, A. F.; Adolpho, L.; Ilha, V.; Giralt, E.; Tarragó, T.; Dalcol, I. I.; Phytother. Res. 2012, 26, 1472. 5. Vertuani, S.; Beghelli, E.; Scalambra, E.; Malisardi, G.; Copetti, S.; Dal Toso, R.; Baldisserotto, A.; Manfredini, S.; Molecules 2011, 16, 7068. 6. Backhousea, N.; Delportea, C.; Apablazaa, C.; Farías, M.; Goïtya, L.; Arraua, S.; Negretea, R.; Castroa, C.; J. Ethnopharmacol. 2008, 119, 160. 7. Borges, N. S.; Dalcol, I.; Gitzel Filho, A.; Rivero, A. C.; Adolpho, L. O.; Marin, D. F.; Anais da 25ª Jornada Acadêmica Integrada, Santa Maria, Brasil, 2010. 8. Funes, L.; Laporta, O.; Cerdán-Calero, M.; Micol, V.; Chem. Phys. Lipids 2010, 163, 190. 9. Lee, J. Y.; Woo, E.; Kang, K. W.; J. Ethnopharmacol. 2005, 97, 561. 10. Brasil, Ministério da Saúde, ANVISA - Agência Nacional de Vigilância Sanitária; Resoluçao RDC 14, de 31/03/2010, MS: Brasília, 2010. 11. Barros, C. B.; Biológico 2002, 64, 175. 12. Ribani, M.; Bottoli, C. B. G.; Collins, C. H.; Jardim, I. C. S. F.; Melo, L. F. C.; Quim. Nova 2004, 27, 771. 13. Brasil, Ministério da Saúde, ANVISA - Agência Nacional de Vigilância Sanitária; RE nº 899, de 29/05/2003, Guia para validaçao de métodos analíticos e bioanalíticos, MS: Brasília, 2003. 14. Carvalho, J. L. C.; Dissertaçao de Mestrado, Universidade Federal do Paraná, Brasil, 2001. 15. Canteli, V. C. D.; Dissertaçao de Mestrado, Universidade Federal do Paraná, Brasil, 2012. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access





