Artigo
|
|
| Glicerofosfolipídios sintéticos para uso como aditivo biocida em tintas anti-incrustante The synthesis of glycerophospholipids for use as a booster biocide in antifouling coatings |
|
William R. BatistaI,II,*; Maria H. C. B. NevesI; Ricardo CoutinhoI; Cláudio C. LopesII; Rosangela S. C. LopesII
IInstituto de Estudos do Mar Almirante Paulo Moreira, Marinha do Brasil, Rua Kioto 253, Praia dos Anjos, 28930-000 Arraial do Cabo - RJ, Brasil Recebido em 12/01/2015 *e-mail: williamromao@yahoo.com.br This paper presents a technological innovation that uses a subclass of glycerophospholipids as a booster biocide in antifouling paint. These glycerophospholipid PAF-analogs are economically and environmentally viable compounds because they are synthesized from a metal-free raw material source-soybean lecithin. The synthesis, which involves transesterification followed by an alkylation reaction, produced a mixture of glycerophospholipids that were characterized by mass spectrometry. Evaluation of the antifouling performance with field tests showed that the replacement of ordinary halogenated booster biocide with the synthesized product gave a better efficiency and an exceptional antifouling activity with a significant reduction in the coverage of the fouling macro-organisms. INTRODUÇÃO O mercado mundial de tintas marítimas anti-incrustantes, utilizadas em revestimentos de cascos de navios, necessita urgentemente de um substituto para o tributil estanho (TBT), principal e mais eficiente agente biocida já utilizado neste segmento industrial. Apesar de mundialmente reconhecido como uma substância eficaz e de ter sido utilizado por longo tempo pela indústria naval, o TBT foi banido em 2008, por leis ambientais internacionais, por ser um causador, cientificamente comprovado, de vários danos ao meio ambiente marinho.1-5 Este trabalho propõe a utilização de glicerofosfolipídios (GPL) como aditivo biocida anti-incrustante em tintas marítimas, especificamente aqueles GPL estruturalmente análogos à substância conhecida por Fator Ativador de Plaquetas (PAF), tendo como princípio de inferência os efeitos antagônicos provocados por esta substância em diferentes tipos de células empregadas em testes in vitro realizados pelas áreas médica e farmacológica.6-12 GPL têm sido usados para reduzir a adesão de proteínas e de bactérias em materiais empregados em certas áreas tecnológicas, tais como: equipamentos de processamento de alimentos, bebidas e fármacos; materiais médicos, por exemplo, próteses, lentes oftálmicas e cateteres; equipamentos filtrantes; etc., sendo suposto que tais propriedades antiaderentes estejam relacionadas às peculiaridades da natureza anfifílica e, por vezes, zwitteriônica de suas estruturas moleculares.13-18 PAF e Lyso-PAF análogos referem-se, respectivamente, aos éteres-lipídios 1-O-alquil-2-acetil-sn-glicero-3-fosfocolina e ao 1-O-alquil-2-OH-sn-glicero-3-fosfocolina, sem vínculo com o comprimento ou com o grau de insaturação do grupo alquila, sendo potentes mediadores biológicos produzidos por vários tipos de células.19-23 Estas substâncias também apresentam, além das propriedades já mencionadas, baixos pesos moleculares (<1000 Daltons), o que facilita a sua difusão através de biofilmes bacterianos e também o seu trânsito quanto aos possíveis mecanismos de absorção celular envolvendo a membrana citoplasmática dos micro-organismos presentes nestes biofilmes.24-29 Outro fator importante é que estes GPL especiais, sem um radical tipo acila na posição sn-2 do glicerol30 (Figura 1), podem atuar como molécula sinalizadora quando em contato ou absorvido pelos micro-organismos, sem sofrer a interrupção de sua ação agonista por enzimas do tipo fosfolipase (PLA), permitindo que ele seja acumulado no invólucro, parede ou interior das células, deflagrando um processo antagônico de resposta celular, que inibirá o desenvolvimento ou destruirá o micro-organismo atingido.31-33
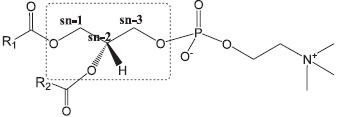 Figura 1. Numerações estereoespecíficas (sn) dos carbonos do glicerol de um GPL
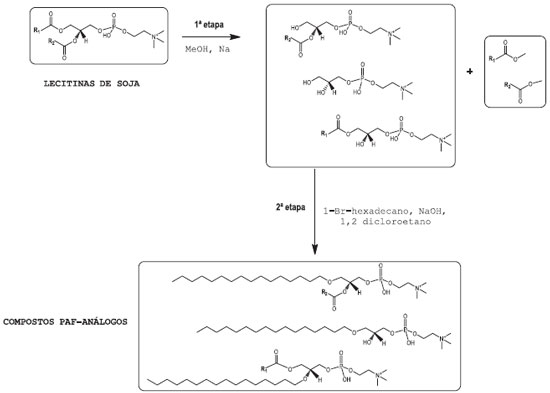
A síntese total de GPL não é uma tarefa trivial, a qual requer a incorporação regiosseletiva de três diferentes substituintes nas três posições possíveis da molécula de glicerol, o que envolve sequências de proteção e desproteção de suas hidroxilas e sequências de alquilação ou acilação e fosforilação, podendo, para este intento, normalmente utilizar-se de procedimentos catalíticos e enzimáticos.34-42 Além disto, tais procedimentos têm sido empregados especificamente em ensaios laboratoriais, trabalhando-se na faixa de micro e miligramas, não estando tais rotas de sínteses relacionadas com a escala de produção de nosso interesse, ou seja, em escala comercial. Para dispor de uma maior quantidade de material biocida foi desenvolvido em nosso grupo de pesquisa, no Laboratório de Síntese e Análise de Produtos Estratégicos - LASAPE, Instituto de Química (UFRJ), uma rota de síntese a partir da transesterificação de lecitinas de soja comercial, visando à obtenção preliminar de GPL do tipo 1-OH-2-O-acil-sn-glicero-3-fosfocolina, 1-O-acil-2-OH-sn-glicero-3-fosfocolina e 1-OH-2-OH-sn-glicero-3-fosfocolina, os quais, em uma segunda etapa de síntese, foram submetidos à reação de alquilação, sendo então obtidas as substâncias de interesse com estruturas químicas semelhantes aos compostos Lyso-PAF-análogos.43-45
PARTE EXPERIMENTAL Instrumentação A análise de massas foi realizada empregando um sistema composto por um cromatógrafo a líquido Shimadzu Prominence UFLC acoplado a um espectrômetro de massas Bruker modelo Esquire 6000 equipado com eletrospray ortogonal e um analisador do tipo ion trap. O cromatógrafo foi operado sob modo gradiente usando uma coluna Hypersil Gold C18 Thermo (250 x 2 mm, 5 µm) e fase móvel composta por ácido trifluoacético (TFA) 0,5% em água / Metanol / Tetrahidrofurano, iniciando a corrida com uma composição de (30/15/55) e uma vazão de 0,2 mL min-1, alcançando aos 15 minutos a composição de (00/12/88) e a vazão de 0,1 mL min-1 que foram mantidos até fim da corrida de 30 minutos. Solventes usados: Metanol grau LC-MS (Tedia); Tetrahidrofurano grau HPLC (Tedia); água grau Milli-Q. O espectrômetro de massas foi operado em modo positivo, scan m/z (150-1050); Resolução normal com (FWHM / m/z) de 0,6 m/z; gás secante nitrogênio a 10 L min-1; temperatura de secagem de 300 ºC e nebulizador a 30 psi; Hélio 5,0 (White Martins) usado como gás de amortecimento do trap; alto vácuo de 10-5 mbar; trap drive 59,1; lente 1 a -5 V; lente 2 a -60 V; saída do capilar a 132,3 V; skimmer 40 V; octopolo 1 DC a 12 V; octopolo 2 DC a 1,7 V e octopolo RF a 194,5 V. Para realização dos experimentos empregando espectrometria de massas sequencial no tempo (EMn), uma amostra do produto final da síntese foi solubilizada em 2 mL de uma mistura de solvente metanol, THF e água (2/1/1) v/v e acidificada com 2 µL de ácido fórmico e introduzida por infusão direta no espectrômetro de massas, vazão de 300 µL h-1, usando uma bomba de infusão (Kd Scientific), sendo obtido os espectros de íons produto EM2 e EM3, em modo positivo, para os íons precursores mais abundantes. O espectro de RMN 1H foi obtido em espectrômetro Bruker AC 200A operando na frequência de 200 MHz. O espectro na região de infravermelho (4000-400 cm-1) foi obtido em espectrofotômetro Perkin-Elmer 1600, usando pastilhas comprimidas em brometo de potássio. Síntese química O Esquema 1 ilustra o procedimento de síntese empregado visando a obtenção de compostos PAF-análogos.
A 1ª etapa da síntese envolveu o tratamento da lecitina de soja com uma solução de metóxido de sódio em metanol e foi realizada sob forte agitação mecânica e sem aquecimento (~25 ºC) por 72 horas, sendo utilizados 1000 mL de metanol grau ACS (Vetec) e 3 g de sódio metálico (Vetec) para cada 40 g de lecitina de soja (Akros organics). A separação do produto de reação foi efetuada por filtração por gravidade em papel de filtro, sendo obtido um produto sólido com aspecto levemente amarelado, com rendimento de 83,5% (m/m), e um resíduo oleoso, que após completa evaporação do metanol forneceu 15% (m/m) de rendimento. Na 2ª etapa da síntese, uma fração do produto sólido obtido da reação de transesterificação (1ª síntese), 1,2-dicloroetano, 1-bromo-hexadecano e solução aquosa de hidróxido de sódio foram adicionados a um balão e mantidos sob forte agitação magnética por 2 horas sob temperatura ambiente (~ 25 ºC). Após este tempo, efetuou-se a evaporação do dicloroetano e se adicionou uma mistura de metanol e hidróxido de amônio em excesso à reação, sendo mantida por mais 2 horas sob agitação. Após evaporação do solvente, re-extração com diclorometano e lavagem com água destilada, obteve-se os produtos alquilados de interesse com rendimento calculado de 60% (m/m).46 Espectrometria de massas As análises por espectrometria de massas, as propostas de caminhos e reações de fragmentação e a classificação dos GPL presentes no produto final de síntese foram realizadas tendo como parâmetro trabalhos existentes sobre análise de massas e classificação de lipídios.47-53 Os espectros de massas encontram-se como material suplementar. Testes de campo Os testes de campo foram realizados, em parceria, pela Divisão de Biotecnologia Marinha do Instituto de Estudos do Mar Almirante Paulo Moreira - IEAPM e pelo laboratório da empresa International Tintas - Akzo Nobel, sendo utilizado um procedimento comparativo entre quatro diferentes revestimentos anti-incrustante isentos de cobre e um revestimento controle (sem qualquer biocida), com duas réplicas cada, os quais foram aplicados em placas de aço carbono (corpos-de-prova) medindo (15 cm × 30 cm). Os corpos-de-prova foram mantidos submersos diretamente na baía da Guanabara-RJ, usando-se balsas flutuantes, sendo avaliados quanto à presença de limo e cracas depois de passado um período de três semanas e, complementarmente, após oito semanas de imersão. Tratamentos usados nas pinturas das placas: Revestimento A - Tinta anti-incrustante comercial Mícron premium tendo o produto da síntese (5% m/m) mais o biocida Econea de linha comercial (2% p/p) como biocidas coadjuvantes; Revestimento B - Tinta anti-incrustante comercial Mícron Premium tendo somente o produto da síntese (5% m/m) como biocida coadjuvante; Revestimento C - Tinta anti-incrustante comercial Mícron Premium tendo somente o biocida Econea (2% m/m) como biocida coadjuvante; Revestimento D - Tinta anti-incrustante comercial Mícron Premium tendo o produto da síntese (10% m/m) mais o biocida Econea de linha comercial (2% p/p) como biocidas coadjuvantes; e Revestimento E - Tinta marítima anticorrosiva Intertuf Vinyl sem aditivos biocidas.
RESULTADOS E DISCUSSÃO Produto de síntese O espectro de massas do produto da 2ª etapa da síntese registrou íons sendo eluídos entre o quinto e o vigésimo minuto da corrida, os quais apresentaram razões massa carga variando entre m/z 480 e m/z 620, tendo sido registrado como íons mais intensos os íons m/z 510,6 e 592,6. Tabela 1 apresenta os íons precursores mais abundantes observados e seus respectivos íons produto EM2 e EM3.
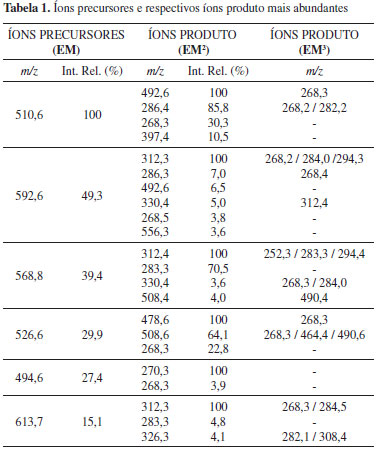
A proposta para o íon precursor m/z 510,6 e seus respectivos caminhos e mecanismos das reações de fragmentação, com base nos principais íons produto obtidos, é apresentada nos Esquemas 2 e 3.
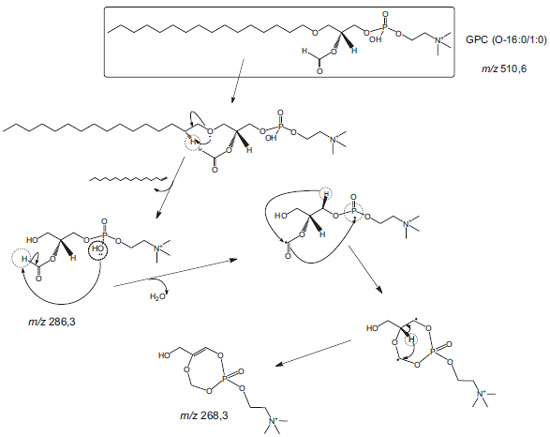 Esquema 2. Produto da 2ª etapa da síntese. Proposta de caminhos e de mecanismos das reações de fragmentação para íon precursor m/z 510,6 e íons produto m/z 286,3 e m/z 268,3
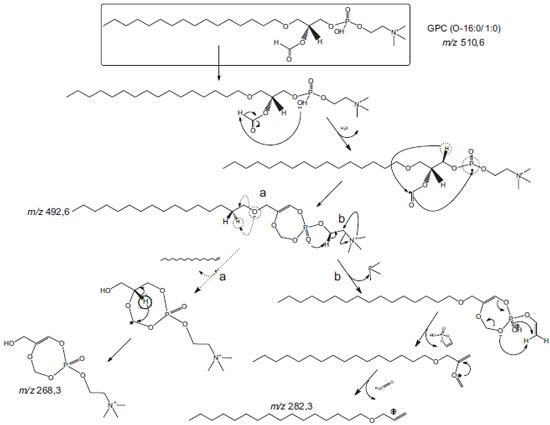 Esquema 3. Produto da 2ª etapa da síntese. Proposta de caminhos e de mecanismos das reações de fragmentação para íon precursor m/z 510,6 e íons produto m/z 492,3, m/z 282,3 e m/z 268,3
Cabe observar que o resultado obtido para o íon m/z 510,6 ensejou dúvidas quanto à presença do radical formil (aldeído), o qual não era esperado para os produtos de síntese. Por este motivo, visando avaliar especificamente a presença de uma possível função aldeído, foram realizadas análises complementares por espectroscopia de ressonância de hidrogênio (RMN 1H) e por espectrofotometria de infravermelho (IV), as quais não identificaram a presença de bandas característica para aldeídos, ou seja, deslocamento químico entre 9-10 e bandas de forte intensidade nas freqüências de 1725 cm-1, devido à deformação axial C=O, e entre 2825-2720 cm-1, devido à deformação axial C-H, indicando, deste modo, que o produto referente ao íon m/z 510,6 trata-se, na verdade, da substância 1-hexadecil-2-OH-sn-glicero-3-fosfocolina que sofreu uma substituição nucleofílica no carbono (sn-2) pela ação do radical formil disponibilizado pelo tratamento prévio da amostra com ácido fórmico. A proposta para o íon precursor m/z 592,5 e seus respectivos caminhos e mecanismos das reações de fragmentação, com base nos principais íons produto obtidos, é apresentada nos Esquemas 4 e 5.
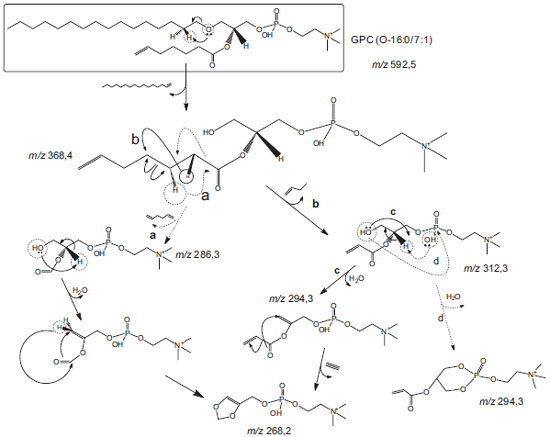 Esquema 4. Produto da 2ª etapa da síntese. Proposta de caminhos e mecanismos fragmentação para íon precursor m/z 592,5 e íons produto m/z 312,3, m/z 294,3, 286,3 e m/z 268,2
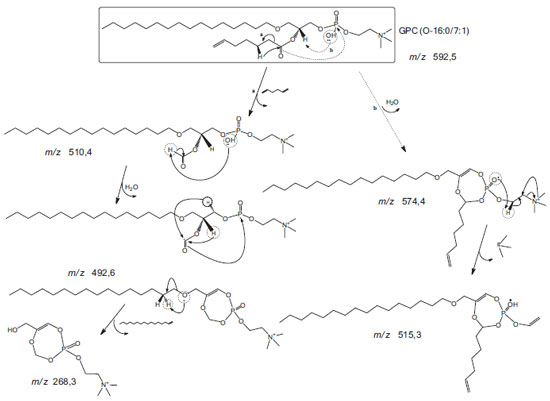 Esquema 5. Produto da 2ª etapa da síntese. Proposta de caminhos e mecanismos fragmentação para íon precursor m/z 592,5 e íons produto m/z 515,6, m/z 492,6 e m/z 268,2
Testes de campo Todos os tratamentos utilizados, com exceção daquele sem produto biocida (revestimento E), apresentaram muito boa inibição do desenvolvimento de limo e da fixação de cracas. A Figura 2 apresenta a comparação visual observada após três e oito semanas para os diversos revestimentos após imersão contínua no campo de testes da empresa International tintas, localizado na Baía da Guanabara - RJ. No painel sem biocida (revestimento E), pintado somente com a tinta primer anticorrosiva, foi observado uma massiva presença de limo e de cracas, mostrando a condição extrema do ambiente marinho da Baía da Guanabara com relação à incrustação marinha, sendo verificado uma forte adesão dos organismos fixados e constatado a dificuldade da retirada manual.
 Figura 2. Fotografias das placas usadas nos testes de campo apresentando uma comparação visual dos efeitos das ações anti-incrustante dos diferentes tratamentos (A-E) após imersão, na Baía da Guanabara, por três semanas (superior) e oito semanas (inferior). Fonte: Divisão de Biotecnologia Marinha - IEAPM
No painel pintado com o revestimento A (tinta base Micron Premium + 5% biocida 2ª síntese + 2% biocida comercial ECONEA) verificou-se somente uma pequena formação de limo e a total ausência de cracas até a 3ª semana, sendo observado uma intensificação da presença de limo na oitava semana, porém com ainda muito boa ação contra o assentamento de cracas. Cabe ressaltar aqui a fraca adesão observada e fácil remoção manual dos organismos fixados. No painel pintado com o revestimento B (tinta base Micron Premium + 5% biocida 2ª síntese), verificou-se também a total ausência de cracas até a terceira semana e uma leve presença de cracas na oitava semana. Contudo, foi constatado, em geral, a fraca adesão e fácil remoção manual dos organismos fixados. No painel pintado com o revestimento C (tinta base Micron Premium + 2% biocida comercial ECONEA) verificou-se também somente uma pequena formação de limo e a ausência de cracas até a terceira semana de imersão, porém, após a oitava semana verificou-se a presença de limo, de pequena quantidade de cracas e de material não consolidado. No painel pintado com o revestimento D (tinta base Micron Premium + 10% biocida 2ª síntese + 2% biocida comercial ECONEA) verificou-se uma pequena formação de limo e a ausência de cracas até a terceira semana e pequena formação de limo e de fixação de cracas após a oitava semana.
CONCLUSÃO Compostos PAF-análogos podem ser satisfatoriamente sintetizados a partir de lecitinas de soja, sendo este produto de síntese ativo biologicamente e de possível incorporação na produção de tintas marítimas anti-incrustantes. Os testes de campo demonstraram que o produto de síntese, quando usado em substituição ao biocida organo-halogenado acessório (booster), apresentou uma melhor eficiência na redução dos organismos incrustantes e apresentou uma muito boa atividade em ambos os testes de campo com significativa redução da cobertura dos macro-organismos incrustantes quando comparado com o controle negativo (sem biocida). Entende-se aqui que o seu uso possa ser de fato relevante ao se considerar uma possível substituição de aditivos biocidas hoje utilizados em tintas marítimas anti-incrustantes, principalmente nas novas tintas isentas de cobre, pois trata-se de um composto biocida isento de metais e com apelo natural, uma vez que estas substâncias são análogas aos compostos naturais do tipo PAF e lyso-PAF. Com base nos resultados obtidos e no acima exposto, conclui-se que a proposta de uso das substâncias aqui avaliadas como aditivo biocida anti-incrutante é uma alternativa viável para a produção de tintas anti-incrustantes, apresentando-se como uma nova e efetiva perspectiva, considerando a exequibilidade operacional da síntese - por utilizar lecitinas de soja, um resíduo da produção de óleo de soja comestível e de biodiesel, como matéria-prima do processo - e seu bom desempenho anti-incrustante comparado a biocidas convencionais e danosos ao meio ambiente.
MATERIAL SUPLEMENTAR Os espectros de massas obtidos e utilizados neste trabalho, Figuras 1S à 8S, estão disponíveis em http://quimicanova.sbq.org.br, na forma de arquivo PDF, com acesso livre.
AGRADECIMENTOS Os autores agradecem ao CNPq e à Petrobras pela bolsa concedida ao primeiro autor; ao Instituto de Estudos do Mar Almirante Paulo Moreira - IEAPM, Instituto de Química - UFRJ e a empresa International Tintas - Akzo Nobel pelo suporte material e infraestrutural, e ao Laboratório de Síntese e Análise de Produtos Estratégicos - LASAPE pela realização das sínteses químicas.
REFERÊNCIAS 1. http://www.imo.org/mediacentre/maritimenewsmagazine/documents/2008/imonewsno408_web.pdf, acessada em Junho 2015. 2. Gipperth, L.; J. Environ. Manage. 2009, 90, S86. DOI: http://dx.doi.org/10.1016/j.jenvman.2008.08.013 PMID: 18976851 3. Sonak, S.; Pangam, P.; Giriyan, A.; Hawaldar, K.; J. Environ. Manage. 2009, 90, S96. DOI: http://dx.doi.org/10.1016/j.jenvman.2008.08.017 PMID: 18977581 4. Quian, P.; Xu, Y.; Fusetani, N.; Biofouling 2010, 26, 223. DOI: http://dx.doi.org/10.1080/08927010903470815 5. Du J.; Chadalavada S.; Chen Z.; Naidu R.; Chem. Eng. J. 2014, 235, 141. DOI: http://dx.doi.org/10.1016/j.cej.2013.09.044 6. Venable, M. E.; Zimmerman, G. A.; McIntyre, T. M.; Prescott, S. M.; J. Lipid Res. 1993, 34, 691. PMID: 8389794 7. Botitsi, E.; Mavri-Vavayanni, M.; Siafaka-Kapadai, A.; J. Lipid Res. 1998, 39, 1295. PMID: 9643362 8. Kulikov, V. I.; Muzya, G. I.; Biochemistry Moscow 1998, 63, 47. 9. Croft, S. L.; Engel, J.; Trans. R. Soc. Trop. Med. Hyg. 2006, 100S, S4. DOI: http://dx.doi.org/10.1016/j.trstmh.2006.03.009 10. Verma, N. K.; Dey, C. S.; Agents Chemother. 2004, 48, 3010, nº8. DOI: http://dx.doi.org/10.1128/AAC.48.8.3010-3015.2004 11. Croft, S. L.; Seifert, K.; Duchêne, M.; Mol. Biochem. Parasitol. 2003, 126, 165. DOI: http://dx.doi.org/10.1016/S0166-6851(02)00283-9 PMID: 12615315 12. Yost, C. C.; Weyrich, A. S.; Zimmerman, G. A.; Biochimie 2010, 92, 692. DOI: http://dx.doi.org/10.1016/j.biochi.2010.02.011 PMID: 20167241 13. Fahy, E.; Cotter, D.; Sud, M.; Subramaniam, S.; Biochim. Biophys. Acta 2011, 1811, 637. DOI: http://dx.doi.org/10.1016/j.bbalip.2011.06.009 PMID: 21704189 14. Sariri, P. R.; Toosi, A. E. K.; Russ. J. Org. Chem. 2003, 39, 471 . DOI: http://dx.doi.org/10.1023/A:1026013714660 15. Goreish, H. H.; Lewis A. L.; Rose S.; Lloyd A. W.; J. Biomed. Mater. Res. 2004, 68A, 1. DOI: http://dx.doi.org/10.1002/jbm.a.10141 16. Iwasaki, Y.; Ishihara, K.; Anal. Bioanal. Chem. 2005, 381, 534. DOI: http://dx.doi.org/10.1007/s00216-004-2805-9 PMID: 15723256 17. Xu J.; Wanga X.; Fan D.; Ji J.; Shen J.; Appl. Surf. Sci. 2008, 255, 538. DOI: http://dx.doi.org/10.1016/j.apsusc.2008.06.098 18. Watanabe, J.; Ishihara, K.; Colloids Surf., B. 2008, 65, 155. DOI: http://dx.doi.org/10.1016/j.colsurfb.2008.04.006 19. Hanaham, D. J.; Annu. Rev. Biochem. 1986, 55, 483. DOI: http://dx.doi.org/10.1146/annurev.bi.55.070186.002411 20. Tokumura, A.; Takauchi, K.; Asai, T.; Kamiyasu, K.; Ogawa, T.; Tsukatani, H.; J. Lipid Res. 1989, 30, 219. PMID: 2715726 21. Prescott, S. M.; Zimmerman, G. A.; Mcintyre, T. M.; J. Biol. Chem. 1990, 265, 17381. PMID: 2170377 22. Tokumura, A.; Prog. Lipid Res. 1995, 34, 151. DOI: http://dx.doi.org/10.1016/0163-7827(95)00001-G PMID: 7480064 23. Owen, J. S.; Thomas, M. J.; Wykle, R. L.; Methods in enzymol. 2007, 434, 105. 24. Jones, N. C.; Osborn, M. J.; J. Biol. Chem. 1977, 252, 7398. PMID: 332695 25. Jones, N. C.; Osborn, M. J.; J. Biol. Chem. 1977, 252, 7405. PMID: 332696 26. Nikaido, H.; Vaara, M.; Microbiol. Rev. 1985, 49, 1. PMID: 2580220 27. Koebnik, R.; Locher, K. P.; Gelder, V.; Mol. Microbiol. 2000, 37, 239. DOI: http://dx.doi.org/10.1046/j.1365-2958.2000.01983.x PMID: 10931321 28. Przetalski, S.; Sarapuk J.; Kleszczyñska H.; Gabrielska J.; Hladyszowski J.; Trela Z.; Kuczera J.; Acta Biochim. Pol. 2000, 47, 627. 29. Nikaido, H.; Microbiol. Mol. Biol. Rev. 2003, 67, 593. DOI: http://dx.doi.org/10.1128/MMBR.67.4.593-656.2003 PMID: 14665678 30. IUPAC-IUB Commission on Biochemical Nomenclature; J. Lipid Res. 1978, 19, 114. PMID: 621435 31. .Marathe, G. K.; Silva, A. R.; Neto, H. C. C. F.; Tjoelker, L. W.; Prescott, S. M.; Zimmerman, G. A.; McIntyre, T. M.; J. Lipid Res. 2001, 42, 1430. PMID: 11518762 32. Fruhwirth, G. O.; Loidl, A.; Hermetter, A.; Biochim. Biophys. Acta 2007, 1772, 718. DOI: http://dx.doi.org/10.1016/j.bbadis.2007.04.009 PMID: 17570293 33. Welch, E. J.; Naikawadi, R. P.; Li, Z.; Lin, P.; Ishii, S.; Shimizu, T.; Tiruppathi, C.; Du, X.; Subbaiah, P. V.; Ye, R. D.; Mol. Pharmacol. 2009, 75, 227. DOI: http://dx.doi.org/10.1124/mol.108.051003 PMID: 18931035 34. Rosenthal, A. F.; Chodsky, S. V.; J. Lipid Res. 1971, 12, 277. PMID: 5579257 35. Rosenthal, A. F.; J. Lipid Res. 1966, 7, 779. PMID: 5971574 36. Witzky, N. M.; Bittman, R.; J. Lipid Res. 1985, 26, 623. 37. Witzky, N. M.; Bittman, R.; J. Lipid Res. 1986, 27, 344. 38. Testet, E; Akermoun, M.; Shimoji, M.; Cassagne, C.; Bessoule, J. J.; J. Lipid Res. 2002, 43, 1150. DOI: http://dx.doi.org/10.1194/jlr.M200075-JLR200 PMID: 12091500 39. Ichihara, K.; Iwasaki, H.; Ueda, K.; Takizawa, R; Naito, H.; Tomosugi M.; Chem. Phys. Lipids 2005, 137, 94. DOI: http://dx.doi.org/10.1016/j.chemphyslip.2005.06.001 PMID: 16054615 40. Rosseto, R.; Bibak, N.; Hajdu, J.; Org. Biomol. Chem. 2006, 4, 2358. DOI: http://dx.doi.org/10.1039/b603788g PMID: 16763679 41. D'arrigo, P.; Servi, S.; Molecules 2010, 15, 1351. 42. D'arrigo, P., Fasoli, E.; Fantoni, G. P.; Rossi, C.; Saraceno, C.; Tessaro, D.; Servi, S.; Chem. Phys. Lipids 2007, 147, 113. DOI: http://dx.doi.org/10.1016/j.chemphyslip.2007.03.008 PMID: 17499652 43. Batista, W. R.; Martins, V. A.; Neves, M. H. C. B.; Coutinho, R.; Crespo, R.; Lopes, R. S. C.; Lopes, C. C.; Br PI 1004858-8, 2010. 44. Batista, W. R.; Martins, V. A.; Neves, M. H. C. B.; Coutinho, R.; Crespo, R.; Lopes, R. S. C.; Lopes, C. C.; Br PI 1004585-6, 2010. 45. Batista, W. R.; Martins, V. A.; Neves, M. H. C. B.; Coutinho, R.; Crespo, R.; Lopes, R. S. C.; Lopes, C. C.; US 8, 657, 943 B2, 2014. 46. Batista, W. R.; Martins, V. A.; Neves, M. H. C. B.; Coutinho, R.; Crespo, R.; Lopes, R. S. C.; Lopes, C. C.; Br 10 2014 014775-6, 2014. 47. Pulfer, M.; Murphy, R. C.; Mass Spectrom. Rev. 2003, 22, 332. DOI: http://dx.doi.org/10.1002/mas.10061 PMID: 12949918 48. Han, X.; Gross, R. W.; Mass Spectrom. Rev. 2005, 24, 367. DOI: http://dx.doi.org/10.1002/mas.20023 PMID: 15389848 49. Milne, S.; Ivanova, P.; Forrester, J.; Brown, A.; Methods 2006, 39, 92. DOI: http://dx.doi.org/10.1016/j.ymeth.2006.05.014 PMID: 16846739 50. Hsu, F.; Turk, J.; J. Am. Soc. Mass Spectrom. 2008, 19, 1681. DOI: http://dx.doi.org/10.1016/j.jasms.2008.07.023 PMID: 18771936 51. Cui, Z.; Thomas, M. J.; J. Chromatogr. B 2009, 877, 2709. DOI: http://dx.doi.org/10.1016/j.jchromb.2009.06.034 52. Nakanishi, H.; Lida, Y.; Shimizu, T.; Taguchi, R.; J. Biochem. 2010, 147, 245. DOI: http://dx.doi.org/10.1093/jb/mvp171 PMID: 19880374 53. Fahy, E.; Subramaniam, S.; Brown, H. A.; Glass, C. K.; Merrill, A. H.; Murphy, R. C.; Raetz, C. R. H.; Russell, D. W.; Seyama, Y.; Shaw, W.; Shimizu, T.; Spener, F.; Meer, G. V.; VanNieuwenhze, M. S.; White, S. H.; Witztum, J. L.; Dennis, E. A.; J. Lipid Res. 2005, 46, 839. DOI: http://dx.doi.org/10.1194/jlr.E400004-JLR200 PMID: 15722563 |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access