Artigo
|
|
| Encapsulação do ácido L-ascórbico no biopolímero natural galactomanana por spray-drying: preparação, caracterização e atividade antioxidante Encapsulation of L-ascorbic acid within the natural biopolymer-galactomannan-using the spray-drying method: preparation, characterization, and evaluation of antioxidant activity |
|
Carlos A. G. de SouzaI,*; Sônia M. C. SiqueiraI; Antônia F. V. de AmorimI; Selene M. de MoraisI; Tamara GonçalvesIII; Rayane N. GomesI; Arcelina P. CunhaII; Nágila M. P. S. RicardoII
ILaboratório de Produtos Naturais, Universidade Estadual do Ceará , 60740-000 Fortaleza - CE, Brasil Recebido em 03/09/2014 *e-mail: cagsouz@gmail.com In this study, the spray drying technique was used to prepare L-ascorbic acid (AA) microparticles encapsulated with galactomannan-an extract from the seeds of the Delonix regia species. The physico-chemical characteristics, antioxidant activity, and encapsulation efficiency of the AA microparticles were evaluated and characterized using thermogravimetric analysis, differential scanning calorimetry, infrared spectroscopy, X-ray diffraction, and scanning electron microscopy. The free-radical scavenging activity of the AA microparticles was determined at different environmental conditions using DPPH (1,1-diphenyl-2-picryl-hydrazyl). X-ray diffraction measurements demonstrated a loss of crystallinity in AA after the encapsulation process, and a DSC scan also showed the loss of the compound's melting peak. Thermogravimetric analysis showed small differences in the thermal stability of galactomannan before and after the incorporation of AA. The mean diameters of the obtained spherical microspheres were in the range of 1.39 ± 0.77 µm. The encapsulation efficiency of AA microparticles in different environmental conditions varied from 95.40 to 97.92, and the antioxidant activity showed values ranging from 0.487 to 0.550 mg mL-1. INTRODUÇÃO O ácido ascórbico (AA) ou Vitamina C é uma vitamina hidrossolúvel muito importante para o organismo. É comum em frutas como goiaba, laranja, maçã, morango, kiwi e vegetais como couve-flor. É essencial na construção da proteína do colágeno, na cicatrização de feridas, na manutenção do sistema imunológico e nervoso saudável e como um antioxidante para ajudar na prevenção de doenças.1 De acordo com a IUPAC a Vitamina C é também chamada de 3-oxo-L-gulofuranolactona. A estrutura química e a fórmula molecular do ácido ascórbico são dadas na Figura 1.
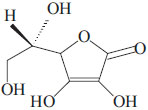 Figura 1. Estrutura do ácido L-ascórbico (C6H8O6)
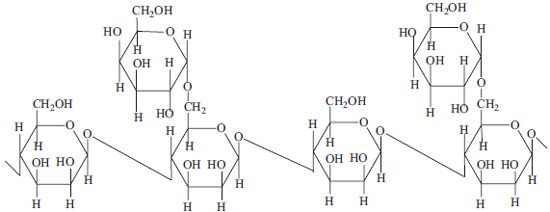
O AA é estável na forma de pó, entretanto esta característica diminui quando dissolvido em água. Fatores ambientais, tais como temperatura, pH, oxigênio, íons metálicos, UV e raios-x afetam a sua estabilidade.2 A fim de ultrapassar esta deficiência, a técnica de encapsulação pode ser o método mais adequado.3 Esta técnica tem solucionado limitações no emprego de ingredientes alimentícios visto que pode reduzir ou eliminar odores indesejáveis, reduzir volatilidade e reatividade e aumentar a estabilidade destes em condições ambientais adversas, como na presença de luz, oxigênio e pH extremos. A microencapsulação é considerada um processo físico no qual um filme fino ou uma camada polimérica é utilizada para envolver sólidos, líquidos e gasosos. Entre as várias técnicas que podem ser empregadas na microencapsulação, existe um método amplamente empregado chamado de spray drying. Esta técnica oferece algumas vantagens como baixa quantidade de solvente residual no produto final, produção de partículas relativamente uniformes e esféricas, boa eficiência e baixo custo do processo.4-6 Na indústria de alimentos, a utilização de equipamentos spray dryer para encapsulação de aromas e conservação de substâncias tem sido amplamente difundida, porém, há muitas limitações na aplicação deste processo, o que demanda estudos constantes sobre a encapsulação.7-10 Palma-Rodriguez e colaboradores utilizaram a técnica de spray drying como método de preparação de micropartículas de AA encapsulado por amidos naturais e modificados de milho, batata e arroz, estas micropartículas mostraram um grande potencial de estabilidade do AA, sofrendo uma menor degradação no seu armazenamento.11 Finotelli e Rocha-Leão prepararam micropartículas por spray drying com diferentes quantidades de AA para evitar a sua oxidação, com possível aplicação na indústria de alimentos.12 Os polissacarídeos foram estudados nas últimas décadas como materiais poliméricos para o encapsulamento de substâncias terapêuticas, porque estes são facilmente disponíveis, apresentando baixa ou nenhuma toxicidade, de baixo custo, susceptíveis a uma grande variedade de modificações químicas, potencialmente degradáveis e boa biocompatibilidade.13-15 A goma da semente da espécie Delonix regia (Flamboyant) é um polissacarídeo que pertence ao grupo de galactomananas. Normalmente, esses polímeros naturais possuem como cadeia principal unidades repetitivas de β-D-manopiranoses ligadas entre si por ponte de oxigênio do tipo 1-4 e cadeias laterais de α-D-galactopiranose ligadas do tipo 1→6. (razão manose / galactose 2:1). A razão manose / galactose é semelhante a da goma guar, mas diferem em termos de posição da ligação OH na cadeia principal: goma flamboyant tem α-D-manose, enquanto a goma guar tem β-D-manose (Figura 2).16
Este polímero apresenta uma série de características atraentes para aplicações biofarmacêuticas, entre as quais a sua alta capacidade de gelificação devem ser destacada.17 A goma da semente de flamboyant carboximetilada foi usada por Betancur e colaboradores na mircroencapsulação da papaína e polissacarídeos semelhantes, como goma guar (Cyamopsis tetragonalobus), goma alfarroba (Ceratonia siliqua) e goma guapuruvu (Schizolobium parahybae) foram investigadas com a mesma finalidade.18-22 A variedade de propriedades físico-químicas torna esse polissacarídeo um material bastante versátil utilizado pelo homem de inúmeras formas, entre elas, na indústria têxtil, farmacêutica, alimentícia, cosmética e na biomedicina.13,23 Os objetivos do presente trabalho foram preparar micropartículas do ácido L-ascórbico em galactomanana pela técnica spray drying, caracterizá-las e investigá-las quanto sua capacidade antioxidante. As micropartículas foram preparadas como alternativa para um potencial aumento da estabilidade do fármaco, com melhor desempenho para possíveis aplicações na área de alimentos e de biotecnologia.
PARTE EXPERIMENTAL Materiais O ácido ascórbico (C6H8O6; 176,12 g mol-1) foi adquirido na CAQ (Casa da Química) Brasil; metanol (SYNTH) Brasil; etanol (grau de pureza 95%, SYNTH) Brasil; DPPH (SIGMA) EUA. Fonte do polisssacarídeo As sementes da espécie D. regia foram coletadas na Universidade Estadual do Ceará (UECE), Fortaleza - CE, Brasil, em janeiro de 2013. Um total de 300 g de sementes foi coletado. A exsicata da espécie encontra-se depositada no Herbário Prisco Bezerra da Universidade Federal do Ceará sob número 53140. Isolamento da galactomanana O isolamento da galactomanana seguiu a metodologia proposta por Vieira e colaboradores, com modificações.24 As sementes foram à inativação enzimática em água a 98 ºC em constante agitação por 1 hora. Em seguida as sementes foram imersas em água destilada por 24 horas e, após esse período de intumescimento, o endosperma foi separado manualmente do tegumento e do embrião. Para a obtenção da galactomanana, os endospermas isolados foram submetidos a três extrações aquosas exaustivas. Em cada extração fez-se uso de 900 mL de água destilada para cada 150 g de endosperma a 75 ºC por um período de 4 horas, sob agitação, até a formação de uma solução viscosa. Após esse procedimento, a solução foi filtrada e armazenada a 4 ºC e o sólido retido, submetido a mais duas extrações até que todo o endosperma fosse completamente desfeito, restando apenas fibras insolúveis. Ao final das três extrações exaustivas, os líquidos armazenados foram reunidos e submetidos a uma filtração a vácuo, sendo em seguida adicionado etanol na proporção 2:1 (etanol/filtrado) para precipitação das galactomananas. Estas foram coletadas e posteriormente liofilizadas num liofilizador da Labconco Freeze Dryer, Modelo 7.750.020. Determinação da massa molar por cromatografia de permeação em gel (GPC) Foi preparada uma solução de 0,1% da goma em água e em seguida foi filtrada com membrana Milipore de porosidade 0,45 µm. A determinação da massa molar foi determinada por cromatografia de permeação em gel (GPC) em um instrumento Shimadzu LC-10AD com detector de índice de refração RID-10A a 40 ºC. A análise foi realizada com uma coluna Ultrahydrogel linear 7,8 x 300 mm, fase móvel de NaNO3 0,1 mol L-1, fluxo de 0,5 mL min-1. O volume injetado da amostra foi de 20 µL. Análise por ressonância magnética nuclear do próton (RMN 1H) A estrutura da galactomanana da D. regia foi determinada usando a espectroscopia de RMN 1H. A ressonância do próton foi relacionada com bases nos dados reportada na literatura para galactomananas.25,26 Foram preparadas soluções das amostras da galactomanana (D. regia) em D2O na concentração de 0,045 mg µL-1, sendo as amostras deixadas em água deuterada nessa concentração por 24 horas sob agitação constante e a temperatura de 80 ºC. Os espectros de ressonância magnética nuclear do hidrogênio (RMN 1H) foram obtidos por meio do espectrômetro Bruker Spectrometers, modelo Avance DRX-500, com transformada de Fourier, no Centro Nordestino de Aplicação e Uso da ressonância magnética nuclear (CENAUREMN), operando na frequência do hidrogênio a 500,13 MHz e utilizando uma sonda dual de 5 mm. Os espectros foram registrados à temperatura de 80 ºC. Foi usado um composto 2,2-dimetil-2 silapentano-5-sulfanato de sódio (DSS) como padrão interno (0,00 ppm para 1H) nas amostras dissolvidas em água deuterada. Para os espectros de RMN 1H são integrados os sinais dos hidrogênios pertencentes aos carbonos anomérico da amostra. Por meio das integrações desses de dois sinais, em torno de 5,19 e 5,47 ppm, foi calculada a razão manose:galactose (M:G) da galactomanana da D. regia.27 Preparação das micropartículas Para a preparação das micropartículas, 2,0 g de galactomanana liofilizada foi pesada e dissolvida em água destilada em agitação constante e aquecimento de 40 ºC por 24 h. Em seguida foi adicionado 200 mg de ácido ascórbico com agitação por 1 hora. Logo após, a solução foi atomizada em aparelho de spray dryer Buchi-290, usando temperatura de entrada de 120 ºC; temperatura de saída de 90 ºC; eficiência do exaustor de 90% e fluxo de bomba de 30%. As micropartículas foram coletadas, armazenadas e cobertas com papel alumínio, à temperatura ambiente para evitar uma possível oxidação sob ação da luz. Eficiência de encapsulamento Curva padrão A solução estoque do AA foi preparada em solução de metanol na concentração de 100 µg mL-1. Diferentes alíquotas desta solução foram transferidas para balões volumétricos de 10 mL cobertos com papel alumínio e o volume completado com metanol a fim de obter soluções de diferentes concentrações (2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22 µg mL-1). A absorbância das soluções foi determinada por espectrometria na região UV-Vis em 243 nm, usando o metanol como branco. A partir da curva de calibração foi obtida a equação 1 de regressão linear entre o valor da absorbância e a concentração do fármaco em µg ml-1. 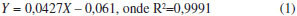 Quantificação de ácido ascórbico nas micropartículas por espectrofotometria UV-Vis. Foi pesado 2 mg de 10 amostras das micropartículas de galactomanana contendo AA, uma amostra padrão protegida do ambiente e as outras em diferentes condições ambientais [temperatura 25 ºC, 60 ºC e sobre ação da luz (λ)] por sete dias e dissolvidas em 10 mL de metanol para obter a solução de 200 µg mL-1 em 10 frascos diferentes, as quais foram analisadas em espectrômetro na região UV-Vis a 243 nm (n=3). A concentração do fármaco foi determinada usando a curva padrão, e a eficiência de encapsulação foi calculada de acordo com a equação 2 : 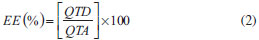 EE= Eficiência de Encapsulação; QTD= Quantidade de fármaco determinado no sistema polimérico; QTA= Quantidade de fármaco teoricamente adicionado no sistema polimérico. Para calcular o teor de fármaco encapsulado, foi utilizada a equação 3: 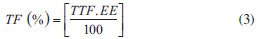 TF (%) = Teor de fármaco encapsulado; TTF (%) = Teor teórico de fármaco encapsulado; EE (%) = Eficiência de Encapsulação. Espectroscopia de absorção na região do infravermelho Os espectros de infravermelho (IV) foram obtidos utilizando um espectrofotômetro modelo Shimadzu FT-IR 8300. As amostras foram trituradas com brometo de potássio de grau espectroscópico (KBr) em pó para obtenção das pastilhas. A medição IV foi feita no intervalo de números de onda de 500-4000 cm - 1. Morfologia das micropartículas A morfologia das amostras de AA, galactomanana (G) e micropartículas de galactomanana contendo ácido ascórbico (GAA) foi mostrada nas micrografias produzidas pelo microscópio eletrônico de varredura, modelo Zeiss DSM 940A (Oberkochen, Alemanha) operando a 15 kV. As amostras foram preparadas em stubs, camada metálica de platina (60 nm de espessura) no evaporador EMS. Análises térmicas As propriedades térmicas das amostras foram determinadas usando Calorimetria Diferencial de Varredura (DSC) e análise termogravimétrica (TGA). As curvas de DSC foram realizadas em um equipamento Shimadzu modelo DSC-50, utilizando cadinho de platina e atmosfera de nitrogênio, com uma vazão de 50 mL min-1 no intervalo de temperatura de 25-500 ºC, a uma taxa de aquecimento de 10 ºC min-1. A massa das amostras foi de 5 mg. As curvas termogravimétricas das amostras foram obtidas por um equipamento Shimadzu modelo TGA-50, usando um cadinho de platina, atmosfera de ar sintético, com 50 mL min-1, entre as bandas de temperatura de 25 a 800 ºC, com taxas de aquecimento de 10 ºC min-1. A massa inicial das amostras analisadas foi de 10 mg. Difração de raios-X As amostras foram analisadas em difratômetro Panalytical, Xpert Pro MPD (Holanda) do departamento de Física da Universidade Federal do Ceará, utilizando radiação CoKα, uma tensão de 40 kV e uma corrente de 40 mA. A taxa de varredura empregada foi de 0,5º min-1 em região de 3º a 90º de ângulo de difração (2θ). As amostras foram trituradas para obtenção de um pó fino antes da análise. Atividade antioxidante frente ao radical DPPH A avaliação quantitativa da atividade antioxidante foi realizada seguindo metodologia usual de Yepez e colaboradores, com algumas modificações.28 Foram pesados 15 mg de AA não encapsulados nas seguintes condições: temperaturas de 25 ºC e 60 ºC, protegido da luz e exposto a luz por 7 dias. Da mesma forma, foram pesados 15 mg de micropartículas de galactomanana contendo ácido ascórbico (GAA) nas mesmas condições ambientais. Em seguida, as amostras foram diluídas em metanol para obtenção da concentração de 10 mg mL-1 e submetidas ao banho ultrassônico do Modelo USC 1400 para liberação do AA das micropartículas no meio e aumentar a solubilidade das micropartículas frente ao metanol, das quais foram retiradas alíquotas para obter as concentrações finais de 5, 1, 0,5, 0,1, 0,05, 0,01 e 0,005 mg mL-1. Foram preparados posteriormente 500 mL da solução metanólica do radical livre DPPH (0,026 mg mL-1). O AA foi utilizado como padrão, devido a sua comprovada ação antioxidante. Em cada tubo de ensaio foram colocados 3,9 mL de solução metanólica de DPPH de coloração púrpura e 0,1 mL da solução metanólica da amostra. O teste foi realizado em triplicata. Depois de 1 hora mediu-se a absorbância em espectrofotômetro, no comprimento de onda de 515 nm. Finalmente, foi calculado o percentual de inibição da amostra (PI%), por meio da equação 4, na qual AbsDPPH é a absorbância inicial da solução de DPPH e AbsAMOSTRA é a absorbância final. 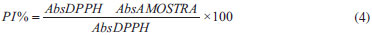 Com os resultados dos PI% obtidos na leitura da absorbância das diferentes concentrações de cada uma das amostras foi possível calcular o índice capaz de inibir 50% dos radicais livres (CI50) em relação ao teor de fármaco incorporado na matrix polimérica na proporção de 15 mg de cada amostra das micropartículas nas diferentes condições ambientais.29
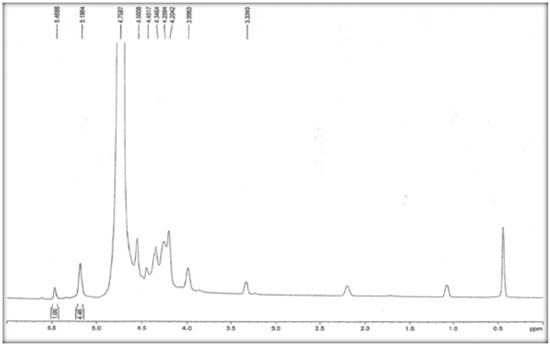
RESULTADOS E DISCUSSÃO Caracterização química da galactomanana A massa molar da galactomanana obtida das sementes da D. regia determinada pelo cromatógrafo de permeação em gel foi de 2,5 × 105 g mol-1, um valor próximo ao encontrado na literatura por Tamaki e colaboradores.30 A proporção de D-manose e D-galactose foi estimada em 4,46 : 1,00 pela medida direta das áreas relativas aos sinais de 1H (Man) e 1H (Gal) (Figura 3). Este resultado está de acordo com trabalhos anteriores para outras galactomananas, incluindo a goma da D. regia.30,31 Com base no assinalamento dos sinais de hidrogênios anoméricos atribuídos por Kapoor e colaboradores foram identificados os sinais de H-1 de β-D-galactose (5,47 ppm) e de α-D-manose (5,19 ppm).32
Eficiência de encapsulação A eficiência de encapsulação das micropartículas GAA que foi realizada na proporção 10:1 (galactomanana: ácido ascórbico), está descrita na Tabela 1.
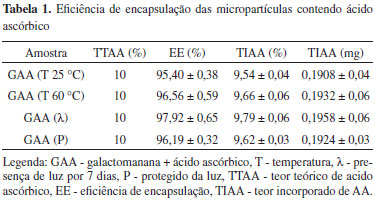
Estes resultados estão de acordo com os de Lee e colaboradores quando relataram a microencapsulação do AA com o poliacilglicerol mono estearato para evitar a oxidação do leite.33 O poliacilglicerol mono estearato foi utilizado como um material de revestimento para microencapsular o AA e complexo de ferro. A maior eficiência de microencapsulação (94,2%) foi encontrada com a relação 5:1 de poliacilglicerol mono esterato/AA. Os resultados mostrados na Tabela 1 também estão próximos aos de Stevanovic e colaboradores, quando relataram o processo de obtenção de nanopartículas de AA com o poli (D,L-láctideo-co-glicolídeo) (DLPLG) em que sua maior eficiência (98,2%) de microencapsulação foi na proporção 85/15% de DLPLG/AA.34 Os resultados também mostram que as diferentes condições ambientais interferiram pouco na eficiência de encapsulação do AA. Para confirmar os resultados obtidos da Tabela 1 foi realizado um tratamento estatístico por meio do teste Q para o intervalo de 95% de confiança, no qual as médias da eficiência de encapsulação podem ser consideradas estatisticamente verdadeiras. Espectroscopia de absorção na região do infravermelho (IV) A Figura 4 mostra o espectro do IV das amostras de AA, galactomanana (G) e das micropartículas GAA analisadas. O espectro de IV do AA mostra as bandas principais proporcionadas pelos grupos funcionais da molécula, tais como: estiramentos C=O lactona (1760 cm-1), C=C (1668 cm-1), OH (3217, 3309, 3404, 3533 cm-1), -CH3, -CH2- ou grupos-CH (2750- 2981 cm-1), C-O (1024 cm-1). O espectro de IV da amostra G mostra bandas de absorção características com picos a 816 e 873 cm-1, que estão relacionados com a presença de ligações glicosídicas, atribuída à α-D-galactopiranose e β-D-manopiranose, respectivamente, a absorção de 1154 cm-1 relacionada com a vibração de estiramento C-O devido ao anel de piranose, uma grande banda em torno de 3438 cm-1 atribuída ao estiramento OH e uma absorção em 2913 cm-1 atribuída ao estiramento C-H. A comparação dos espectros obtidos para o AA, G e as micropartículas GAA com os espectros de IV característicos para o ácido ascórbico e galactomanana dada na literatura confirma que as micropartículas obtidas são compostos de galactomanana e ácido ascórbico.32,35-38 As amostras G e GAA apresentaram uma grande semelhança nos seus espectros de IV, o que mostra que as absorbâncias específicas dos grupos funcionais da G na superfície das micropartículas têm quase as mesmas características químicas da G pura. O estudo sugere que as interações moleculares que podem alterar a estrutura química da G ou AA não ocorreram. Por isso, presume-se que não houve interação química entre os grupos funcionais da galactomanana e o ácido ascórbico.
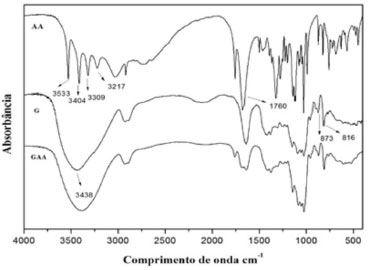 Figura 4. Espectro no IV do ácido L-ascórbico (AA), galactomanana (G) e as micropartículas de galactomanana e AA (GAA)
Microscopia eletrônica de varredura (MEV) O AA, a galactomanana (G) e as micropartículas GAA foram analisadas por microscopia eletrônica de varredura (MEV) (Figura 5), pela qual foram observadas algumas características morfológicas. A imagem MEV do AA mostra a presença de cristais de forma cúbica. A micrografia da G revela uma aparência fibrosa em que as fibras são dispostas de forma aleatória, com variação de tamanho e espessura. A figura da amostra GAA apresenta uma imagem com micropartículas na forma esférica e com um tamanho médio de 1,39 ± 0,77 µm. Por meio da analise das imagens foi possível observar a ausência dos cristais de AA evidenciados na Figura 5 (GAA), sugerindo um eficiente encapsulamento do AA.
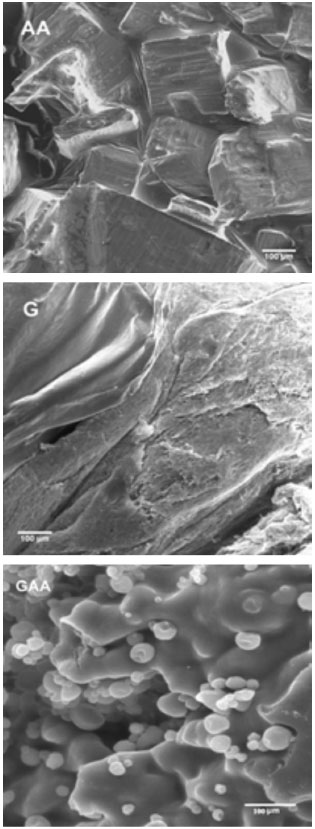 Figura 5. Micrografias de microscopia eletrônica de varredura do AA, da galactomanana (G) e das micropartículas (GAA)
Análises térmicas As análises de DSC e TGA foram realizadas a fim de compreender o comportamento térmico e análise das micropartículas. A Figura 6 mostra os termogramas de DSC do AA, galactomanana (G) e micropartículas de GAA. O DSC foi usado para estudar as transições térmicas que ocorrem sob uma atmosfera inerte. O termograma DSC do AA mostrou um pico endotérmico de 194,38 ºC na temperatura correspondente ao seu ponto de fusão, o que explica a sua cristalinidade.39 Já o termograma DSC da G apresenta picos típicos de polissacarídeo natural40-42 com eventos endotérmicos na faixa de temperatura entre 80,88 ºC e 155,30 ºC, aproximadamente, o que pode ser explicado pela evaporação da água. Resultados semelhantes foram observados em outras galactomananas.35,41
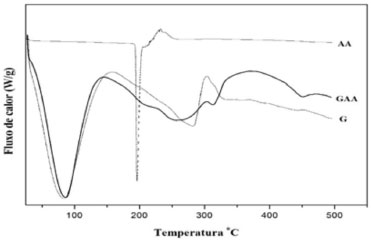 Figura 6. Calorimetria Diferencial de Varredura (DSC) do AA, da galactomanana (G) a e das micropartículas (GAA)
O segundo evento foi atribuído a um pico endotérmico entre 283,37 ºC e 302,47 ºC, associada a decomposição térmica do material. O pico endotérmico forte do AA, que é interpretado como uma temperatura de fusão de uma região cristalina, desapareceu na curva DSC das micropartículas de GAA. Desta forma, a mudança de estado físico do AA sugere que ele tenha perdido a sua estrutura cristalina original.43 A ausência do pico de fusão do AA indica também que o AA pode ter sido completamente encapsulado. A temperatura de transição vítrea (Tg) é um parâmetro relacionado com a mobilidade do sistema e é definido como a temperatura abaixo da qual um polímero amorfo se torna duro e frágil (estado vítreo), e acima da qual o mesmo polímero é macio (estado "borrachoso"), de acordo com Roos & Karel.44 As análises de TGA foram realizadas a fim de compreender o comportamento térmico da galactomanana e como ela pode ser influenciada pela presença do AA (Figura 1S, material suplementar). Foram registrados dois eventos de perda de massa para G. A primeira ocorre próximo de 29,32 ºC e pode ser atribuída à perda de água adsorvida e estrutural. O segundo evento de perda de massa em 202,27 ºC pode ser associado à decomposição térmica de polissacarídeos. Estes valores são próximos aos relatados na literatura para outras fontes de galactomanana.41,42,45,46 Comparando as curvas obtidas para G e GAA observa-se que não foram detectadas mudanças significativas no valor de Tg (191 ºC a 330 ºC) correspondente a galactomanana após a incorporação do AA. Difração de raios-X A difração de raios-X (DRX) é uma técnica que pode ser utilizada para confirmar a eficiência de encapsulação de fármacos em micropartículas, em que a ausência dos picos de difração do fármaco cristalino nas micropartículas indica a eficiência de encapsulação, devido à dispersão formada na matriz polimérica.47 O estado cristalino do AA foi evidenciado no difratograma de DRX (Figura 7); o perfil exibiu vários picos bem definidos em 2 , dentre eles, os principais são: 10.17, 17.58, 25.29 e 54.36, que são similares aos relatados na literatura por Chang e colaboradores.48
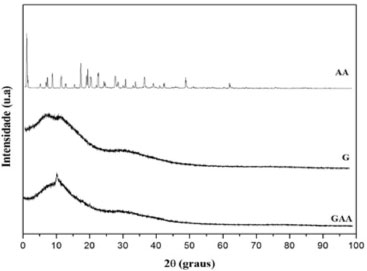 Figura 7. Difração de Raios-X para o AA, a galactomanana (G) e as micropartículas (GAA)
O difratograma das micropartículas contendo o AA (GAA) apresentou picos semelhantes do polímero puro (G), indicando que o fármaco pode estar encapsulado no sistema, na forma amorfa. Estes resultados estão de acordo com outros relatos de estudos de encapsulação.6,43,49-52 A análise DRX do AA encapsulado pela galactomanana não mostrou a presença do AA cristalino, tal como já foi confirmado por análise de DSC e MEV. Atividade antioxidante frente ao radical DPPH A Tabela 2 mostra os resultados obtidos de atividade antioxidante do AA e das micropartículas de AA em galactomanana (GAA) em diferentes condições ambientais em relação ao teor de fármaco encapsulado em cada amostra. A atividade antioxidante do AA não encapsulado protegido da luz (P) está de acordo com aquelas descritas por Ahmed e colaboradores53 e Li e colaboradores.54
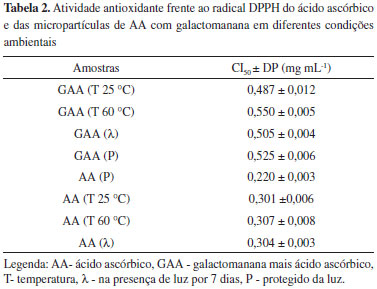
Por meio da analise dos resultados obtidos na Tabela 2, observou-se que houve uma redução da atividade antioxidante do AA nas diferentes condições ambientais testadas, quando comparado com o AA protegido de interferências ambientais, demonstrando sua instabilidade frente às diferentes condições aplicadas.2 As amostras de AA encapsulado na galactomanana tiveram a sua capacidade antioxidante reduzida quando comparadas com o AA não encapsulado, entretanto, observa-se que apesar da redução nos valores de CI50 nas diferentes condições ambientais é notório que a galactomanana protegeu o AA e que as micropartículas apresentam uma boa atividade antioxidante devido a sua liberação durante o processo da solubilidade das amostras. Esses resultados sugerem que a encapsulação pode ser uma estratégia de proteção para substâncias cujas estabilidades são afetadas por fatores ambientais adversos como presença de luz e temperatura, assim como um sistema de liberação do fármaco para redução de perdas das suas propriedades funcionais.
CONCLUSÃO A técnica do spray drying, utilizada neste trabalho, possibilitou a obtenção de micropartículas de galactomanana com alta eficiência de encapsulação do ácido ascórbico (AA). Esse método de microencapsulação assume um papel importante na superação da sua instabilidade química. Os resultados, tanto das características fisico-químicas como da atividade antioxidante do AA microencapsulado com a galactomanana obtida da espécie D. regia estimulam estudos posteriores com maior intervalo de tempo que possam caracterizar com mais eficácia a maior estabilidade das micropartículas, pois apresentam potencial para serem utilizadas em diferentes formas de produtos, ou seja, na forma de comprimidos, gel, sprays, etc., na cosmetologia, indústrias de alimentos como agente protetor da oxidação dos alimentos e como antioxidante na dieta humana.
MATERIAL SUPLEMENTAR O material suplementar refere-se às análises de TGA que foram realizadas a fim de compreender o comportamento térmico da galactomanana e como ela pode ser influenciada pela presença do AA e está disponível em http://quimicanova.sbq.org.br, na forma de arquivo PDF, com acesso livre.
REFERÊNCIAS 1. Reavley, N.; Vitamins etc., Bookman Press: Melbourne, 1998. 2. Uddin, M. S.; Hawlader, M. N. A.; Zhu, H. J.; J. Microencapsulation 2001, 18, 199. DOI: http://dx.doi.org/10.1080/02652040010000352 3. Pierucci, A. P.; Andrade, L. R.; Baptista, E. B.; Volpato, N. M.; Rocha-Leao, M. H.; J. Microencapsulation 2006, 23, 654. DOI: http://dx.doi.org/10.1080/02652040600776523 4. Vila Jato, J. L.; Tecnologia farmacéutica: Aspectos fundamentales de los sistemas farmacêuticos y operaciones básicas, Sintesis Editorial: Madri, 1999. 5. Santos, A. B.; Favaro-Trindade, C. S.; Grosso, C. R. F.; Cienc. Tecnol. Aliment. 2005, 25, 322. DOI: http://dx.doi.org/10.1590/S0101-20612005000200024 6. Sansone, F.; Rossi, A.; Del Gaudio, P.; De Simone, F.; Aquino, R. P.; Lauro, M. R.; AAPS PharmSciTech 2009, 10, 391. DOI: http://dx.doi.org/10.1208/s12249-009-9219-0 PMID: 19381835 7. Sáenz, C.; Tapia, S.; Chávez, J.; Robert, P.; Food Chem. 2009, 114, 616. DOI: http://dx.doi.org/10.1016/j.foodchem.2008.09.095 8. Dian, N. L. H. M.; Sudin, N.; Yusoff, M. S. A.; J. Sci. Food Agric. 1996, 70, 422. DOI: http://dx.doi.org/10.1002/(SICI)1097-0010(199604)70:4<422::AID-JSFA514>3.0.CO;2-5 9. Yoshii, H.; Soottitantawat, A.; Liu, X. D.; Atarashi, T.; Furuta, T.; Aishima, S.; Ohgawara, M.; Linko, P.; Innovative Food Sci. Emerging Technol. 2001 , 2, 55. DOI: http://dx.doi.org/10.1016/S1466-8564(01)00019-4 10. Gharsallaoui, A.; Roudaut,G.; Chambin, O.; Voilley, A.; Saurel, R.; Food Res. Int. 2007, 40, 1107. DOI: http://dx.doi.org/10.1016/j.foodres.2007.07.004 11. Palma-Rodriguez, H. M.; Agama-Acevedo, E.; Gonzalez-Soto, R. A.; Vernon-Carter, J. E.; Alvarez-Ramirez, J.; Bello-Perez, L. A.; Starch-Stärke (2013) doi: 10.1002/star.201200200 DOI: http://dx.doi.org/10.1002/star.201200200 12. Finotelli, P. V.; Rocha-Leao, M. H. M.; 2nd Mercosur Congress on Chemical Engineering and 4th Mercosur Congress on Process Systems Engineering, Rio de Janeiro, Brasil, 2005. 13. Bharadwaj, T. R.; Kanwar, M.; Lal, R.; Gupta, A.; Drug. Dev. Ind. Pharm. 2000, 26, 1025. DOI: http://dx.doi.org/10.1081/DDC-100100266 14. Satturwar, P. M.; Fulzele, S. V.; Dorle, A. K.; AAPS PharmSciTech 2003, 4, 1. DOI: http://dx.doi.org/10.1208/pt040329 15. Morkhade, D. M.; Joshi, S. B.; Indian J. Pharm. Sci. 2007, 69, 263. DOI: http://dx.doi.org/10.4103/0250-474X.33154 16. Kapoor, V. P. A.; Phytochemistry 1972, 11, 1129. DOI: http://dx.doi.org/10.1016/S0031-9422(00)88465-4 17. Grenha, A.; J. Pharm. Bioallied. Sci. 2012, 4, 175. DOI: http://dx.doi.org/10.4103/0975-7406.99013 18. Betancur, A. D.; Pacheco, A. J.; Castellanos, R. A.; Chel, G. L.; Innovative Food Sci. Emerging Technol. 2011, 12, 67. DOI: http://dx.doi.org/10.1016/j.ifset.2010.11.002 19. Dionísio, M.; Grenha, A.; J. Pharm. BioAllied Sci. 2012, 4, 175. DOI: http://dx.doi.org/10.4103/0975-7406.99013 PMID: 22923958 20. Ansari, S. A.; Matricardi, P.; Cencetti, C.; Di Meo, C.; Carafa, M.; Mazzuca, C.; Coviello, T.; BioMed Res. Int. 2013, 2013, 1. DOI: http://dx.doi.org/10.1155/2013/725410 21. Koop, H. S.; Freitas, R. A. D.; Souza, M. M. D.; Savi-Jr, R.; Silveira, J. L. M.; Carbohydr. Polym. (2014) doi: 10.1016/j.carbpol.2014.07.043. DOI: http://dx.doi.org/10.1016/j.carbpol.2014.07.043 PMID: 25458294 22. Maiti, S.; Chowdhury, M.; Chakraborty, A.; Ray, S.; Sa, B.; J. Sci. Ind. Res. 2014, 73, 21. 23. Davison, E.; Aridus 2003, 16, 1. 24. Vieira, I. G. P.; Mendes, F. N. P.; Gallao, M. I.; Brito, E. S.; Food Chem. 2007, 101, 70. DOI: http://dx.doi.org/10.1016/j.foodchem.2005.11.052 25. Egorov, A. V.; Mestechkina, N. M.; Shcherbukhin, V. D.; Appl. Biochem. Microbiol. 2003, 39, 398. DOI: http://dx.doi.org/10.1023/A:1021718614804 26. Egorov, A. V., Mestechkina, N. M., Shcherbukhin, V. D.; Appl. Biochem. Microbiol. 2004, 40, 314. DOI: http://dx.doi.org/10.1023/B:ABIM.0000025959.89870.c7 27. Buriti, F. C. A.; Santos, K. M.O.; Sombra, V. G.; Maciel, J. S.; Sá, D. M. A. T.; Sales, H. O.; Oliveira, G. O.; de Paula, R. C. M.; Feitosa, J. P. A.; Moreira, A. C. O. M.; Moreira, R. A.; Egito, A. S.; Food Hydrocolloids 2014, 35, 512. DOI: http://dx.doi.org/10.1016/j.foodhyd.2013.07.015 28. Yepez, B.; Espinosa, M.; López, S.; Bolaños, G.; Fluid Phase Equilib. 2002, 194, 879. DOI: http://dx.doi.org/10.1016/S0378-3812(01)00707-5 29. Lee, S. E.; Hwang, H. J.; Ha, J. S.; Jeong, H. S.; Kim, J. H.; Life Sci. 2003, 73, 167. DOI: http://dx.doi.org/10.1016/S0024-3205(03)00418-1 PMID: 12738032 30. Tamaki, Y.; Teruya, T.; Tako, M.; Biosci., Biotechnol., Biochem. 2010, 74, 1110. DOI: http://dx.doi.org/10.1271/bbb.90935 31. Bento, J. F.; Mazzaro, I.; Silva, L. M. A.; Moreira, R. A.; Ferreira, M. L. C.; Reicher, F.; Petkowicz, C. L. O.; Carbohydr. Polym. 2013, 92, 192. DOI: http://dx.doi.org/10.1016/j.carbpol.2012.08.113 PMID: 23218282 32. Kapoor, V. P.; Taravel, F. R.; Joseleau, J. P.; Milas, M.; Chanzy, H.; Rinaudo, M.; Carbohydr. Res. 1998, 306, 231. DOI: http://dx.doi.org/10.1016/S0008-6215(97)00241-3 PMID: 9691448 33. Lee, J-B.; Ahn; J.; Lee, J.; Kwak, H. S.; Biosci., Biotechnol., Biochem. 2004, 68, 495. DOI: http://dx.doi.org/10.1271/bbb.68.495 34. Stevanovic, M.; Savic, J.; Jordovic, B.; Uskokovic, D.; Colloids Surf. 2007, 59, 215. DOI: http://dx.doi.org/10.1016/j.colsurfb.2007.05.011 35. Cerqueira, M. A.; Souza, B. W. S.; Simoes, J.; Teixeira, J. A.; Domingues, M. R. M. D.; Coimbra, M. A.; Vicente, A. A.; Carbohydr. Polym. 2011, 83, 179. DOI: http://dx.doi.org/10.1016/j.carbpol.2010.07.036 36. Yuen, S. N.; Choi, S. M.; Phillips, D. L.; Ma, C. Y.; Food Chem. 2009, 114, 1091. DOI: http://dx.doi.org/10.1016/j.foodchem.2008.10.053 37. Dinda, E.; Si, S.; Kotal, A.; Mandal, T. K.; Chem. Eur. J. 2008, 14, 5528. DOI: http://dx.doi.org/10.1002/chem.200800006 38. Stevanovic, M.; Bracko, I.; Milenkovic, M.; Filipovic, N.; Nunic, J.; Filipic, M.; Uskokovic, D. P.; Acta Biomater. 2014, 10, 151. DOI: http://dx.doi.org/10.1016/j.actbio.2013.08.030 PMID: 23988864 39. Garnero, C.; Longhi, M.; J. Pharm. Biomed. Anal. 2007, 45, 536. DOI: http://dx.doi.org/10.1016/j.jpba.2007.07.030 PMID: 17851014 40. Zohuriaan, M. J.; Shokrolahi, F.; Polym. Test. 2004, 23, 575. DOI: http://dx.doi.org/10.1016/j.polymertesting.2003.11.001 41. Vendruscolo, C. W.; Ferrero, C.; Pineda, E. A. G.; Silveira, J. L. M.; Freitas, R. A.; Jiménez-Castellanos, M. R.; Bresolin, T. M. B.; Carbohydr. Polym. 2009, 76, 86. DOI: http://dx.doi.org/10.1016/j.carbpol.2008.09.028 42. Chaires, M. L.; Salazar, M. J. A.; Ramos, R. E. G.; Eur. Food Res. Technol. 2008, 227, 1669. DOI: http://dx.doi.org/10.1007/s00217-008-0892-0 43. Neo, Y. P.; Ray, S.; Jin, J.; Nikolaidis, M. G.; Nieuwoudt, M. K.; Liu, D.; Quek, S. Y.; Food Chem. 2013, 136, 1013. DOI: http://dx.doi.org/10.1016/j.foodchem.2012.09.010 PMID: 23122157 44. Roos, Y.; Karel, M.; J.Food Sci. 1991, 56, 38. DOI: http://dx.doi.org/10.1111/j.1365-2621.1991.tb07970.x 45. Varma, A. J.; Kokane, S. P.; Pathak, G.; Pradhan, S. D.; Carbohydr. Polym. 1997, 32, 111. DOI: http://dx.doi.org/10.1016/S0144-8617(96)00155-5 46. Yi, J. Z.; Zhang, L. M.; J. Appl. Polym. Sci. 2007, 103, 3553. DOI: http://dx.doi.org/10.1002/app.24566 47. Asada, N.; Namba, M.; Kodama, T.; Kyogoku, Y.; Arch. Insect Biochem. Physiol. 2004, 56, 1. DOI: http://dx.doi.org/10.1002/arch.10137 PMID: 15101061 48. Chang, D.; Abbas, S.; Hayat, K.; Xia, S.; Zhang, X.; Xie, M.; Kim, J. M.; Int. J. Food Sci. Technol. 2010, 45, 1895. DOI: http://dx.doi.org/10.1111/j.1365-2621.2010.02348.x 49. Mello, V. A.;Ricci-Júnior, E.; Quim. Nova 2011, 34, 933. DOI: http://dx.doi.org/10.1590/S0100-40422011000600004 50. Li, X.; Chang, S.; Du, G.; Li, Y.; Gong, J.; Yang, M.; Wei, Z.; Int. J. Pharm. 2012, 433, 79. DOI: http://dx.doi.org/10.1016/j.ijpharm.2012.05.009 PMID: 22583850 51. Pralhad, T.; Rajendrakumar, K.; J. Pharm. Biomed. Anal. 2004, 34, 333. DOI: http://dx.doi.org/10.1016/S0731-7085(03)00529-6 PMID: 15013147 52. Xie, C.; Li, X.; Luo, X.; Yang, Y.; Cui, W.; Zou, J.; Zhou, S.; Int. J. Appl. Pharm. 2010, 391, 55. DOI: http://dx.doi.org/10.1016/j.ijpharm.2010.02.016 53. Ahmed, M.; Akter, M. S.; Lee, J. C.; Eun, J. B.; Food Sci. Technol. 2010, 43, 1307. 54. Li, F.; Chen, B.; Ping, Z.; Jia, X.; Guo, X.; Xiao, L.; Liu, L.; Macromol. Biosci. 2014, 14, 280. DOI: http://dx.doi.org/10.1002/mabi.201300282 PMID: 23966285 |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access