Nota Técnica
|
|
| Otimização da extração sólido-líquido com partição em baixa temperatura para determinação de carbofurano em Cucurbita pepo L (“abobrinha”) por cromatografia líquida de alta eficiência Optimization of solid-liquid extraction with low temperature partition for determination of carbofuran in Cucurbita pepo L (“zucchini”) by high performance liquid chromatography |
|
Rogério P. RodriguesI; Waldiclécio R. FariasI; Simone M. GoulartI,*; Adilson C. GoulartII; Joao Paulo V. SantosI; Maria Eliana L. R. de QueirozIII
I Departamento de Química, Instituto Federal de Goiás, Av. Furnas, 55, 75524-010 Itumbiara - GO, Brasil Recebido em 28/06/2017 *e-mail: simone.goulart@ifg.edu.br According to results of the Program of Analysis of Pesticide Residues in Foods of the National Agency of Sanitary in Brazil (2013 to 2015) the zucchini, Cucurbita pepo L is one of the non-hardy vegetables, that presented higher contamination index by pesticides residues. One of these agrochemicals is carbofuran, which although not authorized for this crop, is commonly and illegally used for whitefly control. The objective of this study was to optimize the solid-liquid extraction method with low temperature partitioning (SLE/LTP) for the determination of carbofuran residues in zucchini by high performance liquid chromatography with ultraviolet detector (HPLC-UV). The optimization was performed with a complete factorial design, 23 to evaluate the simultaneous performance of three factors in two levels, in triplicate. The optimized SLE/LTP-HPLC/UV method showed to be selective, simple and efficient, consuming a small amount of sample and solvent extractor. The average recovery percentage was 75.88%. Samples of zucchini purchased in the Itumbiara-GO trade, Brazil, and submitted to the optimized method did not present carbofuran residues. INTRODUÇAO Durante as últimas décadas, o monitoramento de resíduos de agrotóxicos em alimentos no Brasil foi marcado por uma série de esforços isolados de órgaos estaduais de saúde, agricultura e instituiçoes de pesquisas. Esse fato sempre impediu que o país tivesse uma noçao clara dos níveis de agrotóxicos encontrados em seus produtos agrícolas. Em 2001, com o intuito de resolver esse tipo de problema, foi criado pela Agência Nacional de Vigilância Sanitária (ANVISA) o Programa de Análises de Resíduos de Agrotóxicos em Alimentos (PARA), que busca avaliar os níveis de resíduos de agrotóxicos em alimentos de origem vegetal. De acordo com o relatório complementar de pesquisas desenvolvidas pelo PARA no ano de 2012, divulgado em 2014, foram analisadas 1.397 amostras, sendo que 347 (25%) foram consideradas insatisfatórias, com pelo menos um dos fatores indesejáveis: Presença de agrotóxicos acima do Limite Máximo de Resíduo (LMR); Constataçao de agrotóxicos nao autorizados para determinadas culturas, ou as duas irregularidades. Das 229 amostras de abobrinha analisadas, 48% (110 amostras) foram consideradas insatisfatórias, em decorrência, exclusivamente, do uso de carbofurano, agrotóxico nao registrado para a cultura de abobrinha.1 No ano de 2016, foram divulgadas as análises dos anos de 2013 a 2015, sendo constatado que, das 216 amostras analisadas, em 168 foi identificada a presença de resíduos de agrotóxicos nao autorizados para o uso na cultura de abobrinha, sendo encontrado dentre outros agrotóxicos o carbofurano.2 A mosca-branca (Bemisia spp) é uma praga que ataca as culturas de abobrinhas. De acordo com Schmalstig e Mcauslane,3 a praga prejudica a espécie por meio de sua alimentaçao, induzindo o prateamento das folhas. Summers e Stapleton4 ressaltam que essa praga ataca as culturas das espécies de C. pepo, C. moschata e C. máxima. Os carbamatos sao muito eficientes para controle dessa praga em outras culturas, tais como a cultura do feijao, entretanto, nao sao autorizados para uso em culturas de abobrinha, e o uso ilegal do carbofurano nessa cultura é devido a essa eficiência no combate dessa praga.5 O carbofurano (2,3-dihidro-2,2dimethylbenzenofuran-7-ylmethylcarbamate) (Figura 1) pertence à classe química dos carbamatos, classificado pela Agência Nacional de Vigilância Sanitária (ANVISA) como inseticida, cupinicida, acaricida e nematicida. É classificado toxicologicamente como extremamente tóxico. É empregado no solo, principalmente em culturas de algodao, amendoim, arroz, banana, batata, café, cana-de-açúcar, cenoura, feijao, fumo, milho, repolho, tomate e trigo e nas sementes de algodao e arroz.6
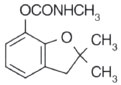 Figura 1. Estrutura química do carbofurano
Pela alta toxicidade dos carbamatos, muitos desses produtos químicos foram proibidos em diversos países, como na Uniao Europeia, Estados Unidos e Canadá.7 No ano de 2015, a ANVISA abriu uma consulta pública para Reavaliar a Toxicidade do Ingrediente Ativo de Agrotóxico Carbofurano no Brasil, resultando em aprovaçao da proposta por 81,67% das respostas.8 O método QuEChERS é o recomendado pela ANVISA para determinaçao de carbofurano em abobrinha por cromatografia.9 Embora seja um método multirresíduo, o QuEChERS é um método bastante laborioso, se comparado a outros métodos de extraçao. Outro método que foi desenvolvido e que tem sido utilizado com sucesso para determinaçao de agrotóxicos em alimentos e demais matrizes por cromatografia é a Extraçao Sólido-Líquido com Partiçao em Baixa Temperatura (ESL/PBT). Este método já foi aplicado em várias matrizes como abacaxi,10 alface,11 alho,12 batata,13,14 cenoura,15 manteiga,16 milho,17 morango,18 solos19 e tomates.20 De acordo com Goulart et al.,21 a técnica apresenta vantagens em relaçao às demais técnicas de extraçao, como praticidade, número reduzido de etapas e baixo consumo de solvente orgânicos. O objetivo deste trabalho foi otimizar o método ESL/PBT para determinaçao de carbofurano em abobrinha por cromatografia líquida de alta eficiência com detector ultravioleta (HPLC-UV) e verificar a presença de carbofurano em amostras de abobrinhas comercializadas no município de Itumbiara - Goiás, Brasil.
PARTE EXPERIMENTAL A otimizaçao do ensaio experimental consistiu na utilizaçao da técnica ESL-PBT, seguida de análise por HPLC-UV conforme metodologia proposta por Goulart et al.21 Reagentes e soluçoes Os reagentes e solventes utilizados foram acetato de etila (99,5% v/v - Mallinckrodt/HPLC) e acetonitrila (99,5% v/v - J.T. Baker/HPLC) e cloreto de sódio (99,5% m/m - Synth). A soluçao padrao estoque na concentraçao de 100,0 mg L -1 de carbofurano (99,9% m/m - Sigma Aldrich) foi preparada em acetonitrila e armazenada em freezer. A partir de diluiçao da soluçao estoque, foi preparada uma soluçao padrao de trabalho contendo o carbofurano na concentraçao de 5,0 mg L -1. Obtençao de amostras Para a otimizaçao da técnica de extraçao sólido-líquido com partiçao em baixa temperatura (ESL/PBT) e análise por HPLC-UV foram utilizadas abobrinhas cultivadas sem adiçao de agrotóxicos (Branco) na zona rural do município de Itumbiara-GO, Brasil. Após coleta, as amostras de abobrinha foram refrigeradas e analisadas no Laboratório de Análise Química Instrumental do Instituto Federal de Goiás - Campus Itumbiara (IFG - Itumbiara), onde foram preparadas. Otimizaçao da técnica ESL/PBT Amostras de abobrinhas isentas de agrotóxicos foram picadas e trituradas em mixer até total homogeneizaçao. Em seguida, 1,0000 g de polpa da amostra foram colocadas em frascos de vidro transparente (22 mL) e fortificadas com 2 µL de soluçao-padrao de carbofurano a 5,0 mg L -1 e homogeneizadas. As amostras fortificadas (na presença e ausência de adiçao de sal) foram acrescentadas água (2 mL) e solventes extrator na proporçao (1:2). O sistema foi agitado em vórtex e as amostras foram levadas ao freezer a -20 ºC por no mínimo 3 horas para separaçao das fases. Após este intervalo, foi retirado 1 mL da fase orgânica e colocado em vial para análise cromatográfica. Para a otimizaçao do método foi empregado um planejamento fatorial completo, 23, para avaliaçao do comportamento simultâneo de três fatores: tempo de agitaçao em vórtex (30 ou 60 s), adiçao de sal (sem ou com 1,5% (m/m) de NaCl) e solvente extrator (acetonitrila- ACN ou acetonitrila:acetato de etila - ACN/ACE 81,25:18,75). Os três fatores foram analisados em dois níveis e as análises foram realizadas em triplicatas. As melhores condiçoes do planejamento foram avaliadas em funçao das porcentagens de extraçao obtidas em cada ensaio. A precisao do método otimizado foi determinada por meio do coeficiente de variaçao (CV) para nove extraçoes idênticas de brancos fortificados a 5 mg L -1. Esses dados foram tratados empregando o programa Excel r. Os dados do planejamento sao apresentados na Tabela 1.
Condiçoes cromatográficas As seguintes condiçoes cromatográficas foram ajustadas para determinaçao de carbofurano por HPLC: Coluna Kinetex 5 µm EVO C 18 - 150 X 4,6 mm; fase móvel (modo isocrático): acetonitrila:água purificada 35:65 v:v; vazao da fase móvel: 0,8 mL min -1; temperatura da coluna: 35 ºC; volume de injeçao 20µL e pressao: 67 kgf. Detector ultravioleta (UV) (λ: 195 nm). A quantificaçao do carbofurano nas amostras de abobrinha foi realizada pelo método da padronizaçao externa utilizando padrao analítico de carbofurano no extrato do branco da matriz. A partir de diluiçoes da soluçao de carbofurano a 5 mg L -1 foram obtidas as soluçoes padrao nas concentraçoes de 0,1 mg L -1, 0,5 mg L -1, 1 mg L -1, 2 mg L -1, 3 mg L -1, 4 mg L -1 e 5 mg L -1. Limite de detecçao e limite de quantificaçao Os limites de detecçao (LOD) e os limites de quantificaçao (LOQ) do método proposto foram determinados pela fortificaçao dos extratos de abobrinha nas concentraçoes mais baixas aceitáveis. LOD e LOQ foram considerados como três e dez vezes, respectivamente, o sinal de ruído de linha de base obtido para as amostras livres de carbofurano (em branco). Os extratos de abobrinha foram obtidos submetendo-se o branco (abobrinha livre de carbofurano) ao método ESL-PBT otimizado nesse trabalho. Foram realizadas várias injeçoes dos extratos, fortificados em concentraçoes decrescentes.22 Aplicaçao do método otimizado em amostras de abobrinha no comércio Após a otimizaçao do método, este foi aplicado em 5 (cinco) amostras de abobrinha coletadas em cinco estabelecimentos comerciais da cidade de Itumbiara-GO, Brasil. As amostras foram refrigeradas e analisadas após 24 h.
RESULTADOS E DISCUSSAO Curva analítica Foram realizadas injeçoes de soluçoes padrao de carbofurano no extrato do branco da matriz abobrinha, com o objetivo de verificar a resposta do detector frente às diferentes concentraçoes do analito (0,1 mg L -1 a 5,0 mg L -1). A partir dos dados obtidos foi construída a curva analítica y = 308605x-10475 com coeficiente de correlaçao igual a 0,9975. Como a mediçao nos ensaios químicos é indireta, a transformaçao da medida do equipamento na unidade de interesse do mensurando é feita utilizando uma comparaçao direta de uma série de soluçoes padrao de concentraçoes conhecidas contra os valores medidos, seguida de transformaçoes matemáticas até a obtençao do resultado final.23 Observa-se que a equaçao da reta apresentou coeficiente de correlaçao igual a 0,9975, considerada uma Correlaçao Altíssima (0,91 < r < 0,99) de acordo com Brito et al.,24 que também afirmam que este parâmetro se refere à capacidade do método de gerar resultados linearmente proporcionais à concentraçao do analito, enquadrados em faixa analítica especificada. Análise cromatográfica As condiçoes cromatográficas otimizadas para análise de carbofurano em abobrinha possibilitaram a identificaçao do pesticida no tempo de retençao de 5,34 min, conforme apresentado no cromatograma da Figura 2.
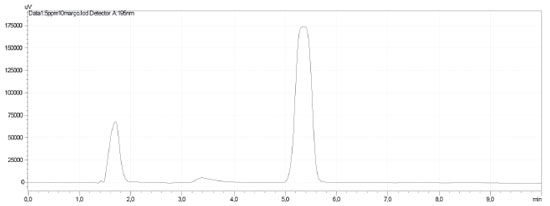 Figura 2. Cromatograma de uma soluçao padrao a 5,0 mg L -1 de carbofuran (tR= 5,34 min) em acetonitrila.
Otimizaçao da técnica ESL/PBT No processo de otimizaçao do método foi empregado um planejamento fatorial completo, 23, para avaliaçao do comportamento simultâneo de três fatores: tempo de agitaçao em vórtex (30 ou 60 s), adiçao de sal (sem ou com 1,5% (m/m) de NaCl) e solvente extrator (acetonitrila- ACN ou acetonitrila:acetato de etila - ACN/ACE 81,25:18,75). Os resultados das combinaçoes dos fatores foram registrados para análise e interpretaçao em planilhas eletrônicas, conforme Teófilo e Ferreira.25 A escolha das melhores condiçoes para aplicaçao da técnica ESL/PBT favorece melhores resultados, levando a maior frequência analítica (agilidade nas análises por unidade de tempo) e menor custo. Os resultados da análise estatística sao apresentados na Tabela 2.
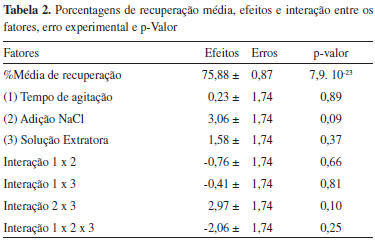
Para verificaçao da significância dos dados apresentados na Tabela 2, foi aplicado o teste t de t-student ao nível de 95% de confiança e 5% significância. Para 8 graus de liberdade com 95% de probabilidade o valor t correspondente é 2,306, dessa forma serao significativos os fatores com valores excedentes a (0 + 2,306 x 1,74) = 4,01, análogo a dizer que serao significativos todos os efeitos cujo valor de p < 0,05.25 Verifica-se na Tabela 2 que estatisticamente, nos níveis estabelecidos, os fatores nao sao significativos ao ponto de interferir no aumento ou diminuiçao das porcentagens de recuperaçao do carbofurano na matriz abobrinha. Entretanto, a fim de selecionar o melhor ensaio para determinaçao e quantificaçao de carbofurano na matriz investigada, é de fundamental importância entender a atuaçao de cada fator no processo. Observando-se o processo de agitaçao das amostras, foi verificado que elevando o tempo de agitaçao de 30 s para 60 s, o percentual de recuperaçao aumentou em média 0,235%. Esta etapa é de fundamental importância no processo analítico por representar o momento de maior interaçao entre o solvente extrator e o analito, proporcionando melhor precisao, praticidade, frequência analítica e alto rendimento.26 Por esse motivo foi escolhido o tempo de agitaçao de 60 s. A adiçao de NaCl ao sistema foi o fator que mais influenciou no aumento das porcentagens de recuperaçao. Com o aumento da força iônica do sistema, observou-se um aumento de 3,06% na eficiência da extraçao. Geralmente, a introduçao de sais, como NaCl, à fase aquosa do sistema permite obter maiores percentuais de recuperaçao para compostos orgânicos, pois diminui a solubilidade destes na fase aquosa, favorecendo a transferência destes para a fase orgânica.26 Com relaçao à soluçao extratora, observou-se que nos ensaios utilizando apenas acetonitrila como solvente extrator, a recuperaçao média foi de 73,1%, enquanto que, empregando a mistura acetonitrila: acetato de etila (81,25: 18,75) obteve-se média de recuperaçao de 76,7%. A recuperaçao média de todos os ensaios foi 75,88%. A precisao do método foi determinada através do coeficiente de variaçao (CV) para nove extraçoes idênticas de brancos fortificados a 5 mg L -1 e os resultados foram 73,7% com coeficiente de variaçao de 5,3%. Resultados semelhantes foram obtidos na determinaçao de agrotóxicos em tomates realizada por Pinho et al.20 quando empregaram a combinaçao de dois solventes. A mesma técnica foi aplicada por Costa et al.11 para determinaçao de agrotóxicos em amostras de alface, obtendo percentuais de recuperaçao entre 72,3% e 103,2%. Atualmente a técnica ESL/PBT foi aplicada na análise de bifenilas policloradas em lodo de esgoto e os percentuais de extraçao foram superiores a 82%.27 Além da eficiência de extraçao e compatibilidade com a técnica cromatográfica, outros fatores devem ser avaliados para escolha do melhor solvente extrator, entre eles a viabilidade econômica e o descarte dos resíduos dos solventes orgânicos. Como as médias de recuperaçao estatisticamente nao diferem entre si, considerando que a acetonitrila é miscível em água e apresenta baixo ponto de fusao (-45 °C), propriedades essenciais para se empregar a ESL/PBT, este foi o solvente extrator escolhido.28 Assim, o ensaio 4 (repetiçoes 10, 11 e 12) com tempo de agitaçao em vortex - 60 s; adiçao de NaCl e ACN como solvente extrator foram escolhidos para dar continuidade ao trabalho, em virtude da viabilidade prática e econômica do experimento. Na Figura 3 está apresentado um cromatograma de um extrato do branco da abobrinha e cromatogramas obtidos de amostras de abobrinha livres de carbofurano, fortificadas e submetidas ao Ensaio 4. Observa-se que o tempo de retençao do carbofurano está entre 5 e 6 minutos. O extrato do branco nao apresenta picos no tempo de retençao dos carbofurano, o que permite afirmar que o método proposto apresenta seletividade.29
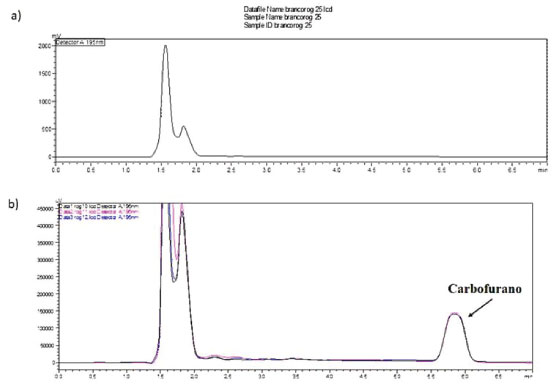 Figura 3. (a) Cromatograma de um extrato obtido de abobrinha isenta dos princípios ativos e (b) Cromatograma de extratos de abobrinha contendo o carbofurano a 5,0 mg L -1.
Limite de detecçao e quantificaçao Os limites de detecçao e quantificaçao do método proposto foram 0,04 mg kg -1 e 0,13 mg kg -1, respectivamente. Resultados semelhantes foram obtidos por Goulart et al.24 na análise de carbofurano em matrizes de bebidas de interesse forense. Este método é conhecido como método do sinal-rúído. Na determinaçao da relaçao sinal-ruído, faz-se a comparaçao entre a mediçao dos sinais de amostras em baixas concentraçoes conhecidas do composto de interesse na matriz e um branco (matriz isenta do composto de interesse) destas amostras.22 O carbofurano nao é registrado na ANVISA para utilizaçao em culturas de abobrinha, embora no último PARA tenha se verificado a presença desse agrotóxico nessa cultura. É importante ressaltar que estudos recentes realizados no município de Itumbiara-GO, alertam sobre a gama de agrotóxicos utilizados nos cultivos da regiao, em especial para a cana-de-açúcar e hortaliças. Em uma pesquisa realizada por Rodrigues et al.30 na cidade de Itumbiara-GO, foi constatado que 100% dos produtores rurais entrevistados utilizam algum tipo de agrotóxico, incluindo os carbamatos, como o carbofurano. No que se refere ao fácil acesso destes produtos identificou-se o relato de suicídio devido ao uso do agrotóxico Furadanr, que apresenta o carbofurano como princípio ativo, além da verificaçao de problemas ambientais relacionados ao descarte inadequado de embalagens e mortes de animais decorrentes de aplicaçoes aéreas de agrotóxicos. Do ponto de vista da segurança alimentar, a ausência de resíduos de carbofurano nas amostras analisadas é de suma importância, porém a quantidade de agrotóxicos utilizados na regiao é grande e os tipos de vegetais comercializados sao inúmeros. Diante deste cenário torna-se evidente a necessidade de manutençao de pesquisas sobre resíduos de agrotóxicos em alimentos e os impactos ambientais decorrentes do uso indiscriminado nas culturas da regiao. Aplicaçao do método de ESL/PBT-HPLC/UV em amostras de abobrinhas comerciais As amostras de abobrinha comercializadas no munícipio de Itumbiara-GO, coletadas e processadas conforme descrito anteriormente foram submetidas, em triplicata, ao método otimizado de ESL/PBT-HPLC/UV. As condiçoes do ensaio 4 (quatro) do planejamento (tempo de agitaçao em vortex - 60 s; adiçao de NaCl e ACN como solvente extrator) foram aplicados nas amostras reais para determinaçao de carbofurano. A 1,0000 g de polpa da amostra comercial de abobrinha, colocada em frascos de vidro transparente (22 mL) foi adicionado o sal NaCl (1,5% m/m). Após, foram acrescentados água (2 mL) e acetonitrila (4 mL) na proporçao (1:2). O sistema foi agitado em vórtex por 60 s e as amostras foram levadas ao freezer a -20 ºC por 3 horas para separaçao das fases. Após este intervalo, foi retirado 1 mL da fase orgânica e colocado em vial para análise cromatográfica. Nao foi evidenciada a presença de carbofurano dentro da faixa de detecçao do aparelho em todas as cinco amostras avaliadas, o cromatograma das análises em triplicata, da amostra de abobrinha 1 é apresentado na Figura 4. Os cromatogramas das amostras 2 a 5 foram semelhantes ao cromatograma da amostra 1. O carbofurano nao é autorizado pela ANVISA para aplicaçao em culturas de abobrinha. Para as culturas de cenoura, repolho e tomate os valores de LMR sao 0,5 mg kg -1, 1,0 mg kg -1 e 0,1 mg kg -1, respectivamente.6
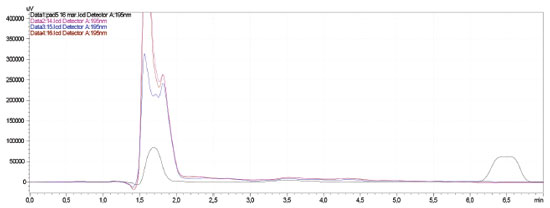 Figura 4. Cromatograma de extratos obtidos de matrizes reais de abobrinha (amostra 1) (—) (—) (—) replicatas comparadas ao padrao do carbofurano 5,0 mg L -1 (—)
CONCLUSAO A técnica ESL/PBT aplicada na determinaçao de carbofurano em matrizes de abobrinha é seletiva, simples e eficaz, consumindo pequenas quantidades de solventes e amostras, com porcentagem média de recuperaçao de 75,88%. Além disso, nao sao necessárias etapas posteriores de clean-up do extrato. Após a PBT os extratos sao analisados diretamente por HPLC-UV. As análises de matrizes reais de abobrinhas comercializadas no município de Itumbiara-GO utilizando a técnica ESL-PBT nao apresentaram resíduos do agrotóxico carbofurano.
AGRADECIMENTOS Ao Ministério da Educaçao (MEC) e a Fundaçao Nacional de Desenvolvimento da Educaçao (FNDE) pelo o apoio financeiro concedido ao Programa de Educaçao Tutorial (PET) do Instituto Federal de Goiás - Campus Itumbiara.
REFERENCIAS 1. Agência Nacional de Vigilância Sanitária (ANVISA). Disponível em http://portal.anvisa.gov.br/documents/111215/117818/Relat%25C3%25B3rio%2BPARA%2B2012%2B2%25C2%25AA%2BEtapa%2B-%2B17_10_14-Final.pdf/3bc220f9-8475-44ad-9d96-cbbc988e28fa, acessado em outubro de 2017. 2. Agência Nacional de Vigilância Sanitária (ANVISA). Disponível em http://portal.anvisa.gov.br/documents/111215/0/Relat%C3%B3rio+PARA+2013-2015_VERS%C3%83O-FINAL.pdf/494cd7c5-5408-4e6a-b0e5-5098cbf759f8, acessado em outubro de 2017. 3. Schmalstig, J. C.; Mcauslane, H. J.; J. Am. Soc. Hortic. Sci. 2001, 126, 544. 4. Summers, C. G.; Stapleton, J. J.; Crop Prot. 2002, 21, 921. 5. Scarpellini, J. R.; Ramiro, Z. A.; Lara, R. I. R.; Santos, J. C. C.; Arq. Inst. Biol. 2002, 69, 23. 6. Agência Nacional de Vigilância Sanitária (ANVISA). Disponível em http://portal.anvisa.gov.br/documents/111215/117782/C06%2B%25E2%2580%2593%2BCarbofurano.pdf/84d57401-49cc-47fd-9db6-2be75c116548, acessado em outubro de 2017. 7. Fundaçao Nacional de Saúde (FUNASA). Disponível em: http://bvsms.saude.gov.br/bvs/publicacoes/funasa/controle_vetores.pdf, acessado em outubro de 2017. 8. http://portal.anvisa.gov.br/documents/33880/2541557/CP%2B114-2015%2B-%2BNota%2Btecnica.pdf/b2b515d7-8e0e-4884-b7a9-525442b1bacb, acessado em outubro de 2017. 9. Prestes, O. D.; Adaime, M. B.; Zanella, R.; Sci. Chromatogr. 2011, 3, 51. 10. Morais, E. H. C.; Rodrigues, A. A. Z.; Queiroz, M. E. L. R.; Neves, A. A.; Morais, P. H. D.; Food Control. 2014, 42, 9. 11. Costa, A. I. G.; Queiroz, M. E. L. R.; Neves, A. A.; Sousa, F. A.; Zambolim, L.; Food Chem. 2015, 181, 64. 12. Moreno, C. M.; Stadler, T.; Silva, A. A.; Barbosa, L. C. A.; Queiroz, M. E. L. R.; Talanta 2012, 89, 369. 13. Rigueira, L. M. B.; Ribeiro, L. K.; Queiroz, M. E. L. R.; Neves, A. A.; Zambolim, L.; Oliveira, R. M.; J. Braz. Chem. Soc. 2013, 24, 2042. 14. Dardengo, R. P.; Goulart, S. M .; Neves, A. A .; Zambolim, L.; Queiroz, M. E. L. R.; Braz. J. Anal. Chem. 2011, 3, 136. 15. Araújo, E. A.; lara, M. C. R.; Reis, M. R.; Viriato, R. L. S.; Rocha, R. A. R.; Gonçalves, R. G. L.; Heleno, F. F.; Queiroz, M. E. L. R.; Tronto, J.; Pinto, F. G.; Food Analytical Methods 2016, 9, 1344. 16. Marthe, D. B.; Bittencourt, L. M.; Queiroz, M. E. L. R.; Neves, A. A.; Quim. Nova 2010, 33, 1389. 17. Freitas, R. S.; Queiroz, M. E. L. R.; Faroni, L. R. A.; Heleno, F. F.; Moura, V. V.; Quim. Nova 2014, 37, 238. 18. Heleno, F. F.; Queiroz, M. E. L. R.; Neves, A. A.; Oliveira, A. F.; Quim. Nova. 2014, 37, 153. 19. Assis, E. C.; Silva, A. A.; Barbosa, L. C.; Queiroz, M. E. L. R.; D’Antonino, L.; Gonçalves, V. A.; Planta Daninha 2011, 29, 683. 20. Pinho, G. P.; Neves, A. A.; Queiroz, M. E. L. R.; Silverio, F. O.; Food Chem. 2010, 121, 251. 21. Goulart, S. M.; Alves, R. D.; Neves, A. A.; Queiroz, J. H.; Assis, T. C.; Queiroz, M. E. L.; Anal. Chim. Acta 2010, 671, 41. 22. Ribani, M.; Bottoli, C. B. G.; Collins, C. H.; Jardim, I. C. S. F.; Melo, L. F. C.; Quim. Nova 2004, 27, 771. 23. Bahia filho, O.; Prada, P. R.; Meneghesso, C.; Lanças, F. M.; Sci. Chromatogr. 2011, 3, 251. 24. Brito, N. M.; Amarante Junior, O. P.; Polese, L.; Ribeiro, M. L.; Pesticidas: Revista de Ecotoxicologia e Meio Ambiente 2003, 13, 129. 25. Teófilo, R. F.; Ferreira, M. M. C.; Quim. Nova 2006, 29, 338. 26. Prestes, O. D.; Friggi, C. A.; Adaime, M. B.; Zanella, R.; Quim. Nova 2009, 32, 1620. 27. Maia, M. R.; Arcanjo, A. L. P.; Pinho, G. P.; Silvério, F. O.; J. Braz. Chem. Soc. 2017, 28, 179. 28. Maštovská. K.; Lehotay, S. J.; J. Chromatogr. A 2004, 1040, 259. 29. European Commission. SANTE/11945/2015. Disponível em: https://ec.europa.eu/food/sites/food/files/plant/docs/pesticides_mrl_guidelines_wrkdoc_11945.pdf, acessado outubro de 2017. 30. Rodrigues, V. C.; Goulart, S. M.; Santos, J. P. V.; Ribeiro Filho, H. A.; Castro, L. M.; Bernadeli, A. A.; Gomes, T. C. F.; Sinergia 2016, 17, 56. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access