Artigo
|
|
| Uso da regressão Linear Múltipla Combinada Com Adição de Padrão (MLR-SA) e análise exploratória de imagens digitais na avaliação do perfil férrico em infusões de plantas medicinais Use of Multiple Linear Regression Combined With Standard Addition (MLR-SA) and exploratory analysis of digital images in the evaluation of ferric profile in medicinal plant infusions |
|
Bruno E. S. Costa* Instituto de Química, Universidade Federal de Catalão, 75704-020 Catalão - GO, Brasil Recebido: 19/01/2025 *e-mail: brunoeliassantos@yahoo.com.br Iron plays an essential role in the metabolic balance of living beings. Iron also acts as an indicator of redox conditions in the aquatic environment, and a nutrient available in the soil for plant cultivation, which can be released during consumption. The iron content in samples of medicinal plant infusions was monitored by colorimetry, through the acquisition of digital images by smartphone, through the formation of the [Fe(H2O)5(SCN)]2+ complex in small sample volumes (500 µL). This work proposes a promising combination of standard addition calibration with multiple linear regression (MLR-SA) combined with exploratory analysis tools (principal component analysis, PCA, and hierarchical cluster analysis, HCA) to characterize an iron bioavailability profile in infusion samples. Calibration models were obtained with up to 97% of variance explained even in conditions of external light interference and matrix effects. The exploratory analysis revealed a ferric profile of commercial infusions distinguishable from infusions of natural origin. The multivariate approach to digital imaging data has proven to be an alternative methodology for affordable and sustainable monitoring of iron in infusion samples. INTRODUÇÃO O ferro é um nutriente essencial para manutenção da homeostase no organismo. A dinâmica de respiração se deve a presença do ferro como um cofator constituinte do complexo proteico da hemoglobina, responsável pelo transporte da molécula de oxigênio a todas as células do corpo. A deficiência de ferro impede a produção e a regeneração dos glóbulos vermelhos na corrente sanguínea, levando a um quadro de anemia ferropriva.1 Para combater esse distúrbio, o consumo de alimentos e bebidas ricas em ferro é recomendado. As principais fontes de ferro na dieta humana são as carnes bovina, frango, peixe, cereais, legumes, frutas e vegetais. No entanto, para alguns indivíduos, pode ser desafiador obter a quantidade adequada de ferro apenas através da dieta. O preparo de infusões de algumas ervas, tais como dente de leão, hibisco, funcho, hortelã e canela, também pode ser benéfico para a saúde, ao disponibilizar ferro como fonte suplementar e ajudar no tratamento contra anemia.2-5 O teor de ferro disponibilizado em infusões de plantas medicinais pode ser monitorado através de técnicas analíticas, tais como a espectrofotometria de absorção molecular no ultravioleta e visível (UV-Vis),6 espectrometria de absorção atômica,7 espectrometria de emissão óptica com plasma indutivamente acoplado (ICP OES),8 espectrometria de massas com plasma indutivamente acoplado (ICP-MS),9 além de técnicas eletroquímicas.10 Entretanto, tais técnicas necessitam de alto investimento para aquisição e etapas laboriosas de preparo da amostra. O uso de imagens digitais em finalidades de determinação, tem sido uma tendência cada vez mais crescente em química analítica.11,12 A intensidade da cor da solução é relacionada com a concentração do analito, e dados quantificáveis são obtidos através da decomposição das imagens em histogramas, que podem ser tratadas por modelos RGB (red, green e blue), HSV (hue, saturation e value), CMYK (cyan, magenta, yellow, e black) e CIELab (definido pela International Commission on Illumination).13,14 A análise de imagens baseada no sistema aditivo de cores RGB vem ganhando espaço como uma ferramenta alternativa de quantificação, pois se destaca pela praticidade, portabilidade, baixo custo operacional e mínima geração de resíduos.15 A simplicidade da técnica sustentada por uma validação adequada, viabiliza o uso de dispositivos de imagem digital, tais como smartphones, tablets, scanners, webcams e câmeras fotográficas com dispositivo de carga acoplada (CCD) como método analítico, e os torna excelentes complementos para espectrofotômetros e instrumentos de monitoramento de campo mais sofisticados.16,17 No sistema RGB, a cor e a intensidade da imagem digital são representadas por valores numéricos que indicam a intensidade de cada canal de cor em um determinado pixel. Em um sistema RGB de 8 bits por canal, o valor de cada canal varia de 0 a 255, totalizando dados de 24 bits para representar a cor de um pixel (bitmap). Através da combinação dos três canais é possível obter 16.777.216 variedades de cores. Os dados dos canais individuais, a combinação deles ou outras informações podem ser relacionados com a concentração do analito. Softwares de processamento de imagem como PhotoMetrix, ImageJ, Chemostat e Matlab são utilizados para converter os dados da imagem digital em sinal analítico adequado.18,19 A disseminação do uso de imagens digitais em finalidades analíticas deve ser fortemente incentivada por questões de sustentabilidade ambiental. A biodisponibilidade de ferro nas ervas medicinais está condicionada a diferentes formas de cultivo que podem estar sujeitas a contaminação. O monitoramento metalômico em espécies vegetais acumuladoras de ferro ou outros elementos metálicos tóxicos podem interferir diretamente na suplementação desejada em questões clínicas, ou de (bio)remediação em questões ambientais. Esse monitoramento pode ser potencializado com o uso de análises de imagens digitais in loco, através da vantagem do desenvolvimento de sistemas portáteis. Por outro lado, deve-se considerar fatores externos ao ambiente que podem afetar na qualidade dos sinais analíticos provenientes dos dados de imagem. Os efeitos de matriz da amostra, interferência luminosa e de concomitantes são desafios que precisam ser superados. Para tanto, estratégias de calibração, como a adição de padrão e técnicas multivariadas são usadas para contornar essas limitações.20,21 Neste trabalho, é proposta a combinação da calibração por adição de padrão com a regressão linear múltipla como uma estratégia de modelagem simultânea dos canais RGB em condições de baixas concentrações de ferro, podendo também controlar um possível mascaramento da coloração vermelha do complexo de Fe3+ com íons tiocianato ([Fe(H2O)5(SCN)]2+), na presença da matriz de infusão vegetal. É a primeira vez que a combinação dessas duas formas de calibração é proposta de forma promissora, a fim de alcançar maior precisão, exatidão e variância explicada em modelagens dos dados obtidos a partir da aquisição de imagens digitais.
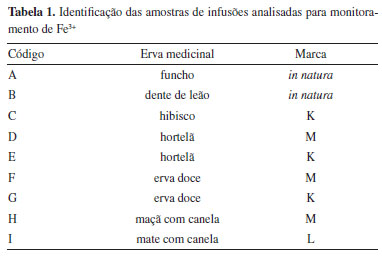
PARTE EXPERIMENTAL Obtenção e preparo das amostras de infusões Foram analisadas nove amostras de infusões de ervas medicinais. A identificação de cada amostra de infusão se deu pela codificação apresentada na Tabela 1. As infusões obtidas pelas amostras de funcho (A) e dente de leão (B) foram preparadas na forma da erva in natura, as quais foram adquiridas em casas de produtos naturais, comercializadas a granel e armazenadas em frascos fechados para evitar contaminação com material particulado. As demais amostras das ervas medicinais foram adquiridas no comércio local, submetidas ao processamento industrial de desidratação e embaladas na forma de sachê com empacotamento lacrado em caixas plásticas, sendo provenientes de marcas distintas, identificadas como marcas "K", "M" e "L".
As infusões de funcho (A) e dente de leão (B) foram preparadas colocando as folhas das plantas em água sob ebulição. A mistura foi deixada em repouso por 10 min, utilizando-se um vidro de relógio para tampar o recipiente, abafando o vapor. Esse procedimento preserva o óleo essencial das plantas. O preparo das infusões das amostras C-I se deu de acordo com as instruções dos rótulos das embalagens, imergindo o sachê com o conteúdo em volume adequado de água, durante o intervalo de 5 a 10 min. Cada infusão preparada teve estabelecido o equilíbrio térmico com o ambiente antes de ser utilizada nos experimentos. Preparo das soluções A metodologia para determinação de ferro nas amostras de infusões se baseou na formação do complexo tiocianato de ferro(III), sendo que o preparo das soluções seguiu os procedimentos reportados por Lourenço et al.22 Todas as soluções foram preparadas utilizando água deionizada obtida do sistema de purificação Milli-Q (Millipore) de resistividade 18,2 MΩ. Toda a vidraria utilizada foi deixada durante a noite em solução aquosa de ácido nítrico a 10% (v/v), seguida de enxágue com água deionizada. A solução estoque de Fe3+ 10,0 mg L-1 foi preparada pela dissolução de quantidade adequada do sal FeCl3.6H2O e utilizada para o preparo das soluções de trabalho na faixa de concentração de 0,1-5,0 mg L-1. A solução do complexante, na concentração de 0,1 mol L-1, foi preparada por dissolução de quantidade adequada do sal KSCN. Uma solução de HCl 0,1 mol L-1 foi preparada a partir do reagente de grau analítico (P.A., 1,18 g cm-3, 38% m/m), para conferir estabilidade ao complexo, evitando ocorrência de hidrólise dos íons férrico. Procedimento de calibração por adição de padrão As curvas analíticas foram construídas através da fortificação das soluções de cada amostra de infusão por adição de padrão de Fe3+, para obtenção das concentrações identificadas a seguir; ponto 1: amostra sem fortificação; ponto 2: fortificação com Fe3+ 0,1 mg L-1; ponto 3: fortificação com Fe3+ 0,5 mg L-1; ponto 4: fortificação com Fe3+ 1,0 mg L-1; ponto 5: fortificação com Fe3+ 2,0 mg L-1; ponto 6: fortificação com Fe3+ 3,0 mg L-1; ponto 7: fortificação com Fe3+ 4,0 mg L-1, e ponto 8: fortificação com Fe3+ 5,0 mg L-1. Para tanto, foram preparados 25,0 mL de solução correspondente a cada ponto da calibração, adicionando-se 1,0 mL da amostra de infusão, seguida da alíquota da solução estoque de Fe3+ e da adição de 1,0 mL da solução de HCl 0,1 mol L-1. Por fim, adicionou-se 10,0 mL da solução do complexante tiocianato (SCN-), fazendo-se a homogeneização e deixando em repouso até o aparecimento e estabilização da coloração vermelha indicativa da formação do complexo [Fe(H2O)5(SCN)]2+. Aquisição das imagens digitais Foram pipetadas alíquotas de 500,0 µL das soluções e dispostas em uma placa de poços transparente feita em acrílico, identificando os spots correspondentes a cada ponto da calibração por adição de padrão. Essa etapa de preenchimento da placa de poços foi realizada sucessivamente, para cada tipo de infusão preparada. A captura das imagens se deu através de um smartphone Samsung Galaxy A8+, utilizando a câmera principal de 16 MP (megapixel), com resolução de 4608 × 3456 pixels e abertura de f/1.7. O smartphone foi posicionado sobre a abertura de uma câmara escura impressa em acrinonitrila butadieno estireno (ABS), com dimensões 22 cm × 15 cm × 10 cm, e equipada na parte inferior com uma fita de LED (do inglês, light-emitting diode), de cor branca (12 V de potência). Para distribuição homogênea da luz e como suporte para a placa de poços, foi utilizada uma base de propileno de cor branca, posicionada a 10 cm da parte inferior contendo os LEDs. Na Figura 1, tem-se a representação real do aparato para captura das imagens em condições de luminosidade constante.

Para a obtenção e tratamento dos dados RGB contidos nas imagens capturadas, foi utilizado o software de processamento de imagens ImageJ® (versão 1.54d).23 No software, as regiões de interesse de cada solução foram manualmente selecionadas, tomando-se o cuidado de manter a reprodutibilidade da distribuição dos pixels (1354 pixels por região), e os histogramas referentes ao bitmap de cada canal foram então obtidos para análise. Análise multivariada dos dados A modelagem dos dados por regressão linear múltipla (MLR) foi realizada com uso do suplemento ferramentas de análise do Microsoft Excel® do pacote Office 2019. Os sinais analíticos para os respectivos canais R, G e B foram tomados simultaneamente para a construção de modelos matemáticos como variáveis independentes, enquanto que a concentração foi tomada como variável dependente, característico dos modelos de calibração inversa. Foi obtido um modelo de calibração MLR para cada tipo de infusão, os quais foram avaliados por análise de variância (ANOVA) a 95% de confiança. O conjunto de dados RGB para os grupos das amostras de infusões também foi modelado com ferramentas de análise exploratória, como a análise por componentes principais (PCA) e análise hierárquica de clusters (HCA), afim de que pudessem revelar perfis característicos da disponibilidade de íons férrico relativos a cada tipo de amostra. Para tanto, foi construída uma matriz de dados oriundos do histograma global (R + G + B) de cada ponto da calibração, assim como para cada tipo de infusão (A1-A8; B1-B8; C1-C8; D1-D8; ...; I1-I8), incluindo as soluções aquosas do padrão do complexo de tiocianato de ferro(III) (P1-P8). A matriz de dados (80 amostras × 256 variáveis: bitmap R + G + B) foi tratada centrando os dados na média para construção dos modelos PCA e HCA, utilizando o software Past (versão 4.03).24
RESULTADOS E DISCUSSÃO Avaliação preliminar das imagens digitais O espectro de emissão da luz branca (policromática) foi obtido através de um espectrofotômetro modular multicanal UV-Vis-NIR, USB4000XR1-ES (Ocean Optics), o qual está apresentado na Figura 2. A luz branca foi proveniente dos LEDs utilizados como fonte de radiação luminosa para a obtenção das imagens na câmara escura.
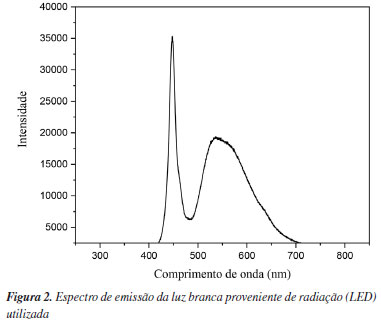
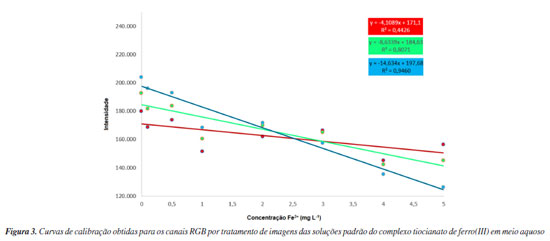
A iluminação é um dos fatores de maior impacto na qualidade das imagens. Uma boa iluminação não apenas assegura uma qualidade superior, como também influencia diretamente na linearidade e na reprodutibilidade do sinal analítico. Todos os LEDs compreendidos neste trabalho operaram em uma voltagem de 12 V, com um máximo de intensidade em aproximadamente 450 nm. Nota-se também uma segunda região com uma banda alargada, correspondente aos comprimentos de onda entre a luz verde (ca. 500 nm) e a luz laranja (ca. 600 nm), decaindo no sentido da radiação da luz vermelha (ca. 700 nm). Como forma de avaliação preliminar, as soluções padrão do complexo de tiocionato de ferro(III) em meio aquoso foram tomadas como referência na construção das curvas de calibração por imageamento digital (Figura 3). A intensidade de cada canal do sistema RGB foi utilizada separadamente como resposta às variações de concentração.
Observa-se que as regressões das calibrações são inversamente proporcionais a concentração e não apresentaram ajuste linear satisfatório para os canais R (linha vermelha) e G (linha verde), variando o coeficiente de determinação (R2) de 0,4426 do canal R, para 0,8071 do canal G. O canal B (linha azul) apresentou a melhor condição de linearidade com R2 = 0,9460, e maior sensibilidade. As intensidades dos canais RGB foram convertidas em sinal analítico (S) para obtenção de curvas de calibração com respostas diretamente proporcionais em relação a concentração de FeIII. Para conversão, foi utilizada a Equação 1,25,26 em que S é definido como o logaritmo decimal negativo da razão entre o valor I, que é o valor da intensidade de R, G ou B da solução contendo o analito, e Ibco, sendo este o respectivo valor da intensidade de R, G ou B para o branco analítico. S = -log (I/Ibco) (1)
Ao aplicar a Equação 1, além de obter calibrações com valores de S crescentes, observa-se uma tendência de maior diferenciação entre os canais do sistema RGB ao expressarem as intensidades de coloração do complexo. Essa observação permite uma análise mais abrangente frente a diferentes concentrações das amostras, resultando em uma resposta analítica mais sensível. A Figura 4 mostra as curvas de calibração construídas.
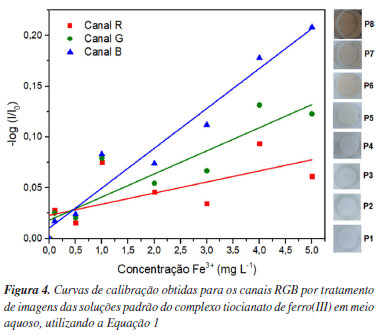
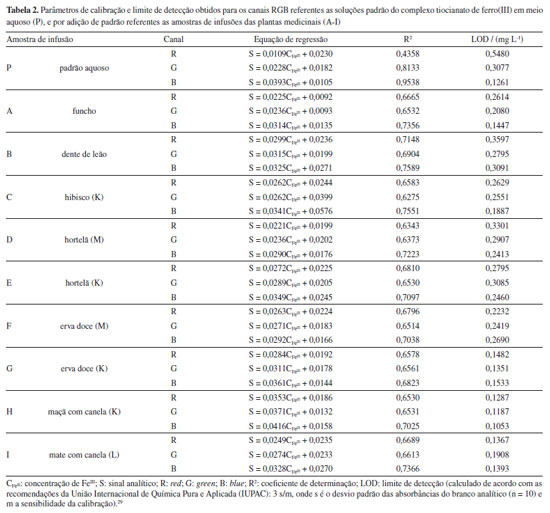
Até o ponto 4 (1,0 mg L-1 de Fe3+), os valores de S permanecem próximos para os três canais. Entretanto, conforme a concentração de ferro é aumentada, a coloração vermelha característica do complexo se torna mais pronunciada, e o sinais analíticos passam a responder aos canais de maneiras distintas. O canal R apresentou baixos valores de S e pequenas variações entre os pontos, resultando em pior desempenho de linearidade e sensibilidade, com valores de R2 de 0,4358 e coeficiente angular de 0,0109. Os canais G e B foram utilizados de forma a complementar a coloração vermelha das soluções, o que proporcionou maior discriminação entre as intensidades de coloração, corroborando com a melhora significativa das linearidades e sensibilidades das curvas de calibração. Dentre as três curvas construídas, o canal B proporcionou uma maior linearidade com valor de R2 de 0,9538 e um coeficiente angular (sensibilidade) de 0,0393. Calibração por adição de padrão (SA) É importante ressaltar a possibilidade de outros elementos metálicos concomitantes serem disponibilizados durante o preparo de infusão das plantas medicinais, os quais podem interferir na complexação com íons tiocianato, a exemplo do cobalto. Como forma de corrigir prováveis efeitos de matriz, a calibração por adição de padrão se torna mais indicada.27,28 As calibrações por adição de padrão para as soluções das amostras de infusões de cada planta medicinal foram testadas, e os parâmetros apresentados na Tabela 2. As Figura 1Sa-1Sc, do Material Suplementar, apresentam as curvas de calibração por adição padrão obtidas para os canais RGB de cada amostra.
Em vista da melhor performance de linearidade e sensibilidade observada para o canal B em todas as amostras, este foi selecionado para a determinação do teor de ferro disponibilizado nas amostras de infusões, com a finalidade de comparação da calibração obtida com a regressão linear múltipla. Regressão linear múltipla combinada com adição de padrão (MLR-SA) A estratégia de combinar duas formas distintas de calibração surgiu da necessidade de minimizar os efeitos de matriz decorrentes da possibilidade de mascaramento do complexo vermelho do tiocianato de ferro(III) formado, em contato com as soluções das amostras, que já apresentam uma coloração natural característica de cada tipo de infusão. A regressão linear múltipla (MLR) se enquadra dentro da categoria de calibração multivariada, proporcionando a vantagem da calibração de primeira ordem, a qual torna possível realizar a modelagem da calibração mesmo na presença de interferentes não conhecidos, desde que estes também estejam presentes nos padrões que constituem o conjunto de calibração.30 Conforme observado na Tabela 2, apesar do canal B se mostrar promissor na calibração por adição de padrão, esta variável isolada não consegue explicar quantitativamente a variância dos dados, uma vez que os valores de R2 não são suficientemente próximos da unidade. Tal fato impede que os modelos univariados obtidos na calibração por adição de padrão sejam empregados em finalidades de predição das amostras. Portanto, houve o interesse em verificar a modelagem simultânea das variáveis independentes RGB para construção da calibração MLR, afim de obter melhora significativa no percentual de variância explicada. Na MLR, obtém-se um modelo matemático do tipo ŷ = Xb, no qual ŷ são as concentrações preditas nas amostras, X é a matriz das variáveis independentes de cada padrão (x1, x2, ..., xn), y é o vetor de concentrações dos padrões a serem modelados (variável dependente) e b o vetor dos coeficientes obtidos da regressão, conforme Equação 2. Essa relação pode ser expandida pela representação da Equação 3: b = (X TX)-1X Ty (2)
ŷ = b0 + b1x1 + b2x2 + ... + bnxn (3) Na adição de padrão convencional, como ocorre na espectrofotometria de absorção no UV-Vis, a calibração é plotada tomando o ponto de concentração zero como a solução da amostra sem fortificação. Os demais pontos que correspondem às amostras fortificadas com o analito tem suas concentrações adicionadas no eixo x, e as respectivas absorbâncias no eixo y, nivelando a contribuição da amostra presente em todos os pontos. A extrapolação da linha de regressão no eixo x, quando se toma nula a variável dependente, fornece a informação quantitativa desejada do analito na amostra. Quando se combina a adição de padrão com a MLR, pode-se aplicar o mesmo raciocínio, levando em consideração que se trata agora de uma calibração inversa: a concentração é tomada como variável dependente, em função do conjunto das variáveis, que no caso são os sinais analíticos, S, associadas aos canais RGB. A plotagem dos dados torna-se espacial, gerando um plano para uma modelagem de duas variáveis (x1 e x2), ou um hiperplano no caso da modelagem igual ou acima de 3 variáveis. De forma análoga a convencional, na MLR-SA, quando se toma nulos os valores de S para todos os canais de cor R, G e B, o valor absoluto do termo independente do modelo obtido (|b0|) fornece a informação quantitativa do analito, por intercepto com o eixo das concentrações. Logo a combinação MLR-SA se torna ideal para aplicação de dados de imagens digitais obtidas em concentrações suficientemente baixas do analito, promovendo uma alternativa às limitações de aplicações analíticas dos dados de imagens digitais apenas para altas intensidades de coloração das amostras. A Tabela 3 apresenta os parâmetros obtidos na calibração MLR-SA de cada amostra de infusão. Cada modelagem foi avaliada por análise de variância (ANOVA) a 95% de confiança e podem ser verificadas nas Tabelas S1-S9 do Material Suplementar.
Com exceção das amostras de erva doce (F e G), todos os demais modelos de calibração MLR-SA obtidos foram estatisticamente significativos (p < 0,05). A combinação das calibrações MLR-SA propiciou obtenção de valores de R2 bem mais próximos da unidade. Nota-se que a abordagem multivariada é capaz de promover melhora significativa da porcentagem de variância explicada pelos modelos em até aproximadamente 97%, valor este mais expressivo em comparação com a calibração por adição de padrão univariada (Tabela 2). As amostras de infusões foram também submetidas a determinação de ferro por espectrometria de absorção atômica por chama (FAAS, PerkinElmer® AAnalyst 400). A concentração de Fe3+ obtida através dos modelos de calibração MLR-SA, bem como por adição de padrão univariado (convencional) foram confrontados com a determinação obtida por FAAS como via de validação cruzada. A Figura 5 apresenta a comparação entre os resultados obtidos.
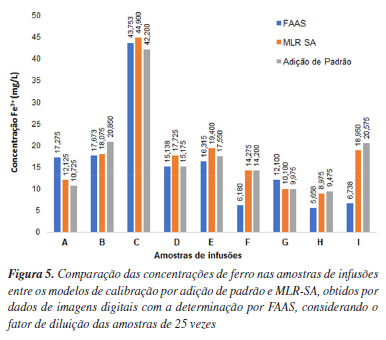
É possível observar que a maior parte das amostras apresentaram razoável concordância quanto ao teor de ferro disponibilizado nas infusões, entre as diferentes formas de calibração testadas. As amostras de infusão de erva doce (marca M), e a de mate com canela na composição (amostras F e I), foram as que apresentaram a maior discrepância em relação ao FAAS. Foi verificado instabilidade na coloração dessas amostras durante o período das análises, comprometendo a integridade dos sinais analíticos gerados durante a aquisição das imagens digitais. Para essas amostras, torna-se necessário um cuidado maior para preservação do complexo [Fe(H2O)5(SCN)]2+ em meio a compostos de taninos que também podem ser extraídos das ervas, e que podem competir com os íons tiocianato no mecanismo de complexação dos íons Fe3+. O íon metálico também pode estar mais sujeito a mudança do estado de oxidação devido a presença de antioxidantes, como o ácido ascórbico. Análise exploratória A matriz de dados utilizada para a abordagem multivariada de agrupamento das amostras por PCA e HCA foi obtida a partir do conjunto de histogramas global do multicanal R + G + B, conforme mostrado na Figura 6.
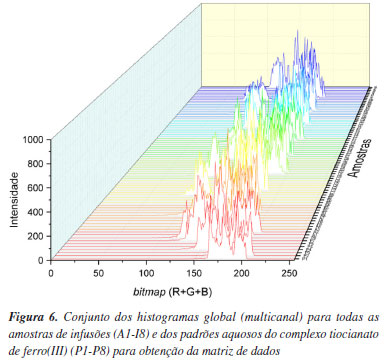
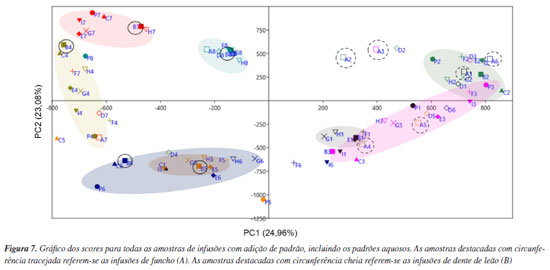
Com relação a PCA, a Figura 12S do Material Suplementar indica uma tendência de variação monotônica a partir de 5 componentes principais. Baseando-se no critério de Kaiser,31 foram escolhidas 5 componentes principais, que cumulativamente respondem por 73,27% da variância explicada dos dados. O gráfico dos scores para PC1 e PC2, apresentado na Figura 7, evidencia que as amostras se distribuem melhor em grupos referentes a concentração de Fe3+ adicionada (ponto 1, ..., ponto 8) em cada tipo de amostra. Essa observação indica a adequação dos tratamentos de calibração para os dados de imagens digitais coletados. Os gráficos dos scores referentes as demais componentes principais (PC3, PC4 e PC5) encontram-se nas Figuras 11Sa-11Sc, do Material Suplementar.
O ponto 8, relativo ao de maior concentração adicionada (5,0 mg L-1) forma um grupo mais definido de amostras, indicando que a intensidade de coloração formada é determinante para uma melhor resolução desse agrupamento. O gráfico dos loadings para PC1 e PC2 (Figura 8), confirma que os bits responsáveis pela intensidade significativa de coloração têm forte contribuição nas amostras e estão correlacionados de formas opostas.
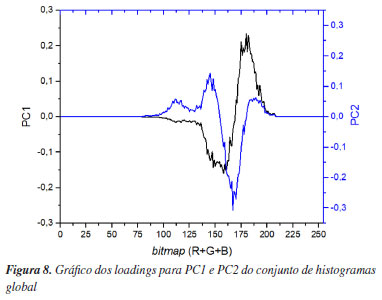
A análise exploratória revelou um perfil férrico associado ao tipo de beneficiamento (natural ou comercial) das ervas medicinais. Foi notável uma categorização das amostras de funcho (A) e dente de leão (B) em relação as demais ervas medicinais, proporcionada pela PC1: na Figura 7, observa-se que 6 amostras das infusões de funcho têm seus scores localizados nos quadrantes à direita (destacadas com circunferência tracejada), enquanto que 5 amostras das infusões de dente de leão, por sua vez, têm seus scores localizados nos quadrantes à esquerda (destacadas com circunferência cheia). As infusões das demais ervas medicinais, que são de beneficiamento comercial, apresentaram seus scores dispersos em todos os quadrantes, sem a predominância de um perfil característico destes. A PC1 foi capaz de indicar, através do perfil férrico das amostras, uma certa diferenciação das infusões das ervas em sua forma in natura (A e B), o que reforça a vantagem da abordagem multivariada dos dados. Afim de confirmar essa observação, a Figura 9 apresenta dois grandes clusters provenientes da aplicação HCA aos mesmos dados, dos quais verifica-se que o conjunto de infusões das ervas medicinais de origem natural (A e B) formam categorias opostas em relação as demais amostras.
CONCLUSÕES A combinação da regressão linear múltipla com a calibração por adição de padrão (MLR-SA) se mostrou promissora em finalidades quantitativas, no que se refere ao monitoramento do teor de íons ferro disponibilizados nas infusões das ervas medicinais testadas. O monitoramento se deu através do tratamento de imagens digitais, através da formação do complexo tiocianato de ferro(III), de forma que a aplicação do método MLR-SA proporcionou a determinação de ferro em níveis de parte por milhão (ppm), com até 97% de variância explicada nos dados de calibração multivariada. Dentre as amostras analisadas, a infusão preparada com hibisco foi a que mais disponibilizou íons ferro de acordo com as análises. O tratamento dos dados de imagens digitais articulados com o uso das ferramentas PCA e a HCA foi útil para revelar um perfil férrico que permitiu categorizar as amostras de infusões preparadas com ervas de beneficiamento in natura (funcho e dente de leão). A abordagem quimiométrica proposta através do tratamento multivariado dos dados de imagens digitais por calibração e análise exploratória se destaca pela vantagem de adequar os dados analíticos adquiridos de forma alternativa, como no caso dos bitmaps de imagens digitais, em detrimento aos efeitos de interferência da matriz da amostra.
MATERIAL SUPLEMENTAR As curvas de calibração obtidas pelo tratamento de imagens digitais, figuras de análise exploratória e as avaliações estatísticas dos modelos testados neste trabalho estão disponíveis em http://quimicanova.sbq.org.br, na forma de arquivo PDF, com acesso livre.
AGRADECIMENTOS Os autores agradecem ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) pelo fomento a bolsa de Pós-doutorado Junior (PDJ, processo 150828/2022-5), ao Instituto de Química da Universidade Federal de Catalão, ao Prof. Dr. E. I. Melo, do Instituto de Ciências Agrárias da Universidade Federal de Uberlândia, Campus Monte Carmelo, (ICIAG - UFU) por disponibilizar a câmara escura para aquisição das imagens digitais deste trabalho, e a Profa. Dra. T. P. O. Xavier, do Instituto Federal de Goiás, Campus Luziânia, pela colaboração no tratamento estatístico dos dados.
REFERÊNCIAS 1. Hirota, K.; Free Radicals Biol. Med. 2019, 133, 118. [Crossref] 2. Durazzo, A.; Carocho, M.; Heleno, S.; Barros, L.; Souto, E. B.; Santini, A.; Lucarini, M.; Measurement: Food 2022, 7, 100050. [Crossref] 3. da Silva, C. L. A.; Ferreira, M. C. P.; Pires, P. C. C.; Ribeiro, R. T.; HU Revista 2020, 45, 389. [Crossref] 4. Gurley, B. J.; Fifer, E. K.; Gardner, Z.; Planta Med. 2012, 78, 1490. [Crossref] 5. Magtalas, M. C.; Balbin, P. T.; Cruz, E. C.; Clemente, R. F.; Buan, A. K. G.; Garcia, J. P.; Lee, K. Y.; Tantengco, O. A. G.; Trop. Med. Health 2023, 51, 27. [Crossref] 6. McGee, E. J. T.; Diosady, L. L.; Food Analytical Methods 2018, 11, 1645. [Crossref] 7. Adolfo, F. R.; do Nascimento, P. C.; Leal, G. C.; Bohrer, D.; Viana, C.; de Carvalho, L. M.; Colim, A. N.; Talanta 2019, 195, 745. [Crossref] 8. Szymczycha-Madeja, A.; Welna, M.; Pohl, P.; Food Analytical Methods 2015, 9, 1398. [Crossref] 9. Tokalioğlu, Ş.; Food Chem. 2012, 134, 2504. [Crossref] 10. Shao, J.; Wang, C.; Shen, Y.; Shi, J.; Ding. D.; Front. Chem. 2022, 9, 818461. [Crossref] 11. Fernandes, G. M.; Silva, W. R.; Barreto, D. N.; Lamarca, R. S.; Gomes, C. F. L.; Petruci, J. F. S.; Batista, A. D.; Anal. Chim. Acta 2020, 1135, 187. [Crossref] 12. Soares, S.; Fernandes, G. M.; Rocha, F. R. P.; TrAC, Trends Anal. Chem. 2023, 168, 117284. [Crossref] 13. Roda, A.; Michelini, E.; Zangheri, M.; Di Fusco, M.; Calabria, D.; Simoni, P.; TrAC, Trends Anal. Chem. 2016, 79, 325. [Crossref] 14. Shishkin, Y.; Dmitrienko, S. G.; Medvedeva, O. M.; Badakova, S. A.; Pyatkova, L. N.; J. Anal. Chem. 2004, 59, 102. [Crossref] 15. Pazzi, B. M.; Pistoia, D.; Alberti, G.; Micromachines 2022, 13, 1585. [Crossref] 16. Capitán-Vallvey, L. F.; López-Ruiz, N.; Martínez-Olmos, A.; Erenas, M. M.; Palma, A. J.; Anal. Chim. Acta 2015, 899, 23. [Crossref] 17. Oliveira, G. C. O.; Machado, C. C. S.; Inácio, D. K.; Petruci, J. F. S.; Silva, S. G.; Talanta 2022, 241, 123244. [Crossref] 18. Schroeder, A. B.; Dobson, E. T. A.; Rueden, C. T.; Tomancak, P.; Jug, F.; Eliceiri, K. W.; Protein Sci. 2020, 30, 234. [Crossref] 19. Singh, H.; Practical Machine Learning and Image Processing for Facial Recognition, Object Detection, and Pattern Recognition Using Python, 1st ed.; Apress: Berkeley, 2019. [Crossref] 20. Ferreira, M. M. C.; Antunes, A. M.; Melgo, M. S.; Volpe, P. L. O.; Quim. Nova 1999, 22, 724. [Crossref] 21. Rosa, T. R.; Siqueira, B. M. M.; Costa, R. A.; dos Reis, J. Z.; Pacheco, W. L. S.; de Moura, P. R. G.; Romão, W.; Filgueiras, P. R.; Quim. Nova 2022, 45, 550. [Crossref] 22. Lourenço, E. C.; Paula, S.; Setti, G. O.; Toci, A. T.; Padilha, J. C.; Silva, E. M.; Boroski, M.; Rev. Virtual Quim. 2021, 13, 192. [Crossref] 23. Rasband, W.; ImageJ, versão 2.0.0-rc-3; National Institutes of Health, USA, 2014. 24. Hammer, Ø.; Harper, D. A. T.; Ryan, P. D.; Palaeontologia Electronica 2001, 4, 9. [Link] accessed in March 2025 25. Vilcapoma, W.; Pérez, J. F.; Braz. J. Anal. Chem. 2024, 11, 85. [Crossref] 26. Oliveira, C. R. S.; Suarez, W. T.; Nahas, H. R. A.; Novaes, F. J. M.; de Almeida, J. P. B.; dos Santos, V. B.; Rev. Virtual Quim. 2024, 16, 307. [Crossref] 27. Trana, L. B.; Nguyen, T. T.; Padungthon, S.; Huy, N. N.; Water Practice and Technology 2023, 18, 3272. [Crossref] 28. Feiteira, F. N.; Barreiros, J. V. P. P.; Pacheco, W. F.; Quim. Nova 2021, 44, 20. [Crossref] 29. Templeton, D. M.; Ariese, F.; Cornelis, R.; Danielsson, L. G.; Muntau, H.; van Leeuwen, H. P.; Lobinski, R.; Pure Appl. Chem. 2000, 72, 1453. [Crossref] 30. Ferreira, M. M. C.; Quimiometria: Conceitos, Métodos e Aplicações, 1ª ed.; Editora da Unicamp: Campinas, 2015. 31. Kaiser, H. F.; Psychometrika 1958, 23, 187. [Crossref]
Editor Associado responsável pelo artigo: Eduardo H. S. Sousa |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access