Artigo
|
|
| Caracterização, análise quimiométrica e ensaios preliminares de adsorção de corantes têxteis em celulose bacteriana: uma tecnologia para tratamento de efluentes com proposta para desenvolvimento de economia sustentável Characterization, chemometric analysis, and preliminary adsorption tests of textile dyes on bacterial cellulose: a technology for effluent treatment with a proposal for the development of a sustainable economy |
|
Rafaela J. L. Gouveia-RamosI,* I. Departamento de Engenharia Agrícola e Ambiental, Universidade Federal Rural de Pernambuco, 52171-900 Recife - PE, Brasil Recebido: 15/07/2024 *e-mail: rafaelajulia020@gmail.com To mitigate the environmental impacts of dyes in the textile industry, this research sought to investigate the removal potential of a bacterial cellulose (BC) produced by Komagataeibacter xylinus. The BC was produced under controlled conditions and then the physicochemical, structural, and morphological properties of the biosorbent were characterized using Fourier transform infrared spectroscopy (FTIR), scanning electron microscopy (SEM), and thermogravimetry (TG). Ten dye samples were collected from the textile laundries in Pernambuco to carry out the adsorption studies. The chemical composition of the dyes was assessed by electronic absorption spectroscopy (UV-Vis), inductively coupled plasma optical emission spectroscopy (ICPOES), and TG. They were also statistically analyzed using principal component analysis (PCA). The treatment tests were conducted in a 24-h adsorption system using ∼ 100 mg of BC and 20.0 mg L-1 of dyes. The most satisfactory response was for phthalocyanine class dyes, with qe (amount of analyte adsorbed at equilibrium) of 1.7234 mg g-1 under acid conditions. In the thermal analysis, it was defined that degradation of CB at 555 ºC allowed recovery of approximately 65% of C10 dye (reactive blue 21) for the impregnated material. A hypothesis was also formulated as an approach to treat textile water waste, to produce an ''eco-dye''. INTRODUÇÃO O setor têxtil e de confecção está entre os quatro maiores produtores de malhas, assumindo também o quinto lugar na produção de jeans do mundo, representando um faturamento de R$ 193,2 bilhões em 2022 e R$ 190 bilhões em 2021. A relevância econômica desse ramo torna-se mais acentuada quando os valores mais recentes são comparados aos R$ 161 bilhões de 2020, durante a pandemia COVID-19. O setor registrou uma produção de aproximadamente 2,1; 2,16 e 1,91 milhões de toneladas nos anos de 2022, 2021 e 2020, respectivamente.1 No entanto, apesar dos dados favoráveis em relação ao faturamento no Brasil, o meio ambiente recebe uma alta carga de resíduos da indústria têxtil. A Associação das Empresas de Limpeza Pública e Resíduos Especiais2 estimou em 2022 que são despejados 4,58 milhões de toneladas de resíduos têxteis, couro e borracha por ano no meio ambiente. O setor têxtil destaca-se pela alta demanda de água em seus processos (tingimento, alvejamento, estamparia e acabamento) que impactam fortemente o meio ambiente devido aos efluentes nocivos gerados. O consumo diário de água em uma indústria têxtil de médio porte com uma produção de cerca de 8 toneladas de tecido por dia é de aproximadamente 400.000 litros de água. Para o tingimento, o consumo específico de água varia de 30 a 50 L kg-1 de tecido, dependendo do tipo de corante utilizado.3 Assim, há necessidade de ações preventivas e corretivas na gestão da água. A recirculação da água no processamento têxtil é recomendada como a abordagem mais promissora, para a construção de uma economia circular sustentável.4 O Arranjo Produtivo Local de Confecções do Agreste Pernambucano (APLCAPE) é um dos maiores polos têxteis do Brasil, empregando cerca de 100.000 pessoas, com uma produção de aproximadamente 900 milhões de peças por ano.5,6 No entanto, é necessário a APLCAPE desempenhar medidas para garantir a sustentabilidade ambiental. Muitas lavanderias estão interessadas em obter o selo verde que atesta adequações à regularização ambiental, visando conquistar novos mercados.7,8 Devido à aplicação de cores em tecidos, o consumidor costuma estabelecer critérios básicos de qualidade do produto. Para garantir essas propriedades, os corantes devem apresentar alta afinidade, uniformidade, resistência aos agentes desbotantes e ainda serem economicamente viáveis.9,10 Corantes são substâncias extraídas de fontes naturais ou obtidas de maneira sintética, podendo ser classificados de acordo com a origem (orgânica ou inorgânica), com função de "colorir" substratos diversos. Essas substâncias podem ser diretamente aplicadas em tecidos, couro, papel, cabelo, etc. Dentre outras características, destacam-se a completa solubilidade no meio, tonalidades coloridas ou fluorescentes, a depender da estrutura do cromóforo principal, que conferem cor a um substrato através de processos absorção/reflexão de luz.11,12 No processo de tingimento de tecidos, diferentes tipos de corantes são usados, dependendo do tipo de fibra, do aspecto visual desejado e das condições de processamento. Os tipos de corantes mais utilizados nesse processo são classificados como reativos, básicos, ácidos, diretos, azo, sulfurizados e pré-metalizados.13 Os corantes azo (-N=N-) são considerados a maior classe de corantes sintéticos utilizados na fabricação têxtil, com uma taxa de perda de 10-15% durante o processo de tingimento.14 Durante o tingimento das roupas uma grande quantidade de corante é utilizada, juntamente com alguns sais (por exemplo, o sulfato básico de Cr3+, Cr(OH)SO4, para o processo de curtume),15 onde esses compostos iônicos aumentam a carga de poluentes e o tempo de descoloração, dificultando o tratamento final dos resíduos.13 Além disso, as águas residuais geradas podem estar em condições ácidas ou alcalinas, o que traz ainda mais desafios para os tratamentos realizados pelo setor têxtil.16 A utilização de corantes sintéticos pode acarretar riscos toxicológicos e danos ambientais, por isso diversos estudos vêm sendo desenvolvidos para identificação, quantificação e degradação desse tipo de poluente.17 As águas residuais da indústria incluem uma variedade de poluentes orgânicos e inorgânicos, tais como corantes e metais potencialmente tóxicos.18 Especificamente, os corantes orgânicos e pigmentos lançados pelo setor têxtil são considerados as principais fontes de poluentes, apresentando grandes riscos para os ecossistemas aquáticos. O aumento da matéria orgânica acarreta a redução dos níveis de oxigênio dissolvido, gerando toxicidade para a flora e fauna aquáticas.19,20 Além disso, a presença de corantes no corpo hídrico causa um bloqueio da incidência da luz solar e redução na transparência da água, o que interfere diretamente na fotossíntese.21,22 Os resíduos têxteis são enquadrados como uma ameaça a vida humana, pois são capazes de afetar o sistema imunológico e causar efeitos tóxicos e carcinogênicos. Por conseguinte, a remoção de contaminantes perigosos antes da sua descarga no meio ambiente constitui um desafio e uma prioridade global. Pelo fato dos corantes serem substâncias resistentes a algumas das técnicas convencionais de tratamento de efluentes industriais, métodos alternativos estão sendo investigados.23 O estado da arte traz processos convencionais de remoção de corantes, como a destilação, a filtração, floculação e coagulação, sendo amplamente utilizados no tratamento de águas residuais, mesmo apresentando desvantagens em seus métodos.24,25 Nos últimos anos, a separação por membranas tem atraído grande interesse na área do tratamento de águas residuais devido às suas vantagens, incluindo o baixo consumo de energia, a baixa toxicidade do material, a fácil reprodutibilidade da síntese, a elevada eficiência de separação e a facilidade de operação.26 Na separação por membranas, várias tecnologias de tratamento de efluentes têm sido desenvolvidas, como a microfiltração, a ultrafiltração, a nanofiltração e a osmose reversa.27 Especificamente, a tecnologia de nanofiltração é a ferramenta mais poderosa para separar moléculas de corantes orgânicos e minerais inorgânicos.28,29 Recentemente, os biopolímeros tornaram-se mais populares em aplicações de membranas devido à seu aspecto sustentável, baixo custo, atoxicidade, excelente capacidade de formação de filmes e fácil disponibilidade.30 Dentro desta lógica, a celulose bacteriana (CB) é pontuada como um biopolímero mais abundante constituído por unidades monoméricas de β-d-glicopiranose denominada celobiose, que é convertida em celulose polimérica, através da junção de unidades de glicose por β(1→4) ligações glicosídicas, gerando cadeias lineares não ramificadas, que se ligam através de forças de van der Waals e ligações de hidrogênio.31,32 A CB tem um enorme potencial para ser utilizada como um novo adsorvente para a separação eficaz de metais potencialmente tóxicos, devido às suas propriedades de elevada capacidade de retenção de água, rede de fibras finas, elevada resistência à tração mecânica, elevada pureza, flexibilidade, elasticidade, ausência de toxicidade e biocompatibilidade.33 Neste sentido, entende-se que para atender as necessidades crescentes da população, como a enorme demanda por água limpa, induziu a comunidade científica a pesquisar e desenvolver materiais baratos e eficientes para tratamento da água contaminada.34,35 Assim, o presente trabalho teve como objetivo investigar a capacidade adsorvente de um biomaterial frente a quatro corantes têxteis e posteriormente propor um processo térmico combinado que permita a recuperação dos corantes, através da calcinação em forno.
PARTE EXPERIMENTAL Reagentes Os reagentes e solventes utilizados apresentam grau analítico e foram utilizados sem prévia etapa de purificação. Os produtos químicos de partida foram ácido clorídrico 36,5% (Dinâmica), ácido nítrico 65% (Neon), ácido succínico 99% (Sigma-Aldrich), D-manitol 99% (Nuclear), extrato de levedura (Himidea), glicerol 99,5% (Dinâmica), hidróxido de sódio 99,8% (Neon), monohidrogenofosfato de sódio dodeca-hidratado 98,0% (Dinâmica) e peptona (Kasvi). Coleta de amostras e soluções de trabalho Todos os corantes têxteis foram adquiridos em um mercado local de lavandaria na cidade de Toritama, Pernambuco, Brasil, tendo como coordenadas geográficas 08º 00' 24" de latitude sul, 36º 03' 24" de longitude oeste, e altitude 349 m. A amostragem de cada corante foi realizada em triplicada, sendo codificadas de acordo com a Tabela 1. Para o preparo das soluções, as amostras de corantes têxteis foram submetidas a uma temperatura de 110 ºC por 12 h para secagem completa e resfriadas em um dessecador. A solução-estoque de cada corante foi preparada com uma concentração de 20,0 mg L-1, utilizando água destilada previamente fervida para retirar os gases do meio e evitar qualquer processo de oxidação indesejada e variação no pH do sistema. Para melhor conservação, todas as soluções de reserva foram armazenadas em frascos âmbar a ~ 5 ºC.
Metodologia de digestão das amostras Para a determinação do teor de metais em cada corante têxtil, uma quantidade de 1,0 g de cada amostra foi solubilizada e decomposta com água-régia (mistura de HCl:HNO3 (3:1)) em uma placa de aquecimento a 100 ºC durante 12 h. Posteriormente, as amostras foram deixadas em repouso até a temperatura ambiente. Por fim, as amostras foram filtradas e adicionadas a um balão volumétrico de 50 mL, e o volume foi aferido com solução de HNO3 a 5% (v/v). Produção de celulose bacteriana (CB) A produção de membrana bacteriana foi adaptada de um trabalho de referência.57 Foi utilizada a bactéria Komagataeibacter xylinus, tendo o glicerol como fonte de carbono. O meio de cultura foi produzido com 30 g L-1 de glicerol, 16 g L-1 de extrato de levedura, 5 g L-1 de peptona, 4 g L-1 de Na2HPO4, e 3,5 g L-1 de ácido succínico. A solução de nutrição foi distribuída em frascos de vidro borosilicato previamente autoclavados a 121 ºC por 15 min. Para a incubação, foram pipetados 5 mL de K. xylinus para meio Hestrin e Schramm (HS) por 48 h em condições estáticas a 30 ºC. Após a obtenção da membrana, a purificação foi realizada via imersão dos filmes em uma solução de NaOH 0,1 mol L-1, sob aquecimento a 80 ºC por 30 min. O processo foi repetido até o meio ficar neutro, pH 7,0. Instrumentação A microscopia eletrônica de varredura (MEV) da superfície da celulose foi realizada em um microscópio eletrônico de varredura (Tescan, MIRA 3) com uma tensão de aceleração de 20 kV e um detector de elétrons secundários Equations. O programa utilizado para medição da BC foi o ImageJ®, versão 1.51n (64-bit) de 2017, desenvolvido pela NIH® (EUA). O perfil vibracional dos grupos funcionais foi obtido pela técnica de espectroscopia vibracional com transformada de Fourier (FTIR) em um espectrofotômetro IR-TRACER-100 (Shimadzu®) utilizando-se pastilhas de KBr em uma faixa de 4000-400 cm-1. O comportamento de absorção foi analisado em um espectrofotômetro ultravioleta-visível (UV-Vis, Shimadzu®), modelo UV-1800 com uma cubeta de quartzo de 10 mm. O intervalo de trabalho foi delimitado entre 380-750 nm. A estabilidade térmica foi verificada no equipamento TGA 50 (Shimadzu®), utilizando atmosfera de N2, com um fluxo de 100 mL min-1 e rampa de aquecimento de 5 ºC min-1 até 800 ºC. O teor de metais foi analisado pela técnica de espectrometria de emissão óptica com plasma indutivamente acoplado (ICPOES). Análise multivariada Os resultados de caracterização química foram processados por análises estatísticas multivariadas por meio do software Minitab®, quanto à análise de componentes principais (PCA) e hierárquico (HCA). As análises estatísticas foram conduzidas usando dados obtidos pelos valores médios de absorbância e o teor de metais de todos os corantes. Um total de 10 amostras de corantes foram processadas utilizando análises quimiométricas. Os clusters foram criados a partir do agrupamento de variáveis de acordo com a cor específica e as concentrações de elementos, sendo contabilizados na forma gráfica bidimensional de PC1 vs. PC2. O programa utilizado foi o Minitab®, versão 19.1 (64-bit), 2019, desenvolvido pela LLC® (EUA). Estudos de estabilidade em função do meio e cinética de adsorção A estabilidade dos corantes têxteis foi avaliada a partir da resposta de absorbância em uma faixa de pH entre 3,0 a 11,0. Os 5,0 mL de solução estoque foram corrigidos com HCl 1,0/0,10 mol L-1 e NaOH 1,0/0,10 mol L-1 até atingir os valores de pH de interesse. O experimento de adsorção foi conduzido pela adição de ~ 100 mg de CB seca (por aproximadamente 6 h, até obter massa constante em estufa a 50 ºC), em forma de um quarto de círculo. A massa de CB foi mantida à temperatura ambiente, sob agitação constante e abrigo de luz em 20,0 mL das soluções estoque dos corantes avaliados. As amostras permaneceram sob agitação constante variando o tempo de contato de 0; 1; 2; 4; 8; 12; e 24 h. Em cada período, foram retirados 2,0 mL do sistema para análise de absorção eletrônica e devolvidos o mais rápido possível ao recipiente para evitar interferência na concentração da solução. O ensaio de adsorção foi realizado em triplicata, e a porcentagem de remoção do corante foi estimada pela Equação 1: 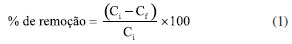 onde Ci representa a concentração inicial (mg L-1) dos corantes; Cf é igual a concentração (mg L-1) medida no intervalo definido. Outro parâmetro avaliado foi a quantidade de corante retido pelo adsorvente no equilíbrio, qe (mg g-1), em um tempo t, definido pela Equação 2: 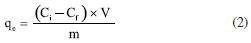 onde V representa o volume da solução (L), e m é a massa seca do adsorvente (g).
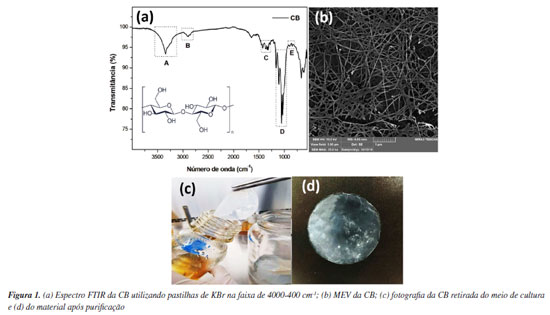
RESULTADOS E DISCUSSÃO Caracterização da CB O comportamento vibracional da CB foi investigado (Figura 1a). A banda A em 3344 cm-1 refere-se ao padrão de estiramento H-O, com um perfil bem conhecido de interação intermolecular entre os grupos hidroxila.57 O pico B em 2897 cm-1 é atribuído ao grupo metileno (-CH2-) presente na zona cíclica da estrutura da CB. O sinal C em 1361 cm-1 mostrou vibrações associadas a grupos metínicos (-CH-).58 Também foi observado que um pico D em 1161 cm-1 foi causado pelo estiramento assimétrico de -C-O-C- do tipo de ligação glicosídica (β1→4).59 Finalmente, em 1109 cm-1, o pico E atribuído à ligação -C-O presente na unidade mínima do polissacárido.60 Na Figura 1b as micrografias demonstram a morfologia caraterística da CB apresentada em microfibras.59 Tanto o tamanho quanto a largura foram medidos no programa ImageJ®, levando a uma ordem de tamanho de 15-42 nm para as fibras de CB. Vale ressaltar que a K. xylinus sintetiza fibras primárias com dimensões laterais na faixa de 7 a 13 nm, que podem se agregar em faixas finas e planas com sua largura chegando a 70 nm.61 O aspecto macroscópico da CB produzida é apresentado na Figura 1c, onde membranas circulares uniformes podem ser comprovadas na Figura 1d.
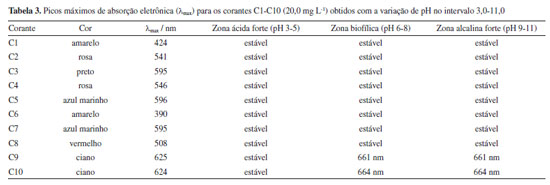
Composição química dos corantes têxteis Para a caraterização inicial dos dez corantes têxteis escolhidos para esta pesquisa, foi realizada a análise por ICP-OES para quantificar o teor de metais em cada amostra e verificar a autenticidade do tipo de corante adquirido no mercado de lavandaria, área apontada neste estudo. Na Tabela 2 estão resumidas as concentrações mais expressivas de metais nas espécies investigadas.
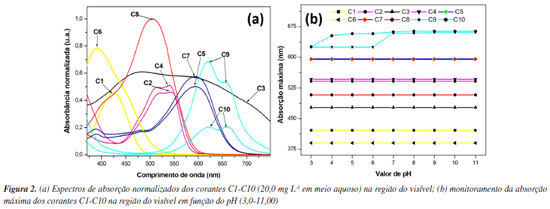
Os dados apresentados na Tabela 2 indicam a presença de alguns metais e metaloides potencialmente tóxicos,62 tais como As, Cu, Mo e Zn (C1, C9 e C10), que não deveriam estar na composição do corante têxtil orgânico de acordo com as informações do rótulo. Este tipo de contaminação pode ocorrer devido a alguns mecanismos, como um processo de purificação ineficiente da produção de corantes15 ou a reutilização negligente de recipientes para mistura de corantes primários afim de se obter diferentes tonalidades de pigmentos.63,64 O segundo mecanismo ocorre normalmente porque a prática de misturar corantes é a mais utilizada recorrentemente para obter tonalidades únicas brilhantes.65,66 O elevado teor de Cu nos corantes C9 e C10 é destacado mediante sua toxicidade em potencial, uma vez que o consumo recorrente de alimentos e água contaminados pode provocar efeitos secundários preocupantes.67 Já é relatado efeitos adversos como vômitos, arritmia, hipotensão, danos renais, hepatite aguda e sangramento gastrointestinal.68 A elevada concentração de Cu2+ também tem relação com a alopecia e diabetes69,70 e pode agravar diagnósticos clínicos críticos como a doença de Wilson.71,72 Para além do cobre, foram também detectados teores significativos de Mo nesta técnica, o que poderá ser explicado pela elevada afinidade entre estes dois elementos em minerais, por exemplo.73 A associação entre o cobre e o molibdênio ocorreu majoritariamente devido à sua afinidade e semelhança química nos minérios, o que os torna um subproduto de outro no processo de purificação industrial.74 Outra questão são os altos níveis de Na em todas as dez amostras, o que pode afetar a salinidade do corpo hídrico e desequilibrar os parâmetros naturais da água doce, causando danos à fauna nativa.75 A eliminação incorreta de efluentes ricos nestes tipos de contaminantes pode causar danos graves ao ambiente através da descarga de poluentes orgânicos e inorgânicos tóxicos na água.76,77 Espectroscopia de absorção eletrônica e análise de estabilidade com variação de pH As soluções-estoque (20,0 mg L-1) de C1-C10 foram submetidas à análise de absorção eletrônica em diferentes valores de pH e seus comprimentos de onda máximos foram definidos na Figura 2. Na etapa seguinte, foi estudada a estabilidade dos corantes têxteis em função do pH do sistema (Tabela 3).
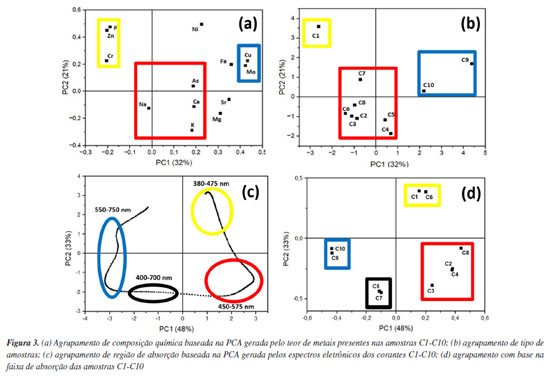
Este ensaio ajudou a compreender o comportamento químico da estrutura do corante e a estimar a possibilidade de rearranjo intramolecular promovido pela acidez da solução.78 Como podemos observar na Figura 2a, cada corante apresentou uma banda na região de sua repectiva coloração complementar, exceto o corante C3, que apresentou uma banda larga cobrindo todo o espectro visível. Os espectros de absorbância dos corantes orgânicos (C1-C8) apresentam transições causadas pelos principais grupos cromóforos nas estruturas químicas, tais como antraquinona,79 porfirina,80 azo81 e sistemas π hiperconjugados.82,83 Os corantes metalorgânicos C9 e C10 mostraram dois picos principais com a contribuição do Cu2+ preso no anel tipo porfirina por ligações coordenativas.84 Na Figura 2b é perceptível alterações na estrutura do pigmento metalorgânico quando a forma ácida é submetida a um meio fortemente alcalino. Este comportamento pode indicar que o íon cobre pode ser liberado na zona ácida (devido à protonação excessiva dos sítios básicos de nitrogênio) e mais facilmente lixiviado para o solo ou para a água quando erroneamente descartado.85 Esta evidência é uma informação crucial para a seleção da natureza do corante para os ensaios de adsorção, tendo em conta o perfil de contaminação bidirecional deste poluente antropogênico. Análise multivariada Com base nos dados extraídos das regiões de absorbância, estabilidade em pH variante e teor de metais quantificados na análise ICP-OES para os dez corantes, foi possível dividir as amostras em clusters menores devido à sua semelhança química e estatística. Foi organizado o agrupamento estatístico via análise de componetes principais (do inglês, principal component analysis - PCA) de acordo com as informações inicialmente disponíveis, como demonstrado na Figura 3.
A primeira conclusão desta abordagem matemática pode ser observada nas Figuras 3a e 3b, extraídas no ICPOES, que a composição química foi a principal responsável pelos critérios de classificação. Nos extremos, temos dois grupos associados à presença de Zn ou Cu/Mo de alguma forma. Os elementos restantes variaram igualmente para C1-C10. Os clusters demarcados na Figura 3b estão divididos pela sua toxicidade, em que C1 é a representação de um elevado nível de Zn para corantes amarelos,86 enquanto C9-C10 foram responsáveis por elevados níveis de Cu/Mo nos corantes azuis. A PCA da Figura 3c baseou-se na faixa de absorbância de cada corante têxtil, o que redimensionou o quantitativo de amostras a quatro grupos. A separação das amostras foi mais notável nessa segunda abordagem, comparada com a baseada no ICP-OES, gerando quatro grupos que foram melhor definidos entre si. Como podemos observar na Figura 3, os representantes dos pigmentos amarelos (C1) e azuis (C10) já haviam sido definidos, e agora foram instituídos representantes para os grupos pretos (C7) e o vermelhos (C8). A representatividade estatística desses corantes (C1, C7, C8 e C10) também é observada na natureza estrutural dos corantes. O efeito oposto na PC1 da Figura 3d distingue os sítios de cromóforos grandes, como a antraquinona e as ftalocianinas, dos aglomerados de corantes monoazo/diazo. Notou-se também que a classe dos corantes diretos (C3, C4 e C8) foi agrupada em um único grupo, para além dos pigmentos reativos. Após a PCA, o quantitativo de dez corantes foi reduzido a quatro grupos com cada representante (C1, C7, C8 e C10), devido à semelhança química e à minimização do número de ensaios, como uma vantagem das abordagens quimiométricas.87,88 Todos os quatro corantes escolhidos foram submetidos ao processo de tratamento por adsorção em CB para investigar o potencial de remoção deste biomaterial adsorvente como uma alternativa barata e viável para o tratamento de águas residuais em grande escala.85 Cinética de adsorção Com base no agrupamento estatístico, C1, C7, C8 e C10ácido e C10básico foram submetidos a testes de adsorção, conforme descrito na seção "Parte Experimental". Foi verificado no estudo de estabilidade, dentre os corantes representativos, que apenas o C10 apresenta sensibilidade química à variação do pH do meio, por esse motivo, sua cinética foi realizada tanto em zona alcalina forte (pH 11,0) como em zona ácida forte (pH 3,0) para posterior comparação em termos de otimização do processo de remoção. Os desempenhos de remoção de CB para C1, C7, C8 e C10ácido e C10básico são apresentados na Figura 4.
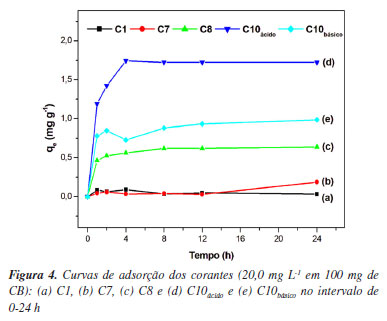
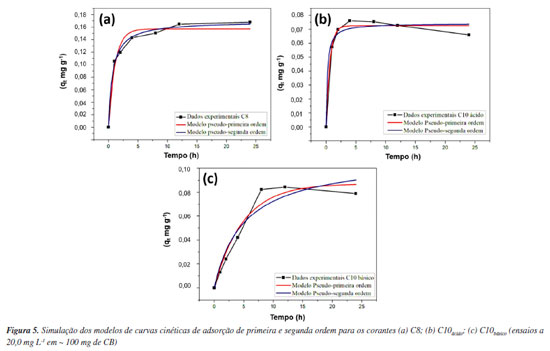
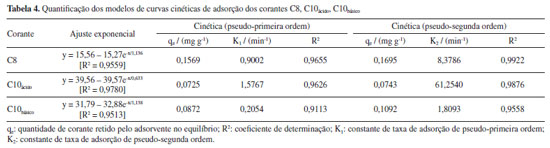
As Figuras 4a e 4b mostram que não houve afinidade química entre os corantes C1 e C7, e a CB para promover o tratamento hipotético das águas residuais. As quantidades de corante C1 e C7 adsorvidas foram inferiores a 0,1000 e 0,2000 mg g-1, repectivamente, por isso suas isotermas de adsorção foram desconsideradas. Os valores de qe oscilaram nos períodos iniciais, sem comportamento definido, o que indica os mecanismos de adsorção e dessorção simultâneos na superfície da CB, o que ilustra a baixa eficiência da membrana como agente purificador para esse dois analitos. Na Figura 4c é visível que o C8 teve melhor interação com a CB e não demonstrou um padrão de dessorção igual ao observado nos corantes anteriores. Até a completa saturação da CB, 16,61% do corante C8 foi extraído do sistema, atingindo um valor máximo de qe de 0,6368 mg g-1. Quando a CB foi empregada nos corantes da classe das ftalocianinas (C9-C10), observou-se o melhor desempenho de remoção dos poluentes têxteis. Em meio ácido (pH 3,0) foi observada uma eficácia de adsorção mais acentuada (43,09%), alcançando um valor de qe de 1,7234 mg g-1 em comparação com o ensaio realizado em solução alcalina (pH 11,0; 33,17%). A quantidade de material adsorvido no meio básico foi de apenas 0,9830 mg g-1 (33,17% remoção do corante), sendo indício do efeito direto da faixa de pH como uma otimização dos métodos para esta classe de corante. Outros pesquisadores89 também apontaram uma boa afinidade entre a CB e os pigmentos de ftalocianina em meio ácido. A importância do controle de pH é descrito em outros trabalhos90 como na adsorção semelhante de íons prata na quitina, onde maiores taxas de adsorção em pH 3,0 foram observados devido à natureza eletrostática do corante, que permite a interação com o solvente no meio ácido resfriado. Um ponto caraterístico observado é que o baixo valor de pH promove o aparecimento de cargas positivas na superfície do absorvente, o que possibilita um aumento na capacidade de adsorção para o corante analisado, pois o composto é aniônico.91 Os modelos matemáticos de isotermas de adsorção para os sistemas C8, C10ácido e C10básico são observados na Figura 5 e as quantificações das curvas estão presentes na Tabela 4.
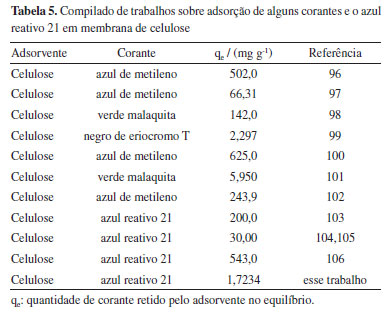
Os parâmetros cinéticos obtidos no processo de adsorção do corante representam regressões lineares nos gráficos de cada modelo, como indicado na Tabela 4. Desta maneira, a avaliação quantitativa dos modelos foi realizada por meio da comparação entre os coeficientes de correlação. Verifica-se na Tabela 4 uma boa concordância entre os resultados teóricos e os dados experimentais quando se aplica o modelo de pseudo-segunda ordem para as curvas com C8, C10ácido e C10básico. O melhor ajuste ao mecanismo de pseudo-segunda ordem vem a ser obtido quando a proximidade dos valores trazidos pelo coeficiente de determinação (R2) é de aproximadamente 1,0. Desta maneira, fica demonstrado que o mecanismo de difusão intrapartícula não deve ser considerada como etapa determinante da velocidade. Quando considerado dentro do processo de transferência de massa, outros mecanismos devem ser inseridos para determinar o processo de adsorção.92 Neste sentido, manipulando-se as isotermas de adsorção do sistema, são utilizadas as equações de Langumuir e Fraundlich.93 Logo, os valores obtidos experimentalmente e as curvas que foram alcançadas foram vistas por meio dos valores estimados nas equações. As isotermas de equilíbrio apresentaram curva sigmoidal, onde é esperado uma monocamada de analito sobre a superfície do adsorvente, aumentando a afinidade da adsorção à medida em que se aumenta a concentração do adsorbato até a saturação.94 Ao analisar a Figuras 5b e 5c, pode ser observado que para C10, independentemente do meio, o perfil da isoterma aproxima-se do modelo de pseudo-segunda ordem, pois seu R2 modela o gráfico de forma a se assemelhar a equação logarítmica desse modelo. Verificou-se também que a adsorção segue o modelo de pseudo-segunda ordem devido a heterogeneidade da CB, confirmando que o controle do mecanismo de velocidade é a adsorção química (reação química).95 Para melhor ilustar o desempenho da CB na remoção de corantes têxteis, diversos trabalhos foram agrupados na Tabela 5. Ao comparar os melhores valores de adsorção entre as três isotermas de C8 e C10, o volume adsorvido pelo método do C10ácido é o que foi escolhido para comparação com a literatura, devido a sua performance superior aos demais tratamentos. Os resultados de qe (1,7234 mg g-1) são inferiores aos presentes na Tabela 5, mas não inviabiliza sua aplicação na adsorção de corantes. Os ensaios preliminares não consideram a otimização dos parâmetros reacionais (concentração do analito/tempo reacional/temperatura), nem propriedades morfológicas do material como área superficial, tamanho de poros, definição do ponto de carga zero ou qualquer tipo de modificação química na estrutura da celulose. Desta forma, os resultados obtidos ainda podem ser melhorados considerando experimentos em maiores escalas, estudo de ciclos de adsorção e dessorção.95
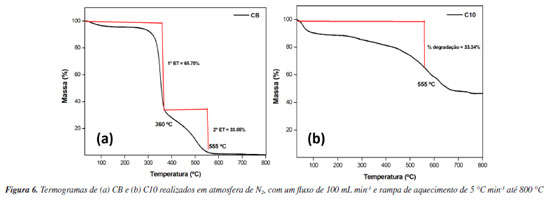
Avaliação térmica da CB e dos corantes têxteis A CB isolada e o C10 foram submetidos à avaliações térmicas afim de compreender a estabilidade de degradação de cada espécie e desta forma propor um processo de recuperação parcial de corantes presentes em águas residuais têxteis. A razão para a seleção do C10 como modelo inicial baseou-se na sua melhor taxa de adsorção e maior valor de qe na abordagem de tratamento com a CB. Os termogramas da CB e C10 são ilustrados na Figura 5. A Figura 6a ilustra o comportamento térmico da CB, onde são destacados dois eventos térmicos (ET) principais, relacionados com a degradação quase completa do polissacarídio a temperatura > 500 ºC.107
Como visto na Figura 6a a CB sofre o primeiro evento de degradação a 360 ºC, onde é perdido 65,75% de massa da membrana. Na temperatura de 555 ºC ocorre o segundo ET, sendo o biopolímero totalmente degradado. Ao comparar a faixa térmica de degradação da CB com os valores observados para o C10 na Figura 6b, constata-se que a temperatura de 555 ºC provoca uma perda em massa de apenas 33,34% do conteúdo do corante. Essa estabilidade térmica superior à CB demostra que o corante têxtil, devido à estabilidade do grupo porfirina, é mais estável termicamente108 do que o bioadsorvente. Com base nessas carcaterísticas, seria possível recuperar uma fração do corantes após um processo de secagem na membrana empregnada, seguido de calcinação em faixas superiores a 555 ºC. Proposta de recuperação de corantes têxteis utilizando a CB Ao considerar o processo de tratamento de efluentes têxteis com CB em larga escala, uma nova estratégia poderia ser empregada como ferramenta do desenvolvimento de pesquisas sustentáveis. Com base na estratégia descrita poderia ser gerado um quantitavo de "cinzas" contendo o próprio corante, ou fragmentos do mesmo, trazendo em sua composição os metais potencialmente tóxicos de volta ao ciclo de produção. Uma aplicação destes resíduos de calcinação poderia ocasionar a produção de um novo "corante ecológico", contendo a substância pura junto com os resíduos metálicos na forma de aditivos. Essa proposta traz uma nova discussão sobre o uso de resíduos industriais e no ramo da pesquisa e desenvolvimento no setor de tintas e pigmentos. Hipoteticamente, o montante de CB empregnado de corantes poderia ser acoplado a um forno de energia solar, após etapa de tratamento do efluente, onde o sistema "CB + corante" seria calcinado a temnperatura > 555 ºC visando a completa degradação do polímero e recuperação significativa do poluente. Uma vez isolado, os "resíduos coloridos" podem ser aplicados em uma proporção percentual específica com o próprio pigmento novo (Figura 7).
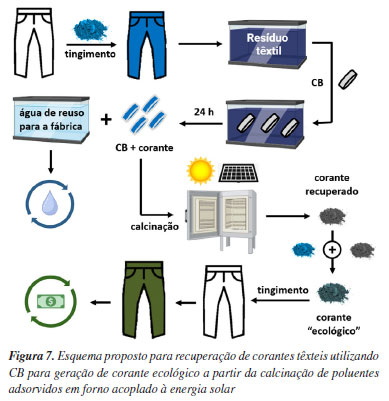
Assim, destaca-se a possibilidade de após a etapa de remoção de corantes pelas características do adsorvente CB, tendo em conta o enorme volume diário de águas residuais e lodo produzidas pela indústria têxtil, será possível recuperar uma quantidade expressiva de corante a partir do uso de energia limpa e renovável, com forno solares, podendo tornar o processo de tingimento mais barato e reduzindo a liberação de metais potencialmente tóxicos no meio ambiente.
CONCLUSÕES Entre todos os tipos de tratamento de águas residuais, a abordagem combinada bio-físico-química tem sido uma ótima metodologia para resíduos têxteis em grande escala. Neste trabalho, foi sintetizada com sucesso uma membrana de CB produzida à base de glicerol, demostrando ser um processo barato, atóxico, reprodutível e versátil para remover eficientemente corantes de corpos aquáticos. Como observado pelas análises, o uso de CB permitiu uma boa taxa de adsorção (qe = 1,7234 mg g-1) para ftalocianinas em comparação a não-afinidade com corantes da classe antraquinona e azo. A avaliação térmica do sistema "CB + corante" forneceu uma perspectiva de um processo de recuperação para a obtenção de parte do pigmento dissolvido nas águas residuais. Esta evidência serviu com base no projeto de uma tecnologia sustentável para tornar o processo industrial de tingimento de roupa mais barato e reduzir consideravelmente a emissão de poluentes tóxicos para o meio ambiente. Novas perspectivas, como a proposta de um centro de tratamento de efluentes e lodo têxtil através de calcinação em forno solar, podem ser viáveis pois, ao investir em tecnologias de energias renováveis, as indústrias não apenas economizam custos operacionais, mas também são direcionadas para a preservação do meio ambiente, garantindo um futuro mais limpo e verde para as gerações futuras.
MATERIAL SUPLEMANTAR O material suplementar desse trabalho está disponível em http://quimicanova.sbq.org.br/, na forma de arquivo PDF, com acesso livre.
AGRADECIMENTOS Os autores agradecem aos órgãos de fomento como à Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES), à Fundação de Amparo à Pesquisa do Estado de Pernambuco (FACEPE) e o Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq). As saudações se estendem aos Laboratório de Medicamentos, Tecnologias, Energia e Soluções Ambientais (LaMTESA) e Centro de Apoio à Pesquisa (CENAPESQ) da UFRPE.
REFERÊNCIAS 1. Associação Brasileira da Indústria Têxtil e de Confecção (ABIT), Perfil do Setor: Dados Gerais do Setor Atualizados em 2024, Referentes ao Ano de 2023 (estimativa), https://www.abit.org.br/cont/perfil-do-setor, acessado em Abril 2025. 2. Associação das Empresas de Limpeza Pública e Resíduos Especiais (ABRELPE); Panorama dos Resíduos Sólidos no Brasil 2022; ABRELPE: São Paulo, 2022. [Link] acessado em Abril 2025 3. Kant, R.; Nat. Sci. 2012, 4, 22. [Crossref] 4. Bilińska, L.; Gmurek, M.; Water Resour. Ind. 2021, 26, 100160. [Crossref] 5. Rocha, R. M.; da Silva Júnior, L. H.; Viana, J. A. B.; Gestão e Desenvolvimento em Revista 2015, 1, 50. [Link] acessado em Abril 2025 6. Silva, F. F.; Feitosa, M. G. G.; Aguiar, V. S. M.; Revista de Administração Mackenzie 2012, 13, 206. [Link] acessado em Abril 2025 7. Santos, B. B.; Vasconcelos, V. M.; Contemporânea 2018, 8, 289. [Crossref] 8. de Amorim, J. F. O.; dos Prazeres, R. V.; dos Santos, C.; Revista Economia Política do Desenvolvimento 2017, 3, 39. [Crossref] 9. Guaratini, C. C. I.; Zanoni, M. V. B.; Quim. Nova 2000, 23, 71. [Crossref] 10. Muthukumar, M.; Selvakumar, N.; Dyes Pigm. 2004, 62, 221. [Crossref] 11. Benkhaya, S.; El Harli, S.; El Herli, A.; Applied Journal of Environmental Engineering Science 2017, 3, 311. [Crossref] 12. Alegbe, E. O.; Uthman, T. O.; Heliyon 2024, 10, e33646. [Crossref] 13. Benkhaya, S.; M' rabet, S.; El Harfi, A.; Inorg. Chem. Commun. 2020, 115, 107891. [Crossref] 14. Sarkar, S.; Banerjee, A.; Halder, U.; Biswas, R.; Bandopadhyay, R.; Water Conservation Science and Engineering 2017, 2, 121. [Crossref] 15. Zanoni, M. V. B.; Yanamaka, H. Em Corantes: Caracterização Química, Toxicológica, Métodos de Detecção e Tratamento; Zanoni, M. V. B.; Yanamaka, H., eds.; Cultura Acadêmica: São Paulo, 2016. 16. Leaper, S.; Abdel-Karim, A.; Gad-Allah, T. A.; Gorgojo, P.; Chem. Eng. J. 2019, 360, 1330. [Crossref] 17. Foguel, M. V.; Pedro, N. T. B.; Wong, A.; Khan, S.; Zanoni, M. V. B.; Sotomayor, M. P. T.; Talanta 2017, 170, 244. [Crossref] 18. Afroze, S.; Sen, T. K.; Water, Air, Soil Pollut. 2018, 229, 225. [Crossref] 19. Choudhary, M.; Kumar, R.; Neogi, S.; J. Hazard. Mater. 2020, 392, 122441. [Crossref] 20. Varjani, S.; Rakholiya, P.; Ng, H. Y.; You, S.; Teixeira, J. A.; Bioresour. Technol. 2020, 314, 123728. [Crossref] 21. Huang, J.; Zhang, K.; Desalination 2011, 282, 19. [Crossref] 22. Malik, A.; Grohmann, E.; Akhtar, R. Em Environmental Deterioration and Human Health; Malik, A.; Grohmann, E.; Akhtar, R., eds.; Springer Dordrecht: New York, 2014. [Link] acessado em April 2025 23. Colindres, P.; Yee-Madeira, H.; Reguera, E.; Desalination 2010, 258, 154. [Crossref] 24. Zhou, S.; Feng, X.; Zhu, J.; Song, Q.; Yang, G.; Zhang, Y.; Van der Bruggen, B.; J. Membr. Sci. 2021, 623, 119058. [Crossref] 25. Zhao, P.; Li, R.; Wu, W.; Wang, J.; Liu, J.; Zhang, Y.; Composites, Part B 2019, 176, 107208. [Crossref] 26. Liu, Y.; Zhang, X.; Lemanski, S.; Nezhad, H. Y.; Ayre, D.; Int. J. Fatigue 2019, 125, 47. [Crossref] 27. Liu, Y.; Gan, D.; Chen, M.; Ma, L.; Yang, B.; Li, L.; Zhu, M.; Tu, W.; Sep. Purif. Technol. 2020, 253, 117552. [Crossref] 28. Long, Q.; Zhang, Z.; Qi, G.; Wang, Z.; Chen, Y.; Liu, Z. Q.; ACS Sustainable Chem. Eng. 2020, 8, 2512. [Crossref] 29. Hu, J.; Li, M.; Wang, L.; Zhang, X.; J. Membr. Sci. 2021, 540, 27. [Crossref] 30. Russo, F.; Galiano, F.; Iulianelli, A.; Basile, A.; Figoli, A.; Fuel Process. Technol. 2021, 213, 106643. [Crossref] 31. Feng, Q. M.; Feng, B.; Lu, Y. P.; Trans. Nonferrous Met. Soc. China 2013, 23, 237. [Crossref] 32. Santos, S. M.; Carbajo, J. M.; Quintana, E.; Ibarra, D.; Gomez, N.; Ladero, M.; Eugenio, M. E.; Villar, J. C.; Carbohydr. Polym. 2015, 116, 173. [Crossref] 33. Souto, T. J. M. P.; Moraes, A. S.; dos Santos Junior, O. P.; de Holanda, R. M.; de Araújo, A. L. S.; Santos, B. S.; de Medeiros, R. M.; Int. J. Sci. Res. Methodol. 2022, 22, 12. [Link] acessado em Abril 2025 34. Puri, C.; Sumana, G.; Appl. Clay Sci. 2018, 166, 102. [Crossref] 35. Seliem, M. K.; Barczak, M.; Anastopoulos, I.; Giannakoudakis, D. A.; Nanomaterials 2020, 10, 684. [Crossref] 36. Guzel, M.; Ak, M.; Org. Electron. 2019, 75, 105436. [Crossref] 37. Nath, K.; Patel, T. M.; Dave, H. K.; Journal of Water Process Engineering 2016, 9, e27. [Crossref] 38. Younes, H.; El-Etriby, H. K.; Mahanna, H.; Int. J. Environ. Sci. Technol. 2022, 19, 5659. [Crossref] 39. Asghari, A.; Dalvand, S.; Miresmaeili, M. S.; Khoramjah, F.; Omidvar, M.; Kambarani, M.; Int. J. Hydrogen Energy 2023, 48, 9776. [Crossref] 40. Moslehnejad, N.; Jahangiri, M.; Vafaee, F.; Salavati-Niasari, M.; Int. J. Hydrogen Energy 2022, 47, 23980. [Crossref] 41. Menezes, O.; Brito, R.; Hallwass, F.; Florêncio, L.; Kato, M. T.; Gavazza, S.; Chem. Eng. Res. Des. 2019, 146, 369. [Crossref] 42. Carvalho, J. R. S.; Amaral, F. M.; Florencio, L.; Kato, M. T.; Delforno, T. P.; Gavazza, S.; Chemosphere 2020, 242, 125157. [Crossref] 43. de Souza, E. J.; Neves, N. S. C. S.; Gomes, R. K. M.; Santos Júnior, S. G.; Charamba, L. V. C.; Campos, N. F.; Napoleão, D. C.; Water Sci. Technol. 2020, 82, 1327. [Crossref] 44. Chaouch, S.; Moussa, A.; Marzoug, I. B.; Ladhari, N.; Color Res. Appl. 2019, 44, 556. [Crossref] 45. Lai, K. C.; Lee, L. Y.; Hiew, B. Y. Z.; Yang, T. C. K.; Pan, G. T.; Thangalazhy-Gopakumar, S.; Gan, S.; J. Taiwan Inst. Chem. Eng. 2020, 114, 57. [Crossref] 46. Alaguprathana, M.; Poonkothai, M.; Ameen, F.; Bhat, S. A.; Mythili, R.; Sudhakar, C.; Environ. Res. 2022, 214, 113859. [Crossref] 47. Aquino, J. M.; Irikura, K.; Rocha-Filho, R. C.; Bocchi, N.; Biaggio, S. R.; Quim. Nova 2010, 33, 2124. [Crossref] 48. Mansouriieh, N.; Sohrabi, M. R.; Vajargah, R. P.; Roudbaraki, H.; Water Sci. Technol. 2017, 76, 1992. [Crossref] 49. Yazdanbakhsh, M.; Tavakkoli, H.; Hosseini, S. M.; Desalination 2011, 281, 388. [Crossref] 50. Khosravi, I.; Yazdanbakhsh, M.; Eftekhar, M.; Haddadi, Z.; Mater. Res. Bull. 2013, 48, 2213. [Crossref] 51. Lucilha, A. C.; Bonancêa, C. E.; Barreto, W. J.; Takashima, K.; Spectrochim. Acta, Part A 2010, 75, 389. [Crossref] 52. Fathi, M. R.; Asfaram, A.; Farhangi, A.; Spectrochim. Acta, Part A 2015, 135, 364. [Crossref] 53. Melo, R. P. F.; Barros Neto, E. L.; Nunes, S. K. S.; Castro Dantas, T. N.; Dantas Neto, A. A.; Sep. Purif. Technol. 2018, 191, 161. [Crossref] 54. Qiu, J.; Wang, H.; Du, Z.; Cheng, X.; Liu, Y.; Wang, H.; J. Appl. Polym. Sci. 2018, 135, 46298. [Crossref] 55. Ahmed, S.; Oumezzine, M.; Hlil, E. K.; J. Mol. Struct. 2021, 1235, 130262. [Crossref] 56. Atrak, K.; Ramazani, A.; Fardood, S. T.; Environ. Technol. 2020, 41, 2760. [Crossref] 57. Jin, Y. H.; Lee, T.; Kim, J. R.; Choi, Y. E.; Park, C.; J. Ind. Eng. Chem. 2019, 75, 158. [Crossref] 58. Quintana-Quirino, M.; Morales-Osorio, C.; Vigueras-Ramírez, G.; Vázquez-Torres, H.; Shirai, K.; Process Biochem. 2019, 82, 1. [Crossref] 59. Taokaew, S.; Nakson, N.; Thienchaimongkol, J.; Kobayashi, T.; J. Biosci. Bioeng. 2023, 135, 71. [Crossref] 60. Souza, E. F.; Furtado, M. R.; Carvalho, C. W. P.; Freitas-Silva, O.; Gottschalk, L. M. F.; Int. J. Biol. Macromol. 2020, 146, 285. [Crossref] 61. Keshk, S. M. A. S.; Carbohydr. Polym. 2014, 99, 98. [Crossref] 62. Ahmed, M. A.; Mohamed, A. A.; Inorg. Chem. Commun. 2023, 148, 110325. [Crossref] 63. Dehnavi, E.; Shams-Nateri, A.; Khalili, H.; Pigm. Resin Technol. 2016, 45, 52. [Crossref] 64. Bafrooei, F. K.; Khalili, H.; Safi, M.; Indian J. Fibre Text. Res. 2018, 43, 112. [Link] acessado em Abril 2025 65. Zhang, H.; Yang, H.; Xie, K.; Hou, A.; Gao, A.; Dyes Pigm. 2018, 159, 576. [Crossref] 66. Kim, K. R.; Ng, F.; Zhou, J.; Hu, J.; Text. Res. J. 2019, 89, 87. [Crossref] 67. Pal, A.; Prasad, R.; BioMetals 2015, 28, 1. [Crossref] 68. Sailer, J.; Nagel, J.; Akdogan, B.; Jauch, A. T.; Engler, J.; Knolle, P. A.; Zischka, H.; Redox Biol. 2024, 75, 103256. [Crossref] 69. Anant, J. K.; Inchulkar, S. R.; Bhagat, S.; European Journal of Pharmaceutical and Medical Research 2018, 5, 232. [Link] acessado em Abril 2025 70. Rahimzadeh, M. R.; Rahimzadeh, M. R.; Kazemi, S.; Moghadamnia, A. A.; Advances in Public Health 2024, 2024, 6001014. [Crossref] 71. Schilsky, M. L.; Clinics in Liver Disease 2017, 21, 755. [Crossref] 72. Aggarwal, A.; Bhatt, M.; Curr. Opin. Neurol. 2020, 33, 534. [Crossref] 73. Berzina, A. N.; Berzina, A. P.; Gimon, V. O.; Minerals 2016, 6, 1. [Crossref] 74. Orrego, P.; Hernández, J.; Reyes, A.; Hydrometallurgy 2019, 184, 116. [Crossref] 75. Lu, M.; Su, M.; Liu, N.; Zhang, J.; Fish Shellfish Immunol. 2022, 124, 401. [Crossref] 76. Zeng, X.; Zhang, G.; Wen, J.; Li, X.; Zhu, J.; Wu, Z.; Chemosphere 2023, 318, 137869. [Crossref] 77. Tanveer, K.; Mahmood, M. S.; Ashraf, M.; Khan, A.; Pak. J. Zool. 2022, 54, 2381. [Crossref] 78. Patil, A. R.; Shastri, L. A.; Tilakraj, T. S.; Inamdar, S. R.; Shastri, S. L.; Hebbar, N. U.; Pawar, V.; Sunagar, V. A.; J. Mol. Struct. 2022, 1254, 132363. [Crossref] 79. Deng, Y.; Ye, D.; Guo, Y.; Zhou, G.; Jiang, H.; Frontiers in Physics 2021, 9, 1. [Crossref] 80. Atav, R.; Çağman, F. N.; Şahin, H.; Çolakoğlu, Ö.; J. Nat. Fibers 2022, 19, 15882. [Crossref] 81. Güneş, Y.; Atav, R.; Namırtı, O.; Text. Res. J. 2012, 82, 994. [Crossref] 82. Martins, G. B. C.; Sucupira, R. R.; Suarez, P. A. Z.; Rev. Virtual Quim. 2015, 7, 1508. [Crossref] 83. Yahya, M.; Nural, Y.; Seferoğlu, Z.; Dyes Pigm. 2022, 198, 109960. [Crossref] 84. El Aggadi, S.; Kaichouh, G.; El Abbassi, Z.; Cherkaoui, O.; Mohammed, F.; El Hourch, A.; Mater Today: Proc. 2021, 45, 7278. [Crossref] 85. El Aggadi, S.; El Hourch, A.; Pol. J. Environ. Stud. 2021, 30, 3425. [Crossref] 86. Ilgün, C.; Sevim, A. M.; Çakar, S.; Özacar, M.; Gül, A.; Sol. Energy 2021, 218, 169. [Crossref] 87. da Costa, H. C.; Pereira, S. D. F. P.; Santos, L. P.; de Oliveira, A. F. S.; Silva, T. D. M.; Silva, C. S.; Rocha, R. M.; Freitas, K. H. G.; dos Santos, D. C.; Cruz, E. S.; ACS Omega 2020, 5, 32899. [Crossref] 88. Lubes, G.; Goodarzi, M.; Chem. Rev. 2017, 117, 6399. [Crossref] 89. Aydın, N.; Cıfcı, D. I.; Gunes, E.; Gunes, Y.; Atav, R.; J. Text. Inst. 2022, 114, 1301. [Crossref] 90. Longhinotti, E.; Pozza, F.; Furlan, L.; Sanchez, M. N. M.; Klug, M.; Laranjeira, M. C. M.; Fávere, V. T.; J. Braz. Chem. Soc. 1998, 9, 435. [Crossref] 91. Mall, I. D.; Srivastava, V. C.; Agarwal, N. K.; Dyes Pigm. 2006, 69, 210. [Crossref] 92. Alafnan, S.; Awotunde, A.; Glatz, G.; Adjei, S.; Alrumaih, I.; Gowida, A.; J. Pet. Sci. Eng. 2021, 207, 109172. [Crossref] 93. Ghosal, P. S.; Gupta, A. K.; J. Mol. Liq. 2017, 225, 137. [Crossref] 94. Giles, C. H.; Smith, D.; J. Colloid Interface Sci. 1974, 47, 755. [Crossref] 95. Girish, C. R.; International Journal of Civil Engineering and Technology 2017, 8, 80. [Link] acessado em Abril 2025 96. Abou-Zeid, R. E.; Salama, A.; Al-Ahmed, Z. A.; Awwad, N. S.; Youssef, M. A.; Cellul. Chem. Technol. 2020, 54, 237. [Link] acessado em Abril 2025 97. Yuan, J.; Yi, C.; Jiang, H.; Liu, F.; Cheng, G. J.; ACS Appl. Polym. Mater. 2021, 3, 699. [Crossref] 98. Chinthalapudi, N.; Kommaraju, V. V. D.; Kannan, M. K.; Nalluri, C. B.; Varanasi, S.; Carbohydr. Polym. Technol. Appl. 2021, 2, 100098. [Crossref] 99. Mokhtari, A.; Sabzi, M.; Azimi, H.; Carbohydr. Polym. 2021, 265, 118075. [Crossref] 100. Abouzeid, R. E.; Owda, M. E.; Dacrory, S.; J. Appl. Polym. Sci. 2022, 139, 1. [Crossref] 101. Radoor, S.; Karayil, J.; Jayakumar, A.; Parameswaranpillai, J.; Siengchin, S.; J. Polym. Environ. 2021, 29, 2126. [Crossref] 102. Qiao, H.; Zhou, Y.; Yu, F.; Wang, E.; Min, Y.; Huang, Q.; Pang, L.; Ma, T.; Chemosphere 2015, 141, 297. [Crossref] 103. Hu, D.; Wang, P.; Ma, Q.; Wang, L.; Desalin. Water Treat. 2016, 57, 10604. [Crossref] 104. Kobya, M.; Dolaz, M.; Goren, A. Y.; J. Chromatogr. A 2024, 1715, 464631. [Crossref] 105. Kale, R. D.; Potdar, T.; Gorade, V.; Sustainable Environ. Res. 2019, 29, 7. [Crossref] 106. Ma, Q.; Wang, L.; J. Taiwan Inst. Chem. Eng. 2015, 50, 229. [Crossref] 107. de Jesus, L. C. C.; da Luz, S. M.; Leão, R. M.; Zattera, A. J.; Amico, S. C.; Rev. Mater. 2019, 24, 1. [Crossref] 108. Zhu, S. E.; Yang, W. J.; Zhou, Y.; Pan, W. H.; Wei, C. X.; Yuen, A. C. Y.; Chen, T. B. Y.; Yeoh, G. H.; Lu, H. D.; Yang, W.; Chem. Eng. J. 2022, 442, 136367. [Crossref]
Editor Associado responsável pelo artigo: Cassiana C. Montagner |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access