Artigo
|
|
| Processo de hidrometalurgia para extração de CuII presente em placas de circuito impresso utilizando peróxido de hidrogênio e ácidos como agente lixiviantes Hydrometallurgy process for extraction of copper present in printed circuit boards using hydrogen peroxide and acids as leaching agents |
|
Camila Ferreira PintoI; Eduarda Maia GuimarãesII; Marquele Amorim TonhelaI; Sandra Cristina DantasII; Ana Claudia Granato MalpassII; Geoffroy Roger Pointer MalpassI,II,* I. Programa de Pós-Graduação Multicêntrico em Química (PPGMQ-MG), Universidade Federal do Triângulo Mineiro, 38064-200 Uberaba - MG, Brasil Recebido: 19/02/2025 *e-mail: geoffroy.malpass@uftm.edu.br With the increasing use of electronic devices and the reduction of their useful life, the generation of electronic waste has grown significantly. This study investigates the hydrometallurgical process of copper extraction from computer printed circuit boards, using hydrochloric acid and hexafluorosilicic acid, combined with hydrogen peroxide, as leaching agents. The process optimization was performed using response surface methodology, evaluating the influence of variables such as hydrochloric acid concentration, temperature and volume of hexafluorosilicic acid. Two factorial designs were conducted to analyze the significance of the variables. Temperature showed a positive influence, being fixed at 40 ºC in the subsequent experiments. Hydrochloric acid concentration was identified as the most significant variable, with high extraction rates associated with higher concentrations of H3O+ ions. Using 3 mol L-1 of hydrochloric acid, 17.7 mL of hexafluorosilicic acid and 20 mL of hydrogen peroxide, an extraction of 58.3% of copperII ions was obtained in relation to the theoretical concentration present in the samples. Additionally, the leaching reaction generated pure hydrogen gas, according to gas chromatography analysis. INTRODUÇÃO Lixo eletrônico é qualquer tipo de equipamento eletroeletrônico (EEE) não funcional, quebrado ou descartado, como resíduo, sem a intenção de reciclar.1-3 Ele pode ser dividido em várias classificações, e entre elas se encontra a placa de circuito impresso (PCI). As placas de circuito impresso tornam-se resíduos quando dispositivos eletrônicos chegam ao fim de sua vida útil.4,5 Estão presentes em geladeiras, máquinas de lavar, TVs, computadores, telefones celulares, CD/DVD players, rádios, câmeras, entre outros.6,7 Com o ritmo acelerado das inovações e com a frequência de substituição desses equipamentos, as PCIs tornaram-se um dos fluxos de resíduos que mais crescem no mundo.8 As PCIs possuem alta concentração de metais comuns (cobre, zinco, chumbo, arsênio, mercúrio, cromo, cádmio e paládio) e preciosos (ouro, prata e platina), sendo o CuII o metal mais abundante, como também contêm diferentes elementos perigosos e componentes químicos complexos, como retardadores de chama bromados (BFR) e clorofluorcarbonetos (CFC).2,9 Assim, os resíduos de PCIs são uma fonte de mineração urbana economicamente atraente para reciclagem, devido ao alto teor de metais, muitas vezes maior do que seus respectivos recursos primários, que são os minérios destinados à metalurgia.1 Além disso, quando essas placas não são recicladas de maneira ambientalmente correta, representam um grave perigo para o ecossistema durante o tratamento convencional em aterros e com incineração.4 De acordo com o último Relatório Global do Lixo Eletrônico (Global E-waste Monitor),10 publicado em 2024, o mundo produziu 62 milhões de toneladas de lixo eletrônico em 2022, o que equivale a 7,8 kg por pessoa, dos quais 13,8 milhões de toneladas representam uma taxa global de coleta e reciclagem formalmente documentada de 22,3%. O início do monitoramento global por esses relatórios foi em 2014, quando foram gerados 44,4 milhões de toneladas, e então a geração global cresceu 9,2 milhões de toneladas em 5 anos, com uma produção de lixo eletrônico de 53,6 milhões de toneladas em 2019, enquanto que em apenas três anos, de 2019 a 2022, houve um crescimento da geração de lixo eletrônico de 8,4 milhões de toneladas. Além disso, em 2019, apenas 17,4% do total de lixo gerado foi corretamente coletado, documentado e reciclado.1 Apesar da taxa de coleta e reciclagem ter aumentado cerca de 5% entre 2019 e 2022, ela ainda não acompanha a taxa de crescimento do lixo eletrônico mundial. Logo, para a sustentabilidade a longo prazo é necessário o estudo de novas tecnologias de reciclagem de resíduos de PCIs, que considerem sua complexidade e heterogeneidade, já que possuem uma composição pouco estável, pois a concentração de metais varia entre uma placa e outra, em função do tipo de aparelho eletroeletrônico.5 Além disso, a presença de plásticos, cerâmicas e numerosos elementos metálicos leva à dificuldade na liberação e separação de cada fração, como também deixa o processo de recuperação muito complexo, principalmente quando estão presentes em concentrações muito baixas.4 Esse artigo tem como objetivo estudar o processo hidrometalúrgico de extração de CuII; presente em PCIs de computadores, utilizando como agentes lixiviantes, ácido clorídrico e ácido hexafluorossilícico em conjunto com peróxido de hidrogênio. Para isso, foi realizada a otimização do processo em relação à solução proposta, e às condições operacionais para obter maior extração de CuII da amostra de PCIs, como também, foi analisada a possibilidade de produzir gás hidrogênio por meio dessa reação de lixiviação.
PARTE EXPERIMENTAL Pré tratamento das placas de circuito impresso Foram utilizadas PCIs obsoletas de computadores de mesa que seriam descartados (Figura 1), sendo então chamadas de resíduos de PCIs de computadores. Essas placas foram doadas ao Laboratório de Processos Químicos, Tecnológicos e Ambientais pelo Instituto Agronelli de Desenvolvimento Social com sede em Uberaba-MG.

O pré-tratamento é composto por várias etapas, conforme apresentado na Figura 2.
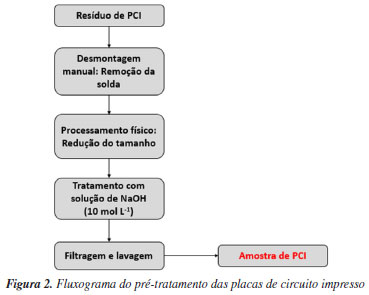
A primeira etapa consiste na remoção manual dos componentes eletrônicos com a utilização de um soprador térmico (T > 300 ºC), um alicate de bico curvo e uma morsa de bancada, para que a superfície fique lisa e os componentes sejam descartados da forma correta. Foi utilizado um soprador, pois a solda quando exposta ao calor funde-se, facilitando a retirada dos componentes. Em seguida, foi realizado o corte em tiras dessas placas usando uma serra de fita de bancada, da marca Lynus, modelo Hobby SFM-250. E por fim, as tiras de placas foram cortadas em quadrados e reduzidas a tamanhos menores que 2 mm, com a utilização de alicates de corte (Figura 3).

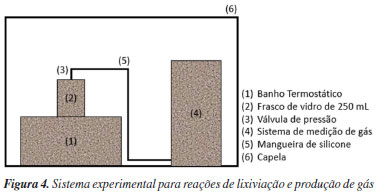
Antes de iniciar os processos de lixiviação, as placas cortadas foram submetidas a um banho com solução de hidróxido de sódio (10 mol L-1 NaOH) por 24 h. Essa etapa de pré-tratamento com NaOH tem por finalidade dissolver a camada de resina epóxi e remover contaminantes orgânicos da superfície das placas, expondo completamente os metais para a reação de lixiviação. A extensão do contato (24 h versus 144 h) foi baseada em estudos11 que mostram maior remoção de epóxi e melhor acesso ao cobre com tempos mais longos de imersão em NaOH. Foi utilizada uma bomba à vácuo, um Erlenmeyer de vidro de 500 mL, um funil de vidro e um papel de filtro com porosidade de 28 µm (Quanty®). Reações de lixiviação As reações de lixiviação estudadas foram realizadas com a utilização de um aparato experimental apropriado para promover o controle da temperatura do experimento, como também para medir o volume e evitar escape de gás produzido. Para isso, o sistema foi fechado com o uso de uma válvula de pressão ligada ao frasco de vidro, no qual foram inseridas a solução de lixiviação e a amostra de PCIs, em cada experimento. Esse frasco de vidro foi colocado em banho-maria dentro de um banho termostático, para controle da temperatura. Além disso, o frasco com a válvula de pressão foi conectado a uma mangueira de silicone, que direciona o fluxo de gás para o sistema de medição de gás. Esse sistema consiste em uma proveta invertida preenchida com água. Todo o sistema experimental foi montado dentro de uma capela, como ilustrado na Figura 4.
Reações de lixiviação com ácido clorídrico e ácido hexafluorossilícico, planejamento fatorial 2k, k = 3 Testes preliminares guiaram a escolha das variáveis, dos níveis estudados e das condições operacionais para esses experimentos, como nos trabalhos recentes de lixiviação de CuII de pesquisadores do mesmo grupo de pesquisa do Laboratório de Processos Químicos, Tecnológicos e Ambientais da Universidade Federal do Triângulo Mineiro (UFTM).12 As soluções de lixiviação foram compostas por ácido hexafluorossilícico (H2SiF6), ácido clorídrico (HCl) e peróxido de hidrogênio (H2O2, 35 volumes). O ácido hexafluorossilícico atua promovendo a quebra das ligações Si-O-Cu na matriz epóxi das placas, facilitando o ataque ácido aos sítios de cobre e, assim, melhorando a liberação de íons CuII na solução. As amostras de PCIs foram submetidas ao processo de pré-tratamento completo por 24 h. Assim, foi realizado um planejamento estatístico para guiar a execução dos experimentos, com o objetivo de obter o máximo de informações válidas com o menor número de experimentos.13 Os experimentos seguiram um planejamento fatorial 2k, sendo k = 3, com 4 réplicas no ponto central. Esse tipo de planejamento fatorial é útil nos estágios iniciais de um trabalho experimental, pois esse procedimento fornece o menor número de corridas com os quais as 3 variáveis podem ser estudadas em um planejamento fatorial completo, ou seja, são amplamente usados em experimentos de varredura de variáveis. Além disso, o planejamento 2k com pontos centrais é uma excelente maneira de se obter uma indicação de curvatura.13,14 Foi utilizado o software Statistica®10 (StatSoft, Estados Unidos, 2011) e a variável de resposta, concentração, em mol L-1, de íons CuII; xtraídos na solução lixiviada foi obtida pela titulação complexométrica com EDTA (ácido etilenodiaminotetracético). Nesses experimentos foi analisada a concentração de CuII (variável de resposta) extraídos das amostras, e não foi avaliada a produção de gás. Foram preparadas soluções padrão nas concentrações de 0,5; 1,0; 2,0; 5,0 e 10,0 × 10-3 mol L-1, as quais foram utilizadas para a construção da curva analítica, que apresentou excelente linearidade (R2 = 0,9992). O limite de detecção (0,12 × 10-3 mol L-1) e o limite de quantificação (0,40 × 10-3 mol L-1) foram determinados. Foram avaliadas as variáveis temperatura, concentração de ácido clorídrico, em mol L-1, e volume de ácido hexafluorossilícico na solução de lixiviação. As variáveis e seus níveis são mostrados na Tabela 1.
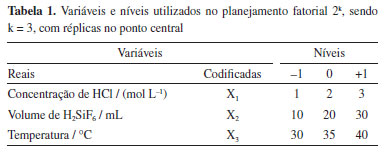
Nos experimentos foram utilizados um volume total de solução ácida de 100 mL, divididos da seguinte forma: 50 mL de solução de ácido clorídrico, 30 mL de solução de ácido hexafluorossilícico, ou seja, quando usados 10 ou 20 mL de ácido hexafluorossilícico, os respectivos 20 ou 10 mL restantes foram completados com água destilada, e 20 mL de peróxido de hidrogênio (35 volumes). Essa solução foi denominada de solução de lixiviação. A fração de PCIs utilizadas em cada experimento foi igual a 1:10, ou seja, foram utilizados 10 g de PCIs, com granulometria menor que 2 mm, para 100 mL de solução de lixiviação. Em um Erlenmeyer foram inseridas a solução de lixiviação e a amostra de PCIs tratadas, e este foi colocado em banho-maria dentro de um banho termostático. Estudos indicam que a utilização em conjunto de ácido e de peróxido de hidrogênio aumenta a eficiência de extração dos metais presentes nas PCIs.15 A matriz de planejamento experimental está descrita na Tabela 2.
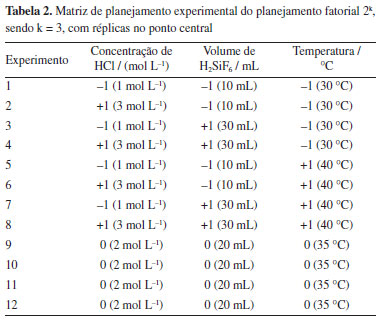
Finalizado o tempo de cada experimento, igual a 24 h, as soluções foram levadas para um banho de gelo, com objetivo de cessar a reação. Em seguida, o conteúdo de cada Erlenmeyer foi submetido ao processo de filtração à vácuo. Assim, a solução lixiviada, resultante do processo de filtração, foi armazenada em um frasco para posterior quantificação de íons CuII por titulação complexométrica com EDTA. Os resíduos de PCIs que ficaram retidos no filtro de papel foram transferidas para um vidro de relógio e levadas para uma estufa a 60 ºC para completa secagem do material. A partir da análise estatística dos resultados obtidos em cada experimento é possível avaliar a influência e significância estatística das variáveis, na variável de resposta: concentração, em mol L-1, de íons CuII; xtraídos na solução lixiviada obtida pela titulação complexométrica com EDTA. Reações de lixiviação com ácido clorídrico e ácido hexafluorossilícico, planejamento fatorial 2k, k = 2 Para alcançar maiores valores de taxa de lixiviação, com consequente, maior concentração de íons CuII; xtraídos, foi proposto um novo planejamento fatorial 2k, com 2 variáveis, e réplicas em todos os pontos. Além de aumentar o tempo de pré-tratamento com solução de NaOH para 144 h, equivalente a 6 dias. Assim, a temperatura, como já comprovado seu efeito positivo e significativo na resposta, foi fixada e mantida constante no seu nível +1, igual a 40 ºC. As variáveis utilizadas foram concentração de ácido clorídrico e volume de ácido hexafluorossilícico, enquanto o volume de peróxido de hidrogênio continuou constante. A variável de resposta também continuou sendo a concentração de íons CuII; xtraídos na solução lixiviada. As variáveis e seus níveis são mostrados na Tabela 3.

O procedimento experimental foi realizado da mesma maneira que foi feito no planejamento fatorial 2k, com 3 variáveis. A matriz de planejamento experimental está descrita na Tabela 4.
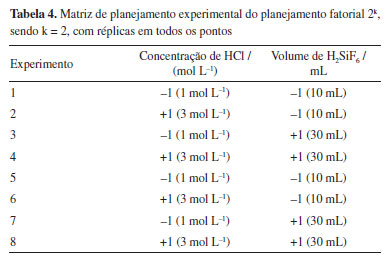
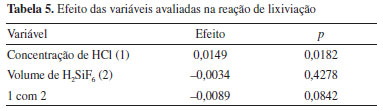
A partir da análise estatística dos resultados obtidos em cada experimento foi possível avaliar a influência e a significância estatítica das variáveis indicadas na Tabela 5, na variável de resposta: concentração, em mol L-1, de íons CuII; xtraídos da amostra de placas na solução lixiviada, obtida por análise no espectrofotômetro UV-visível.
Caminho de máxima inclinação Para realizar a otimização do valor da variável de resposta, concentração de íons CuII; xtraídos, ou seja, encontrar o ponto ótimo em que a resposta possui um valor máximo nas condições do experimento, foi realizado o caminho de máxima inclinação, utilizando os conceitos da metodologia de superfície de resposta, e construída a Tabela 6.
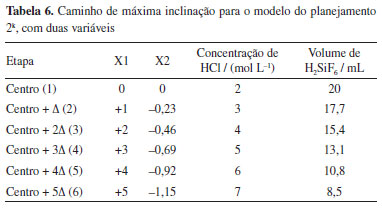
A variável concentração de ácido clorídrico apresenta o maior coeficiente em módulo no modelo, por isso foi escolhida como a base. A base tem seu deslocamento de 1 unidade, para mais ou para menos. Os deslocamentos codificados são convertidos de volta às unidades originais e os novos níveis das variáveis são determinados. E então esses experimentos foram realizados seguindo o mesmo procedimento experimental dos planejamentos fatoriais. Foi realizado o pré-tratamento com solução de NaOH por 144 h, como também foi utilizado 20 mL de peróxido de hidrogênio, com temperatura de 40 ºC, em todos os experimentos, com duração de 24 h. Os resultados de concentração de íons CuII foram analisados pelo espectrofotômetro UV-Vis. Avaliação de produção de gás com solução de lixiviação Para avaliar a produção e a composição do gás, na reação de lixiviação entre a amostra de PCIs e a solução de lixiviação, composta por ácido clorídrico, ácido hexafluorossilícico e peróxido de hidrogênio, foi realizado um experimento de lixiviação com as seguintes condições: (i) concentração de ácido clorídrico igual a 3 mol L-1; (ii) volume de ácido hexafluorossilícico igual a 17,7 mL; (iii) volume de peróxido de hidrogênio igual a 20 mL; (iv) temperatura igual a 40 ºC; (v) amostra de PCIs (10 g) com pré-tratamento por 144 h. Esse experimento foi realizado seguindo o procedimento experimental completo, com utilização do frasco com a mangueira ligada a um sistema de coleta de amostras em ampolas gasométricas, para posterior análise por cromatografia gasosa. Foi utilizado o cromatógrafo a gás Shimadzu GC-2014, equipado com um detector de condutividade térmica (TCD) devidamente calibrado e uma coluna Carboxen-1010 plot.
RESULTADOS E DISCUSSÃO Reação de lixiviação com ácido clorídrico e ácido hexafluorossilícico, planejamento fatorial 2k, k = 3 Com a titulação complexométrica é possível identificar a quantidade de CuII que está presente na solução lixiviada por meio da complexação dos íons CuII disponíveis com a solução de EDTA, e essa é a variável resposta. Para avaliar os efeitos da concentração de HCl, do volume de ácido hexafluorossilícico (H2SiF6) e da temperatura sobre a taxa de lixiviação, ou seja, a concentração de íons CuII; xtraídos em solução lixiviada, o planejamento fatorial 2k, com 3 variáveis e 4 réplicas no ponto central, foi analisado estatísticamente, com auxílio do software Statistica. Os resultados obtidos pela titulação complexométrica são mostrados na Tabela 7.
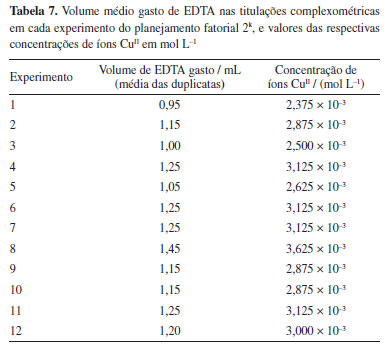
Pode-se notar que o experimento que apresentou a maior remoção de íons CuII foi aquele em que a concentração de HCl, o volume de H2SiF6 e a temperatura estavam no nível +1 (3 mol L-1, 30 mL e 40 ºC, respectivamente). Enquanto que o experimento que apresentou a menor taxa de remoção de íons CuII foi aquele em que as mesmas variáveis estavam no nível -1 (1 mol L-1, 10 mL e 30 ºC, respectivamente). A partir do cálculo dos efeitos de cada variável (Tabela 8), observa-se que todas as variáveis são consideradas significativas e com efeitos positivos, sendo a concentração de ácido clorídrico o efeito dominante, seguida da temperatura e depois do volume de ácido hexafluorossilícico, considerando uma significância estatística de p-valor ≤ 0,05.
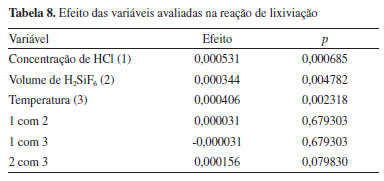
O diagrama de Pareto permite identificar, de forma rápida e clara, os efeitos estatisticamente significativos, facilitando a visualização e interpretação dos resultados experimentais. Os efeitos cujos retângulos estiverem à direita da linha divisória (p = 0,05) devem ser considerados no modelo matemático.13,14 Na Figura 5 é mostrado o gráfico de Pareto com as variáveis avaliadas. Os valores obtidos confirmam os resultados da Tabela 8, evidenciando a significância estatística das três variáveis e a intensidade dos seus efeitos. É possível notar que a concentração de ácido clorídrico é a variável com efeito dominante, seguida da temperatura e depois pelo volume de ácido hexafluorossilícico, enquanto que todas as interações entre as variáveis não foram consideradas significativas.
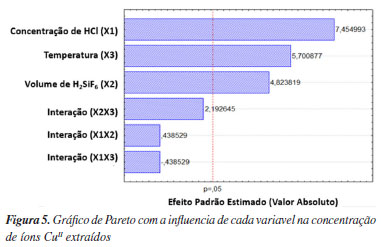
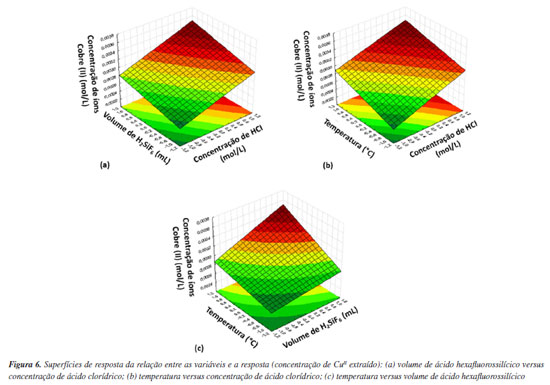
A concentração de ácido clorídrico foi a variável que apresentou a maior significância. Isso já era esperado, pois diversos estudos5,15-17 relacionam fortemente as maiores taxas de lixiviação com maiores concentrações de íons H+ na solução, principalmente quando utilizado peróxido de hidrogênio simultaneamente, gerando um ambiente oxidante que tem a capacidade de acelerar a reação de lixiviação e aumentar a recuperação de metais.3,11,18-20 A temperatura também apresentou uma influência positiva na recuperação de CuII; ou seja, quanto maior a temperatura em que a reação ocorre, maior a taxa de lixiviação e maior a concentração de CuII recuperado. A variável volume de ácido hexafluorossilícico também apresentou significância e influência positiva na recuperação de íons CuII; ou seja, quanto maior o volume de ácido hexafluorossilícico, maior a recuperação de CuII; já que é considerado um ácido bastante corrosivo para a maioria dos metais.21 O ácido hexafluorossilícico também apresenta influência positiva quando usado junto com ácido sulfúrico e peróxido de hidrogênio na lixiviação de PCIs, conseguindo extrair cerca de 15,58 g L-1 de íons CuII lixiviados, em 50 mL de solução, de acordo com uma pesquisa realizada pelo mesmo grupo do Laboratório de Processos Químicos, Tecnológicos e Ambientais.12 Os resultados apresentados pelo diagrama de Pareto também podem ser visualizados através das superfícies de respostas. A Figura 6 apresenta as superfícies de resposta correspondentes para cada par de variáveis em função da resposta, concentração de íons CuII; xtraídos. É possível visualizar que quanto maior o nível das variáveis volume e ácido hexafluorossilícico e concentração de ácido clorídrico, maior a concentração de íons CuII; sendo que a inclinação é maior para a concentração de ácido clorídrico, enfatizando que o seu efeito seja dominante, como pode ser visto na Figura 6a. O mesmo acontece quando se relacionam temperatura e concentração de ácido clorídrico, e, temperatura e volume de ácido hexafluorossilícico, Figuras 6b e 6c, com o aumento do nível das duas variáveis, há o aumento da concentração de íons CuII.
A partir dessa análise estatística foi possível determinar o modelo de regressão, ou modelo estatístico. Esse modelo é capaz de prever novas observações, desde que se esteja limitado à faixa experimental.13,14 Assim, com coeficiente de correlação igual a 0,95886, o modelo proposto está indicado na Equação 1. 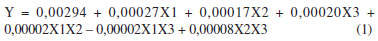 sendo: X1 a concentração de ácido clorídrico, X2 o volume de ácido hexafluorossilícico e X3 a temperatura. O ácido hexafluorossilícico (H2SiF6) foi selecionado porque sua forte acidez (pKa ≈ -5) e sua capacidade de complexar resíduos epóxi silicosos podem potencializar a liberação de metal. Embora no segundo planejamento fatorial 2k, com k = 2, seu efeito estatístico tenha sido mascarado pela ação dominante do HCl e pelo pré-tratamento prolongado com NaOH (que já expõe o cobre ao máximo), o H2SiF6 permanece valioso na lixiviação ácida mista para a quebra de ligações Si-O-Cu.20,21 Trabalhos futuros podem explorar razões maiores de H2SiF6 ou adição sequencial para revelar todo o seu potencial. Com essas superfícies de resposta foi possível avaliar os efeitos das variáveis na concentração de íons CuII; xtraídos da amostra de placa, como explicado anteriormente. No entanto, a porcentagem máxima de CuII removida foi muito baixa, igual a 1,15% do total teórico de CuII presente em 10 g de PCIs. Com essas informações, para aumentar a taxa de lixiviação de CuII; foi necessário inserir algumas modificações: - Aumentar o tempo de pré-tratamento com NaOH, para 144 h (6 dias), para remover o máximo do epóxi na superfície da amostra de placas, a fim de aumentar a exposição do CuII; , consequentemente, melhorar a taxa da reação de lixiviação.11 - Como a temperatura foi considerada uma variável significativa e com efeito positivo, foi realizado um novo planejamento fatorial 2k, com 2 variáveis, em que a temperatura foi fixada no nível +1, igual a 40 ºC. Reação de lixiviação com ácido clorídrico e ácido hexafluorossilícico, planejamento fatorial 2k, k = 2 Os resultados de absorbância obtidos pela análise no espectrofotômetro UV-Vis são mostrados na Tabela 9, assim como a concentração de íons CuII; xtraídos na solução lixiviada.
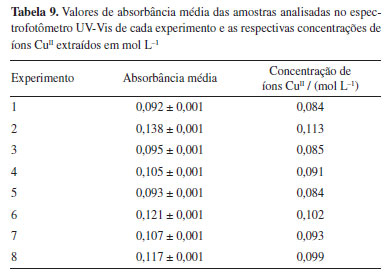
Pode-se notar que o experimento que apresentou a maior remoção de íons CuII foi aquele em que a concentração de HCl era de 3 mol L-1, e o volume de H2SiF6 era 10 mL, correspondente a 0,113 mol L-1 de CuII. Enquanto que o experimento que apresentou a menor taxa de extração de íons CuII (0,084 mol L-1) foi aquele em que as mesmas variáveis eram 1 mol L-1 e 10 mL. A partir do cálculo dos efeitos de cada variável (Tabela 5), observou-se que apenas a variável concentração de ácido clorídrico é considerada significativa e com efeitos positivos, enquanto que a variável volume de H2SiF6 possui efeitos negativos, porém não é considerada significativa, visto que o valor de p é maior que 0,05. Na Figura 7 é mostrado o gráfico de Pareto com as variáveis avaliadas. Os dados obtidos confirmam os dados da Tabela 5, evidenciando a significância estatística de apenas uma variável e a intensidade dos efeitos de todas as variáveis. É possível notar que a concentração de ácido clorídrico é a única variável significante, enquanto o volume de H2SiF6 e a interação entre as variáveis não foram consideradas significativas.
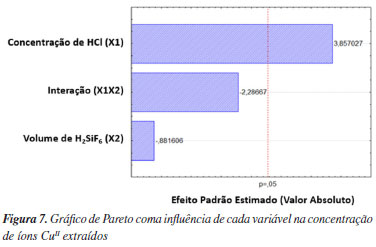
A concentração de ácido clorídrico foi a variável que apresentou a maior significância. Diversos estudos relacionam fortemente as maiores taxas de lixiviação com maiores concentrações de íons H+ na solução,5,15-17 principalmente quando utilizado peróxido de hidrogênio simultaneamente, gerando um ambiente oxidante que tem a capacidade de acelerar a reação de lixiviação e aumentar a recuperação de metais.3,11,18-20 Os resultados apresentados pelo diagrama de Pareto também podem ser visualizados através da superfície de resposta. A Figura 8 apresenta a superfície de resposta correspondente para o par de variáveis em função da resposta, concentração de íons CuII; xtraídos. É possível visualizar que quanto maior o nível da concentração de ácido clorídrico, maior a concentração de CuII; xtraído, enquanto as variações no volume de H2SiF6 não geraram influência significativa na resposta. A inclinação da superfície quando há variação na concentração de ácido clorídrico, enfatiza seu efeito positivo e dominante na resposta.
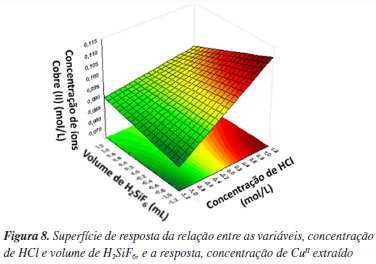
Nesse caso, é possível concluir que o ácido hexafluorossilícico não exerce uma influência significativa na lixiviação de CuII de PCIs, em conjunto com ácido clorídrico e peróxido de hidrogênio, nas condições e concentrações usadas nos experimentos realizados. No entanto, sua ação pode ter sido mascarada pela ação dominante do HCl e pelo pré-tratamento prolongado com NaOH, sendo a concentração de ácido clorídrico com peróxido de hidrogênio as responsáveis pela lixiviação do CuII; nessas condições. A partir dessa análise estatística foi possível determinar o modelo de regressão, ou modelo estatístico. Esse modelo é capaz de prever novas observações, desde que se esteja limitado à faixa experimental.14 Assim, com coeficiente de correlação igual a 0,839, o modelo proposto está indicado na Equação 2. 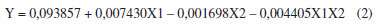 sendo: X1 a concentração de ácido clorídrico, X2 o volume de ácido hexafluorossilícico. A porcentagem máxima de CuII removida, que foi obtida no experimento 2, no qual a concentração de ácido clorídrico foi igual a 3 mol L-1, e o volume de ácido hexafluorossilícico foi igual a 10 mL, foi de 35,9% do total teórico de CuII presente em 10 g de amostras de placas de circuito impresso, equivalente a 0,113 mol L-1. Como a superfície de resposta apresenta um plano, não é possível identificar qual o ponto que resulta em um valor máximo de concentração de íons CuII; xtraídos. Para otimizar o sistema, é necessário utilizar a metodologia de superfícies de resposta, e o primeiro passo é realizar o caminho de máxima inclinação, para informar para qual direção a resposta está crescendo e depois disso buscar um ponto ótimo, se houver. Caminho de máxima inclinação Para a realização dos experimentos, as soluções lixiviadas de cada experimento foram filtradas e armazenadas para análise no espectrofotômetro UV-Vis. As análises foram realizadas em triplicata. A Tabela 10 mostra esses resultados.
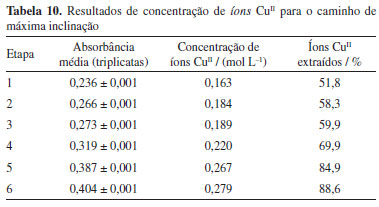
De acordo com esse caminho de máxima inclinação, nota-se que não houve indicação de máximo ou mínimo em sua superfície, já que quanto maior a concentração de ácido clorídrico e menor o volume de ácido hexafluorossilícico, houve maior remoção de íons CuII. Foi obtida uma concentração máxima de 0,279 mol L-1, que corresponde a 88,6% da quantidade máxima de CuII presente na amostra de placas, quando utilizou a concentração de 7 mol L-1 de ácido clorídrico e 8,5 mL de ácido hexafluorossilícico, em conjunto com 20 mL de peróxido de hidrogênio, a 40 ºC por 24 h. Cálculo do valor teórico de CuII O valor teórico de CuII; m 10 g de PCIs foi estimado a partir do conteúdo de cobre em placas de circuito, tomado como 12% (peso/peso) conforme Baldé et al.10 Assim, a quantidade molar máxima de CuII disponível foi calculada por: 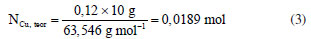 Todos os percentuais de extração referem-se a essa quantidade teórica de 0,0189 mol de CuII. Como não houve indicação de máximo, nesse caso não haverá um ponto ótimo para esse sistema nessas condições. Pode-se concluir que quanto maior a concentração de ácido clorídrico e menor o volume de ácido hexafluorossilícico, maior será a extração de íons CuII da amostra de PCIs no intervalo, na temperatura e nas condições estudadas. Avaliação de produção de gás com a solução de lixiviação Como não houve a determinação de um ponto ótimo, ou seja, não foi possível realizar a otimização desse sistema nos intervalos estudados, foram escolhidas as condições das variáveis estudadas para a realização desse experimento, com objetivo de determinar a composição do gás produzido pela reação de lixiviação com a amostra de PCIs. Assim, foram escolhidas as condições do experimento 2 do caminho de máxima inclinação (3 mol L-1 de ácido clorídrico e 17,7 mL de ácido hexafluorossilícico). Essa condição foi escolhida pois houve uma grande remoção de CuII das placas, equivalente a 58,3%. No experimento com concentração de ácido clorídrico de 7 mol L-1 a remoção foi maior, igual a 88,6%, porém essa é uma concentração de ácido muito alta, que gera limitações operacionais, risco de segurança, como também dificuldade no tratamento do efluente gerado após o tratamento. O experimento foi realizado, e amostras de gás foram retiradas, de tempo em tempo, de acordo durante 1 h e 30 min. Essas amostras de gás foram coletadas em ampolas gasométricas e armazenadas para posterior análise por cromatografia gasosa. A análise por cromatografia gasosa identificou a presença de apenas H2 na amostra gasosa, em uma pureza de > 99,9%. Assim, conclui-se que gás hidrogênio está em constante produção desde o início da reação de lixiviação do CuII contido nas PCIs com solução de lixiviação composta por ácido clorídrico, ácido hexafluorossilícico e peróxido de hidrogênio.
CONCLUSÕES O processo hidrometalúrgico de extração de CuII presente nas PCIs de computadores, com a utilização de ácido clorídrico, ácido hexafluorossilícico e peróxido de hidrogênio como agentes lixiviantes foi estudado, a significância e a influência das variáveis avaliadas foram determinadas. A temperatura foi considerada uma variável significante e com influência positiva na resposta, ou seja, quanto maior a temperatura, maior a extração de íons CuII; no intervalo analisado. Concluiu-se também que a concentração de ácido clorídrico é a variável mais significativa para o processo, já que altas taxas de lixiviação estão relacionadas com maiores concentrações de íons H+ na solução. Essa variável possui efeito positivo e dominante em relação às outras. A variável volume de ácido hexafluorossilícico não possui significância estatística no processo, no intervalo avaliado, ou seja, variações em sua quantidade não foi capaz de influenciar na resposta de maneira direta. O pré-tratamento com solução de NaOH se mostrou essencial para a exposição e remoção do CuII nas PCIs. Os experimentos evidenciaram que quanto maior o tempo de contato das placas com essa solução, maior a concentração de íons CuII; xtraída. Após a determinação da significância das variáveis, foi realizado um caminho de máxima inclinação para identificar um valor máximo ou mínimo para a resposta. No entanto, nos experimentos desse caminho, a concentração de íons CuII; xtraídos aumentou de acordo com o aumento da concentração de ácido clorídrico. Logo, não há região otimizada para determinar um ponto ótimo desse sistema, nesse intervalo. Assim, utilizando uma solução de ácido clorídrico de 3 mol L-1, volume de ácido hexafluorossilícico igual a 17,7 mL e 20 mL de peróxido de hidrogênio (35 volumes), foi possível obter uma extração de íons CuII igual a 58,3% em relação a concentração teórica de CuII presente nas amostras de placas de circuito impresso. Além disso, essa reação de lixiviação foi capaz de produzir gás hidrogênio puro, de acordo com análises de cromatografia gasosa. Apesar de concentrações elevadas de HCl (3 mol L-1) maximizarem a extração de CuII; elas introduzem sérios desafios de segurança e impacto ambiental. Soluções fortemente ácidas intensificam a corrosão de equipamentos, aumentam o risco de exposição química e geram efluentes que demandam neutralização e tratamento especializado. Para contornar essas limitações em escala piloto ou industrial, propomos: (i) Recuperação e reciclagem de HCl por destilação fracionada ou por unidades de troca iônica, reduzindo o consumo de reagentes; (ii) Emprego de revestimentos resistentes à corrosão (por exemplo, aço inox 316L ou polímeros compatíveis) nas superfícies em contato com o ácido; (iii) Adoção de circuitos fechados de lixiviação, viabilizando o reuso do ácido e minimizando o volume de efluente gerado. Tais medidas permitem equilibrar a eficiência de extração com critérios de segurança e menor impacto ambiental.
DECLARAÇÃO DE DISPONIBILIDADE DE DADOS Todos os dados estão disponíveis no texto.
AGRADECIMENTOS Os autores agradecem as agências de fomento CAPES,CNPq (303662/2025-5, 313447/2021-7) e FAPEMIG (APQ-00038-24).
CONTRIBUIÇÕES DO AUTOR Camila Ferreira Pinto: curadoria de dados, análise formal, investigação, visualização, redação de rascunho original e redação-revisão e edição; Eduarda Maia Guimarães: investigação, redação de rascunho original; Marquele Amorim Tonhela: curadoria de dados, investigação, redação de rascunho original e redação-revisão e edição; Sandra Cristina Dantas: análise formal, administração de projetos, recursos, redação de rascunho original e redação-revisão e edição; Ana Claudia Granato Malpass: análise formal, investigação, administração de projetos, redação de rascunho original e redação-revisão e edição; Geoffroy Roger Pointer Malpass: conceituação, curadoria de dados, análise formal, aquisição de financiamento, investigação, administração de projetos, recursos, redação de rascunho original e redação-revisão e edição.
REFERÊNCIAS 1. Forti, V.; Baldé, C. P.; Kuehr, R.; Bel, G.; The Global E-waste Monitor 2020: Quantities, Flows, and the Circular Economy Potential, 2020. [Link] acessado em julho 2025 2. Nithya, R.; Sivasankari, C.; Thirunavukkarasu, A.; Environ. Chem. Lett. 2021, 19, 1347. [Crossref] 3. Thakur, P.; Kumar, S.; Environ. Sci. Pollut. Res. 2020, 27, 32359. [Crossref] 4. Ghosh, B.; Ghosh, M. K.; Parhi, P.; Mukherjee, P. S.; Mishra, B. K.; J. Cleaner Prod. 2015, 94, 5. [Crossref] 5. Hao, J.; Wang, Y.; Wu, Y.; Guo, F.; Resour., Conserv. Recycl. 2020, 157, 104787. [Crossref] 6. Kaya, M.; Waste Manage. 2016, 57, 64. [Crossref] 7. Wu, Z.; Yuan, W.; Li, J.; Wang, X.; Liu, L.; Wang, J.; Front. Environ. Sci. Eng. 2017, 11, 8. [Crossref] 8. Ji, X.; Yang, M.; Wan, A.; Yu, S.; Yao, Z.; Int. J. Environ. Res. Public Health 2022, 19, 7508. [Crossref] 9. Zhang, L.; Xu, Z.; J. Cleaner Prod. 2016, 127, 19. [Crossref] 10. Baldé, C. P.; Kuehr, R.; Yamamoto, T.; McDonald, R.; D'Angelo, E.; Althaf, S.; Bel, G.; Deubzer, O.; Fernandez-Cubillo, E.; Gray, V.; Herat, S.; Honda, S.; Iattoni, G.; Khetriwal, D. S.; di Cortemiglia, V. L.; Lobuntsova, Y.; Nnorom, I.; Pralat, N.; Wagner, M.; The Global E-waste Monitor 2024, 2024. [Link] acessado em julho 2025 11. Anwer, S.; Panghal, A.; Majid, I.; Mallick, S.; Int. J. Environ. Sci. Technol. 2022, 19, 9731. [Crossref] 12. Lana, F. A.; Silveira, Á. W. F.; Pinto, C. F.; Lima, A. F.; Fornazari, A. L. T.; Silva, P. P.; Fernandes, D. M.; Tonhela, M. A.; Granato, A. C.; Malpass, G. R. P.; Rev. Virtual Quim. 2022, 14, 637. [Crossref] 13. Neto, B. B.; Scarminio, I. S.; Bruns, R. E.; Como Fazer Experimentos: Pesquisa e Desenvolvimento na Ciência e na Indústria, 4ª ed.; Bookman: Campinas, 2001. 14. Calado, V.; Montgomery, D.; Planejamento de Experimentos Usando Statistica; e-Papers: Rio de Janeiro, 2003. 15. Jadhav, U.; Hocheng, H.; Sci. Rep. 2015, 5, 14574. [Crossref] 16. Bas, A. D.; Deveci, H.; Yazici, E. Y.; Sep. Purif. Technol. 2014, 130, 151. [Crossref] 17. Yang, H.; Liu, J.; Yang, J.; J. Hazard. Mater. 2011, 187, 393. [Crossref] 18. Jadhav, U.; Su, C.; Hocheng, H.; Environ. Sci. Pollut. Res. 2016, 23, 24384. [Crossref] 19. Hsu, E.; Barmak, K.; West, A. C.; Park, A.-H. A.; Green Chem. 2019, 21, 919. [Crossref] 20. Birloaga, I.; De Michelis, I.; Ferella, F.; Buzatu, M.; Vegliò, F.; Waste Manage. 2013, 33, 935. [Crossref] 21. Mosaic Fertilizantes, Ficha de Informações de Segurança de Produtos Químicos, Ácido Fluossilícico, https://mosaicco.com.br/fileLibrary/publicFiles/0-FISPQ____cido_Fluossil_cico___Rev.01.pdf, acessado em julho 2025.
Editor Associado responsável pelo artigo: Eduardo H. S. Sousa |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access