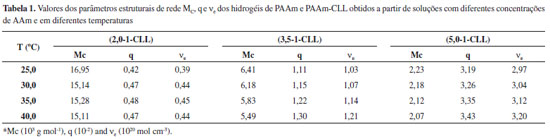
Artigo
|
|
| Caracterização mecânica e estrutural de um dispositivo PDLC baseado em hidrogéis de PAAm e cristal líquido liotrópico LP/DeOH/H2O Mechanical and structural characterization of a PDLC device based on PAAm hydrogels and KL-DeOH-H2O lyotropic liquid crystal |
|
Fauze A. AouadaI,*; Marcia R. de MouraI; Paulo R. G. FernandesII; Adley F. RubiraIII; Edvani C. MunizIII
IDepartamento de Física e Química, Faculdade de Engenharia de Ilha Solteira, Universidade Estadual Paulista, 15385-000 Ilha Solteira - SP, Brasil Recebido em 09/01/2014 *e-mail: faouada@yahoo.com.br In this work, a novel device based on polyacrylamide (PAAm) hydrogels and KL-DeOH-H2O lyotropic liquid crystal (LLC), with potential for application as Polymer Dispersed Liquid Crystals (PDLC), was proposed and its properties characterized. The confinement of LLC promoted significant changes in spectroscopic, morphological, optical, hydrophilic, structural and mechanical properties due to the interaction between the LLC-PAAm matrix and entropic parameter changes. The mechanical and structural properties can be controlled by adjusting AAm, temperature and presence of LLC, which can be useful for technological applications of these systems in optical devices. INTRODUÇAO Os cristais líquidos sao caracterizados por possuírem grau de ordem molecular intermediário entre a ordem orientacional dos sólidos cristalinos e líquidos isotrópicos1 (Figura 1S, Material Suplementar).2 As transiçoes de fases ocorrem pela quebra da ordem posicional e/ou orientacional das moléculas, aumentando ou diminuindo seus graus de liberdade (entropia). Este efeito pode ser acelerado pela variaçao na temperatura. Devido a essa peculiaridade, os cristais líquidos apresentam anisotropia em suas propriedades ópticas, elétricas e magnéticas, semelhantes às de um sólido cristalino anisotrópico, e propriedades mecânicas semelhantes de um líquido, o que caracteriza sua fluidez.3-5 Os cristais líquidos sao classificados em duas grandes categorias: os termotrópicos (CLTs) e os liotrópicos (CLLs). Os CLTs sao constituídos por arranjos de moléculas anisométricas orgânicas (moléculas alongadas ou em forma de discos), cujas propriedades se manifestam pela açao do calor, em geral nas vizinhanças do ponto de fusao do material.2,6 Os CLLs sao sistemas químicos formados por misturas binárias, ternárias ou quaternárias de substâncias anfifílicas tais como álcoois de cadeia longa, saboes e detergentes usualmente tendo água como solvente.7,8 Nessas misturas as moléculas anfifílicas acima de uma concentraçao específica, chamada concentraçao micelar crítica (CMC), formam aglomerados de moléculas que podem assumir formas e dimensoes diferentes, chamadas micelas.9-11 O confinamento de materiais eletro-ópticos em matrizes poliméricas tem despertado um especial interesse devido às suas aplicaçoes tecnológicas. As mais conhecidas sao os PDLC's12-16 (Polymer Dispersed Liquid Crystals), que sao utilizados em displays e em cortinas eletrônicas. Existem essencialmente duas formas de preparaçao de PDLC's: i) por encapsulamento; ii) por separaçao de fases. O método de encapsulamento consiste em misturar o cristal líquido com um polímero dissolvido em água. Quando a água é evaporada, o cristal líquido é circundando pelo polímero, gerando assim, pequenos sistemas formados por gotas distribuídas (ou confinadas) por todo o polímero. Já o método de separaçao de fases consiste basicamente em preparar um sistema formado por uma mistura homogênea de cristal líquido e monômero. Após o início da reaçao de polimerizaçao obtêm-se aglomerados de gotas de cristal líquido dispersos na matriz polimérica.17 Outra forma de confinamento de CL consiste em introduzi-los no interior de hidrogéis.18-22 A motivaçao em estudar esses sistemas nao está apenas nos aspectos de pesquisa básica em Física e em Química, mas também sob o ponto de vista tecnológico, como por exemplo, a fabricaçao de dispositivos eletro-ópticos, tais como os displays. Por sua vez, os hidrogéis sao polímeros capazes de absorver grande quantidade de água.23-25 Estruturalmente sao constituídos por uma ou mais redes poliméricas tridimensionalmente estruturadas, formadas por cadeias macromoleculares interligadas por ligaçoes covalentes (reticulaçoes) ou interaçoes físicas.26 Em trabalho publicado recentemente pelo nosso grupo de pesquisa20 foram estudadas as propriedades hidrofílicas, morfológicas e ópticas de hidrogéis birrefringentes obtidos pela incorporaçao do CLL LP/DeOH/H2O em matrizes de poliacrilamida (PAAm). Como continuaçao, nesse trabalho, descrevemos as propriedades mecânicas, estruturais e espectroscópicas desses mesmos hidrogéis objetivando a aplicaçao desses sistemas como dispositivos ópticos PDLC's. Vale ressaltar que os métodos de obtençao de PDLC sao empregados principalmente para os CLT, sendo que os PDLC a base de CLL sao pouco investigados. O que motivou ainda mais o desenvolvimento do presente trabalho.
PARTE EXPERIMENTAL Síntese do laurato de potássio (LP) O surfactante dodecanoato de potássio, também conhecido como laurato de potássio (LP), foi obtido por meio da reaçao de neutralizaçao do ácido láurico (Acros) com aquecimento e em presença de etanol (Sigma), descrita na equaçao abaixo:
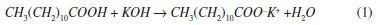
Preparaçao da mesofase liotrópica O cristal líquido liotrópico (CLL) utilizado neste trabalho foi preparado apresentando a seguinte composiçao (em massa): LP 24,79%; decanol (DeOH) 6,24% e H2O 68,97%. A preparaçao da amostra, efetuada a temperatura ambiente, obedeceu a seguinte ordem: no tubo de ensaio foi introduzida parte da quantidade desejada de LP e sobre este foi adicionado DeOH. O tubo de ensaio foi agitado e, logo em seguida foi adicionado o restante de LP, de forma a obter a razao LP/DeOH desejada. Foi adicionada, entao, a quantidade de água necessária para se atingir a concentraçao de 68,97% (m/m). O tubo foi fechado e selado com parafilme, a fim de evitar perdas por evaporaçao e conseqüentemente alteraçao das propriedades do CLL resultante. O processo de homogeneizaçao da amostra foi realizado manualmente e, para eliminar as possíveis bolhas e espumas, utilizou-se uma centrífuga. O processo foi repetido várias vezes até que a amostra se apresentasse totalmente homogênea. As transiçoes de fase desse sistema ternário sao: 1) TIRe→nem ≅ 19 ºC e 2) Tnem→ISO ≅ 29 ºC,27 na qual IRe é a fase isotrópica reentrante, nem a fase nemática e ISO a fase isotrópica. Síntese dos hidrogéis de PAAm com CLL confinado Os hidrogéis de PAAm com CLL confinado foram sintetizados em ambiente selado por meio de polimerizaçao fotoquímica radicalar do monômero acrilamida, AAm, (Aldrich), na presença de N',N'-metileno-bisacrilamida, MBAAm (Plusone), que atua como agente de reticulaçao. Como iniciador da fotopolimerizaçao utilizou-se periodato de potássio, KIO4 (Vetec). A síntese foi efetuada adicionando o monômero AAm, o agente de reticulaçao MBAAm, e o KIO4 em 1,0 mL de CLL. As concentraçoes de AAm, utilizadas na síntese foram 2,0; 3,5 e 5,0 mol L-1, mantendo a concentraçao de agente reticulante constante em relaçao a concentraçao molar de AAm. A soluçao resultante foi inserida entre duas lâminas de vidro com dimensoes (em mm) de 76 x 26 x 1,1, com espaçador de 1,0 mm de espessura e exposta por 40 minutos em lâmpada de vapor de Hg (λ = 254 - 580 nm). Para identificaçao das diferentes formulaçoes adotou-se a seguinte notaçao (A-M-CLL), onde A é a concentraçao molar de AAm, M é a concentraçao de MBAAm (% em relaçao à conc. de AAm) e CLL refere-se a presença de cristal líquido liotrópico. Ressonância magnética nuclear (RMN) A caracterizaçao do LP foi realizada por meio de ressonância magnética nuclear de 1H utilizando o mesmo equipamento, porém usando sonda para líquidos. Para obtençao dos espectros, as soluçoes de ácido láurico e LP foram preparadas em CDCl3 e D2O, respectivamente. Os espectros de ressonância magnética nuclear de sólidos CP/MAS (Cross Polarization Magic Angle Spinning) do LP e dos hidrogéis de PAAm contendo ou nao CLL confinado foram obtidos utilizando um espectrofotômetro Varian modelo Oxford 300 operando em frequência de 300 MHz. Depois de compactadas em um rotor de zircônia (5,0 mm de diâmetro), as amostras liofilizadas foram giradas com frequência de rotaçao de 4.000 Hz. O tempo de contato e o intervalo entre os pulsos de sequências foram de 1,0 ms e 1,0 s, respectivamente. Espectroscopia fotoacústica na regiao do infravermelho (FTIR) Os hidrogéis foram também caracterizados por meio de espectroscopia fotoacústica na regiao do infravermelho. Para isso, foi utilizado um espectrofotômetro Bomem FT-IR modelo MB 100. Os espectros com resoluçao de 2 cm-1 foram obtidos entre 1000 a 4000 cm-1 acumulando 128 scans. Propriedades mecânicas A resistência à compressao (dureza) dos hidrogéis foi determinada por meio de testes de tensao máxima de compressao (σmax). Para isso, foi utilizado o equipamento Texture Analyzers (Stevens L. F. R. A) contendo corpo de prova circular de 12,7 mm de diâmetro. A velocidade de descida do corpo de prova foi programada para 0,2 mm s-1. A temperatura do hidrogel foi controlada usando um banho termostático. Valores de σmax a diferentes temperaturas foram obtidos medindo-se a força (f) necessária para comprimir em 1 mm as membranas dos hidrogéis, equaçao 2.28
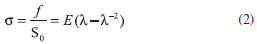
na qual σ é a tensao aplicada, em Pa m-2, f é o valor da força exercida, S0 é a área do corpo de prova e λ é a deformaçao relativa. Valores de f foram obtidos em seis pontos distintos da membrana. A espessura média das membranas dos hidrogéis sintetizados foi de 3,0 mm. Determinou-se, a partir da inclinaçao da reta obtida pela aplicaçao da equaçao 2, o módulo elástico (E) de cada hidrogel na temperatura desejada. A densidade aparente de reticulaçao, ve, foi determinada utilizando a equaçao:29
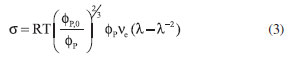
na qual R é a constante dos gases, T é a temperatura absoluta, ΦP,0 e ΦP sao as fraçoes volumétricas de polímero no hidrogel no estado relaxado (logo após a reticulaçao) e no estado intumescido no equilíbrio, respectivamente. Propriedades estruturais O parâmetro massa molar média entre retículos (MC)30 descreve a massa molar numérica entre duas junçoes consecutivas, que podem ser formadas por retículos químicos, entrelaçamentos físicos, regioes cristalinas e complexos poliméricos. Outros parâmetros, tais como densidade de reticulaçao (q),31 a qual é proporcional à fraçao molar de agente de reticulaçao utilizado, e número de cadeias efetivamente elásticas por unidade de volume, simbolizado por ve,32 também sao importantes para a caracterizaçao estrutural da rede de um hidrogel. As propriedades estruturais MC, q e ve foram obtidas utilizando-se as seguintes equaçoes:
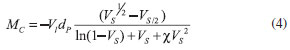
na qual Vl é o volume molar do solvente (água) (mL mol-1), dp é a densidade do polímero (PAAm) (~ 1,10 g mL-1), VS é a fraçao de volume do gel intumescido e χ é o parâmetro de interaçao entre o solvente e o polímero (~ 0,466).33

na qual M0 representa a massa molar da unidade repetitiva.

na qual NA é o número de Avogadro.
RESULTADOS E DISCUSSAO Caracterizaçao do laurato de potássio (LP) por ressonância magnética nuclear (RMN) Nas Figuras 2Sa e 2Sb sao mostrados os espectros de RMN de 1H do ácido láurico e laurato de potássio (LP), respectivamente. Pode-se observar na Figura 2Sa um sinal em d =12,0 ppm referente ao próton da carboxila pertencente ao ácido láurico. Ao término da reaçao, o produto foi formado por substituiçao do próton da carboxila por uma molécula de potássio, o que pode ser constatado pelo desaparecimento dessa banda no espectro. Ressonância magnética nuclear (RMN) de sólidos A Figura 1 apresenta os espectros de ressonância magnética nuclear CP/MAS referentes à hidrogéis de PAAm puro, LP e hidrogéis de PAAm-LP/DeOH/H2O. No espectro referente ao LP, observa-se a presença do sinal em δ =15,84 ppm, que é referente ao carbono metilênico do LP (carbono 1, ver Figura 1). Sinais referentes aos carbonos C2, C3 e C4-9 sao observados em δ = 26,12; 29,60 e 34,45 ppm. No espectro referente ao hidrogel constituído apenas de PAAm reticulada, esses sinais nao sao observados. No espectro referente ao hidrogel de PAAm-CLL, sao observados sinais provenientes do LP, bem como mudanças espectrais em diferentes regioes, o que indica que os cristais de LP foram incorporados e permaneceram confinados dentro das cadeias de PAAm mesmo após o processo de liofilizaçao.
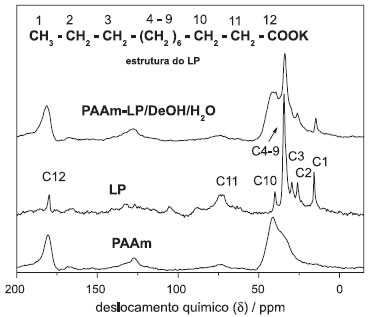 Figura 1. Espectro de ressonância magnética nuclear de sólidos CP/MAS de hidrogéis de PAAm, PAAm-LP/DeOH/H2O e laurato de potássio (LP)
Espectroscopia fotoacústica na regiao do infravermelho (FTIR) Na Figura 2 sao mostrados os espectros de FTIR fotoacústica do LP, hidrogéis de PAAm e hidrogéis de PAAm-LP/DeOH/H2O. Analisando o espectro referente ao hidrogel constituído por PAAm,34 observa-se a presença de bandas em 3425-3193 cm-1 (deformaçao axial), 1606 cm-1 (deformaçao angular) e 800-664 cm-1 (deformaçoes angulares simétricas fora do plano) atribuídas a ligaçao N-H do grupo amida. Foram observadas bandas relativas ao grupamento CH2 em 1375 cm-1 e 825 cm-1. As bandas em 2925-2860 cm-1 sao referentes a estiramentos assimétricos e simétricos desse mesmo grupamento. Nas regioes entre 1120-1030 cm-1 (estiramentos simétricos e assimétricos) e 466 cm-1 (deformaçao axial) se referem aos modos vibracionais da ligaçao C-C. Observa-se, ainda, em 1668 cm-1 e 1466 cm-1 deformaçoes axiais relativas à carbonila e a ligaçao C-N, respectivamente.
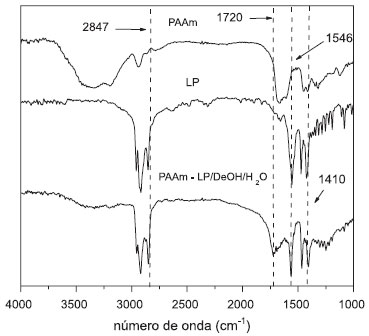 Figura 2. Espectros de espectroscopia fotoacústica na regiao do infravermelho (FTIR) dos hidrogéis de PAAm, PAAm-LP/DeOH/H2O e LP
No espectro do LP, a banda na regiao de 2847 cm -1 foi atribuída ao carbono metilênico. Ainda no mesmo espectro, observam-se também bandas em 1720 cm-1 referente à carbonila, 1546 cm-1 e 1390-1420 cm-1 que podem ser atribuídas a grupamento CH2 adjacentes à carbonila, deformaçoes da ligaçao de C - O, deformaçao angular CH3, deformaçao angular de (CH)n para n > 3. A modificaçao das propriedades espectroscópicas dos hidrogéis de PAAm pela inserçao de LP foi constatada pelo aparecimento das bandas supracitadas características do composto LP. Separadamente, o hidrogel de PAAm-CLL do tipo (2,0-1-CLL) foi submetido a 4 ciclos de intumescimento/secagem a 30,0 ºC. Em cada ciclo o hidrogel permaneceu durante 24 horas. Depois de cada ciclo o hidrogel foi seco e pesado. Nesse estudo nao foram observadas mudanças significativas nos valores de grau de intumescimento (Q): 1º ciclo → Q = 35,3 ± 1,0 g g-1 (ou 3530%); 2º ciclo → Q = 34,9 ± 0,9 g g-1 (ou 3490%); 3º ciclo → Q = 33,8 ± 1,3 g g-1 (ou 3380%)e 4º ciclo → Q = 35,0 ± 0,7 g g-1 (ou 3500%), variaçao < 5,0%. Vale ressaltar que a unidade de Q expressa em g g-1 representa a quantidade de água absorvida pelo hidrogel por grama de hidrogel seco. Após cada ciclo, no recipiente onde o hidrogel foi intumescido, nao foi observado traço de decanol, o que indica que o mesmo nao difundiu para fora do hidrogel. Assim, a hidrofilicidade de tal hidrogel nao foi alterada mesmo após o processo de intumescimento/secagem e, provavelmente, suas propriedades birrefringentes também nao sofreram alteraçoes. Nas micrografias da Figura 3S, obtidas por microscopia eletrônica de varredura, observa-se que hidrogel de PAAm possui superfície extremamente porosa. Pode-se observar também que hidrogéis com CLL confinado (Figuras 3Sb e 3Sc) apresentam superfície bem mais rugosa quando comparada com a superfície dos hidrogéis de PAAm sem CLL (Figura 3Sa). Em ampliaçoes maiores (Figura 3Sc), as superfícies dos hidrogéis com CLL apresentam em todas suas extensoes cristais bem definidos que sao provenientes do LP. A presença desses cristais proporciona aos hidrogéis propriedades birrefringentes, as quais sao altamente desejáveis para aplicaçao dos hidrogéis como dispositivos ópticos. Na Figura 4S é analisada a textura e a birrefringência do hidrogel com CLL incluso. Foi observado que amostras com o CLL confinado na matriz polimérica apresentam birrefringência (anisotropia óptica). Por outro lado, as texturas observadas nas amostras (2,0-1-0), portanto sem CLL confinado, sao típicas de sistemas isotrópicos (coloraçao escura), nos quais a anisotropia óptica é nula. Dessa forma, pode-se atribuir a birrefringência apresentada exclusivamente à presença do CLL. Vale ressaltar que, em um meio isotrópico, a luz incidente em uma dada amostra propaga-se segundo uma onda esférica.35 Logo, o índice de refraçao apresentado pelo meio é invariante com a direçao de polarizaçao da luz incidente. Em um meio anisotrópico (ou birrefringente), a velocidade de propagaçao da luz é dependente da direçao de polarizaçao. Tais meios birrefringentes possuem dois índices de refraçao principais: ordinário (no) e extraordinário (ne) e a birrefringência apresentada pelo meio é definida como sendo a diferença entre esses dois índices, Δn = ne - no. Dessa forma, para determinar a birrefringência em cristais líquidos, é necessário que as moléculas do cristal líquido estejam orientadas. Isto é possível por exposiçao em campo magnético e/ou campo elétrico. Depois de serem orientadas, o meio em que as mesmas se encontram passa a apresentar uma única direçao preferencial, ou seja, um único eixo óptico. Nesse trabalho, os sistemas nao foram submetidos à induçao, seja por campo magnético, seja por campo elétrico. Isto é, as micelas de CLL sofreram orientaçao apenas pelo confinamento nos hidrogéis de PAAm. Isto pode disponibilizar a aplicaçao desses dispositivos como displays ópticos em temperaturas onde as fases nemáticas sao predominantes, 19 ºC < T Nem < 29 ºC. Propriedades mecânicas e estruturais O módulo de elasticidade é obtido a partir do gráfico de tensao vs deformaçao, sendo E a inclinaçao do gráfico na regiao elástica (pequenas deformaçoes).36 Porém, esses gráficos nao sao sempre lineares, salvo em alguns materiais, por exemplo os metálicos. Assim, alguns cuidados sao necessários na determinaçao de E. Nesse trabalho, os valores de E para os hidrogéis foram obtidos para intervalos de pequenas deformaçoes, o que garante que as deformaçoes observadas sao realmente elásticas. A avaliaçao das propriedades mecânicas dos hidrogéis constituídos por PAAm e CLL foi realizada determinando-se os valores de tensao máxima de compressao (σmax), módulo elástico (E) e densidade aparente de reticulaçao (ve). Curvas representativas de tensao-deformaçao para diferentes hidrogéis utilizando-se deformaçao unixial sao mostradas na Figura 3. Pode-se observar uma boa linearidade entre as propriedades, principalmente para pequenas deformaçoes, sendo essas utilizadas para a obtençao dos valores do módulo elástico. Isso mostra que a deformaçao do hidrogel é elástica, ou seja, o hidrogel retorna a sua conformaçao inicial quando a força é removida.37,38 Além disso, pode-se notar na Figura 3 uma diferença significativa no comportamento mecânico dos hidrogéis. Se fixarmos um valor de deformaçao relativa, por exemplo em 0,4, nota-se que a tensao máxima necessária para termos essa deformaçao aumenta consideravelmente com o aumento da concentraçao de acrilamida. Nesse caso específico, os valores de tensao máxima de compressao sao 1,9; 10,5 e 17,9 kPa para 2,0; 3,5 e 5,0 mol L-1 de acrilamida, respectivamente. Por outro lado, se fixarmos um valor de tensao máxima de compressao, por exemplo em 10 kPa, os valores de deformaçao relativa para os hidrogéis contendo 3,5 e 5,0 mol L-1 de acrilamida sao 0,38 e 0,24, respectivamente.
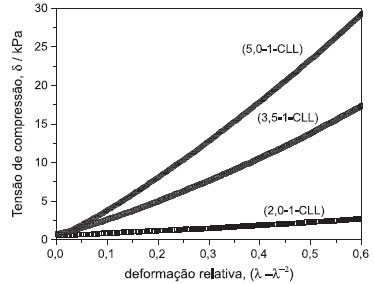 Figura 3. Curvas representativas de tensao-deformaçao utilizando deformaçao uniaxial para os hidrogéis (2,0-1-CLL), (3,5-1-CLL) e (5,0-1-CLL) obtidas a 25,0 ºC
A dependência do módulo elástico (E) em funçao da temperatura para diferentes hidrogéis é mostrada na Figura 4, na qual se observa que o aumento da concentraçao de AAm, em uma temperatura constante, provoca aumento nos valores de E devido ao aumento da rigidez da matriz polimérica. Nessas condiçoes os materiais sao mais rígidos e, consequentemente, as cadeias poliméricas sao menos flexíveis, acumulando um menor volume de água. Os valores de tensao máxima de compressao apresentaram o mesmo comportamento, por isso nao serao mostrados. Por exemplo, a 25 ºC, os valores de tensao máxima de compressao foram 3,6; 24,5 e 40,7 kPa para 2,0; 3,5 e 5,0 mol L-1 de AAm, respectivamente.
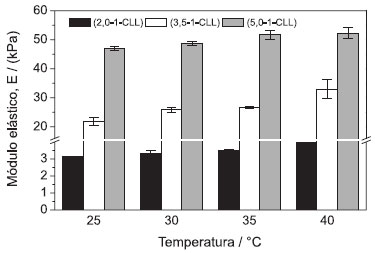 Figura 4. Dependência do módulo elástico (E) com a temperatura para os diferentes hidrogéis estudados. As medidas foram realizadas em replicatas e as barras de erros correspondem ao desvio padrao (D.P.) (média ± D.P., n = 6)
Assim como observado em medidas de E, maiores concentraçoes de AAm ocasionam aumento significativo nos valores de ve, Tabela 1. Por exemplo, o valor calculado de ve para o hidrogel (2,0-1-CLL) é cerca de 0,071 x 10-4 mol cm-3 a 25,0 ºC. Já os valores de ve para hidrogéis (3,5-1-CLL) e (5,0-1-CLL), nessa mesma temperatura, foram 0,33 e 0,58 x 10-4 mol cm-3, respectivamente. Pode-se observar também que as propriedades mecânicas dos sistemas PDLC baseados em hidrogéis de PAAm e CLL sao sensíveis à variaçao da temperatura. Por exemplo, em 40,0 ºC os valores de ve aumentaram de 0,083 para 0,86 x 10-4 mol cm-3 (aumento de mais de 10 vezes) quando a concentraçao de AAm foi variada de 2,0 para 5,0 mol L-1. O aquecimento dos sistemas pode provocar mudanças no arranjo e tamanho micelar (ordem estrutural), visto que nessa temperatura o CLL encontra-se em sua fase isotrópica. Essas variaçoes entrópicas podem contribuir no aumento das interaçoes CLL-matriz. Por outro lado, se a interaçao CLL-matriz polimérica for aumentada, a quantidade relativa de água a ser retida pelos hidrogéis diminui, o que torna os mesmos mais rígidos. Isso pode ser comprovado pelo incremento nos valores de E e ve ao variar a temperatura de análise. O que pode ser uma vantagem, visto que alguns hidrogéis nao apresentam propriedades mecânicas compatíveis com as propriedades requeridas no campo industrial. Além disso, em trabalho anterior20 foi demonstrado que a hidrofilicidade do sistema (2,0-1-CLL) diminui bruscamente com o aumento da temperatura. Por exemplo, a 10,0 ºC o grau de intumescimento, simbolizado por Q, foi igual a 51,5 g g-1 (5150%), enquanto que a 45,0 ºC Q diminui para 34,3 g g-1 (3430%), reduçao de 33,4%. Além disso, foi verificado que o decréscimo em Q é mais pronunciado até temperaturas de aproximadamente 22,0 ºC, temperatura próxima da transiçao de fase TIRe → Nem.
A possibilidade de obtençao de matrizes poliméricas com diferentes características (principalmente hidrofilicidade e rigidez) possibilita formar sistemas com estruturas micelares com variados graus entrópicos (conferindo diferentes propriedades birrefringentes), o que pode se tornar alternativas extremamente interessantes na aplicaçao desses em sistemas PDLC's. Os estudos dos parâmetros estruturais de redes dos hidrogéis com e sem CLL confinado, mostrado na Tabela 1, foram realizados analisando-se três propriedades importantes: massa molar média entre retículos (MC), densidade de reticulaçao (q) e número de cadeias efetivamente elásticas por unidade de volume (ve). Nota-se nitidamente que os fatores concentraçao de AAm e temperatura influenciam substancialmente nas propriedades estruturais dos hidrogéis. Este efeito já era esperado, uma vez que os mesmos também influenciam nas propriedades morfológicas e mecânicas dos hidrogéis. De maneira geral, o aumento da concentraçao de acrilamida e temperatura provocam diminuiçao de MC e incremento de q e ve. Isto é mais um indício de que as propriedades do ambiente de confinamento podem ser controladas e, se for o caso, otimizadas para viabilizar a aplicaçao como sistemas PDLC's.
CONCLUSOES Foi proposto neste trabalho um novo dispositivo óptico PDLC por meio do confinamento, em ambiente totalmente selado, do cristal líquido liotrópico obtido pela mistura ternária LP/DeOH/H2O em hidrogéis de PAAm. O confinamento de cristal líquido em hidrogéis formados por redes com diferentes flexibilidades proporciona ao cristal liquido diferente mobilidade devido às alteraçoes de rigidez que a matriz polimérica pode experimentar. A diferença na mobilidade implica também na alteraçao na entropia dos arranjos micelares, que por sua vez afeta diretamente suas propriedades, principalmente as ópticas. Em consequência foram observadas mudanças significativas nas propriedades espectroscópicas, morfológicas e estruturais. Os fatores concentraçao de AAm e temperatura influenciam substancialmente as propriedades estruturais e mecânicas dos hidrogéis. Este efeito já era esperado, uma vez que os mesmos também influenciam as propriedades morfológicas dos hidrogéis. De maneira geral, o aumento desses fatores provoca diminuiçao de MC e incremento de q e ve. Da mesma forma, a presença de CLL confinado contribui para o aumento da rigidez da matriz de PAAm. Além disso, a presença do cristal líquido proporcionou aos hidrogéis de PAAm propriedades birrefringentes, o que é uma propriedade imprescindível para fabricaçao de PDLC's.
MATERIAL SUPLEMENTAR No material suplementar, disponível gratuitamente em http://quimicanova.sbq.org.br na forma de arquivo PDF, está apresentado na Figura 1S um esquema, em termos de ordem orientacional, a diferença entre cristais líquidos, sólidos cristalinos e líquidos isotrópicos. Na Figura 2S é apresentada à caracterizaçao da formaçao de laurato de potássio (LP) por RMN. Na Figura 3S sao apresentadas micrografias obtidas por Microscopia Eletrônica de Varredura das superfícies dos hidrogéis (2,0-1-0) e (2,0-1-CLL). Na Figura 4S sao mostradas micrografias obtidas por Microscopia Optica de Luz Polarizada das amostras (2,0-1-0) e (2,0-1-CLL) em três diferentes ângulos de polarizaçao a 25,0 ºC.
AGRADECIMENTOS Os autores agradecem à Coordenaçao de Aperfeiçoamento de Pessoal de Nível Superior (CAPES) e ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) pelas bolsas concedidas e pelo suporte financeiro.
REFERENCIAS 1. Chandrasekhar, S.; Liquid Crystals, Cambridge University Press: Cambridge, 1992. 2. Bechtold, I. H.; Revista Brasileira de Ensino de Fisica 2005, 27, 333. 3. Jan, L. S. S.; Radiman, M. A.; Siddig, S. V.; Muniandy, M. A.; Jamali, H. D.; Colloids Surf., A 2004, 251, 43. 4. Hoppe, C. E.; Galante, M. J.; Oyanguren, P. A.; Williams, R. J. J.; Mater. Sci. Eng., C 2004, 24, 591. 5. Tanabe, Y.; Furue, H.; Hatano, J.; Mater. Sci. Eng., B 2005, 120, 41. 6. de Gennes, P. G.; Prost, J.; The Physics of Liquid Crystals, Oxford University Press: Oxford, 1993. 7. Brown, G. H.; Doane, J. W.; Neft, V. D.; A Review of the Structure and Physical Properties of Liquid Crystals, CRC: Cleveland, 1971. 8. Nielsen, J. A.; Birgeneau, R. J.; Kaplan, M.; Litster, J. D.; Safinya, C. R.; Phys. Rev. Lett. 1997, 39, 1668. 9. Marchal, F.; Nardello-Rataj, V.; Chailloux, N.; Aubry, J.-M.; Tiddy, G. J. T.; J. Colloid Interface Sci. 2008, 321, 177. 10. Montecinos, R.; Ahumada, H.; Araya-Maturana, R.; Olea, A. F.; Weiss-López, B. E.; J. Colloid Interface Sci. 2007, 316, 126. 11. Li, D.; Fujikawa, D.; Yoshimura, T.; Uota, M.; Sakai, G.; Kijima, T.; J. Mol. Liq. 2008, 138, 113. 12. Gao, Y. Z.; Song, P.; Zhang, T.; Yao, W.; Ding, H.; Xiao, J.; Zhu, S.; Cao, H.; Yang, H.; RSC Adv. 2013, 3, 23533. 13. Wang, J.; Shi, S.; Han, X.; Zhou, S.; Zhang, B.; Colloid Polym. Sci. 2012, 290, 1659. 14. Deshmukh, R. R.; Malik, M. K.; J. Phys. Chem. Solids 2013, 74, 215. 15. Wang, L.; Meng, F.; Sun, Y.; Yang, H.; Composites, Part B 2013, 45, 780. 16. Marin, L.; Popescu, M.; Zabulica, A.; Uji-I, H.; Fron, E.; Carbohydr. Polym. 2013, 95, 16. 17. Jesus, M. M. A. de; Dissertaçao de Mestrado, Universidade Estadual de Maringá, Brasil, 2005. 18. Aouada, F. A.; Dissertaçao de Mestrado, Universidade Estadual de Maringá, Brasil, 2005. 19. Aouada, F. A.; de Moura, M. R.; Fernandes, P. R. G.; Rubira, A. F.; Muniz, E. C.; Eur. Polym. J. 2005, 41, 2134. 20. Aouada, F. A.; de Moura, M. R.; Fernandes, P. R. G.; Mukai, H.; da Silveira, A. C. F.; Itri, R.; Rubira, A. F.; Muniz, E. C.; Eur. Polym. J. 2006, 42, 2781. 21. Wu, Z. L.; Kurokawa, T.; Gong, J. P.; Polym. J. 2012, 44, 503. 22. Lin, I.; Birchall, L. S.; Hodson, N.; Ulijn, R. V.; Webb, S. J.; Soft Matter 2013, 9, 1188. 23. Brito, C. W. de Q.; Rodrigues, F. H. A.; Fernandes, M. V. da S.; Silva, L. R. D. da; Ricardo, N. M. P. S.; Feitosa, J. P. A.; Muniz, E. C; Quim. Nova 2013, 36, 40. 24. Kowalczyk, A.; Fau, M.; Karbarz, M.; Donten, M.; Stojek, Z.; Nowicka, A. M.; Biosens. Bioelectron. 2014, 54, 222. 25. Aouada, F. A.; Muniz, E. C.; Vaz, C. M. P.; Mattoso, L. H. C.; Quim. Nova 2009, 32, 1482. 26. Oviedo, I. R.; Mendez, N. A. N.; Gomez, M. P. G.; Rodriguez, H. C.; Martinez, A. R.; Int. J. Polym. Mater. 2008, 57, 1095. 27. Kimura, N. M.; Dissertaçao de Mestrado, Universidade Estadual de Maringá, Brasil, 2003. 28. Muniz, E. C.; Geuskens, G.; J. Membr. Sci. 2000, 72, 287 29. Goda, T.; Watanabe, J.; Takai, M.; Ishihara. K.; Polymer 2006, 47, 1390. 30. Singh, T. R. R.; McCarron, P. A.; Woolfson, A. D.; Donnelly, R. F.; Eur. Polym. J. 2009, 45, 1239. 31. Bajpai, A. K.; Giri, A.; Carbohydr. Polym. 2002, 53, 271. 32. Lin, Z.; Wu, W.; Wang, J.; Jin, X.; React. Funct. Polym. 2007, 67, 789. 33. Amsden, B.; Macromolecules 1999, 32, 874. 34. Aouada, F. A.; Moura, M. R. de; Menezes, E. D.; Nogueira, A. R. A.; Mattoso, L. H. C.; R. Bras. Ci. Solo 2008, 32, 1643. 35. Wahlstrom, E. E.; Cristalografia Optica, Editora da USP: Rio de Janeiro: 1969. 36. Van Vlack, L; Princípios de ciências dos materiais, Edgard Bluchen: Sao Paulo, 1970. 37. Buchholz, F. L.; Graham, A. T.; Modern Superabsorbent Polymer Technology, Wiley-VCH: New York, 1997. 38. Callister, W. D.; Materials Science and Engineering: An Introduction, Wiley: New York, 1999. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access