Artigo
|
|
| Evaluación térmica del curado de adhesivos base SBR usando peróxido de dicumilo Thermal evaluation of curing of SBR based adhesives using dicumyl peroxide |
|
Beatriz Adriana Salazar-CruzI; José Luis Rivera-ArmentaI,*; Ricardo García-AlamillaI; Ana María Mendoza-MartínezI; Alejandro Esquivel de la GarzaII; Sergio Moctezuma EspiricuetoII
IDivisión de Estudios de Posgrado e Investigación, Instituto Tecnológico de Ciudad Madero, 89440, Ciudad Madero, Tamaulipas, México Recebido em 28/09/2014 *e-mail: jlriveraarmenta@itcm.edu.mx Curing is an important process in adhesive formulation, but scant reports on the study of the kinetics of curing in adhesive are currently available, particularly for formulations including styrene-butadiene copolymers. The focus of the present work was to thermodynamically quantify the curing reaction in pressure-sensitive adhesives (PSA) obtained from styrene-butadiene copolymers, the effect of dicumyl peroxide (DCP) ratio, which acts as a crosslinking agent, and also evaluate the effect of two reactive adhesive resins, sylvalite and piccolyte. Kinetic parameters were determined by differential scanning calorimetry (DSC) in an isothermic and dynamic mode, gel content was determined as was swelling degree, given these characteristics can be associated with the curing reaction. The kinetic study showed the curing reaction was first order, according to the Ozawa and Kissinger equation. Resins have affinity to BR segment, while in the case of sylvalite and piccolyte to the PS segment, varying behavior with dicumyl peroxide in the adhesive mixture. Lower swelling values were associated with an increase in crosslinking, indicative a curing reaction took place, and the gel content test was used to corroborate the results. INTRODUCCIÓN Recientemente, los copolímeros con bloques poliestirenicos han resultado ser materiales de elección en una gran variedad de aplicaciones en adhesivos. De manera particular, los adhesivos sensitivos a la presión (PSA) se pueden obtener con la adición de copolímeros dibloque, y otros ingredientes tales como resina adhesivas.1-3 Por otro lado, la compatibilidad de las resinas adhesivas en los copolímeros del tipo estireno-isopreno-estireno (SIS), estireno-butadieno aleatorizado (SBR), estireno-butadieno-estireno (SBS) y estireno-etileno-butadieno-estireno (SEBS), son compatibles al bloque intermedio o terminal del copolimero impartiendo diferentes propiedades viscoelásticas. Las resinas adhesivas influyen en el incremento de la Tg del bloque intermedio o del bloque terminal, dependiendo de su compatibilidad con cualquiera de los bloques y la compatibilidad de la resina adhesiva con el bloque intermedio disminuye el valor del módulo en la zona del plateau, lo cual genera la adhesividad del material. Las resinas adhesivas que son compatibles con ambos bloques ocasionan un incremento en la Tg del bloque intermedio y disminuyen la Tg del bloque terminal dependiendo del peso molecular y la Tg de las resinas adhesiva. Los elastómeros tipo estireno-butadieno (SBR) tienen una gama de aplicación en adhesivos debido a su desempeño en un rango de temperaturas amplio, lo que permite orientarlos aplicaciones adhesivas en cintas, etiquetas, embalaje, adhesivos no tejidos, adhesivos industriales, edificio, construcción, etc. El desempeño de adhesivos que utilizan SBR en su formulación depende de factores como el contenido de estireno, tipo de estructura (radial o lineal), viscosidad, entre otros.4 Algunos estudios en adhesivos sensitivos a la presión que contienen copolímeros en bloques han sido reportados,5-7 en los estudios se discuten: el efecto del sustrato y las resina adhesivas en las fuerzas de despegue para adhesivos hot melt (HM) con SIS,5 y el efecto de los SIS en adhesivos PSA mezclados con resina adhesivas como diciclopentadieno hidrogenadas (H-DCPD),6 así como el estudio de copolímeros con etilen vinil acetato (EVA) en adhesivos hot melt sensitivos a la presión HMPSAs.7,8 Sin embargo, de los reportes existentes no existe información sobre el estudio de la reacción de curado empleando copolímeros base estireno-butadieno, por lo que en el presente trabajo se reporta la evaluación térmica de la reacción de curado empleando como agente de curado peróxido de dicumilo en adhesivos formulados a partir de elastómeros estireno-butadieno (SBR).
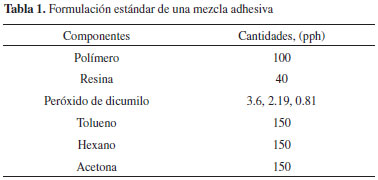
EXPERIMENTAL Materiales Copolímero estireno- butadieno (SBR) de estructura lineal al azar en bloque con un contenido de estireno total de 25% y un 17.5% de estireno en bloque en el copolímero, suministrado por Dynasol Elastómeros.4 Resina politerpene estirenada, comercialmente identificada como Piccolyte®HM106, con una temperatura de ablandamiento de 106 ºC y una viscosidad Brookfield® a 140 ºC de 4300 cP, suministrada por Pinova Inc.®.9 Resina éster de pentaeritritol, comercialmente identificada como Sylvalite® RE100L, con una temperatura de ablandamiento de 100 ºC y una viscosidad Brookfield a 150 ºC de 955 cP, suministrada por Arizona Chemical Inc®.10 Peróxido de dicumilo (PDC), suministrado por Retilox® Co.11 Los solventes utilizados fueron n-hexano, tolueno y acetona grado ACS, suministrado por Aldrich Chemical Co. Proceso de mezclado La mezcla adhesiva se llevó a cabo en un reactor de vidrio agitado mecánicamente con un equipo IKA EUROSTAR modelo RW16. El mezclado se desarrolló a temperatura ambiente por un periodo de dos horas, se realizó una formulación tipo para esta investigación, la cual se especifica en la Tabla 1 en donde se mantiene constante la cantidad de las resinas piccolyteHM106 y sylvaliteRE100L, variando la cantidad de peróxido de dicumilo, las cantidades de los componentes fueron establecidas en partes por cien de hule (pph).
Elaboración de películas adhesivas Las películas adhesivas fueron elaboradas vertiendo una cantidad constante de la mezcla adhesiva en un recipiente de papel siliconado de 10 × 5 × 2 cm llevándolas a una campana de extracción hasta la completa evaporación del solvente, estas películas se utilizaron para posteriores análisis. Las películas fueron curadas a 170 ºC por un periodo de dos horas. Hinchamiento en tolueno El hinchamiento de materiales es un método tradicional para evaluar el entrecruzamiento de polímeros 12 siendo la técnica gravimétrica la más utilizada para cuantificar el solvente captado. El peso inicial del material fue registrado y después la muestra fue sumergida en recipientes conteniendo tolueno a 25 ºC por 24 h y agitación mecánica. Se removió material del tolueno, se secó con papel absorbente para retirar el exceso de solvente en su superficie y posteriormente se pesó en una balanza analítica para determinar la ganancia en peso. Finalmente se determinó la cantidad de solvente absorbida por material expresada en porcentaje, usando la Ecuación (1).12 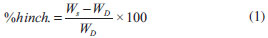 donde Ws es el peso de la muestra hinchada, WD es el peso de la muestra en seco. El contenido gel (%Gel) se calculó de acuerdo con la Ecuación (2):13 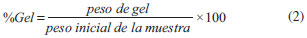 La fracción de volumen del adhesivo hinchado (V2m) fue determinada por la ecuación (3),14 estimada mediante el ensayo de hinchamiento en tolueno (rs = 0.8669 g cm-3),1 este parámetro puede ser correlacionado con la densidad de entrecruzamiento.  donde WD y Ws son el peso de la muestra seca e hinchada, ρ es la densidad del polímero y ρs la densidad del solvente. Análisis termogravimétrico Se estudió la descomposición de los componentes de la formulación debido a la aplicación de calor a través de un equipo TA Instruments modelo STD2960. Los ensayos fueron conducidos a una rampa de calentamiento de 10 ºC min-1 entre 40 y 700 ºC en una atmosfera de N2 sobre muestras de peso aproximado de 10 mg. Con este ensayo, se buscaba obtener la estabilidad térmica de los componentes de la mezcla adhesiva, así como una correlación con el ensayo de DSC para determinar los cambios que estaban asociados con la pérdida de peso en la formulación. Tanto este ensayo como el de DSC, se realizaron sobre muestras de material no procesado (no reticulado) para observar, precisamente, estas reacciones y los cambios que producen en función del intercambio térmico dentro de las celdas de ensayo. Calorimetría diferencial de barrido (DSC) Las propiedades térmicas se midieron con un equipo Perkin Elmer DSC8000 en un rango de temperatura de 40 a 250 ºC; los pesos de las muestras fueron aproximadamente de 10 mg. Esta técnica fue utilizada para estudiar la cinética a partir de experiencias dinámicas e isotérmicas. a) Método dinámico En este método se utilizaron diferentes rampas de calentamiento de 2, 5, 7, 10, 13, 15, 17 y 20 ºC min-1. Cuando la muestra es sometida a calentamiento mediante DSC, se pone de manifiesto un proceso exotérmico cuyo máximo aparece una temperatura llamada temperatura pico (Tp), los modelos aplicados a los parámetros de cálculo de la energía de activación se basan en el desplazamiento que sufre dicho pico al modificar la rampa de calentamiento (q) de la muestra. El desplazamiento observado es una consecuencia de la expresión matemática de la ley cinética y fue estudiada por Kissinger,15 y por Ozawa16 donde aplican métodos diferentes para el cálculo de la energía de activación. Método Ozawa Según el método de Ozawa, la energía de activación cumple la Ecuación (4). 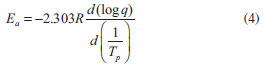 Representando log (q) frente a 1/Tp, se obtiene una recta cuya pendiente dará el valor de Ea. Método Kissinger El método propuesto por Kissinger, la energía de activación está dada por la Ecuación (5). 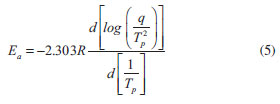 La representación de log b) Método isotérmico El procedimiento de trabajo consistió en llevar la muestra desde temperatura ambiente hasta la temperatura de estudio 170 ºC y se mantuvo en condiciones isotermas hasta observarse la recuperación de la línea base en el termograma tras el proceso exotérmico. Los valores del grado de conversión (α) y la rampa de reacción (r) a un tiempo dado, se relacionan con los datos proporcionados por el equipo DSC a través de las ecuaciones (6) y (7).  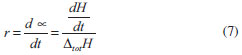 donde Δt H, es el calor de reacción desarrollado en el tiempo t, obtenido por integración parcial del área en la curva de DSC; Δtot H, es el calor de reacción desarrollado en el proceso completo y dH/dt es el flujo de calor medido por el equipo. El orden de la reacciones para sistema con peróxido de dicumilo son próximos a la unidad de acuerdo con la bibliografía,17-19 donde se supone mecanismos de reacción de primer orden para los procesos de reticulación de polímeros/peróxido. A partir de los parámetros cinéticos obtenidos se intentó reproducir la evolución del grado de conversión con respecto al tiempo, curva que había sido obtenida a partir de los datos experimentales. Dichas curvas corresponden a la forma integrada de la ley general de rampa de reacción. Esta ecuación ha sido integrada para el caso de un mecanismo de orden n,17 y está dada por la ecuación (8). 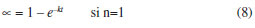
RESULTADOS Y DISCUSIÓN Prueba de hinchamiento En la Figura 1, se presentan los resultados de % de hinchamiento y % Gel de la mezcla adhesiva con SBR y con resinas piccolyte y sylvalite. Se puede observar que al incluir en la formulación las resinas se presenta una disminución en el % de hinchamiento y un aumento en el %Gel de los adhesivos, indicando con esto que el entrecruzamiento del adhesivo SBR sin resina es menor que cuando se adicionaron las resinas. Las mezclas adhesivas al pasar por un proceso de curado presentan un efecto de reticulación, indicado por el alto contenido de % Gel y el efecto inverso del % hinchamiento, mostrado claramente en la muestra SBR/Sylvalite/2.19 pph peróxido, también se observó una tendencia del efecto reticulante a medida que aumentaba la cantidad de agente entrecruzante adicionado. Este comportamiento se presenta por el rompimiento de la molécula de peróxido de dicumilo, generando radicales libres, los cuales se estabilizan con hidrógenos de la cadena polimérica, siendo la parte más débil la del grupo vinílico, provocando inestabilidad en la cadena principal la cual se estabiliza con otra de igual composición lo que aumenta la reticulación en la estructura, esto se ve influenciado mas significativamente por la resina sylvalte RE100L debido a su afinidad con el bloque vinílico. Por otro lado las mezclas adhesivas preparadas con resina piccolyte HM106 presentan un % hinchamiento mayor, debido principalmente a la compatibilidad que esta presenta hacia el bloque de PS, ocasionando impedimento estérico para el proceso de curado, indicando un menor efecto reticulante. Es importante observar que los valores de hinchamiento posteriores a la relación de 2.19 pph de peróxido de dicumilo, no presentan cambios significativos en la mayoría de la serie de mezclas adhesivas, por lo que se establece que la adición óptima puede ser hasta esa relación, debido a que cantidades mayores no presentan cambios significativos en los resultados.
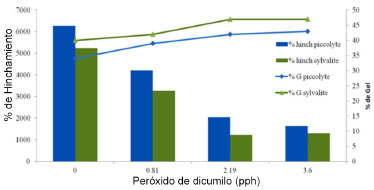 Figura 1. Efecto del % hinchamiento y % Gel en adhesivos SBR comparando las resinas Piccolyte HM106 y Sylavlite RE100L, a diferentes relaciones de peróxido de dicumilo
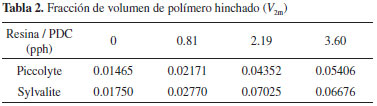
El factor V2m mostrado en la Tabla 2, el cual está relacionado con la densidad de entrecruzamiento, nos indica que para las mezclas adhesivas con la resina piccolyte HM106 el número de cadenas que no están incorporadas en la red sigue siendo mucho mayor en comparación a las mezclas con la resina sylvalite RE100L. Cabe mencionar que la adición tanto de las resinas como del agente de entrecruzamiento afectan este parámetro de fracción volumen ya que todos los valores para las mezclas adhesivas con resinas y agente de entrecruzamiento son mayores que la mezcla adhesiva con adhesivo basado en SBR.
Análisis de estabilidad térmica por TGA Las curvas de TGA presentan la pérdida de peso de las formulaciones en función del aumento de la temperatura. Como se observa en la Figura 2, la descomposición del peróxido de dicumilo inicia aproximadamente a 100 ºC y el copolímero alrededor de 300 ºC, esta información es relevante para asegurar la estabilidad térmica del copolímero siendo más estable que el agente reticulante. La temperatura inicial de descomposición es utilizada para predecir la estabilidad térmica de los materiales.18 La derivada de la curva muestran que la temperatura máxima de descomposición es de 450 ºC para el SBR y de 160 ºC para el peróxido de dicumilo mostrado en la Tabla 3, lo anterior es indicativo que cualquier proceso exotérmico observado por debajo de 200 ºC implica solo la activación de peróxido para formar radicales y formación de redes tridimensionales, resultado del entrecruzamiento. Las derivadas de las curvas termogravimétricas, muestran los datos de descomposición máxima y son utilizados como temperaturas de descomposición.18
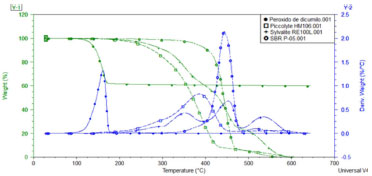 Figura 2. Curva TGA para el peróxido de dicumilo, resina Piccolyte HM106 y Sylvalite RE100L y copolimero

Evaluación del proceso de descomposición /reticulación de las mezclas adhesivas por DSC El estudio se centró en los sistemas SBR/peróxido de dicumilo, en concentraciones de 0.81 y 3.60 pph de peróxido de dicumilo y las variaciones correspondientes con la resina piccolyte HM106 y sylvalite RE100L. Se observó que las temperaturas pico (Tp) encontradas por DSC para el peróxido de dicumilo son ligeramente mayores (164 - 172 ºC) a la temperatura mostrada en la Figura 2 para el peróxido de dicumilo, donde se muestra una Tp para el peróxido de dicumilo de 161.56 ºC (método TGA). De acuerdo con los resultados también se puede observar que las muestras dan lugar a un proceso exotérmico suficientemente energético, con valores de ΔH que van de -41 a -56 J g-1, como para permitir el estudio de la cinética del proceso de reticulación. Al mismo tiempo, los valores de los parámetros cinéticos que se obtengan podrán ser extrapolados a sistemas con menor contenido en peróxido.18 Lo anterior nos ayuda a establecer la temperatura para el estudio cinético en mediciones isotérmicas, la elección de las condiciones de estudio se realizaron tras varias pruebas a diferentes temperaturas, es importante mencionar, que temperaturas de estudio bajas conducen tiempos de isoterma muy elevados, picos exotérmicos anchos y de poca intensidad, lo que en ocasiones podría dar lugar a relaciones señal/ruido inadecuadas. Se encontró que en caso de las películas adhesivas era necesaria una temperatura de 170 ºC. En la Figura 3 se muestra, la curva de DSC obtenida para el estudio cinético en modo isotermo en el caso de los sistemas SBR/0.81PDC/sylvalite a 170 ºC. En el caso de los demás materiales las curvas DSC obtenidas fueron similares.
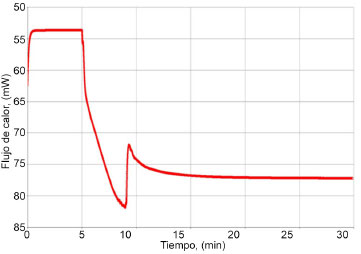 Figura 3. Curva DSC típica obtenida en modo isotérmico para la mezcla SBR/0.81PDC/sylvalite @ 170 ºC
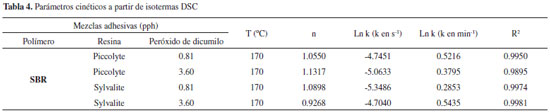
Mecanismo de reacción de entrecruzamiento de orden n En la Tabla 4 se muestran los parámetros de ajuste obtenidos para sistemas polímero/peróxido/resina estudiados, como lo es n y ln k, así como el cuadrado del coeficiente de correlación de ajuste (R2). Los valores encontrados para el orden de la reacción concuerdan con lo reportado por Brazier,20 esto es definido con coeficientes de correlación cercanos a la unidad.15,19
La reproducción de las curvas α vs t mostrado en la Figura 4, presenta una concordancia aceptable entre los valores experimentales y las curvas correspondientes al mecanismo de orden n.
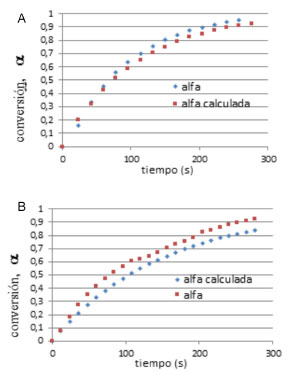 Figura 4. Reproducción de curvas α vs tiempo a partir de parámetros cinéticos de mezclas adhesivas SBR/Sylvalite/3.PDC (A) y SBR /Piccolyte/3.60PDC (B)
Los resultados presentados hasta el momento han sido obtenidos por aplicación de procedimientos para lo que es necesario obtener la entalpía total de reacción, DtotH, lo que supone la integración del área bajo la curva DSC asociado con la reacción de reticulación. En estudios isotérmicos para sistemas EVA/peróxido y SBS/peróxido se obtienen picos anchos y poco intensos, lo que da lugar a una alta dispersión de datos experimentales. El estudio para la determinación de parámetros cinéticos como energía de activación y factor de frecuencia en los procesos de descomposición del peróxido y formación de redes poliméricas son establecidas por condiciones dinámicas.21 Análisis cinético a partir de curvas dinámicas En la Figura 5, se presentan las curvas DSC obtenidas a diferentes velocidades de calentamiento, de las cuales se obtuvo el valor de la temperatura Tp y los valores de entalpía del pico que se atribuye a la reacción de curado. Puede observarse que la Tp se recorre a temperaturas más bajas conforme la velocidad de calentamiento disminuye en la mezcla adhesiva.
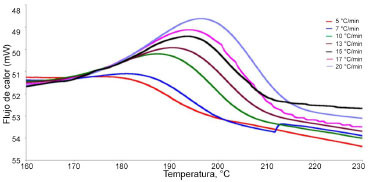 Figura 5. Influencia de la velocidad de calentamiento en la Tp en la mezcla SBR/3.6 pph PDC
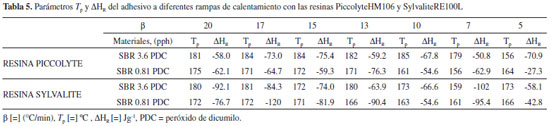
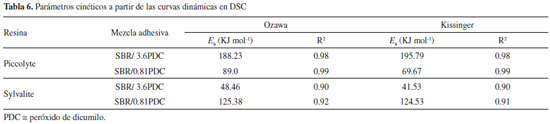
A partir de los resultados de las curvas DSC, se obtuvieron los valores de la entalpía de reacción y la Tp los cuales se presentan en la Tabla 5. Se puede observar que en todos los casos se observa un desplazamiento en la Tp que está asociada con la reacción de curado, apareciendo a temperaturas superiores con el cambio de la rampa de calentamiento. La Tabla 6 muestra los valores de la energía de activación obtenidos por la aplicación de los dos modelos propuestos así como los valores de error tipo. La concentración de peróxido afecta de forma directamente proporcional a la energía de activación generando mayor reticulación de los sistemas a altas concentraciones, aunado a ello también se ve influenciado este efecto por la compatibilidad de las resinas hacia los bloques presentes en el copolímero. La presencia de dobles enlaces presentes en el bloque de polibutadieno, dependiendo de su posición facilitará el proceso de reticulación.17 Wu y col.,22 reportan que altas concentraciones de PDC genera la formación de altas concentraciones de radicales libres en el sistema, provocando una cantidad considerable de dobles enlaces por la estructura SBS, generando reacción de reticulación entre cadenas poliméricas.
Akiba y col.23 establece que para polibutadienos con alto contenido dobles enlaces 1,2- presentan mayores eficiencias de reticulación, lo que sugiere que las unidades de vinilo de cadena lateral se someten a reacciones de adición más fácilmente que los dobles enlaces en la cadena. Aunque existe una cierta dispersión de resultados en cuanto a la energía de activación calculada por diferentes métodos, en general, los valores obtenidos son coherentes con valores encontrados con polímeros similares.17 Es interesante notar que, si bien la energía de activación es un parámetro cinético que se obtiene por ajustes matemáticos, proporciona una idea clara de la cantidad de reticulación presente en el sistema. Es importante mencionar que el método Kissinger presenta los mismos inconvenientes que el método de Ozawa aplicado a la Tp.
CONCLUSIONES Con base en los resultados, tenemos que el efecto por la adición de la resina sylvalite RE100L es más significativo en la reacción de curado, debido a su afinidad con el bloque de BR, lo anterior de acuerdo con los resultados de la prueba de hinchamiento donde los adhesivos presentaron menor % hinchamiento e inversamente mayor factor de V2m. En el análisis cinético se comprueba también este efecto, generándose mayor ajuste en las curvas de simulación de conversión con respecto al tiempo para las muestras formuladas con resina sylvaliteRE100L. En las entalpías de reacción para las curvas dinámicas se observa que los adhesivos con la resina sylvaliteRE100L presentan también valores mayores en comparación a las mezclas adhesivas con la resina piccolyteHM106. Es importante mencionar que este fenómeno no está asociado únicamente a la descomposición del peróxido, sino también a la reticulación del polímero. La Ea está supeditada al tipo de resina comercial utilizada y al contenido de PDC, con base a lo anterior, debido a la compatibilidad que la resina piccolyte presenta con el bloque PS se genera impedimento estérico, provocando una disminución en el proceso de entrecruzamiento aunado a la distribución de la estructura química del bloque PB en el copolímero SBR.
RECONOCIMIENTOS A la Dirección General de Educación Superior Tecnológica (DGEST) por el apoyo con beca de manutención a uno de los autores B.A. Salazar Cruz y a Dynasol Elastomeros por proporcionar los elastómeros para la realización del estudio.
REFERENCIAS 1. Chu, S. G. Viscoelastic properties of pressure sensitive adhesives; In: Handbook of pressure sensitive adhesive technology; Satas, D., ed.; 2nd ed., Van Nostrand Reinhold: New York, 1989, chap. 8. 2. Kanderski, M.; Ofna, Española de patentes y marcas ES2429964 T3, 2013. 3. Hansen, D. D.; Eur pat. Off. EP0612822B1, 1994. 4. http://www.dynasolelastomers.com/products/ssbr/s-1205/, accesada Octubre 2013. 5. Kim, D. J.; Kim, H. J.; Yoon, G. H.; Int. J. Adhes. Adhes. 2005, 25, 288. DOI: http://dx.doi.org/10.1016/j.ijadhadh.2004.10.001 6. Kim, D. H.; Do, H. S.; Kim, H. J.; J. Appl. Polym. Sci. 2006, 102, 2839. DOI: http://dx.doi.org/10.1002/app.24571 7. Park, Y. J.; Joo, H. S.; Kim, H-J.; Lee, Y. K.; Int. J. Adhes. Adhes. 2006, 26, 571. DOI: http://dx.doi.org/10.1016/j.ijadhadh.2005.09.004 8. Takemoto, M.; Kajiyama, M.; Mizumachi, H.; Takemura, A.; Ono, H.; J. Appl. Polym. Sci. 2001, 83, 719. DOI: http://dx.doi.org/10.1002/app.2266.abs 9. http://www.pinovainc.com/, accesada Octubre 2013. 10. www.arizonachemical.com/, accesada Octubre 2013. 11. http://www.retilox.com.br/espanol/productos, accesada Septiembre 2013. 12. Orozco-Guareño, E.; Hernández, S. L.; Gómez-Salazar, S.; Rev. Mex. Ing. Quím. 2011, 10, 465. 13. Morales Rivera, A.; Zuluaga Corrales, H. F.; Rev. Fac. Ing. 2006, 37, 82. 14. Mansilla, M. A.; Ghilarducci, A.; Salva, H.; Marzocca, A. J.; Abstracs IBEROMET XIX, Viña del Mar, Chile, 2010. 15. Kissinger, H. E.; Anal. Chem. 1957, 29, 1702. DOI: http://dx.doi.org/10.1021/ac60131a045 16. Dannenberg, M.; Jordan, M. E.; J. Polym. Sci. 1958, 3, 127. DOI: http://dx.doi.org/10.1002/pol.1958.1203112215 17. Escoto Palacios, Tesis doctoral, Universidad de Alicante, España, 1995. 18. Vallat, M., Ruch, F., David, M.; Eur. Polym. J. 2004, 40, 1575. DOI: http://dx.doi.org/10.1016/j.eurpolymj.2004.01.026 19. Loan, L. D.; J. Appl. Polym. Sci., 1963, 7, 2259. DOI: http://dx.doi.org/10.1002/app.1963.070070624 20. Brazier, D. W.; Schwartz, N. V.; Thermochim. Acta 1980, 39, 7. DOI: http://dx.doi.org/10.1016/0040-6031(80)80052-9 21. Ellul, D.; Tsou, A. H.; Hu, W.; Polymer 2004, 45, 3351. DOI: http://dx.doi.org/10.1016/j.polymer.2004.03.029 22. Wu, G.; Jiang Y., Ye, L.; Zeng, S.; Yu, P.; Xu, W.; Int. J. Adhes. Adhes. 2010, 30, 43, DOI: http://dx.doi.org/10.1016/j.ijadhadh.2009.08.002 23. Akiba, M.; Hashim, A. S.; Prog. Polym. Sci. 1997, 22, 475. DOI: http://dx.doi.org/10.1016/S0079-6700(96)00015-9 |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access






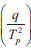 entre 1/Tp será una recta cuya pendiente dará el valor de Ea. Los modelos anteriores en especial el método de Kissinger, son utilizados para el cálculo de la energía de activación del proceso de descomposición, así como del proceso de reticulación de los polímeros.
entre 1/Tp será una recta cuya pendiente dará el valor de Ea. Los modelos anteriores en especial el método de Kissinger, son utilizados para el cálculo de la energía de activación del proceso de descomposición, así como del proceso de reticulación de los polímeros.