Educação
|
|
| Ressonância magnética nuclear de substâncias organofluoradas: um desafio no ensino de espectroscopia Nuclear magnetic resonance of organofluorine compounds: a challenge in the teaching of spectroscopy |
|
Frederico Silva Castelo BrancoI,II; Bárbara V. SilvaII; Gabriel Freitas do RioII; Mábio Joao SantanaIII; Luiz Henrique Keng Queiroz JúniorIII; Angelo C. PintoII; Núbia BoechatI; Luciano Morais LiaoIII,*
IDepartamento de Síntese de Fármacos, Instituto de Tecnologia de Fármacos, Fundação Oswaldo Cruz, Farmanguinhos - Fiocruz, 21041-250 Rio de Janeiro - RJ, Brasil Recebido em 16/05/2015 *e-mail: lucianoliao@ufg.br Nuclear magnetic resonance is a technique that is widely used for elucidating and characterizing organic substances. Organofluorine substances have applications in many areas from drugs to liquid crystals, but their NMR spectra are often challenging due to fluoride coupling with other nuclei. For this reason, NMR spectra of this class of substances are not commonly covered in undergraduate and graduate chemistry courses and related fields. Thus, the aim of this work was the presentation and discussion of 1H, 13C, and 19F NMR spectra of eleven organofluorine substances which, in the case of 1H and 13C nuclei, showed classic patterns of first-order coupling and the effects of the fluorine nucleus in different chemical and magnetic environments. In addition, the observation of long distance coupling constants was possible through the use of apodization functions in the processing of the spectra. It is expected that the examples presented herein can be utilized and discussed in undergraduate and graduate NMR spectroscopy disciplines and thus improve the teaching and future research of organofluorine compounds. INTRODUÇAO O flúor foi descrito pela primeira vez por Georgius Agricola, em 1529, que atribuiu à sua descoberta o nome de fluorita, o que mais tarde veio a ser identificado como fluoreto de cálcio (CaF2).1 O termo "flúor", em latim, significa "fluir". Este elemento recebeu esta denominaçao devido à fluorita, que era usada para separar os metais do minério ao diminuir o seu ponto de fusao. O flúor elementar (F2) só foi isolado séculos mais tarde, por meio da eletrólise da mistura de bifluoreto de potássio (KHF2) em ácido fluorídrico (HF) realizada por Henri Moissan, em 1886, laureado 40 anos depois, em 1906, com o prêmio Nobel de Química.2,3 Com 9 prótons e 9 elétrons, massa atômica de 19 u, raio atômico de 50 pm e estado de oxidaçao -1, o flúor é caracterizado por elevada dureza química e, especialmente, por possuir a maior eletronegatividade entre os elementos conhecidos. A introduçao do flúor em moléculas orgânicas faz com que elas tenham muitas aplicaçoes industriais, pois proporciona novos efeitos a estas moléculas. Estes efeitos estao atribuídos a quatro principais características:2-10
Os organofluorados sao encontrados em sistemas refrigerantes, propelentes em aerossóis, plásticos, solventes, surfactantes, cristais líquidos e, principalmente, em fármacos e agroquímicos.2-10 Até 2010, 20% de todos os medicamentos em uso e 30% dos 30 mais utilizados eram organofluorados.8 As ressonâncias magnéticas nucleares de 19F, 1H e 13C de moléculas organofluoradas A ressonância magnética nuclear é a técnica mais importante para a elucidaçao estrutural de uma molécula e permite a detecçao de muitos núcleos, tais como 1H, 13C, 15N, 29Si e 31P. RMN de 19F de organofluorados Em decorrência da vasta aplicaçao industrial dos organofluorados, a espectroscopia de ressonância magnética nuclear de flúor (19F RMN) ganhou grande relevância. Atualmente, os espectrômetros de ressonância magnética nuclear, disponíveis em indústrias e instituiçoes acadêmicas, possuem a sonda (parte interna do aparelho, na qual se insere a amostra a ser analisada, com frequência específica para cada núcleo, em um determinado campo magnético) para o núcleo de flúor. Este fato, acrescido à importância dos organofluorados, faz com que o espectro de RMN de 19F seja o terceiro mais utilizado, após os de 1H e 13C.11-13 O núcleo do flúor tem a vantagem de ter 100% de abundância natural e alta razao giromagnética, é 20% menos sensível que 1H, e ressona a 94% da radiofrequência do 1H. Os espectros de RMN de 19F de organofluorados sao geralmente de primeira ordem e possuem o intervalo de deslocamento químico muito maior que o de 1H, com cerca de 350 ppm. Além disso, a intensidade dos sinais no espectro de RMN de 19F é bastante informativa, pois fornece o número relativo deste elemento naquele sinal, bem como os possíveis acoplamentos que estes possam realizar entre si. Levando-se em conta que moléculas fluoradas sao essencialmente ausentes no meio biológico, para análises in vivo nao há sobreposiçao de sinais de fundo, ou seja, as moléculas fluoradas aplicadas no organismo podem ser estudadas por RMN de 19F sem que haja a interferências de sinais de substâncias endógenas, como há no caso dos de RMN de 1H, 13C e 15N. Esta vantagem permite que a RMN de 19F seja usada para estudar complexos multiproteicos e para o monitoramento direto in vivo em estudo de metabolismo de fármacos contendo flúor.6,14,15 A RMN de 19F também tem sido muito utilizada na detecçao de impurezas nos processos de fabricaçao de farmoquímicos. O fluorotriclorometano, o fluorofórmio (CFCl3), é o padrao interno aceito para assinalar o deslocamento zero na RMN de 19F embora o sinal nao seja um singleto. O sinal do CFCl3 apresenta quatro linhas de intensidades diferentes, devido ao efeito isotópico dos núcleos de cloro com deslocamentos químicos diferentes. Cada linha corresponde a um dos quatro possíveis isotopômeros: CF35Cl3, CF35Cl237Cl, CF35Cl37Cl2, CF37Cl3. A intensidade relativa dos sinais, similarmente ao que observamos na espectrometria de massas, pode ser explicada pela razao isotópica 35Cl x 37Cl, com abundância natural de aproximadamente 75/25. Entretanto, a maioria dos organofluorados possui blindagem maior do que o CFCl3, e por isto apresentam valores de deslocamentos químicos negativos. Os que estao mais desblindados do que o CFCl3 mostram deslocamentos químicos positivos, tais como os fluoretos de acila. A Figura 1 apresenta de forma resumida as faixas, em ppm, para os deslocamentos químicos dos organofluorados.
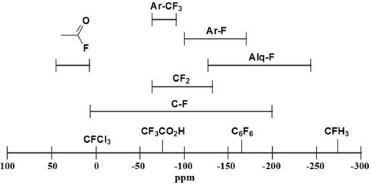 Figura 1. Resumo das faixas de deslocamentos químicos esperados para os organofluorados
As constantes de acoplamento homonuclear F-F (JF-F), em geral, sao relativamente maiores do que as observadas para H-H,11 por exemplo, em um acoplamento geminal, a duas ligaçoes (F-C-F), o JF-F está entre 100 e 200 Hz. Estes valores sofrem interferência dos átomos vizinhos, como, por exemplo, os cis-vicinais (F-C-C-F) apresentam constantes de acoplamento expressivamente menores que os trans-vicinais e estas constantes diminuem com o aumento do número de átomos de flúor ou de substituintes eletronegativos, podendo apresentar valores positivos e negativos. As constantes de acoplamento heteronucleares JF-X, por exemplo JF-C ou JF-H, apresentam o mesmo comportamento, como exemplificado na Tabela 1.11
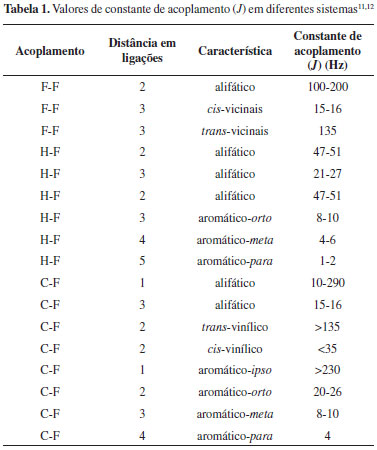
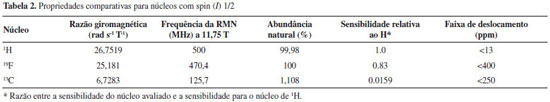
Os acoplamentos escalares, a exemplo JF-F ou JF-X, sao diretamente relacionados à estrutura do sistema estudado. De tal modo que tanto em moléculas flexíveis quanto em sistemas rígidos há a possibilidade de transmissao do acoplamento nao apenas via ligaçao química propriamente dita, mas também via proximidade espacial ou ligaçao de hidrogênio. Nota-se ainda que em estruturas flexíveis, a temperatura e o solvente, por vezes, têm relaçao direta com o valor da constante de acoplamento.16 RMN de 1H de organofluorados O número quântico de spin (I) nuclear de flúor é 1/2, permitindo o seu acoplamento com prótons e carbonos vizinhos, com tempos de relaxaçao suficientemente longos para serem observados e com valores de integraçao confiáveis. As análises das constantes de acoplamentos JH-F, JC-F e JF-F sao importantes evidências na elucidaçao das estruturas dos organofluorados. A Tabela 2 correlaciona as propriedades dos núcleos de H, C e F com spin (I) 1/2.
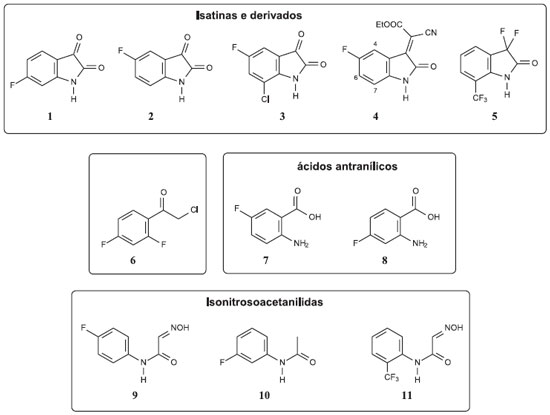
As constantes de acoplamentos de H-F em compostos alifáticos sao maiores que as observadas para H-H e diminuem com a presença de outro átomo de F ou substituinte eletronegativo ligados ao átomo de carbono (Tabela 1). No entanto, para sistemas aromáticos com mais de um átomo de flúor, os espectros sao de segunda ordem e as constantes de acoplamento sao aproximadamente as mesmas observadas para H-H, as quais podem sofrer influência de substituintes no anel aromático (Tabela 1). Além disso, os acoplamentos a longas distâncias merecem atençao especial, pois podem fornecer informaçoes sobre a estrutura, confirmando ou evidenciando o padrao de substituiçao em um anel aromático.12 Por outro lado, tal como na RMN de 1H, estes acoplamentos de longa distância podem ser observados com mais de seis ligaçoes, o que demanda uma análise minuciosa de todos os sinais no espectro.12 RMN de 13C de organofluorados Os espectros de RMN de 13C geralmente sao realizados com desacoplamento do núcleo de 1H. No entanto, nao é comum obter-se espectros de organofluorados de RMN de 13C desacoplados, tornando as suas análises bem mais complexas devido aos desdobramentos dos sinais relativos ao acoplamento spin-spin destes núcleos. As constantes de acoplamentos observadas para C-F sao altas, podendo atingir até 290 Hz. As constantes de acoplamentos em sistemas trans-vinílicos sao muito maiores que as de cis-vinílicos. Estas constantes sao menores na presença de substituintes eletronegativos (Tabela 1). Destaca-se ainda, que as constantes de acoplamento aumentam com o número de átomos de flúor. Em sistemas aromáticos, a constante de acoplamento diminui com o aumento do número de ligaçoes, podendo alcançar valores maiores do que 230 Hz, para sistemas orto e próximos a 4 Hz em sistemas para (Tabela 1). O acoplamento C-F pode levar a espectros bastante congestionados, principalmente os que contêm mais de um átomo de flúor, induzindo o usuário ao erro no assinalamento dos sinais. No entanto, a análise cuidadosa dos sinais, e suas respectivas constantes de acoplamento, podem fornecer informaçoes fundamentais sobre a estrutura destas substâncias. Diante do exposto, o objetivo deste trabalho é exemplificar a RMN de 1H e 13C de compostos organofluorados, relacionando o efeito do flúor no ambiente químico e na multiplicidade dos sinais, uma vez que essa nao é uma abordagem comum nas disciplinas de espectroscopia em cursos de graduaçao e pós-graduaçao em química. Um exemplo será correlacionado ao seu espectro de RMN de 19F. Neste trabalho, foram selecionadas substâncias que apresentam um ou mais átomos de flúor, em diferentes posiçoes, de forma a serem obtidos espectros variados e com distintos padroes de multiplicidade de sinais (Figura 2). Estes compostos podem ser divididos em quatro classes:
As isatinas sao heterociclos versáteis usados como matéria-prima para a obtençao de outros derivados, pois apresentam grupos com diferentes reatividades, podendo sofrer ataques nucleofílicos em suas carbonilas de cetona e de amida, além de poderem atuar como nucleófilos em reaçoes de acilaçao e alquilaçao e de sofrer substituiçao eletrofílica no anel aromático. Estes compostos apresentam inúmeras aplicaçoes, sendo materiais de partida para a síntese de fármacos, como o antineoplásico sunitinibe. As isatinas podem ser sintetizadas por diferentes metodologias, sendo o método de Sandmeyer o mais empregado.17,18 Os derivados 3,3-difluoroxindóis (ex. 5), obtidos pela fluoraçao de isatinas com dietilamino trifluoreto de enxofre (DAST) também sao intermediários sintéticos versáteis.19,20 A 2-cloro-2',4'-difluoroacetofenona (6) é um importante intermediário sintético de alguns antifúngicos, como o fluconazol e o voriconazol. Esta substância pode ser obtida a partir da acilaçao de Friedel-Crafts do 1,3-difluorbenzeno, com o uso de cloreto de cloroacetila e cloreto de alumínio como catalisador.21 O ácido antranílico, também conhecido como vitamina L, é uma substância de origem natural precursora do aminoácido triptofano. Este ácido está envolvido na produçao de leite materno. Em meio biológico é sintetizado a partir do ácido corísmico, porém, pode ser obtido sinteticamente a partir da oxidaçao do orto-xileno ou da isatina.17,22 Ele pode sofrer tanto substituiçao no anel aromático, quanto adiçao à carboxila. Por possuir um grupamento amino comporta-se também como nucleófilo. Devido a essa versatilidade, os derivados de ácido antranílico sao usados largamente em química medicinal e como intermediários em síntese orgânica.23 As isonitrosoacetanilidas sao as precursoras das isatinas por meio do método de Sandmeyer. Esta metodologia consiste em reagir anilinas, hidrato de cloral e hidroxilamina em meio aquoso para gerar a isonitrosoacetanilidas, que sofrem ciclizaçao, em ácido sulfúrico, gerando as respectivas isatinas.17,24
MATERIAIS E MÉTODOS As amostras 1-4 e 6-11 foram solubilizadas em DMSO-d6 e analisadas no espectrômetro Bruker Avance III 500 de 11,75 T (500,13 MHz para o 1H), equipado com sonda TBI (triple resonance broadband inverse) de 5 mm, com gradiente de campo na direçao z. Tetrametilsilano (TMS) foi usado como padrao interno. Os arquivos gerados foram lidos e analisados através do software TopSpin 3.1 (© 2011 Bruker BioSpin). Os sinais de interesse foram ampliados por meio de ferramenta do próprio programa, tiveram seus picos atribuídos e as integraçoes e constantes de acoplamento calculadas. A amostra 5 foi solubilizada em (CD3)CO e analisada no espectrômetro Bruker HC200 operando em 188 MHz para 19F e 50 MHz para 13C, onde foi usado como padroes internos o TMS para 13C e CFCl3 para 19F. Para a simulaçao da multiplicidade, para cada sistema de spins, utilizou-se o programa WINDNMR.25 Os valores das constantes de acoplamento e a multiplicidade, determinados diretamente nos espectros, foram inseridos no programa, sendo posteriormente necessário apenas o ajuste da ampliaçao e da intensidade dos sinais para comparaçao com os dados experimentais.
RESULTADOS E DISCUSSAO Na análise de sistemas acoplados, o tipo de processamento utilizado para obter os espectros de RMN tem um papel fundamental na determinaçao da multiplicidade e constantes de acoplamentos dos sinais. Nesse aspecto a multiplicaçao por funçoes exponenciais de apodizaçao como Lorentz-Gauss (LB e GB), muito frequentemente utilizadas em RMN, tem o objetivo de atribuir maiores resoluçoes ou razao sinal/ruído aos espectros. Essas funçoes atuam de maneiras distintas no FID (decaimento livre de induçao), atribuindo maior peso para a regiao inicial, quando se busca aumento da sensibilidade, ou maior peso para a regiao final quando se objetiva resoluçao. Dessa forma, durante o processamento, o uso de funçoes de apodizaçao é importante, pois valores negativos atribuidos à funçao Lorentziana melhoram a resoluçao do sinal. Por outro lado, valores positivos ampliam a relaçao sinal/ruído. A multiplicaçao por uma gaussiana tem relaçao direta com a posiçao na qual a funçao de apodizaçao multiplicará o FID. Ao utilizar-se a funçao de apodizaçao gaussiana, por exemplo, confere-se maior peso à porçao central e final do FID e, com isso, obtém-se melhor resoluçao espectral.26 Esse efeito é melhor visualizado na Figura 3, na qual sao apresentadas as representaçoes gráficas de dois espectros provenientes da mesma matriz de dados, contudo processados de formas diferentes. Para o espectro (b) foi aplicada apenas a transformada de Fourier (TF), enquanto que para o (a) utilizou-se a funçao de apodizaçao gaussiana, antes da TF, sendo possível observar a nítida melhoria na resoluçao dos sinais, permitindo assim a melhor atribuiçao da multiplicidade, bem como a determinaçao mais precisa das constantes de acoplamento.
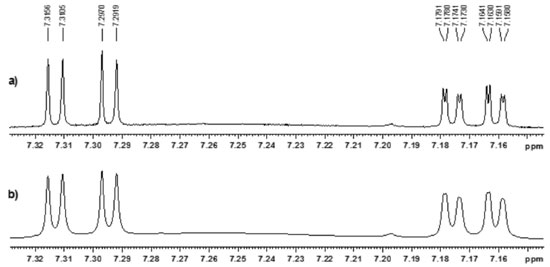 Figura 3. Comparaçao de sinais de RMN de 1H processados com (a) e sem (b) a aplicaçao da funçao de apodizaçao Lorentz-Gauss (lb = - 0,3; gb = 0,3)
Após a determinaçao das multiplicidades e constantes de acoplamentos de 1H para todos os compostos, foram realizadas simulaçoes, utilizando os valores encontrados, no pacote computacional WINDNMR,25 com o intuito de corroborar as atribuiçoes feitas manualmente. Como exemplificado na Figura 4, foram obtidos pela simulaçao espectros com multiplicidades similares às encontradas nos espectros de RMN de 1H das substâncias deste estudo, salvo para o composto 9, que apresentou um sistema de acoplamento de segunda ordem AA'BB'X, que nao pode ser completamente resolvido manualmente. Nesse caso, a correta determinaçao das constantes de acoplamento necessita de cálculos computacionais com alto grau de complexidade, em que o protocolo se inverte, ou seja, as constantes só podem ser claramente definidas computacionalmente.
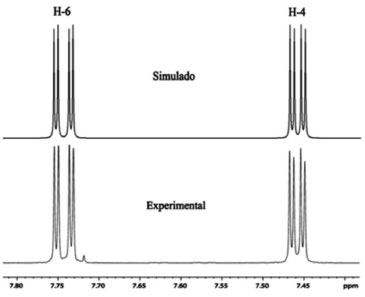 Figura 4. Comparaçao entre sinais de RMN de 1H, simulado e experimental, para a substância 3
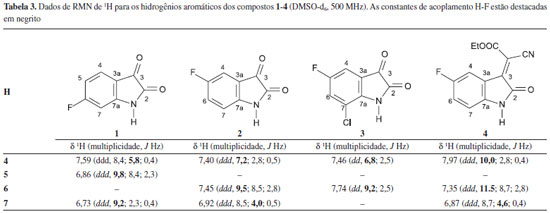
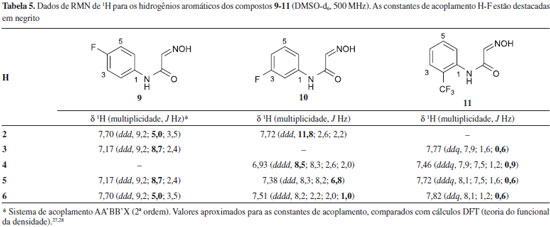
Análise dos espectros de RMN de 1H Isatinas (1-3) e derivado (4) Nos espectros de RMN dos compostos 1-3, o flúor, tanto na posiçao 5 quanto na 6, acopla com os hidrogênios nas posiçoes 1,2 (orto) e 1,3 (meta), resultando em sinais com multiplicidades bem complexas. No caso do composto 1 (Figura 2S), H-4 acopla com H-5 (J = 8,4 Hz), com o flúor (J = 5,8 Hz) e com H-7 (J = 0,4 Hz), formando um duplo duplo dupleto (ddd) em 7,59 ppm. H-5 acopla com o flúor (J = 9,8 Hz), com H-4 (J = 8,4 Hz) e com H-7 (J = 2,3 Hz) gerando um duplo duplo dupleto (ddd) em 6,86 ppm. H-7 forma um duplo duplo dupleto em 6,73 ppm ao acoplar com o flúor (J = 9,2 Hz), com H-5 (J = 2,3 Hz) e com H-4 (J = 0,4 Hz). Como previsto, o acoplamento orto H-F apresentou uma maior constante de acoplamento que o orto H-H (Tabela 1). H-4 do composto 2 aparece como um duplo duplo dupleto em 7,40 ppm, devido ao seu acoplamento com o flúor (J = 7,2 Hz), com H-6 (J = 2,8 Hz) e com H-7 (J = 0,5 Hz). O deslocamento de H-4 da substância 2 em relaçao a H-4 do composto 1, para menor frequência, deve-se ao efeito de estabilizaçao, pelo flúor, dos elétrons n do nitrogênio. Este efeito é mais importante no composto 2 porque o flúor está em posiçao para em relaçao ao nitrogênio. Esta estabilizaçao propicia uma maior densidade eletrônica no anel, blindando H-4 e tornando, consequentemente, seu sinal menos deslocado. Ainda no composto 2, H-6 se apresenta como um duplo duplo dupleto devido ao acoplamento com o flúor (J = 9,5 Hz), com H-7 (J = 8,5 Hz) e H-4 (J = 2,8 Hz). H-7 acopla com H-6 (J = 8,5 Hz), com o flúor (J = 4,0 Hz) e com H-4 (J = 0,5 Hz) gerando outro duplo duplo dupleto (Tabela 3) (Figura 5).
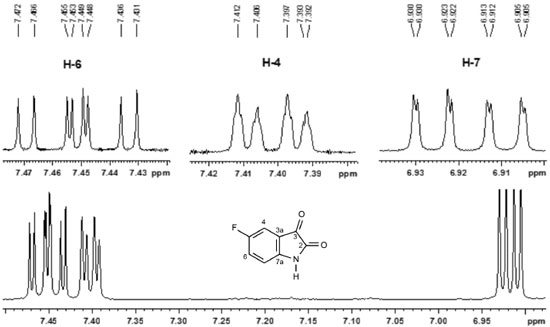 Figura 5. Espectro de RMN de 1H para os hidrogênios aromáticos da substância 2. Nos sinais ampliados aplicou-se a funçao de apodizaçao Lorentz-Gauss (lb = - 0,4; gb = 0,4)
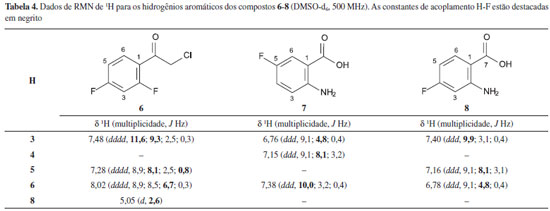
O espectro do composto 3 (Figura 3S), é bem simples, nele sao observados os dois duplos dupletos relativos a H-4 e H-6 em 7,46 e 7,74 ppm, respectivamente, os quais acoplam entre si e com o flúor (Tabela 3). Já no caso do composto 4 (Figura 4S) seria de se esperar que os sinais relativos aos hidrogênios aromáticos fossem similares aos do composto 2. No entanto, observa-se que o H-4 se apresenta significativamente mais deslocado em 4 (7,97 ppm) do que no composto 2 (7,40 ppm). Isso se deve ao efeito de anisotropia diamagnética do oxigênio da carbonila do grupamento cianoacetato de etila sobre H-4. O padrao de multiplicidade aqui observado é similar àquele descrito para o composto 2 (Tabela 3). 2-cloro-2',4'-difluoroacetofenona (6) O composto 6 apresentou um espectro bastante complexo no que se refere à multiplicidade dos sinais, devido ao fato de apresentar dois átomos de flúor no anel aromático. O H-3 acopla com F-2/F-4 (J =11,6 e 9,3 Hz), com H-5 (J = 2,5 Hz) e com H-6 (J = 0,3 Hz) formando um duplo duplo duplo dupleto em 7,48 ppm. Para H-5, é possível observar o acoplamento de longa distância para com F-2 (J = 0,8 Hz), sem a necessidade do uso de funçoes de apodizaçao. Observa-se ainda, os acoplamentos com F-4 (J = 8,1 Hz), H-6 (J = 8,9 Hz) e H-3 (J = 2,5 Hz) gerando outro sinal duplo duplo duplo dupleto, situado em 7,28 ppm. Finalmente, H-6 apresenta-se como um duplo duplo duplo dupleto em 8,02 ppm ao acoplar com H-5 (J = 8,9 Hz), com F-2/F-4 (J = 8,5 e 6,7 Hz) e H-3 (J = 0,3 Hz) (Tabela 4) (Figura 6). Observa-se ainda um dupleto em 5,05 ppm (J = 2,6 Hz), que se refere a H-8, situado na cadeia lateral, acoplando com o F-2 via espaço, conforme observado em casos correlatos na literatura.16
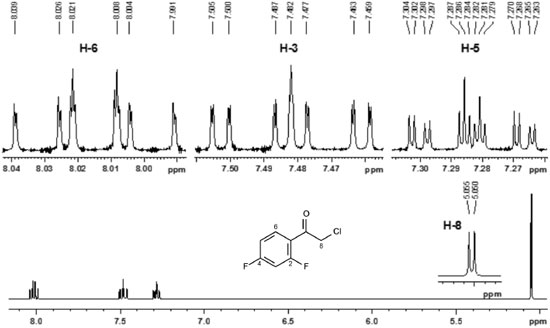 Figura 6. Espectro de RMN de 1H para os hidrogênios aromáticos e H-8 da substância 6. Nos sinais ampliados aplicou-se a funçao de apodizaçao Lorentz-Gauss (lb = - 0,3; gb = 0,3)
Derivados do ácido antranílico (7 e 8) Devido ao fato dos derivados 7 e 8 conterem um grupamento amino, que aumenta a densidade eletrônica do anel, os sinais dos hidrogênios aromáticos se apresentam menos deslocados, ou seja, mais blindados, do que os do composto 6. No composto 7 (Figura 5S), para H-3 observa-se um duplo duplo dupleto em 6,76 ppm devido ao acoplamento com o H-4 (J = 9,1 Hz), com o flúor (J = 4,8 Hz) e com H-6 (J = 0,4 Hz). H-4 acopla com H-3 (J = 9,1 Hz), flúor (J = 8,1 Hz) e H-6 (J = 3,2 Hz), formando um duplo duplo dupleto em 7,15 ppm. Já H-6 se apresenta como um duplo duplo dupleto em 7,38 ppm ao acoplar com flúor (J = 10,0 Hz), H-4 (J = 3,2 Hz) e com H-3 (J = 0,4 Hz) (Tabela 4). No caso do composto 8 (Figura 6S), observa-se um duplo duplo dupleto em 7,40 ppm relativo a H-3 acoplando com o flúor (J = 9,9 Hz), H-5 (J = 3,1 Hz) e H-6 (J = 0,4 Hz). H-5 é observado como um duplo duplo dupleto em 7,16 ppm devido ao acoplamento com H-6 (J = 9,1 Hz), flúor (J = 8,1 Hz) e H-3 (J = 3,1 Hz). Finalmente, H-6 acopla com H-5 (J = 9,1 Hz), flúor (J = 4,8 Hz) e com H-3 (J = 0,4 Hz) formando um duplo duplo dupleto em 6,78 ppm (Tabela 4). Isonitrosoacetanilidas (9-11) O espectro do composto 9 caracteriza-se pela presença de dois duplos duplos dupletos com integraçao de dois hidrogênios cada e um simpleto em 7,63 ppm relativo a H-9. Foram ainda observados dois simpletos em 10,23 e 12,17 ppm, referentes aos hidrogênios dos grupos NH e OH, respectivamente. A princípio, seria esperado que H-2 e H-6 fossem equivalentes, assim como e H-3 e H-5, já que o anel apresenta um plano de simetria. Desta forma, deveriam ser esperados duplos dupletos com integraçao de 2H para ambos os sinais. No entanto, os hidrogênios se apresentaram como ddd, possivelmente devido a diferença de ambiente magnético gerada pela conformaçao da estrutura, gerando um desdobramento do sinal (Tabela 5) (Figura 7). Nesse caso, o sistema de spins observado é de 2ª ordem do tipo AA'BB'X. Assim, os valores das constantes de acoplamento sao aproximados e foram comparados com cálculos DFT (teoria do funcional da densidade).27,28
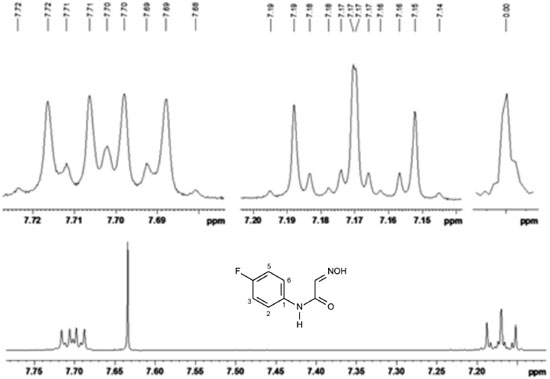 Figura 7. Espectro de RMN de 1H para os hidrogênios aromáticos da substância 9. Aplicaçao da funçao de apodizaçao Lorentz-Gauss (lb = - 0,15). Largura da linha do TMS ½ altura é 0,34 Hz
Para o composto 10 (Figura 7S) é observado um duplo duplo dupleto em 7,72 ppm relativo a H-2, cujos acoplamentos ocorrem com o flúor (J = 11,8 Hz), com H-4 (J = 2,6 Hz) e H-6 (J = 2,2 Hz). Neste sinal, ocorreu a sobreposiçao com o simpleto relativo a H-9. Para H-4 observa-se um duplo duplo duplo dupleto em 6,93 ppm, relativo ao acoplamento com o flúor (J = 8,5 Hz), H-2 (J = 2,6 Hz), H-5 (J = 8,3 Hz) e H-6 (J = 2,0 Hz). H-5 apresentou-se como um duplo duplo dupleto em 7,38 ppm devido aos acoplamentos com H-4 (J = 8,3 Hz), H-6 (J = 8,2 Hz) e com o flúor (J = 6,8 Hz). H-6 foi observado como um duplo duplo duplo dupleto devido ao acoplamento com H-5 (J = 8,2 Hz), H-2 (J = 2,2 Hz), H-4 (J = 2,0 Hz) e o acoplamento para com o flúor (J = 1,0 Hz) (Tabela 5). Finalmente, pode se observar o simpleto relativo à H-9 em 7,70 ppm, dentro do sinal de H-2. No espectro do composto 11 é possível observar um grande aumento na complexidade da multiplicidade observada para todos os hidrogênios aromáticos, devido aos acoplamentos com os átomos de flúor do grupamento CF3, que sao realizados a longa distância e, consequentemente, com pequenas constantes de acoplamento, dificultando muito a resoluçao do sinal. Nesse caso, as multiplicidades só podem ser claramente elucidadas com o uso das funçoes de apodizaçao e simulaçao computacional. Os sinais de H-3 e H-6 foram observados como dois duplos duplos quartetos, respectivamente em 7,77 e 7,82 ppm. Por outro lado, H-4 e H-5 foram observados como duplos duplos duplos quartetos em 7,46 e 7,72 ppm, respectivamente (Tabela 5) (Figura 8).
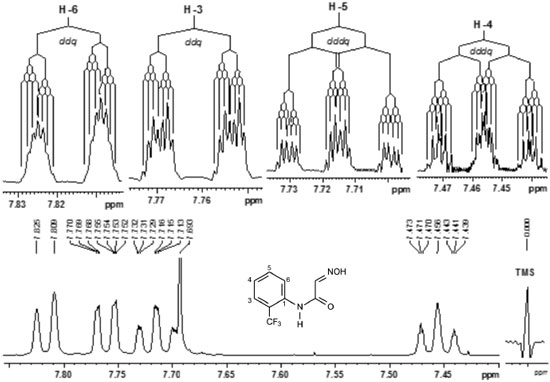 Figura 8. Espectro de RMN de 1H para os hidrogênios aromáticos da substância 11. Nos sinais ampliados aplicou-se a funçao de apodizaçao Lorentz-Gauss (lb = - 0,8; gb = 0,8), incluindo o sinal do TMS. Para sinal em 7,46 ppm utilizou-se lb = -0.5 e gb = 0,0
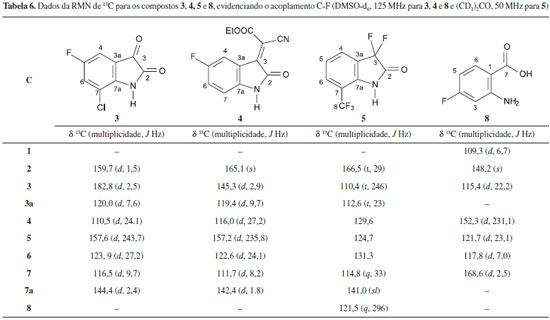
Análise dos espectros de RMN de 13C Para discussao dos acoplamentos C-F, foram realizados espectros de RMN de 13C, desacoplando C-H, das substâncias 3, 4, 8 e 5. Por meio desses espectros, acoplamentos C-F a seis ligaçoes foram observados. No caso do composto 3, verificou-se que todos os carbonos da molécula, inclusive os carbonílicos, acoplaram com o flúor, formando dupletos. Como esperado, pôde-se constatar que as constantes de acoplamento diminuem com o aumento da distância entre o carbono e o flúor. Desta forma, o acoplamento de curta distância entre o flúor e C-5, carbono ipso, apresentou um valor extremamente alto de constante de acoplamento, J = 243,7 Hz. Os acoplamentos entre o flúor e os carbonos orto, C-4 e C-6, apresentaram J = 24,1 e 27,2 Hz, respectivamente, enquanto que os acoplamentos meta, com C-3a e C-7 foram realizados com J = 7,6 e 9,7 Hz. Já os acoplamentos com C-2, C-3 e C-7a apresentaram valores de constante de acoplamento próximos a 2,0 Hz, devido a maior distância (Tabela 6).
O composto 4 apresentou um espectro semelhante ao de 3 no que se refere aos carbonos aromáticos. No entanto, o carbono carbonílico C-3 nao acopla com o flúor e o sinal desse carbono é observado como um simpleto (Tabela 6). O espectro de RMN 13C de 5 é bem mais complexo, devido à presença de dois grupamentos fluorados: um CF3 ligado ao anel aromático e um difluorometileno benzílico (CF2). Os átomos de flúor do CF3 acoplam com C-8 e formam um quarteto em 121,5 ppm com considerável constante de acoplamento (J = 296 Hz). Além disso, acoplam também com o C-7 gerando um quarteto (J = 33 Hz) em 114,8 ppm relativo a C-7. Já os átomos de flúor do CF2 acoplam com C-2, C-3 e C-3a formando tripletos em 166,5 ppm (J = 29 Hz), 110,4 ppm (J = 246 Hz) e 112,6 ppm (J = 23 Hz) respectivamente (Tabela 6). Para a substância 8 apenas o carbono que sustenta o grupo NH2 (C-2) nao apresentou acoplamento com o flúor, embora estivesse a três ligaçoes (Tabela 6). Por outro lado, foi observado, em 168,6 ppm, um dupleto relativo a C-7 (J = 2,5 Hz), referente ao acoplamento da carbonila com o flúor a cinco ligaçoes (Figura 9).
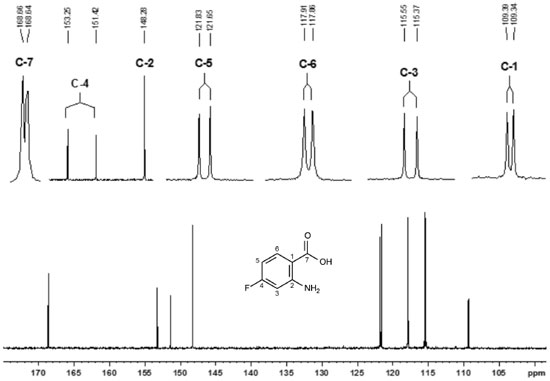 Figura 9. Espectro de RMN de 13C da substância 8. Os sinais ampliados demonstram claramente o acoplamento C-F
Análise do espectro de RMN de 19F da substância 5 A molécula 5 foi escolhida para a discussao dos espectros de RMN de 19F pelo fato de ter cinco átomos de flúor. Como mencionado, nos espectros de RMN de 19F este núcleo está mais blindado e, por isto, apresenta sinais em valores negativos. Enquanto nos espectros de RMN de 1H e 13C pode-se observar o acoplamento do flúor com estes núcleos, no espectro de RMN 19F, é usual a realizaçao do espectro desacoplado de outros núcleos, desta forma, observa-se apenas os acoplamentos F-F (Figura 8S). No caso da substância 5 estes átomos do grupo CF3 nao acoplam com os do CF2 devido à longa distância entre este si e apresentam sinais em regioes distintas e características do espectro. O grupo CF3 mostrou um simpleto em -61,28 ppm, enquanto o CF2 um simpleto em -112,49 ppm.
CONCLUSAO Neste artigo, os espectros de RMN de 1H e de 13C de onze substâncias mostraram padroes clássicos de acoplamento de primeira ordem e os efeitos do núcleo do flúor em diferentes ambientes químicos e magnéticos. Adicionalmente, o espectro de RMN de 19F mostrou os sinais para átomos de flúor também em diferentes ambientes químicos. Espera-se que esse trabalho possibilite o melhor entendimento dos espectros de RMN de moléculas organofluoradas, por meio dos exemplos apresentados, visto que a sua análise é muitas vezes complexa, devido aos desdobramentos dos sinais, relativos ao acoplamento spin-spin com o núcleo de 1H e 13C. Os exemplos podem ser apresentados e discutidos em disciplinas de espectroscopia de RMN, tanto em cursos de graduaçao como de pós-graduaçao e, assim, solidificar a importância destes efeitos na caracterizaçao das estruturas. Destaca-se, ainda, a importância do uso das funçoes de apodizaçao no processamento dos espectros para observaçao de constantes de acoplamento à longa distância.
MATERIAL SUPLEMENTAR O material suplementar contém os espectros de RMN de 1H dos compostos 1, 3, 4, 6, 7 e 9, bem como os espectros de RMN de 13C e 19F do composto 5. Esse material está disponível gratuitamente em http://quimica-nova.sbq.org.br, na forma de arquivo PDF.
AGRADECIMENTOS Os autores agradecem ao CNPq pelas bolsas concedidas, ao MCT/FINPEP, à FAPERJ, à CAPES, à Universidade Federal do Rio de Janeiro - UFRJ, à Universidade Federal de Goiás, à FAPEG e à Fundaçao Oswaldo Cruz pelo suporte dispensado.
REFERENCIAS 1. Greenwood, N. N.; Earnshaw, A.; Chemistry of the elements, 2nd ed., Butterworth Heinemann: Oxford, 1998. 2. Moissan, H.; C. R. Hebd. Seances Acad. Sci. 1896, 128, 1543. 3. Kirsch, P.; Modern Fluoroorganic Chemistry, Wiley-VCH: Weinheim, 2004. 4. Dinoiu, V.; Rev. Roum. Chim. 2006, 51, 1141. 5. Banks R.E.; Organofluorine Chemistry and their Industrial Applications, John Wiley & Sons: Chichester, 1979. 6. Ojima I.; Fluorine in Medicinal Chemistry and Chemical Biology, Wiley-Blackwell: Chichester, 2009. 7. DuPont, DuPont HFC-134a Properties, Uses, Storage, and Handling. Disponível em: http://www2.dupont.com/Refrigerants/en_US/assets/downloads/h45945_hfc134a_push.pdf (acessado em 10/01/2014) 8. O'Hagan, D.; J. Fluorine Chem. 2010, 131, 1071. DOI: http://dx.doi.org/10.1016/j.jfluchem.2010.03.003 9. Kirk, K. L.; J. Fluorine Chem. 2006, 127, 1013. DOI: http://dx.doi.org/10.1016/j.jfluchem.2006.06.007 10. O'Hagan, D.; Harper, D. B.; J. Fluorine Chem. 1999, 100, 127. DOI: http://dx.doi.org/10.1016/S0022-1139(99)00201-8 11. Dolbier, W. R.; Guide to Fluorine NMR for Organic Chemists, Wiley: Hoboken, 2009. 12. Everett, T. S.; J. Chem. Educ. 1988, 65, 422. DOI: http://dx.doi.org/10.1021/ed065p422 13. Gerig, J. T.; Fluorine NMR. Online textbook, 2001, disponível em: http://www.biophysics.org/Portals/1/PDFs/Education/gerig.pdf. Acessado em 01/04/2015. 14. Marsh, E. N. G.; Suzuki Y.; ACS Chem. Biol. 2014, 9, 1242. DOI: http://dx.doi.org/10.1021/cb500111u PMID: 24762032 15. Chen, H.; Viel, S.; Ziarelli, F.; Peng, L.; Chem. Soc. Rev. 2013, 42, 7971. DOI: http://dx.doi.org/10.1039/c3cs60129c PMID: 23864138 16. Hierso, J. C.; Chem. Rev. 2014, 114, 4838. DOI: http://dx.doi.org/10.1021/cr400330g PMID: 24533483 17. Silva, J. F. M.; Garden, S. J.; Pinto, A. C.; J. Braz. Chem. Soc. 2001, 12, 273. DOI: http://dx.doi.org/10.1590/S0103-50532001000300002 18. Silva, B. V.; J. Braz. Chem. Soc. 2013, 24, 707. DOI: http://dx.doi.org/10.1590/S0103-50532013000100018 19. Boechat, N.; Kover, W. B.; Bastos, M. M.; Pinto, A. C.; Maciel, L. C.; Mayer, L. M. U.; Da Silva, F. S. Q. Sá, P. M.; Mendonça, J. S.; Wardell, S. M. S. V. Arruda, M. S. L.; J. Braz. Chem. Soc. 2008, 19, 445. DOI: http://dx.doi.org/10.1590/S0103-50532008000300011 20. Ferreira S. B.; Revista Virtual de Química 2009, 1, 160 DOI: http://dx.doi.org/10.5935/1984-6835.20090018 21. França, R. R. F.; Carvalho, A. S.; Branco, F. S. C; Pinto, A. C.; Boechat, N.; Revista Virtual de Química 2014, 6, 1483. 22. Maki, T.; Takeda, K.; Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH: Weinheim, 2002. 23. Wiklund, P.; Bergman, J.; Curr. Org. Chem. 2006, 3, 379. 24. Da Silva, B. N. M.; Bastos, R. S.; Silva, B. V.; Pinto, A. C.; Quim. Nova 2010, 33, 2279. DOI: http://dx.doi.org/10.1590/S0100-40422010001000043 25. Reich, H. J.; J. Chem. Educ. 1995, 72, 1086. DOI: http://dx.doi.org/10.1021/ed072p1086.2 26. Hoch, J. C.; Stern, A.; NMR Data Processing, Wiley-Liss: New York, 1996. 27. Hohenberg, P.; Kohn, W.; Phys. Rev. B: Condens. Matter Mater. Phys. 1964, 136, 864. DOI: http://dx.doi.org/10.1103/PhysRev.136.B864 28. Kohn, W.; Sham, L.; Phys. Rev. A: At., Mol., Opt. Phys. 1965, 140, 1133. DOI: http://dx.doi.org/10.1103/PhysRev.140.A1133 |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access