Assuntos Gerais
|
|
| Gilbert lewis e o centenário da teoria de ligação por par de elétrons# Gilbert lewis and the centennial of the electron pair theory of chemical bonding |
|
Carlos A. L. Filgueiras
Departamento de Química, Universidade Federal de Minas Gerais, 31270-901 Belo Horizonte - MG, Brasil Recebido em 21/06/2016 *e-mail: calfilgueiras@gmail.com The year 2016 marks the centennial of the first approach to describe all types of chemical bonds by means of a unified theory, that of the electron pair, as proposed by the American chemist Gilbert Newton Lewis (1875-1946). Lewis probably became the best known chemist of the twentieth century. Any highschool student anywhere has heard of him and uses concepts such as Lewis acids and bases. His seminal ideas, albeit modified with time, remain a source of inspiration as the basis of much that came later. Lewis established his theory in a series of articles, the most important dating from 1916. His life and achievements are the stuff of much study and debate, as this essay aims to show. INTRODUÇAO Alguns poucos químicos estabeleceram, ao longo da história, conceitos e teorias que vieram a ter uma influência profunda na ciência, desafiando o tempo, mesmo que vários aspectos de suas teorias se tenham modificado com o passar dos anos. Assim, Lavoisier, no último quartel do século XVIII, sepultou a antiga teoria dos quatro elementos, que vinha desde a Grécia antiga, ao demonstrar que a água, longe de ser elementar, é um composto que pode ser facilmente resolvido em seus constituintes, estes sim elementares, o oxigênio e o hidrogênio. Tampouco o ar é elementar, como também o demonstrou Lavoisier, sendo constituído por uma mistura de gases. Estes sao aspectos basilares da nova química estabelecida pelo químico francês, e marcam o que se considera o início da química moderna.1-3 Na década seguinte à morte trágica de Lavoisier, John Dalton propôs sua teoria atômica, pondo pela primeira vez em bases operacionais o conceito de átomo, que ocupara as mentes de tantos filósofos por mais de dois milênios. A partir de Dalton, foi possível trabalhar quantitativamente os átomos, determinando suas massas e estabelecendo relaçoes estequiométricas em bases sólidas, tirando a química de seu estado eminentemente descritivo. Isto foi possível mesmo sem que se tivesse uma demonstraçao experimental direta da existência dos átomos, o que só se logrou no início do século XX. O próprio Dalton foi um dos pioneiros desta nova atitude, determinando pesos atômicos e estabelecendo a lei das proporçoes múltiplas.4 Pouco mais de um século depois, Gilbert Newton Lewis estabeleceu a primeira teoria de ligaçao química abrangente, que agrupava num único conceito todos os tipos de ligaçao química, permitindo mostrar relaçoes entre substâncias iônicas, covalentes, moleculares e mesmo metálicas, até entao sem qualquer nexo conceitual comum. Ora, o objeto de estudo da química é exatamente a natureza da ligaçao entre os átomos dos elementos. Estes tendem a interagir, formando compostos os mais variados, num processo de formaçao e ruptura de ligaçoes, que é a preocupaçao central desta ciência. Por isso se pode apreciar a importância da contribuiçao de Lewis, e é por isso que ele pode ser posto ao lado dos dois antecessores mencionados anteriormente. De acordo com Sason Shaik, enquanto Lavoisier e Dalton empreenderam uma "revoluçao composicional" na química, Lewis encabeçou uma "revoluçao estrutural".5 Muito se discute que nao existiria uma filosofia química, ao contrário do que sucede na física ou na biologia, que debatem temas como a gênese do universo ou a natureza da vida. Ora, assim como Lavoisier e Dalton, Lewis foi um verdadeiro filósofo químico, e é isto que se quer ressaltar aqui, pois foi o primeiro a introduzir na química uma nova forma ampla de pensar sobre como e por que os átomos se ligam para formar compostos, isto é, o problema fundamental da química, como se salientou acima. Mesmo que o entendimento sobre a natureza da ligaçao química tenha evoluído extraordinariamente em um século, os químicos sao devedores a Lewis de ideias originais e fecundas, que moldaram profundamente boa parte da química que se seguiu.
VIDA Gilbert Newton Lewis nasceu em 1875 em Weymouth, Massachusetts, filho do advogado Francis Wesley Lewis e de Mary Burr Lewis, e morreu em 1946 em seu laboratório de Berkeley. A família se mudou para a cidade de Lincoln, no estado de Nebraska quando ele tinha nove anos. Ele havia aprendido a ler sozinho aos três anos de idade. Na adolescência entrou para a Universidade de Nebraska, mas depois transferiu-se para Harvard, onde se graduaria em 1896. Há divergências em seus biógrafos quanto à data de sua ida para Harvard, apontada como tendo ocorrido em 18927 ou 18936. Apesar de ter também muito interesse em economia, graduou-se em Química em 1896.6-8 Em 1898 completou seu mestrado em Harvard, com a dissertaçao intitulada "O elétron e a molécula".9 Note-se que a descoberta do elétron por J.J.Thomson havia ocorrido apenas no ano anterior. Lamentavelmente, como conta seu último ex-aluno Michael Kasha, a dissertaçao de Lewis desapareceu e Kasha diz que, apesar de ter visto o exemplar de Lewis em seu gabinete, após sua morte nao conseguiu localizar nenhum exemplar da dissertaçao, por mais que buscasse, mesmo nas bibliotecas de Harvard.9 Seria muito interessante conhecer o teor desse texto, uma vez que o assunto diz respeito àquilo por que Lewis viria se tornar mais conhecido. Em 1899 ele receberia o PhD por Harvard, trabalhando sob a orientaçao de Theodore William Richards, que seria o primeiro químico americano a receber o Prêmio Nobel, em 1914, pelo desenvolvimento de métodos para a determinaçao exata de pesos atômicos.10 Sua tese de PhD se intitulou "Algumas relaçoes eletroquímicas e termoquímicas de amálgamas de zinco e cádmio", e gerou seu primeiro artigo, em coautoria com o orientador.11 Como dizem os autores no artigo, seu propósito foi sobretudo descrever um método conveniente para medir a força eletromotriz diretamente de uma célula eletroquímica, mostrando que amálgamas de cádmio e de zinco em baixas concentraçoes obedecem as leis para soluçoes diluídas, e permitem também estudar suas propriedades termodinâmicas. Depois de mais um ano como instrutor em Harvard, Lewis recebeu uma bolsa de estudos para estagiar por um semestre com Wilhelm Ostwald em Leipzig e outro semestre com Walther Nernst em Göttingen. As personalidades desses dois químicos alemaes nao poderiam ser mais diferentes. Enquanto a estada em Leipzig fez Lewis se sentir bem e bastante estimulado, em virtude da atitude encorajadora de Ostwald, o estágio em Göttingen fê-lo sentir-se miserável, em consequência da rudeza e agressividade de Nernst.8 Ao retornar aos Estados Unidos passou mais três anos como instrutor em Harvard e foi nesse período, a partir de 1902, que ele começou a desenvolver suas ideias a respeito do octeto eletrônico e seu papel na formaçao de ligaçoes químicas, escrevendo um memorando que permaneceu inédito por muito tempo. Anos depois, em seu livro Valence and the Structure of Atoms and Molecules12, de 1923, ele próprio revelaria:
A Figura 1 a seguir reproduz o desenho mencionado por Lewis.
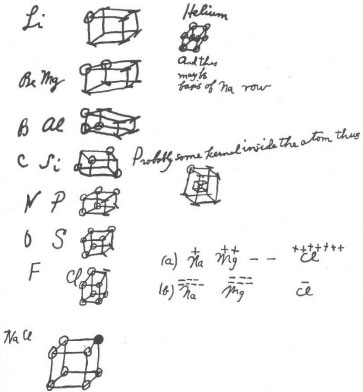 Figura 1. Desenhos de Lewis do memorando de 1902, reproduzidosem seu livro "Valence", de 1923
Em 1904 Lewis foi nomeado para os cargos de superintendente de pesos e medidas das Filipinas e químico do Birô de Ciência em Manila. As Filipinas eram entao um protetorado americano, tomado à Espanha depois da derrota desta na Guerra Hispano-Americana de 1898. Lewis levou consigo para as Filipinas um único livro, a Physikalische Chemie de Nernst, usando-o para corrigir seus "erros".9 A inimizade entre Lewis e Nernst pode ter contribuído para que Lewis jamais tivesse ganhado o Prêmio Nobel.8 Das Filipinas ele trouxe o hábito de fumar charutos o tempo todo. Em 1905 Lewis retornou aos Estados Unidos e foi para o Massachusetts Institute of Technology, onde trabalhou estreitamente com Arthur Amos Noyes. Sua produçao na área de termodinâmica foi extraordinária, de sorte que em 1912 ele já era professor titular e diretor de pesquisa no MIT. Nesse mesmo ano Lewis se casou com Mary Hinckley Sheldon, filha de um professor de línguas romances em Harvard, com quem teve dois filhos e uma filha.6 Sua reputaçao fez com que ele fosse convidado ainda em 1912 a assumir a direçao do Instituto de Química da Universidade da Califórnia em Berkeley. Lá ele reorganizou toda a química e tornou Berkeley uma das instituiçoes líderes nessa ciência. Em Berkeley ele permaneceu até o fim de sua vida, desenvolvendo uma carreira de enorme brilho em várias áreas científicas. A liderança de Lewis era tao positiva que, como disse seu colega Joel Hildebrand, "o departamento se tornou muito maior que a soma de seus membros individuais".7 O chefe continuamente estimulava a iniciativa e a criatividade de professores e estudantes, fazendo com que o ambiente acadêmico fosse o mais frutífero e agradável possível. Ao recrutar jovens colaboradores, eles eram designados instrutores e professores de química, e nao de uma de suas subdivisoes, como relata Hildebrand.7 Seu famoso livro de 1923, Valência e a estrutura de átomos e moléculas12, surgiu dos seminários de discussao desses temas com colegas e alunos. Por isso, sua generosa introduçao ao livro diz: "a meus colegas e estudantes da Universidade da Califórnia, sem cuja ajuda este livro nao teria sido escrito. Em nossos muitos anos de discussao dos problemas de estrutura atômica e molecular, algumas das ideias aqui apresentadas surgiram do grupo, ao invés de um indivíduo; de modo que, num certo sentido eu sou apenas o editor desse grupo".13 Durante a Primeira Guerra Mundial Lewis deixou provisoriamente seu posto para trabalhar no esforço de guerra como cientista na Europa, a partir de dezembro de 1917, em virtude do perigo representado pela guerra química que entao se praticava. Ele organizou a Escola de Defesa contra Gases da Força Expedicionária Americana, que treinava 200 oficiais por semana para o exército americano, o que causou um enorme decréscimo nas baixas de ataques por gases. Ele foi condecorado pelos Estados Unidos com a Distinguished Service Medal e pela França, que lhe outorgou a Legiao de Honra7, e deixou o serviço militar com o posto de tenente-coronel. Após a guerra Lewis iniciou um longo e frutífero trabalho em termodinâmica com seu ex-aluno Merle Randall, um de cujos resultados foi a publicaçao pelos dois do famoso livro Termodinâmica e a energia livre de substâncias químicas, em 1923, com ediçoes posteriores.14 Em sua vida profissional ele orientou mais de uma centena de doutorados e vários de seus alunos ganharam o Prêmio Nobel, como Glenn Seaborg e Melvin Calvin. Ele próprio foi indicado 35 vezes para o prêmio, sem jamais recebê-lo.8 Possivelmente nenhum orientador de teses teve tantos orientados seus a receber o galardao da Academia Sueca. Como exemplo, Harold Urey obteve em 1922 seu doutorado em Berkeley, onde havia estudado termodinâmica com Lewis, e em 1931, já como professor de química em Columbia, anuncia a descoberta do deutério, que lhe valeria o Prêmio Nobel em 1934. Durante esses três anos Lewis e colaboradores publicaram 26 artigos sobre o deutério e inúmeros aspectos da água pesada.8 Todavia, Lewis nem sequer foi lembrado como co-recipiente do prêmio com Urey. Talvez essa omissao tenha contribuído para que Lewis renunciasse a sua condiçao de membro da National Academy of Sciences dos Estados Unidos em 1934.15 Lewis recebeu inúmeras outras honrarias ao longo da vida, entre as quais serao mencionadas apenas algumas, como os títulos de doutor honoris causa das universidades de Chicago, Liverpool, Madrid, Pennsylvania e Wisconsin. Também foi eleito como membro honorário de várias entidades, como a Royal Institution of Great Britain, a Royal Society, a Chemical Society of London, a Academia das Ciências da India, a Academia Sueca, a Academia da Dinamarca e o Franklin Institute of Pennsylvania. Recebeu igualmente as medalhas Nichols, Gibbs, Davy, Arrhenius, Richards e da Society of Arts and Sciences.7 O caráter introvertido e pouco gregário de Lewis pode ter contribuído para que ele nunca tivesse recebido o Prêmio Nobel. Ele era arredio e pouco dado a viajar, apesar de sua prolífica produçao, seja de artigos ou discípulos. Sua inimizade com Irving Langmuir (1881-1957, Prêmio Nobel em 1932), o extrovertido químico de quem Lewis suspeitava querer apropriar-se de suas ideias a respeito da natureza da ligaçao química, contribuiu para o que muitos dizem ter sido o caráter depressivo de Lewis.16 Lewis foi indicado para o Prêmio Nobel de 1922 a 1944. A primeira indicaçao deveu-se a seu antigo orientador de doutorado Theodore Richards, por sua contribuiçao à termodinâmica química e à teoria de ligaçao química. Já em 1924, Svante Arrhenius, consultado sobre sua contribuiçao para o conhecimento da ligaçao química, declarou-a "insignificante", e exaltou, ao contrário, a contribuiçao de Langmuir, o rival de Lewis. Talvez tenham pesado algumas críticas anteriores de Lewis a Arrhenius, o qual, todavia, no final da vida (Arrhenius morreria em 1927), nao se mantinha tao atualizado com a ciência.8 Após receber nove indicaçoes no ano de 1926, o relatório à Academia Sueca é redigido por Theodor Svedberg, que recomenda ser prematuro atribuir o prêmio a Lewis naquele momento. O curioso é que quem o recebeu em 1926 foi o próprio Svedberg.8 Como escreveu Coffey, "em retrospecto, o trabalho de Lewis sobre o papel do par de elétron na química foi sua conquista científica mais significativa, particularmente se seu trabalho sobre ácidos e bases e em fotoquímica forem examinados como parte do mesmo empreendimento como sua descoberta da ligaçao covalente". O mesmo autor diz ainda que a atitude prevalente entre os químicos suecos após a revoluçao quântica era claramente desfavorável a modelos nao-matemáticos simplificados baseados no par eletrônico, sem levar em conta a utilidade que eles pudessem ter em outras áreas da química. Outros físico-químicos, todavia, como Louis Hammett e Christopher Ingold, ambos os quais indicaram Lewis para o prêmio, nao concordavam com este ponto de vista. Coffey acrescenta ainda que a grande ironia é que as maiores contribuiçoes de Lewis beneficiaram a química orgânica, disciplina em que ele havia recebido um D como conceito em seu curso de graduaçao.17 Se vivesse mais alguns anos, talvez Lewis tivesse compartilhado o Prêmio Nobel de 1954 com Linus Pauling, que o tinha como um importante predecessor. De fato, o prêmio de Pauling, que reconhecia seu papel no tratamento quântico de ligaçoes direcionais, devia muito ao papel de Lewis em abrir esse caminho.17 Uma lenda persistente diz que Lewis se teria suicidado por envenenamento no laboratório em virtude de uma série de fatores, como seu temperamento depressivo, por achar que seu tempo como pesquisador de ponta já pertencia ao passado e por ter sido deixado de lado na concessao dos Prêmios Nobel. Seu último doutorando, Michael Kasha, que o encontrou morto no laboratório na tarde de 23 de março de 1946, conta, todavia, uma história diferente em artigo publicado em 1984. Lewis, um grande perito em lidar com baixas temperaturas e sistemas de vácuo, estava na época trabalhando com cianeto de hidrogênio liquefeito. Seu interesse se deveu a ele ter lido na literatura que o HCN líquido pode variar sua constante dielétrica por um fator de até 100, dependendo da temperatura. Esta propriedade, relata Kasha, levou Lewis a dizer-lhe: "este seria um meio bastante interessante para testar o efeito da constante dielétrica na cor das tinturas". Lewis havia trabalhado bastante na fotoquímica relacionada à variaçao de cor das tinturas orgânicas. Kasha narra que, ao passar pelo laboratório às 14 horas daquele sábado, nao viu o professor e sentiu um forte cheiro de cianeto. Ao entrar, deparou-se com Lewis estendido no chao e um líquido borbulhando na capela, desprendendo o intenso odor de cianeto. Imediatamente ele chamou outros pesquisadores e, cobrindo o nariz, quebrou a vidraça da janela com um tijolo e jogou bastante bicarbonato sobre o líquido borbulhante na capela. Lewis foi levado imediatamente ao hospital da universidade, mas já chegou morto. Kasha afirma ainda que uma autópsia revelou que a causa da morte havia sido um infarto agudo do miocárdio. Kasha conclui que depois do ataque cardíaco a pressao no frasco com cianeto líquido que estava no Dewar havia aumentado, fazendo com que o líquido em ebuliçao se derramasse pela capela. Kasha também diz que nao havia no cadáver de Lewis as marcas características da cianose, que sao um arroxeamento das unhas e dos lábios.9 Todavia, ao contrário do que afirma Kasha, a realidade é que nao foi feita autópsia no cadáver, o que introduz mais um elemento de dúvida. Kasha também diz que antes de sua morte no laboratório, Lewis havia ido almoçar com um "distinto visitante", sem dizer quem ele era. Contudo, em entrevista dada a Patrick Coffey, o autor de Cathedrals of Science, em 2004, Kasha se lembrou de quem era o "distinto visitante": ninguém menos que Irving Langmuir. Coffey relata que foi à Biblioteca do Congresso, num lance detetivesco, e consultou os papéis de Langmuir, que lá se acham. Para sua surpresa descobriu que em 23 de março de 1946, no dia da morte de Lewis, Berkeley havia conferido a Langmuir um título honorário. Este também havia sido convidado a proferir uma série de conferências na universidade. A premiaçao ocorreu no período da manha e Lewis nao esteve presente. Aparentemente, segundo Coffey, Wendell Latimer e Joel Hildebrand arranjaram um almoço privado na tentativa de aproximar os dois eminentes químicos. Nada se sabe do que pudesse ter ocorrido naquele almoço. O certo é que pouco depois Gilbert Lewis jazia morto em seu laboratório. A ausência dos sintomas de envenenamento por cianeto no cadáver de Lewis, como testemunharam Kasha e outros, pode ser um indício de que a morte nao se deveu a envenenamento, mas poderia ter sido causada por algum problema cardíaco em decorrência do constrangimento e da tensao sofridos por Lewis ao ter que conviver por alguns momentos com seu rival. Lewis passou à história da ciência sobretudo por duas áreas importantes em que muito contribuiu: a teoria da ligaçao química e a termodinâmica química, área em que introduziu uma série de conceitos, como atividade e fugacidade. No final da vida teve grande destaque seu papel no desenvolvimento da fotoquímica. Ele foi o autor de muitos trabalhos experimentais envolvendo o óxido de deutério, e foi também o descobridor, em 1924, do dímero da molécula de oxigênio, O4, que se obtinha pela dissoluçao de oxigênio em nitrogênio líquido. A medida que a concentraçao de O2 paramagnético aumentava, a concentraçao da molécula diamagnética O4 também aumentava, até que se estabelecia um equilíbrio, como mostravam seus dados de susceptibilidade magnética. De fato, Lewis publicou em 1924, em J. Amer. Chem. Soc. um artigo intitulado "O Magnetismo do Oxigênio e a Molécula de O2".18 Neste artigo ele combina aspectos experimentais e teóricos, e começa por afirmar: "uma das propriedades características do oxigênio é seu pronunciado paramagnetismo. Isto distingue o oxigênio molecular tao fortemente de outros compostos em que se supoe o oxigênio ligado por uma ligaçao dupla que eu concluí recentemente que nao há qualquer ligaçao dupla na molécula de O2. Ao contrário, supus que os dois elétrons que se pensava constituíssem a segunda ligaçao estao na realidade separados, de modo que cada átomo tenha um elétron desemparelhado, de acordo com a fórmula" (dada na Figure 2).
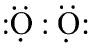 Figura 2. Estrutura proposta por Lewis para a molécula de O2
De fato, "o oxigênio tem as propriedades de uma molécula com elétrons desemparelhados, pois ele tem uma cor apreciável, e uma reatividade muito maior do que comumente se lhe atribui." A partir daí prevê a possibilidade de dimerizaçao da molécula, dando o tetraoxigênio, que ele passa a discutir. Nesse período pré-quântico da química, de fato nao se poderia esperar uma descriçao da molécula de dioxigênio como a entendemos hoje, mas a honestidade intelectual de Lewis ao interpretar seus dados experimentais é notável. Como escreveu Linus Pauling em 1984, a respeito da reaçao de dimerizaçao do dioxigênio para dar o tetraoxigênio: "ele conseguiu justificar os valores experimentais da susceptibilidade magnética das soluçoes de oxigênio (líquido) em nitrogênio (líquido), pela suposiçao de que há um equilíbrio entre moléculas paramagnéticas de dioxigênio e as moléculas diamagnéticas de tetraoxigênio, O4. Dos valores da susceptibilidade magnética ele foi capaz de obter a variaçao da energia livre padrao de Gibbs e a variaçao de entalpia da reaçao."19 A existência do dímero de O2, contudo, permaneceu em suspenso até o século XXI, por falta de uma comprovaçao direta de sua existência. Nos últimos anos, contudo, as ideias de Lewis geraram uma torrente de trabalhos de enorme interesse. Em 2001 um grupo italiano conseguiu determinar experimentalmente a existência do chamado oxozônio, O4, por espectrometria de massas do íon O4+.20 A literatura recente tem um grande número de artigos sobre os alótropos mais pesados do oxigênio, tanto experimentais como teóricos, que mostram, por exemplo, a existência da forma sólida O8, chamada de oxigênio vermelho, em pressoes muito altas. Quanto ao alótropo O4, ele é um cluster que pode apresentar duas estruturas calculadas distintas, uma cíclica, formando um quadrilátero reverso, com simetria D2d, e outra trigonal plana, com simetria D3h. Esta última é muito interessante, por completar uma sequência homóloga que engloba BO33-, CO32- e NO3-, além de ser semelhante ao SO3.21,22 A catolicidade dos interesses de Lewis está demonstrada nos inúmeros assuntos sobre os quais ele publicou, como economia ou a causa das glaciaçoes. Um artigo seu, intitulado "A Termodinâmica da Glaciaçao" foi publicado postumamente em Science, como menciona Kasha.9 Lewis foi um pesquisador que nao reconhecia barreiras epistemológicas artificiais. Nas primeiras décadas do século XX, químicos e físicos raramente se falavam, à exceçao de alguns cientistas fora do padrao. Isso foi o que levou, por exemplo, à demora dos químicos em tomar conhecimento da teoria do campo cristalino, formulada por um físico, Van Vleck. Lewis, um excelente matemático, foi o primeiro cientista americano a se ocupar da teoria da relatividade de Einstein, e em 1908-9 publicou vários artigos sobre o tema.23 O tema retornaria em 1926, em seu livro intitulado The Anatomy of Science, que também apresenta um pronunciado pendor filosófico.24 Em seus últimos anos ele confessaria a Michael Kasha que as moléculas orgânicas se tinham tornado a alegria de seus dias, apesar de, durante a maior parte da vida, ele ter detestado a química orgânica porque havia recebido um conceito ruim num curso dessa disciplina quando estudante em Harvard.9 Lewis também é responsável pela palavra fóton e seu uso em ciência, em substituiçao à antiga expressao quantum de luz. Embora a palavra fóton já tivesse sido usada antes por outros pesquisadores, notadamente nos campos de psicologia e fisiologia 25, a introduçao do termo por Lewis em 1926, num artigo em Nature, foi o que acabou adotado universalmente.26 Todavia, Lewis considerava o fóton mais uma partícula subatômica que uma unidade de energia.
A TEORIA DE LIGAÇAO ELETRONICA A Teoria de Lewis da Ligaçao Química fundamentada sobre o conceito de par de elétrons foi desenvolvida principalmente em três artigos seminais: o primeiro, publicado em J. Amer. Chem. Soc. em 1913, intitula-se "Valência e Tautomerismo"27, e contém o germe do que viria a seguir. Neste artigo, Lewis adota os termos "número de valência" e "número polar", designando o que chamamos de valência e número de oxidaçao, respectivamente. Em suas palavras, o número de valência é "o número de posiçoes, ou regioes ou pontos no átomo em que ocorre a ligaçao a pontos correspondentes em outros átomos"; já o número polar é "o número de elétrons negativos que um átomo perdeu". Numa nota de rodapé ele acrescenta a propósito dos compostos polares e nao-polares: "nao se deve supor que um dado composto corresponda totalmente e sempre a qualquer um dos dois tipos". Mais adiante acrescenta: "Aos compostos polares e nao-polares podemos adicionar um terceiro, o metálico. No primeiro tipo os elétrons ocupam posiçoes fixas no átomo. No segundo, os elétrons se movem livremente de átomo a átomo dentro da molécula. No terceiro tipo, ou metálico, o elétron é livre de se mover fora da molécula." O último parágrafo deste artigo novamente enfatiza a convicçao de Lewis: "todos os compostos químicos conhecidos podem ser agrupados nas três classes: nao-polar, polar e metálico, exceto quando o mesmo composto possa cair em parte ou temporariamente em dois desses grupos". O segundo artigo, também publicado em J. Amer. Chem. Soc., em 1916, intitula-se "O átomo e a molécula"28, e é o mais importante deles. Nele, Lewis começa por discutir a necessidade de considerar uma teoria da estrutura atômica, a qual ele já utilizava havia alguns anos na interpretaçao de fenômenos químicos, mas só entao resolvera publicar. A diferença fundamental entre os compostos polares e nao-polares é que, "nos primeiros um ou mais elétrons sao ligados por forças suficientemente fracas, de modo que possam tornar-se separados de suas posiçoes primitivas nos átomos e, no caso extremo, passam completamente para outro átomo." Já nos compostos chamados de nao-polares "os elétrons pertencentes ao átomo individual sao seguros por tais forças que nao se movem para longe de suas posiçoes normais, enquanto na molécula polar os elétrons, sendo mais móveis, movem-se separando a molécula em uma parte positiva e uma negativa." Ele reconhece que a polaridade pode variar amplamente quando diz: "uma molécula, ou mesmo parte de uma molécula, pode passar de um tipo extremo ao outro, nao por uma variaçao súbita e descontínua, mas por gradaçoes imperceptíveis." Entre as publicaçoes de Lewis de 1913 e 1916, e pouco antes desta última, saíra publicado um importante artigo do físico alemao Walther Kossel (1888-1956) na revista Annalen der Physik29, sob a influência das descobertas recentes de Rutherford, Bohr e da escola alema de física, em que Kossel discute a formaçao de moléculas em termos da estrutura atômica. Kossel trata longamente da formaçao de compostos polares (i.e., iônicos) pela perda ou ganho de elétrons e a consequente formaçao de espécies carregadas eletricamente que se atraem, estabilizando as estruturas dos produtos. No artigo de Lewis de 1916, como ele já havia começado a fazer em 1913, a questao é bastante ampliada, abrangendo todos os tipos de ligaçoes, como está citado acima, quando ele se refere aos compostos iônicos, por ele chamados de polares, aos compostos moleculares, chamados de nao-polares, e às substâncias metálicas. Na seçao intitulada "O átomo cúbico" do artigo de 1916, Lewis se refere ao memorando privado usado por ele desde 1902 e no qual ele havia proposto o que chamara de "teoria do átomo cúbico." O assunto só veio a público a partir do artigo de 1916. Este é o famoso conceito pelo qual os elétrons de valência de um átomo se distribuem pelos vértices de um cubo, variando de 0 a 8. Sua teoria é apresentada na forma de 6 postulados, que sao:
Em seguida ele passa a discutir cada um dos postulados, que será aqui resumido:
Ao discutir a ligaçao entre dois átomos, diz: "para expressar essa ideia de uniao química em símbolos eu sugeriria o uso de dois pontos, arranjados de forma a representar os dois elétrons que agem como as conexoes entre os dois átomos. Deste modo podemos escrever Cl2 como Cl:Cl". O artigo de Lewis é bastante extenso e ele discorre longamente sobre vários tópicos ligados a seus conceitos, dando um grande número de exemplos para ilustrar suas ideias. O terceiro artigo, de 1923, é o texto de uma conferência pronunciada por ele na Faraday Society de Londres e publicada naquele mesmo ano nas Trans. Far. Soc.31 Seu título é "Conferência Introdutória: Valência e o Elétron". Este artigo resume e clarifica suas ideias, como quando ele diz, referindo-se aos compostos orgânicos: "eu propus representar toda ligaçao como um par de elétrons ligados conjuntamente por dois átomos". Na seçao intitulada "O Par de Elétrons como a Ligaçao Química" ele antecipa a questao da influência dos pares de elétrons nao ligantes na geometria das moléculas: "Estejamos lidando com compostos orgânicos ou inorgânicos, a ligaçao química é sempre o par de elétrons. Por mais importante que seja o par de elétrons para a teoria total da valência, deve-se observar que tal par nao é fundamentalmente diferente de outros pares que nao formam ligaçoes." Em seguida, usando o termo "octeto", cunhado por Langmuir em 1919, ele discute a sequência N3-, [NH]2-, [NH2]-, NH3 e [NH4]+, mostrando como a estrutura do octeto do nitrogênio sofrerá distorçoes pela presença desigual de elétrons ou átomos. No período entre seus dois últimos artigos, Irving Langmuir havia publicado em J. Amer. Chem. Soc., em 1919, um longo artigo intitulado "O Arranjo de Elétrons nos Atomos e Moléculas".32Além de organizar e avançar nas ideias de Lewis, Langmuir introduz em seu artigo duas novas expressoes, que sao usadas até hoje. A primeira aparece quando, ao discutir o arranjo cúbico dos elétrons, de acordo com Lewis, ele diz: "chamaremos este grupo estável de 8 elétrons de octeto". Mais adiante, sob o título "Valência, Número de Coordenaçao e Covalência", escreve Langmuir: "denotaremos pelo termo covalência" as ligaçoes envolvendo compartilhamento de elétrons. Langmuir foi o grande popularizador da teoria de Lewis, de tal sorte que ela passou a ser conhecida por muitos como teoria de Lewis-Langmuir, para grande desgosto de Lewis.33 Durante o ano de 1916, quando publicou seu artigo mais famoso sobre as ligaçoes químicas, Lewis manteve extensa correspondência com Niels Bohr, e convidou-o a passar um semestre em Berkeley para dar um curso sobre a estrutura atômica e molecular. Infelizmente Bohr nao pôde atender ao convite.33 Lewis, todavia, nao se cansava de preocupar-se com o que se chamava o átomo dos físicos e o átomo dos químicos. Para um químico tao próximo da física como Lewis, este era um problema que precisava de uma soluçao. O aparentemente insolúvel problema do compartilhamento eletrônico foi finalmente equacionado em 1925 com o surgimento do Princípio da Exclusao de Pauli e do conceito de spin eletrônico, que permitiram racionalizar as ideias de Lewis de um ponto de vista físico.33 O próprio Lewis escreveu em seu famoso artigo de 1938 sobre ácidos e bases, mostrando uma aguda percepçao dos problemas em jogo:
Em 1923 Lewis publicou seu famoso livro "Valência e a estrutura de átomos e moléculas", já mencionado acima, no qual ele discorre mais demoradamente sobre suas ideias relativas às ligaçoes químicas. Uma consequência importante do conceito de ligaçao por par de elétrons é o conceito de ácidos e bases de Lewis, que muitos, equivocadamente, chamam de "teoria de ácidos e bases de Lewis", quando se trata de um conceito, ou definiçao, que é muito diferente de uma teoria. A mesma observaçao se pode fazer com relaçao a outros conceitos de ácido e base, como o de Arrhenius, do século XIX, que às vezes também é chamado de teoria, quando na realidade é um conceito derivado da teoria da dissociaçao eletrolítica de Arrhenius. Lewis viria a dedicar-se a estudar o conceito de ácidos e bases já no final de sua carreira, sobretudo em seu artigo de 1938 publicado pelo J. Franklin Institute.34 Lewis aqui foi de uma engenhosidade e originalidade incríveis. As definiçoes precedentes de ácidos e bases pressupunham um meio em que as interaçoes ocorriam (água, no caso da definiçao de Arrhenius, em que os ácidos podiam doar H+, e as bases podiam doar OH-, sempre em meio aquoso), ou a presença de uma dada espécie química (íon hidrogênio que podia ser doado pelos ácidos, ou recebido pelas bases, na definiçao de Brønsted-Lowry). A definiçao de Lewis era muito mais abrangente e universal, pois levava em conta um componente de toda a matéria, os elétrons, que podiam ser doados pelas bases e recebidos pelos ácidos. A definiçao de acidez e basicidade de Lewis foi de certa forma uma enorme propulsora do progresso no estudo de mecanismos de reaçao de compostos orgânicos. Como a maioria das reaçoes orgânicas nao se passa em meio aquoso, as definiçoes anteriores só tinham uma aplicabilidade muito restrita na química orgânica. O aspecto mais surpreendente da Teoria de Ligaçao Química de Lewis é o fato de ela ter sido formulada 10 anos antes do surgimento da mecânica quântica, e ser ainda atual em muitos de seus aspectos. Se atentarmos para usar "densidade eletrônica" no lugar de usar exclusivamente "par de elétrons", temos aí uma atualizaçao das ideias de Lewis, que se mostram resistentes ao tempo dessa maneira. O que se chamava no século XVIII "afinidade eletiva" deu origem ao conceito muito mais preciso de "ligaçao química". Um dos maiores admiradores de Lewis no século XX foi Linus Pauling, que dedicou-lhe seu livro mais conhecido, The Nature of the Chemical Bond35, de 1939. Em artigo posterior, assim disse Pauling: "Quando penso na história da ligaçao química, pergunto-me por que algumas das descobertas feitas na era da mecânica quântica da década de 1930 nao foram descobertas antes. A escala de eletronegatividades dos elementos é um exemplo. Ela foi formulada em 1933... A ideia básica, atribuída à mecânica quântica em 1933, é que o caráter iônico parcial de uma ligaçao a torna mais estável, com energia mais baixa do que uma ligaçao covalente pura entre átomos desiguais. Esta ideia nao é derivada da mecânica quântica."19 Pauling continua dizendo que Langmuir formulara o princípio da eletroneutralidade, mas fizera pouco caso dele, e Lewis o ignorou. Foi por essa razao que o conceito e a escala de eletronegatividades levaram bem mais tempo para surgir.19
CONCLUSAO As ideias e conceitos apresentados aqui o foram de forma bastante sucinta com o intuito de salientar o papel central de Lewis no desenvolvimento da química no século XX. Sua obra foi tao fundamental que marcou de forma indelével boa parte do que se seguiu, como o próprio Pauling reconhece. Poucos sao os cientistas a quem se pode atribuir um papel tao marcante no curso da ciência. Lewis permanece como um desses poucos.
REFERENCIAS 1. Tosi, L., Quím. Nova 1989, 12, 33. 2. Filgueiras, C. A. L., Quím. Nova 1995, 18, 219-224. 3. Filgueiras, C. A. L., Lavoisier - o estabelecimento da química moderna, Odysseus, Sao Paulo, 2002, pp. 1-197. 4. Filgueiras, C. A.L., Química Nova na Escola 2004, 20, 38. 5. Shaik, S., J. Comput. Chem. 2006, 28, 51. 6. Tiernan, N. F., J. Chem. Educ. 1985, 62, 569. 7. Hildebrand, J. H., Biog. Memoirs Nat. Acad. Sci. (U.S.) 1958, 31, 208. 8. Gonçalves-Maia, R., Lewis, Editora Livraria da Física, Sao Paulo, 2016, 1-85. 9. Kasha, M., J. Chem. Educ., 1984, 61, 204. 10. James, L. K., ed., Nobel Laureates in Chemistry 1901-1992, American Chemical Society and the Chemical Heritage Foundation, Washington, 1993, pp. 100-107. 11. Richards, T. W., e Lewis, G.N., Proc. Amer. Acad. Arts and Sciences, 1898, 34, 87. 12. Lewis, G. N., Valence and the Structure of Atoms and Molecules, Dover Publications, [1923] 1966, N. York, pp. 29-30. 13. Idem, ibid., p. 1. 14. Lewis, G. N., e Randall, M., Thermodynamics and the Free Energy of Chemical Substances, 1923, McGraw-Hill, N. York. 15. Coffey, P., Cathedrals of Science - the Personalities and Rivalries that made Modern Chemistry, Oxford University Press, N. York, 2008, p. 303. 16. Gillespie, R. J., Robinson, E. A., J. Comput. Chem. 2006, 28, 87. 17. Coffey, P., op. cit., p. 300. 18. Lewis, G. N., J. Amer. Chem. Soc. 1924, 46, 2027. 19. Pauling, L., J. Chem. Ed. 1984, 61, 261. 20. Cacace, F., de Petris, G., Troiani, A., Angew. Chem., Int. Ed. 2001, 40, 4062. 21. Gadzhiev, O. B., Ignatov, S. K., Kulikov, M. Y., Feigin, A. M., Razuvaev, A. G., Sennikov, P. G., Schrems, O., J. Chem. Theory Comput., 2013, 9, 247. 22. Prasad, O., Sinha, L., Misra, N., Narayan, V., Srivastava, R. K., Mishra, H. N., Der Pharma Chemica, 2009, 1, 79. 23. Lewis, G. N., a) Technol. Quart. 1908, 21, 212; b) Phil. Mag., 1908, 16, 705; c) Ann., Naturphil. 1908, 7, 429; d) Proc. Amer. Acad. 1909, 44, 711; Phil. Mag., 1909, 18, 510. 24. Lewis, G. N., The Anatomy of Science, Yale University Press, New Haven, 1926. 25. Kragh, H., arXiv preprint arXiv:2014, 1401.0293- arxiv.org. 26. Lewis, G. N., Nature 1926, 118, 874. 27. Lewis, G. N., J. Amer. Chem. Soc. 1913, 35, 1448. 28. Lewis, G. N., J. Amer. Chem. Soc. 1916, 38, 762. 29. a) Kossel, W., Ann. Phys. 1916, 49, 229; b) Leicester, H. M., ed., Sourcebook in Chemistry 1900-1950, Harvard Un. Press, Cambridge, 1968. 30. Braga, J. P., Filgueiras, C. A. L., Quím. Nova 2013, 36, 1073. 31. Lewis, Trans. Far. Soc. 1923, 19, 452. 32. Langmuir, I., J. Amer. Chem. Soc. 1919, 41, 868. 33. Simoes, A., J. Comput. Chem., 2006, 28, 62. 34. Lewis, G. N., J. Franklin Institute 1938, 118, 293. 35. Pauling, L., The Nature of the Chemical Bond and the Structure of Molecules and Crystals, Cornell University Press, Ithaca, [1939], 3rd ed., 1960.
#This paper is part of the PubliSBQ Special Issue in honor of the late Prof. Angelo da Cunha Pinto. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access





