Educação
|
|
| Uso de nanobastões de ouro para o desenvolvimento de aulas práticas de nanotecnologia Use of gold nanorods for the development of practical classes in nanotechnology |
|
Cyntia Silva Ferreira1,*; Luiz Orlando Ladeira2; Cristiano Fantini Leite2; Flávio Guimaraes da Fonseca3; Erica Milena de Castro Ribeiro1; Alice Freitas Versiani3; Jorge Fernando de Souza Silva1; Cíntia Lopes de Brito Magalhaes1; Breno de Mello Silva1
1. Departamento de Ciências Biológicas, Universidade Federal de Ouro Preto, 35400-000 Ouro Preto - MG, Brasil Recebido em 05/10/2016 *e-mail: csf.ferreira@gmail.com A gold nanoparticles functionalization experiment was conducted in a biotechnology summer course at UFOP as a model for the introduction of the laboratory practice in nanotechnology for postgraduate courses in the areas of chemistry and biotechnology. The gold nanorods were synthesized by the seed method and then, functionalized with anti-IL-6 antibodies using the reagents EDAC/NHS and polyethyleneimine (PEI). This nanocompound was tested against the binding with the specific antigen (IL-6) and changes in the longitudinal plasmon absorption spectrum showed the coupling efficiency, which was also verified by the decrease in zeta potential. The experiment was satisfactory, with a positive feedback from participants, and could be implemented in nanotechnology practical classes from postgraduate courses, as a way for improve education in the emergent area of nanobiotechnology. INTRODUÇAO O universo da nanotecnologia se expandiu consideravelmente na esfera da pesquisa científica em todo mundo nos últimos anos e constitui uma área que certamente acarretará em enormes retornos econômicos. Materiais e tecnologias em escala nanométrica têm sido empregados em diversas áreas, tais como no setor alimentício, sistemas de energia renovável, bioinformática e na medicina.1-4 Além disso, constituem matéria-prima nobre para o desenvolvimento de dispositivos e sistemas multifuncionais que se adequam aos mais variados produtos e processos industriais. Perante a complexidade e relevância da nanotecnologia, emerge a necessidade de abordagens práticas e sistêmicas nos cursos de graduaçao e também de pós-graduaçao. Entretanto, apesar de já desenvolvidos e utilizados há algum tempo em pesquisas de diversas áreas, os conceitos da nanotecnologia ainda nao sao abordados em muitos cursos teóricos e práticos de pós-graduaçao no Brasil. Neste contexto, uma classe de nanomateriais de grande potencial tecnológico e educacional sao as nanopartículas de ouro (AuNPs), que possuem propriedades ópticas, magnéticas e estruturais interessantes para aplicaçoes químicas e biológicas. Sao ainda as nanopartículas metálicas mais estáveis que se tem conhecimento.5,6 Elas podem ser sintetizadas em diversos tamanhos e formatos, tais como nanoesferas, nanobastoes, nanogaiolas, nanoestrelas e nanoconchas.5 A síntese das AuNPs geralmente é econômica, pois embora demande reagentes onerosos, estes sao empregados em concentraçoes muito baixas.7 Entre as várias aplicaçoes das nanopartículas de ouro, o sensoriamento é tido como uma das áreas de maior interesse na atualidade. Nesse contexto, dentre as diferentes formas de nanopartículas, é dada grande atençao às nanoesferas e nanobastoes de ouro. Isso se deve ao grande volume de conhecimento obtido sobre a característica mais peculiar das nanopartículas de ouro, a chamada ressonância plasmônica de superfície (SPR). A SPR se caracteriza pela oscilaçao coletiva dos elétrons de conduçao das partículas metálicas desencadeada pela exposiçao à luz, a qual pode ser detectada por espectroscopia.8,9 Descritas pela primeira vez por Faraday em 1857, as nanoesferas de ouro sao usualmente sintetizadas a partir de uma reaçao de reduçao aquosa de ácido cloroáurico (HAuCl4) por citrato de sódio.10,11 Já os nanobastoes de ouro sao frequentemente sintetizados pelo método mediado por sementes, descrito por Murphy e colaboradores em 2001,12,13 no qual os nanobastoes sao preparados à partir da adiçao de nanoesferas recobertas por citrato (sementes), à uma soluçao contendo HAuCl2 em elevadas concentraçoes, resultante da reduçao de HAuCl4 por ácido ascórbico (C6H8O6) na presença do surfactante brometo de cetiltrimetilamônio (CTAB) e íons de prata. O CTAB é essencial para a síntese controlada em forma de bastoes, devido ao fenômeno de ligaçao preferencial às diferentes faces dos bastoes após o início do crescimento das sementes.14 Quanto à propriedade de SPR e sua aplicabilidade como sensores, as nanoesferas de ouro apresentam uma banda de absorçao plasmônica na regiao do espectro visível, em torno de 520 nm. Por outro lado, os nanobastoes exibem duas bandas de SPR, visto que a oscilaçao coletiva dos elétrons pode ocorrer em dois sentidos, dependendo da polarizaçao da luz incidente. Assim, para os nanobastoes existe uma banda de absorçao no comprimento de onda semelhante ao das nanoesferas (denominada banda transversal),15 e uma banda longitudinal (>600nm) como resultado da absorçao induzida pelo eixo longo dos nanobastoes, a qual varia de acordo com sua relaçao de aspecto (comprimento/largura). Com o aumento dessa razao, que pode ser determinado tanto pela modificaçao do tamanho da nanopartícula quanto pela ligaçao de moléculas em sua superfície, a cor do ouro em soluçao é alterada do azul para o vermelho e o comprimento de onda de ressonância de plasmon é deslocado.16-19 A existência da banda de absorçao plasmônica longitudinal apresenta-se como o principal diferencial e grande vantagem dos nanobastoes frente às nanoesferas, no que diz respeito à sua aplicaçao como sensores. A ligaçao de uma molécula ao nanobastao causa uma ligeira mudança no ambiente dielétrico próximo e consequentemente um desvio no pico de absorçao da banda longitudinal, alteraçao que pode ser facilmente observada por meio da análise espectrofotométrica.14,19 Assim, as medidas de absorçao óptica podem ser realizadas nas suspensoes coloidais de nanobastoes puros e acoplados a diversos ligantes e/ou agentes biológicos. O mesmo nao é possível com nanoesferas de ouro, já que possuem apenas uma banda de absorçao plasmônica que nao sofre deslocamento após tais interaçoes. Portanto, os nanobastoes de ouro oferecem alta sensibilidade de absorçao óptica após qualquer ligaçao física ou química na sua superfície, alterando de maneira mensurável o pico de absorçao óptica relacionado ao modo longitudinal.12,14,17 Para que as nanopartículas de ouro apresentem aplicabilidade, o CTAB empregado na síntese deve ser removido ou substituído antes das etapas de funcionalizaçao química com ligantes e/ou moléculas de interesse, tais como polietileno glicol (PEG), oligonucleotídeos, peptídeos, polímeros ou sílica inorgânica.14,19 Moléculas bi-funcionais sao amplamente empregadas (Tabela 1), e geralmente possuem grupos de ácido carboxílico que atuam como ligantes químicos para bioconjugaçao através de acoplamento mediado por carbodiimida via amina primária.20
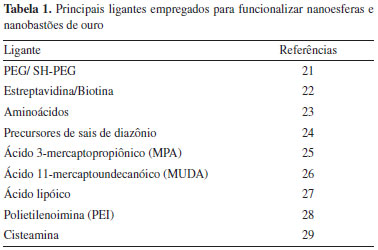
Todos os eventos de funcionalizaçao descritos acima podem ser facilmente monitorados através da ressonância plasmônica de superfície, já que a ligaçao de biomoléculas na superfície das nanopartículas altera o ambiente circundante e afeta a densidade de cargas dos elétrons ali presentes, o que acarreta em deslocamento da banda de absorçao longitudinal.30 Nesse contexto, existem inúmeras aplicaçoes baseadas nas alteraçoes da ressonância plasmônica de superfície. Uma delas é o biosensoriamento, conhecido por nanoSPR, obtido pela ligaçao de biomoléculas (como anticorpos) aos nanobastoes já acoplados a um ligante. A posterior interaçao com o alvo conclui a detecçao, resultando em um deslocamento observável da banda longitudinal.19 Estes nanomateriais, portanto, podem ser empregados em ensaios de biosensoriamento químico, com fácil detecçao do resultado final por meio da verificaçao do deslocamento da banda de absorçao plasmônica longitudinal em espectrofotômetro.7 Trabalhos contendo propostas para introduçao da nanociência em cursos de graduaçao envolvendo nanopartículas sintetizadas a partir de diferentes materiais (incluindo pontos de carbono, ouro e prata) já foram documentados.31-33 Alguns autores demonstraram a aplicabilidade de aulas práticas sobre síntese de nanopartículas de prata e ouro.32,33 Nesses trabalhos, além dos métodos de síntese, foram abordadas as principais propriedades ópticas - dependentes do formato e tamanho - e catalíticas das nanopartículas de ouro.33 Recentemente foi reportada uma proposta de aula prática sobre nanopartículas de ouro depositadas em filmes de biopolímeros, na qual os alunos puderam verificar a atividade antimicrobiana da nanopartícula.34 No entanto, apesar da relativa facilidade com que as nanopartículas de ouro podem ser preparadas e modificadas quimicamente, nao há ainda relatos da utilizaçao destes nanomateriais em aulas práticas com foco em aplicaçoes biotecnológicas. A experiência prática de sintetizar e manipular estes nanomateriais seria de grande relevância na formaçao acadêmica de estudantes de pós-graduaçao para a expansao e consolidaçao do conhecimento teórico e prático da nanotecnologia no Brasil. Além de envolver conceitos de química (como teorias de ligaçao metálica, estrutura atômica, reaçoes de oxidaçao-reduçao e espectroscopia), a prática experimental em nanotecnologia utilizando AuNPs como biosensores envolve também conceitos bioquímicos como interaçoes antígeno-anticorpos e conformaçao de moléculas. Este caráter interdisciplinar agrega conhecimento aos alunos e valor aos cursos, já que a nanotecnologia é uma nova área que vem ganhando espaço no Brasil e no mundo. Portanto, o presente trabalho retrata a experiência de uma aula prática de funcionalizaçao de nanobastoes de ouro, realizada durante o III Curso de Verao em Biotecnologia na Universidade Federal de Ouro Preto (UFOP). Essa é uma iniciativa de divulgaçao da nanobiotecnologia, de significativa importância para o avanço tecnológico e valorizaçao da pesquisa. Além disso, este trabalho descreve as etapas de acoplamento do ligante polietilenoimina (PEI) à superfície de nanobastoes de ouro e posterior ligaçao com o anticorpo anti-Interleucina 6 (IL-6). A IL-6 é uma proteína pró-inflamatória, glicosilada com peso molecular de 26 kDa, identificada pela primeira vez em 1980, produzida por macrófagos, células dendríticas, algumas células TCD4+ (dos tipos Th2 e Th17) e também por células nao imunes (fibroblastos e células endoteliais).35,36 Este é, portanto, um modelo para o desenvolvimento de novos ensaios de detecçao de biomoléculas que podem ser aplicados à pesquisa e ao ensino, na formaçao de pós graduandos em química e em biotecnologia.
PARTE EXPERIMENTAL Reagentes Para a síntese de nanopartículas de ouro foram utilizados os reagentes ácido tetracloroáurico 99% (Sigma-Aldrich), brometo de cetiltrimetilamônio P.A. (CTAB, Sigma-Aldrich), ácido ascórbico e nitrato de prata, ambos com pureza mínima de 99% (Aldrich). As nanopartículas foram funcionalizadas com o ligante polietilenoimina 50% w/v em água (Sigma-Aldrich). Foi utilizado o par anticorpo-antígeno do kit para ELISA de IL-6 humana (BD OptEIATM). Os anticorpos foram suspendidos em tampao fosfato salino (PBS), em cloridrato de N-etil-N'-(3-dimetil-aminopropil)carbodiimida P.A. (Sigma-Aldrich) e em N-hidroxisuccinimida 98% (Sigma-Aldrich). Para bloqueio da superfície dos nanobastoes, foi utilizada a albumina sérica bovina com pureza mínima de 98% (GE, Sigma). Todas as soluçoes aquosas foram preparadas com água deionizada e filtrada (18 MΩ) e as vidrarias lavadas exaustivamente com ácido nítrico 65% (Vetec). Síntese de nanobastoes de ouro As nanopartículas de ouro foram sintetizadas pelo método mediado por semente.13,37 Nesta síntese, as sementes de ouro foram preparadas por meio da mistura de 2,25 mL de HAuCl4 (5 mmol L-1), 1,25 mL de CTAB (0,2 mol L-1) e 0,9 mL de soluçao resfriada de NaBH4 (1 mmol L-1) sob agitaçao contínua, resultando em uma soluçao marrom-amarelada. A soluçao de crescimento foi obtida misturando-se 5 mL de soluçao HAuCl4 (1 mmol L-1) com 5 mL de CTAB (0,2 mol L-1) e AgNO3 (4 mmol L-1). Entao, 0,07 mL de ácido ascórbico (0,0788 mol L-1) foram adicionados durante agitaçao vagarosa. Nessa etapa o ácido ascórbico age como agente redutor e altera a cor da soluçao de amarelo intenso para transparente. Por fim, 0,012 mL da soluçao semente foram adicionados à soluçao recém-preparada para iniciar o crescimento dos nanobastoes. A cor da soluçao se alterou gradualmente entre os primeiros 15-20 min, até se estabilizar em tom arroxeado. Os nanobastoes foram purificados retirando-se o excesso de CTAB por dupla centrifugaçao a 5.600 g por 15 min e redispersos em água ultrapura deionizada. Funcionalizaçao de nanobastoes de ouro Para permitir o acoplamento dos anticorpos, foi realizada a ligaçao de PEI à superfície dos nanobastoes de ouro. Esse reagente é capaz de mediar a ligaçao covalente nanobastao-anticorpo devido aos vários grupos amina reativos.38 Para isso, 250 µL de soluçao de nanobastoes de ouro foram centrifugados a 4000 g por 10 min, ressuspendidos em 250 µL de PEI (0,3% em água ultra pura) e incubados a temperatura ambiente em banho ultrassônico por 30 min, para desestabilizaçao do CTAB presente na superfície das nanopartículas e acoplamento do PEI. Em seguida, a soluçao foi novamente centrifugada a 4000 g por 10 min e ressuspendida em 250 µL de anticorpos anti-IL-6 a 0,4 µg mL-1 previamente preparados. A soluçao dos anticorpos foi preparada adicionando-se 18,7 µL de EDAC/HNS (0,4 mol L-1 / 0,1 mol L-1), 0,4 µg mL-1 dos anticorpos anti-IL-6 e tampao fosfato salino (PBS 1X, pH 7.4, NaCl, KCl, Na2HPO4, KH2PO4 em água ultra pura) para um volume final de 250 µL e, em seguida, incubada por 30 min a 4 °C. Por fim, a reaçao de acoplamento dos nanobastoes funcionalizados ao PEI com os anticorpos foi realizada por 60 min à temperatura ambiente em banho ultrassônico. Ao final deste tempo foram novamente centrifugadas a 4000 g por 10 min e ressuspendidas em 100 µL de PBS contendo 62 µg mL-1 de BSA, para realizar o bloqueio de possíveis regioes livres remanescentes na superfície dos nanobastoes de ouro. Transcorridos 30 min de incubaçao à temperatura ambiente, a soluçao foi centrifugada a 4000 g por 10 min e ressuspendida em 100 µL de PBS contendo 100 pg mL-1 do antígeno específico IL-6. Instrumentaçao Os espectros de absorçao plasmônica das soluçoes coloidais foram obtidos em um espectrofotômetro Shimadzu UV-1800, utilizando-se cubetas de quartzo de 1 cm de caminho óptico. As amostras foram também analisadas por leitura de potencial zeta, com o qual é possível aferir estabilidade e comprovar a ligaçao de moléculas nas nanopartículas, através da modificaçao da sua carga superficial quando dessa interaçao. Para as leituras, 10 µL de amostra ressuspendida em PBS foram diluídos em 1,5 mL de água ultra pura e entao, aplicados em cubetas específicas. As medidas foram feitas utilizando Zetasizer (NanoSeries - Malvern). Além disso, os dados resultantes da leitura em espectrômetro UV-Vis-NIR foram normalizados utilizando o software PeakFit V.4 e os gráficos foram gerados em GraphPad Prism® e Origin v. 8.0. Segurança e riscos Todos os procedimentos experimentais sao de simples execuçao e nao expoem os alunos a riscos, desde que sejam realizados seguindo-se as normas básicas de biossegurança. Deve ser dada atençao especial aos seguintes reagentes:
RESULTADOS E DISCUSSAO Síntese de nanobastoes de ouro O procedimento de síntese permitiu a obtençao de uma soluçao coloidal de cor arroxeada altamente estável de nanobastoes de ouro. Tal como na síntese de nanoesferas, a formaçao dos nanobastoes envolve a reduçao de AuCl4- para Au0 pela açao do borohidreto de sódio, e, em seguida do ácido ascórbico, que atuam como agentes redutores.32 O processo de síntese de nanobastoes mediado por sementes consiste no alongamento assimétrico de nanoesferas de ouro (sementes) em apenas uma direçao, devido à interaçao com o surfactante CTAB e íons de prata. Diferentes teorias tentam explicar tal fenômeno de crescimento assimétrico direcionado.39,40 Basicamente, os átomos de ouro encontram-se organizados em uma estrutura cúbica de face centrada e é suposto que a deposiçao de outros átomos de ouro (presentes na soluçao de crescimento) cause a quebra de assimetria dessa estrutura e o início do crescimento na direçao em que ocorreu essa deposiçao inicial.12,14 A partir desse ponto, essa diferença estrutural acarreta em diferenças conformacionais e faces com diferentes energias de superfície, fato que, por sua vez, é responsável pela interaçao preferencial do surfactante (e dos íons de prata) com regioes específicas do bastao em crescimento.14,19 A face em que o crescimento foi iniciado apresenta um espaçamento entre os átomos que é mais propício à interaçao do CTA+ do que com as demais. Por outro lado, as demais faces apresentam maior energia de superfície, a qual é estabilizada pela interaçao com o CTAB. Na soluçao de crescimento, os átomos de ouro encontram-se na forma de AuCl2- ligado à micelas de CTAB. A interaçao entre os campos elétricos do AuCl2- (carregado negativamente) e da semente em crescimento (carregada positivamente) faz com que as colisoes entre as partículas sejam mais frequentes na extremidade em que o crescimento foi iniciado, direcionando o alongamento em forma de bastao.14 Além do papel exercido pelo CTAB, os íons de prata também sao importantes no controle da síntese por exercerem duas atividades fundamentais.12,19 A primeira consiste em diminuir a densidade de carga dos íons brometo e reduzir a repulsao entre as moléculas de CTAB ligadas às faces nao-crescentes da semente, aprimorando a forma dos bastoes. A segunda funçao exercida pelos íons de prata é a limitaçao do tamanho dos bastoes. Isso ocorre devido à reduçao dos íons Ag+ a Ag0 que ocorre na presença de outros metais (como o ouro) e posterior deposiçao lenta nas faces em que houve alongamento, limitando o comprimento dos bastoes a aproximadamente 100 nm.14,41 Ao final das etapas da síntese os alunos observaram que a soluçao resultante apresentou uma coloraçao arroxeada, e desta soluçao foi separada uma alíquota para a análise espectroscópica na regiao UV-Vis-NIR (Figura 1A). Além disso, quando disponível, os alunos podem realizar imagem por microscopia eletrônica de transmissao (TEM) para visualizaçao do material sintetizado (Figura 1B). Previamente à realizaçao do experimento, os alunos nao consideravam a hipótese do ouro assumir diferentes cores. Os alunos responderam em questionário que o ouro certamente possui cor amarela, podendo assumir diferentes tonalidades apenas quando associado a outros metais. Nenhum aluno fazia ideia da maneira pela qual poderiam ser sintetizadas nanopartículas de ouro em laboratório e ficaram satisfeitos com o resultado e aprendizado, principalmente com a variedade de cores que as nanopartículas metálicas podem assumir. Dessa forma, esse experimento possibilitou a discussao dos conceitos de ressonância plasmônica de superfície e confinamento quântico, responsáveis, respectivamente, pela origem e variedade de cores das nanopartículas em funçao do tamanho.32
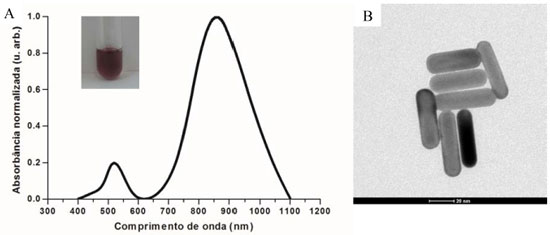 Figura 1. A: Espectro de absorçao na regiao do ultravioleta-visível-infravermelho próximo (UV-Vis-NIR), com picos de absorçao plasmônica transversal (520 nm) e longitudinal (863 nm). Inserçao: aspecto visual da soluçao de nanobastoes de ouro. B: Imagem de microscopia eletrônica de transmissao (TEM) representativa de um resultado de síntese através do protocolo aqui descrito
Montagem do biosensor Os anticorpos anti-IL-6 foram acoplados aos nanobastoes de ouro por intermédio do reagente polietilenoimina (PEI), que se liga eletrostaticamente à superfície do ouro. Tal etapa é de suma importância para que ocorra a ligaçao covalente de um dos grupos amina (-NH2) expostos no PEI com o grupo carboxila (-COOH) presente na porçao C-terminal do anticorpo. As imunoglobulinas da classe G (IgG) sao constituídas de duas cadeias pesadas, unidas entre si por pontes dissulfeto, e duas cadeias leves, unidas às cadeias pesadas também por pontes dissulfeto (Figura 2). Quando digeridas pela enzima papaína, as IgGs sao separadas em uma regiao constante (Fc), que determina as funçoes efetoras do anticorpo, e duas regioes variáveis (Fab), responsáveis pela especificidade de ligaçao para cada antígeno.42 Durante a ligaçao ao reagente PEI, essas regioes devem permanecer livres para permitir o posterior acesso do antígeno. Por esse motivo, a ligaçao é estabelecida com os grupos carboxila das cadeias pesadas das IgGs, localizadas na extremidade da porçao Fc.
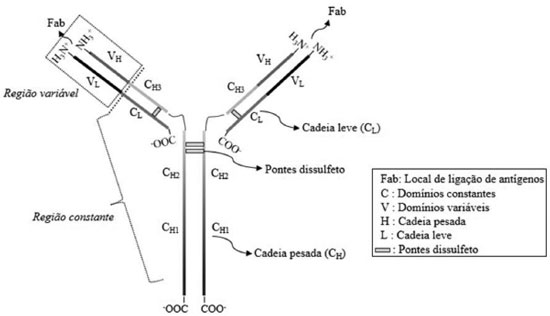 Figura 2. Estrutura tridimensional básica de um anticorpo. Cada cadeia pesada (H) e leve (L) possui uma regiao variável (V) e uma regiao constante (C). As duas cadeias pesadas sao unidas entre si e entre uma cadeia leve por pontes dissulfeto. A porçao C-terminal contendo grupos carboxila está localizada na regiao constante das cadeias pesadas e a porçao N-terminal contendo grupos amina situa-se na regiao variável que engloba ambas as cadeias leves e pesadas
A ligaçao amida do grupo carboxila presente na porçao C-terminal do anticorpo com os grupos amina do PEI é obtida por meio de uma reaçao de acoplamento ("crosslinking"), realizada com o emprego de um agente acoplante (N-etil-N'-(3-dimetil-aminopropil) carbodiimida - EDAC) e um agente estabilizante (N-hidroxisuccinimida - NHS). Ambos reagentes servem como ativadores do grupo carboxila. A despeito do uso isolado do EDAC já resultar em um composto com a capacidade de formar uma ligaçao amida, a reaçao entre esse composto e o NHS forma um éster com menor probabilidade de sofrer hidrólise, aumentando a probabilidade da reaçao entre o C-terminal ativado e a amina primária do PEI. As reaçoes ocorridas em cada etapa sao mostradas na Figura 3. Além disso, a Figura 4 resume as principais etapas de síntese e funcionalizaçao dos nanobastoes de ouro, necessárias para a construçao do biosensor no desenvolvimento da aula prática.
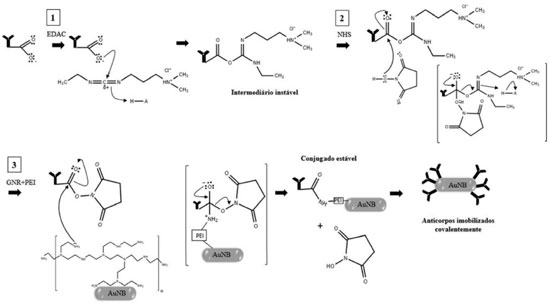 Figura 3. Esquema de reaçao de "crosslinking" entre PEI e o anticorpo anti-IL-6 empregando EDAC e NHS. 1: Reaçao de adiçao eletrofílica do EDAC ao anticorpo. 2: Substituiçao nucleofílica do EDAC por NHS, formando um éster de NHS. 3: Reaçao entre o anticorpo contendo o éster de NHS e a amina primária do PEI para formaçao da ligaçao amida. AuNB: Nanobastoes de ouro
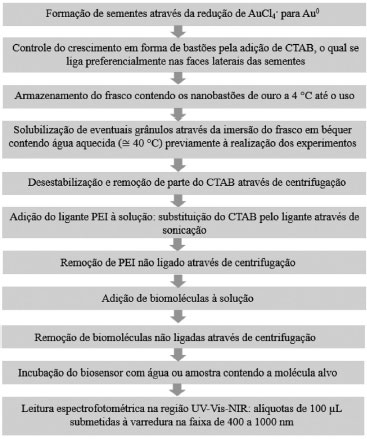 Figura 4. Principais etapas de síntese e funcionalizaçao de nanobastoes de ouro para desenvolvimento da aula prática utilizando biosensor
A ligaçao de moléculas na superfície dos nanobastoes altera o ambiente circundante e afeta a densidade de cargas dos elétrons ali presentes, acarretando em um deslocamento da banda de absorçao longitudinal.5 Dessa forma, após adiçao do reagente polietilenoimina (PEI) à soluçao contendo nanobastoes de ouro, pôde ser observado um deslocamento de 62 nm para a esquerda (blue-shift), comprovando a ligaçao. O blue-shift do pico de absorçao plasmônica longitudinal indica que houve uma diminuiçao da constante dielétrica no meio circundante. Em seguida, verificou-se a efetiva ligaçao do anticorpo anti-IL-6 ao PEI, sendo observado um deslocamento de 29 nm para a direita (red-shift), devido ao aumento do índice de refraçao do ambiente circundante. Ambos os deslocamentos podem ser facilmente visualizados na Figura 5, comprovando a ligaçao do linker PEI (linha tracejada) e o posterior acoplamento do anticorpo anti-IL6 (linha pontilhada).
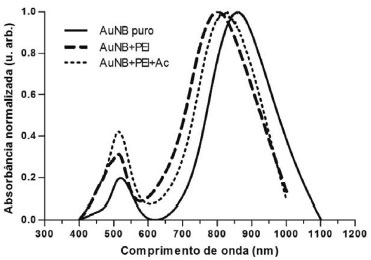 Figura 5. Espectros de absorçao óptica da funcionalizaçao de nanobastoes de ouro (AuNBs). Espectro resultante de AuNBs puros com pico máximo de absorçao plasmônica longitudinal de 863 nm em linha contínua; ligaçao de PEI (0,3%) aos AuNBs com pico máximo de absorçao plasmônica longitudinal de 801 nm em linha tracejada e; ligaçao de 0,4 µg mL-1 de anticorpo anti-IL-6 com pico máximo de absorçao plasmônica longitudinal de 830 nm em linha pontilhada
Posteriormente, considerando que a proteína modelo albumina sérica bovina (BSA) possui capacidade de se adsorver facilmente à superfície de nanopartículas de ouro43, os nanobiosensores foram incubados com BSA (62 µg mL-1) para permitir o bloqueio de possíveis sítios dos nanobastoes que nao tenham sido ocupados. Nesta reaçao, houve um deslocamento de apenas 4 nm para a esquerda, em relaçao à banda de absorçao plasmônica longitudinal de nanobastoes já ligados ao PEI e aos anticorpos (Figura 6). Esse deslocamento nao é significativo no que concerne ao efeito de biosensoriamento, mas sugere que o BSA tenha sido adsorvido aos locais nos quais o reagente PEI nao havia se ligado. Além disso, após novas adiçoes de BSA, nao ocorre deslocamento, o que corrobora a hipótese do completo bloqueio. A ocupaçao de possíveis sítios remanescentes impede posteriores ligaçoes inespecíficas na superfície dos nanobastoes, que poderiam ocasionar resultados falsos na etapa do biosensoriamento. Dessa forma, a finalizaçao de tais etapas resultam na completa funcionalizaçao dos nanobastoes de ouro, que podem ser, a partir de entao, considerados nanobiosensores.
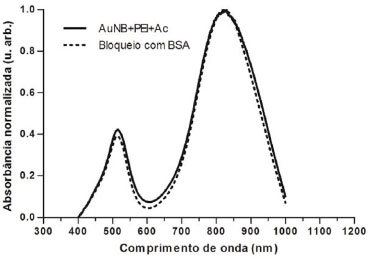 Figura 6. Espectros de absorçao óptica do bloqueio de nanobastoes de ouro com a proteína albumina bovina sérica (BSA). Espectro resultante de nanobastoes puros ligados ao PEI (0,3%) e à 0,4 µg mL-1 de anticorpo anti-IL-6 com pico máximo de absorçao plasmônica longitudinal de 830 nm em linha contínua e; ligaçao de 62 µg mL-1 de BSA aos nanobastoes com pico máximo de absorçao plasmônica longitudinal de 826 nm em linha tracejada
Detecçao nanosonda-alvo Após a etapa de preparo da nanosonda, a superfície dos nanobastoes encontra-se recoberta por anticorpos ligados e os sítios livres bloqueados com BSA. Dessa forma, o nanosensor encontra-se apropriado para os eventos de interaçao com o antígeno alvo. Portanto, a soluçao de nanobastoes de ouro foi incubada com o antígeno específico IL-6 (100 pg mL-1) e sua interaçao efetiva com o anticorpo resultou em deslocamento significativo de 25 nm para a direita, como pode ser visualizado na Figura 7.
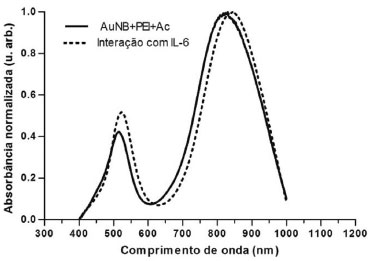 Figura 7. Espectros de absorçao óptica do biosensoriamento de AuNBs. Espectro resultante do nanobiosensor com pico máximo de absorçao plasmônica longitudinal de 826 nm em linha contínua e; ligaçao de 100 pg mL-1 de IL-6 aos AuNBs com pico máximo de absorçao plasmônica longitudinal de 851 nm em linha tracejada
A visualizaçao desse deslocamento na banda de absorçao plasmônica longitudinal finaliza o experimento, comprovando de maneira simples uma interaçao sonda-alvo. Além de verificar a ligaçao de moléculas/biomoléculas na superfície dos nanobastoes por meio do deslocamento do comprimento de onda da banda de absorçao plasmônica longitudinal, existem outras maneiras que confirmam o biosensoriamento. Dessa forma, todas as reaçoes de troca de ligantes ou detecçao de analitos podem ser avaliadas também pelo pico Raman das biomoléculas (especialmente das ligaçoes Au-S em cerca de 260 cm-1), pela estabilidade dos bioconjugados em soluçao tamponada ou ainda através de espectroscopia no infravermelho por transformada de Fourier (FTIR). As ligaçoes químicas possuem modos vibracionais com assinaturas em comprimentos de onda específicos, e, dessa forma, as ligaçoes envolvidas nas interaçoes PEI-nanobastao e biosensor-antígeno podem ser comprovadas por meio da técnica de FTIR.44,45 Além disso, as interaçoes podem também ser analisadas através de alteraçoes do potencial zeta, o qual pode ser medido e avaliado em suspensoes coloidais.14 O potencial zeta, ou potencial eletrocinético, é uma propriedade física exibida por qualquer partícula em suspensao, muito empregado na otimizaçao de formulaçoes de suspensoes e emulsoes, auxiliando também na prediçao da estabilidade a longo prazo.46 Dessa forma, o potencial zeta constitui uma medida tanto da estabilidade quanto da ligaçao de moléculas nas partículas, uma vez que os valores mais negativos ou positivos estao associados com soluçoes mais estáveis, já que a repulsao entre as nanopartículas reduz a agregaçao das mesmas.47 Após confirmaçao da interaçao sonda-alvo, visualizada através do deslocamento do pico de absorçao plasmônica longitudinal por meio da espectroscopia na regiao UV-Vis-NIR, foi realizada leitura do potencial zeta. Devido à simplicidade de execuçao, o potencial zeta pode ser empregado, quando disponível, de maneira complementar para aprimorar a análise pelos estudantes e introduzir os conceitos básicos dessa técnica. Ressaltamos que a realizaçao de uma aula prática somente com a visualizaçao espectroscópica do deslocamento da banda de absorçao plasmônica longitudinal é suficiente para que os alunos comtemplem a interaçao nanosonda-alvo. Os nanobastoes de ouro sao sintetizados com CTAB, uma molécula carregada positivamente que confere estabilidade. Após a ligaçao de outras moléculas na superfície das nanopartículas, parte deste CTAB é retirada e, entao, a medida do potencial zeta deve ser reduzida. Isso acontece uma vez que a soluçao perde parte da estabilidade oferecida pelo CTAB. No caso de moléculas carregadas positivamente o valor do potencial zeta continua positivo, e em caso contrário, o valor se torna negativo.48 Portanto, quando o PEI é misturado aos nanobastoes de ouro carregados positivamente, a carga líquida é diminuída. Da mesma forma, a cada nova ligaçao efetiva, a carga tende a diminuir, se negativando de maneira dependente da carga dos ligantes. Em todos os casos o valor do potencial zeta deve ser diferente de zero, garantindo a estabilidade. A Figura 8 mostra as leituras obtidas, em que houve uma diminuiçao dos valores em mV para os controles (AuNB+PEI+Ac; AuNB+Bloqueio com BSA), em relaçao à soluçao pura de nanobastoes de ouro (AuNB). Na leitura após adiçao de BSA (124 µg mL-1), um alvo inespecífico, os valores de potencial zeta foram equiparados àqueles encontrados para o nanosensor, enquanto na presença de IL-6 o valor em mV se tornou negativo, com diferença estatística significativa em relaçao à nanosonda, comprovando sua detecçao.
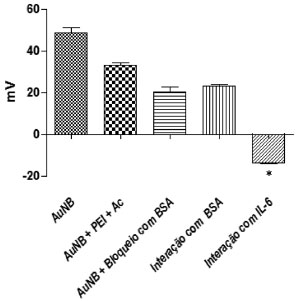 Figura 8. Potencial Zeta (mV) para as diferentes condiçoes de preparo e detecçao do nanobiosensor. *intensidade em mV significativamente diferente em relaçao ao nanobastao funcionalizado ao anticorpo anti-IL-6 (p ≤ 0,05). n = 10
A análise do potencial zeta complementa a avaliaçao da interaçao nanosonda-alvo e fornece uma indicaçao da estabilidade do sistema coloidal, sendo útil para a introduçao desse conceito aos estudantes. Se todas as nanopartículas em suspensao possuem valores altos de potencial zeta negativo ou positivo, elas tenderao a se repelir umas às outras e nao haverá tendência para que as nanopartículas se unam. No entanto, se as nanopartículas apresentam baixos valores de potencial zeta, nao haverá força para evitar que elas se agreguem.46 No caso do experimento de biosensoriamento, os alunos puderam verificar, através das leituras de potencial zeta, que houve ligaçao efetiva em cada etapa, sempre mantendo a estabilidade do sistema. Ao término dos experimentos, os alunos responderam um questionário a respeito da experiência adquirida e suas perspectivas futuras para o emprego da nanotecnologia (Quadro 1). No âmbito da vida profissional, todos os alunos vislumbraram aplicabilidade das nanopartículas de ouro em suas pesquisas de iniciaçao científica, e se sentiram entusiasmados quanto à isso. Alguns exemplos incluíram novas formas de diagnóstico, detecçao de substâncias no meio ambiente e direcionamento de drogas. De maneira geral, os alunos participantes do curso demonstraram vago conhecimento em relaçao ao tema e afirmaram que o curso lhes proporcionou um aprofundamento conceitual na área da nanotecnologia, com o qual foi possível uma melhor compreensao de todas as etapas da abordagem prática na síntese dos nanobastoes de ouro.

As respostas do questionário aplicado foram satisfatórias e mostraram que a aula prática realizada desempenhou um impacto positivo na vida acadêmica dos participantes, uma vez que adquiriram o conhecimento multidisciplinar das diversas aplicaçoes da nanotecnologia. Todos os participantes avaliaram o material didático como adequado e suficiente (apostila contendo o roteiro prático e os conceitos descritos nesse trabalho). Além disso, todos os alunos consideram que a introduçao de aulas práticas envolvendo nanopartículas de ouro é de relevante importância para a formaçao profissional nos cursos de pós-graduaçao nas áreas de química e/ou biotecnologia. Na esfera educacional, é fundamental que a interaçao dos alunos com o ambiente da pesquisa seja cada vez mais incentivada, com a aplicaçao prática do conhecimento teórico desenvolvido em sala. Isso demostra a conveniência dessa aula prática para a revisao de conceitos de química e bioquímica, sendo viável sua utilizaçao em cursos de pós-graduaçao, nos quais os estudantes já sao capazes de aplicar esses conceitos interdisciplinares para seu desenvolvimento técnico-científico. Consideramos que, uma vez seguidas as diretrizes contidas nesse trabalho, a utilizaçao de nanobastoes de ouro para aplicaçao em aulas práticas de nanotecnologia em maior escala será bem sucedida. Em vista disso, a síntese dos nanobastoes de ouro, a posterior confecçao do nanobiosensor, a comprovaçao da detecçao do alvo específico por espectroscopia UV-Vis-NIR e a análise complementar do potencial zeta foram etapas realizadas satisfatoriamente e se mostraram capazes de estimular ainda mais o interesse dos alunos pela nanotecnologia.
CONCLUSAO A proposta de uma aula prática envolvendo nanobastoes de ouro foi desenvolvida com êxito e os alunos demostraram interesse em se aprofundar nos diversos conceitos da nanotecnologia. A funcionalizaçao dos nanobastoes de ouro com polietilenoimina e anticorpos, e posterior detecçao de IL-6, foi realizada por um grupo de quatro graduandos sob supervisao de um aluno da pós-graduaçao. A partir dos ensaios realizados e dos resultados alcançados, sugerimos que o biosensor proposto pode ser utilizado para o estabelecimento de uma ou duas aulas práticas, uma vez que é simples e multidisciplinar, abrangendo conhecimentos de física, biologia e principalmente química. Devido à dificuldade média no entendimento da prática, ela é proposta para alunos de pós-graduaçao, sendo factível e gerando muitos retornos para a formaçao do estudante. Essa abordagem contribui ainda para a divulgaçao da nanotecnologia e, consequentemente, para o avanço tecnológico e valorizaçao da pesquisa nesta área. Por fim, poderá expandir horizontes aos estudantes, transmitindo novas perspectivas de pesquisas e campos de trabalho.
AGRADECIMENTOS Aos alunos participantes do III Curso de Verao em Biotecnologia da UFOP, que participaram da aula prática em nanotecnologia e auxiliaram na obtençao dos resultados. Ao Laboratório de Nanomateriais do Departamento de Física da Universidade Federal de Minas Gerais e ao Laboratório Multiusuários da Escola de Farmácia da Universidade Federal de Ouro Preto. As instituiçoes de fomento FAPEMIG (projeto FAPEMIG CDS - APQ 01510-14), CAPES e CNPq.
REFERENCIAS 1. Hullmann, A.; Scientometrics 2007, 70, 739. 2. Hussein, A. K.; Renewable Sustainable Energy Rev. 2015, 42, 460. 3. Fangueiro, J. F.; Silva, A. M.; Garcia, M. L.; Souto, E. B.; Eur. J. Pharm. Biopharm. 2015, 95, 307. 4. Perret, G.; Ginet, P.; Tarhan, M. C.; Baccouche, A.; Lacornerie, T.; Kumemura, M.; Jalabert, L.; Solid-State Electron. 2016, 115, 66. 5. Daniel, M.-C.; Astruc, D.; Chem. Rev. 2004, 104, 293. 6. Pissuwan, D.; Valenzuela, S.; Cortie, M. B.; Biotechnol. Genet. Eng. Rev. 2008, 25, 93. 7. Wilson, R.; Chem. Soc. Rev. 2008, 37, 2028. 8. Jensen, T. R.; Malinsky, M. D.; Haynes, C. L.; VanDuyne, R. P.; J. Phys. Chem. B 2000, 104, 10549. 9. Santos, J. F. L.; Santos, M. J. L.; Thesing, A.; Tavares, F.; Griep, J.; Rodrigues, M. R. F.; Quim. Nova 2016, 39, 1098. 10. Faraday, M.; Phil. Trans. R. Soc. London 1857, 147, 145. 11. Turkevich, J.; Stevenson, P. C.; Hillier, J.; Anal. Chem. 1951, 55, 475. 12. Vigderman, L.; Khanal, B. P.; Zubarev, E. R.; Adv. Mater. 2012, 24, 4811. 13. Nikoobakht, B.; El-sayed, M. A.; Chem. Mater. 2003, 15, 1957. 14. Huang, X.; Neretina, S.; El-Sayed, M. A.; Adv. Mater. 2009, 21, 4880. 15. Huang, X.; El-Sayed, M. A.; J. Adv. Res. 2010, 1, 13. 16. El-Sayed, S. L. and M. A.; J. Phys. Chem. B 1999, 103, 8410. 17. Jain, P. K.; Huang, X.; El-Sayed, I. H.; El-Sayed, M. A.; Acc. Chem. Res. 2008, 41, 1578. 18. Chang, S.-S.; Lee, C.-L.; Wang, C. R. C.; J. Phys. Chem. B 1997, 101, 6661. 19. Yang, D.-P.; Cui, D.-X.; Chem. Asian J. 2008, 3, 2010. 20. Hwang, S.-Y.; Tao, A. R.; Pure Appl. Chem. 2011, 83, 233. 21. Wang, W.; Wei, Q.-Q.; Wang, J.; Wang, B.-C.; Zhang, S.-H.; Yuan, Z.; J. Colloid Interface Sci. 2013, 404, 223. 22. Hu, C.; Dou, W.; Zhao, G.; Electrochim. Acta 2014, 117, 239. 23. Wangoo, N.; Bhasin, K. K.; Mehta, S. K.; Suri, C. R.; J. Colloid Interface Sci. 2008, 323, 247. 24. Adabo, A. H.; Zeggari, R.; Said, N. M.; Bazzi, R.; Elie-caille, C.; Marquette, C.; Martini, M.; Tillement, O.; Perriat, P.; Chaix, C.; Boireau, W.; Roux, S.; J. Colloid Interface Sci. 2016, 467, 271. 25. Nietzold, C.; Lisdat, F.; Analyst 2012, 137, 2821. 26. Chen, S.; Zhao, Q.; Zhang, L.; Wang, L.; Zeng, Y.; Huang, H.; Sens. Actuators, B 2015, 221, 1391. 27. Mattoussi, H.; Mauro, J. M.; Goldman, E. R.; Anderson, G. P.; Sundar, V. C.; Mikulec, F. V; Bawendi, M. G.; J. Am. Chem. Soc. 2000, 122, 12142. 28. Pyshnaya, I. a.; Razum, K. V.; Poletaeva, J. E.; Pyshnyi, D. V.; Zenkova, M. a.; Ryabchikova, E. I.; Biomed Res. Int. 2014, 2014, 1. 29. Ma, Y.; Jiang, L.; Mei, Y.; Song, R.; Tian, D.; Huang, H.; Analyst 2013, 138, 5338. 30. Tiwari, P.; Vig, K.; Dennis, V.; Singh, S.; Nanomaterials 2011, 1, 31. 31. Vaz, R.; Vieira, K. O.; Machado, C. E.; Ferrari, J. L.; Schiavon, M. A.; Quim. Nova 2015, 38, 1366. 32. Junior, M. A. M.; Santos, L. S. S.; Gonçalves, M. do C.; Nogueira, A. F.; Quim. Nova 2012, 35, 1872. 33. Silva, A. G. M.; Rodrigues, T. S.; Macedo, A.; Silva, R. T. P.; Camargo, P. H. C.; Quim. Nova 2014, 37, 1716. 34. Quadros, C. C.; Brunelli, M. F.; Faria, V. W.; Scheeren, C. W.; Quim. Nova 2016, 39, 1015. 35. Hirano, T.; Int. Rev. Immunol. 1998, 16, 249. 36. Rincon, M.; Trends Immunol. 2012, 33, 571. 37. Xu, X.; Zhao, Y.; Xue, X.; Huo, S.; Chen, F.; Zou, G.; Liang, X.-J.; J. Mater. Chem. A 2014, 2, 3528. 38. Zapp, E.; Westphal, E.; Gallardo, H.; de Souza, B.; Cruz Vieira, I.; Biosens. Bioelectron. 2014, 59, 127. 39. Pérez-Juste, J.; Liz-Marzán, L. M.; Carnie, S.; Chan, D. Y. C.; Mulvaney, P.; Adv. Funct. Mater. 2004, 14, 571. 40. Murphy, C. J.; Sau, T. K.; Gole, A. M.; Orendorff, C. J.; Gao, J.; Gou, L.; Hunyadi, S.E.; Li, T.; J. Phys. Chem. B 2005, 109, 13857. 41. Alkilany, A. M.; Thompson, L. B.; Boulos, S. P.; Sisco, P.N.; Murphy, C. J.; Adv. Drug. Deliv. Rev. 2012, 64, 190. 42. Abbas, A.; Lichtman, A.; Pillai, S.; Cellular and molecular immunology, 8th ed., Elsevier: Philadelphia, 2014. 43. Boulos, S. P.; Davis, T. A.; Yang, J. A.; Lohse, S. E.; Alkilany, A. M.; Holland, L. A.; Murphy, C. J.; Langmuir 2013, 29, 14984. 44. Vonnemann, J.; Beziere, N.; Böttcher, C.; Riese, S.B.; Kuehne, C.; Dernedde, J.; Licha, K.; von Schacky, C.; Kosanke, Y.; Kimm, M.; Meier, R.; Ntziachristos, V.; Haag, R.; Theranostics 2014, 4, 629. 45. Zhu, H.; Chen, Y.; Yan, F-J.; Chen, J.; Tao, X-F.; Ling, J.; Yang, B.; He, Q-J.; Mao, Z-W.; Acta Biomaterialia 2016, doi: 10.1016/j.actbio.2016.12.050. 46. Hunter, R. In Zeta potential in colloid science: principles and applications; Ottewilla, R. H., Rowell, R. L., eds.; Academic Press: London, 1981. 47. Chumakova, O. V.; Liopo, A. V.; Andreev, V. G.; Cicenaite, I.; Evers, B. M.; Chakrabarty, S.; Pappas, T. C.; Esenaliev, R. O.; Cancer Lett. 2008, 261, 215. 48. Liopo, A.; Conjusteau, A.; Tsyboulski, D.; Ermolinsky, B.; Kazansky, A.; Oraevsky, A.; J. Nanomed. Nanotechnol. 2012, S2, 1. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access





