Artigo
|
|
| Determinação rápida e simples de Citrato de Sildenafila (Viagra® e genéricos) empregando eletrodo impresso de carbono em sistemas fia e bia com detecção amperométrica Fast and simple determination of Sildenafil Citrate (Viagra® and generics) using carbon screen-printed electrode in fia and bia systems with amperometric detection |
|
Rafael S. Backes1; Tiago J. Guedes2; Wallans T. P. dos Santos*,2,3; Rodrigo A. B. da Silva*,4
1. Faculdade de Ciências Exatas e Tecnológicas, Universidade Federal da Grande Dourados, 79804-970 Dourados - MS, Brasil Recebido em 13/12/2016 *e-mail: wallanst@yahoo.com.br; rabsilva@ufu.br This work presents two amperometric methods for Sildenafil Citrate (SC) determination in erectile dysfunction drugs (Viagrar and Generics), using Batch Injection Analysis (BIA) and Flow Injection Analysis (FIA) systems with a cell for Screen Printed Electrodes (SPE). In Britton- Robinson buffer solution (pH 2), the SC presented an irreversible anodic peak at around +1.0 V vs. Ag pseudo-reference electrode, using five different working electrodes of commercial SPE. The carbon SPE (unmodified) was selected as the best working electrode, providing good sensitivity, precision and low-cost. The SC amperometric detection for two proposed methods was performed at +1.1 V. The best conditions for SC determination by hydrodynamic systems were obtained through injection volumes of 50 and 150 µL at flow rates of 100 and 75 µL s-1, for BIA and FIA respectively. In these conditions, BIA system showed the best sensitivity (0.188 µA mol-1 L) and theoretical analytical frequency (360 h-1) for SC determination. The repeatability studies were similar for both systems with relative standard deviation of approximately 3.0%. The SC analyses in pharmaceutical samples obtained by two proposed methods were compared to HPLC-UV method. INTRODUÇAO O citrato de sildenafila (CS) é o princípio ativo do Viagrar (Pfizer), cujo medicamento é o mais usado no mundo para o tratamento da disfunçao erétil masculina. No organismo, o CS inibe a enzima fosfodiesterase tipo 5 (PHD5), causando o aumento na circulaçao sanguínea e o relaxamento muscular peniano.1 Após expirar a patente do Viagrar no Brasil em 2010, vários laboratórios passaram a produzir medicamentos genéricos e similares com CS, além de suas formulaçoes manipuladas pelas farmácias magistrais. Apesar da reduçao do custo dos medicamentos em virtude desta concorrência, a aquisiçao de formulaçoes falsificadas e contrabandeadas no mercado negro é um problema recorrente no Brasil, com predominância para o medicamento Pramil fabricado no Paraguai.2 Até o presente momento, nao há nenhum método analítico oficial descrito pela Farmacopeia Brasileira ou pelos compêndios internacionais para o controle de qualidade de formulaçoes de CS. Na literatura sao reportados vários trabalhos para análise de CS em amostras farmacêuticas por métodos cromatográficos, principalmente, por Cromatografia Líquida de Alta Eficiência (HPLC, High Performance Liquid Chromatography).3-8 Apesar da robustez desses métodos na determinaçao de SC em amostras farmacêuticas, o custo elevado das análises e o maior tempo requerido nestes protocolos sao inconvenientes para um controle de qualidade de rotina nas indústrias farmacêuticas. Além disso, esses métodos cromatográficos utilizam solventes orgânicos na composiçao da fase móvel, gerando grandes quantidades de resíduos tóxicos. Neste sentido, na literatura sao descritos outros métodos que buscam contornar esses problemas para determinaçao de CS em medicamentos, como por exemplo, utilizando a eletroforese capilar9, espectrofotometria UV-VIS,10-15 dispersao de Rayleigh16 e, em destaque, o eletroanalítico devido à sua alta sensibilidade, seletividade e baixo custo de instrumentaçao.17-28 Dentre esses métodos eletroanalíticos para a determinaçao de CS, as técnicas voltamétricas de pulso diferencial e onda quadrada sao as mais aplicadas usando diversos eletrodos de trabalho, como por exemplo: gota pendente de mercúrio,17 filme de bismuto,18 filme de chumbo,19 carbono vítreo,20, 21 pasta de diamante,22 pasta de carbono modificada,23 carbono vítreo modificado com óxido de grafeno,24 diamante dopado com boro (BDD, Boron-Doped Diamond)25 e eletrodos impressos (SPE, Screen- Printed Electrode).26, 27 Apesar do sucesso destes métodos, a maioria dos eletrodos sólidos utilizados nesses trabalhos está sujeita à passivaçao (envenenamento) devido à adsorçao de espécies na superfície desses materiais. Na prática, este problema pode ser corrigido mediante o polimento e tratamento eletroquímico entre as medidas ou substituiçao do eletrodo após cada análise, como no caso dos eletrodos descartáveis. Outra alternativa para diminuir a adsorçao das espécies consiste em reduzir o tempo de contato entre o analito e a superfície do eletrodo de trabalho. Esta possibilidade pode ser alcançada utilizando sistemas hidrodinâmicos, como na Análise por Injeçao em Fluxo (FIA, Flow Injection Analysis) ou Análise por Injeçao em Batelada (BIA, Batch Injection Analysis). Nesses sistemas a técnica de detecçao eletroquímica mais utilizada é a amperometria. Neste contexto, o CS foi determinado em formulaçoes farmacêuticas por Lopes et al.28 empregando um eletrodo de BDD em sistema FIA com detecçao amperométrica de múltiplos pulsos. Vários outros fármacos também foram determinados por FIA ou BIA com detecçao amperométrica, mostrando o grande potencial de aplicaçao desses métodos hidrodinâmicos.29, 30 O sistema FIA é uma técnica que foi proposta em 1975 por Ruzicka e Hansen, na qual a soluçao contendo o analito é injetada durante o percurso de um fluxo com uma soluçao carregadora, que é movida por um sistema propulsor até o detector. 31 Já na técnica BIA, proposta em 1991 por Wang e Taha, um injetor introduz a soluçao do analito diretamente sobre a superfície de um detector, que está localizado em um recipiente (célula BIA) contendo uma soluçao inerte estacionária ou sob convecçao (na presença de agitaçao magnética ou mecânica).32 De acordo com a literatura, ambos os sistemas apresentam similaridade na proposta de análises realizadas continuamente e com menor intervençao do analista, apresentando picos transientes com alta frequência analítica, precisao e baixo consumo de amostras e reagentes. Embora o sistema BIA pode ser mais prático e portátil, o sistema FIA é mais versátil, uma vez que permite a adiçao de etapas no percurso antes da detecçao do analito, como o tratamento da amostra, processo de separaçao, reaçoes e/ou aquecimento.30 Dessa forma, como FIA e BIA oferecem vantagens para aplicaçao de métodos analíticos, faz-se necessário uma avaliaçao de qual sistema é o mais adequado para cada analito. No cenário atual, os SPE descartáveis têm sido bastante utilizados para a eletroanálise de vários fármacos, incluindo CS.26, 27 Em uma recente revisao de Couto et al.33 é destacado o uso de SPE para a determinaçao individual e simultânea de aproximadamente cinquenta fármacos em medicamentos e matrizes biológicas. De modo geral, o uso destes SPE é atraente, pois sao dispositivos práticos e portáteis que permitem realizar medidas em apenas uma gota de soluçao. Além disso, os SPE evitam a tediosa etapa de polimento do eletrodo (tal como ocorre em outros eletrodos sólidos), pois caso ocorra a passivaçao da superfície do seu eletrodo de trabalho, um novo SPE pode ser utilizado. Todavia, devido ao custo relativamente alto dos SPE (sobretudo os comerciais), a sua substituiçao após um limitado número de medidas pode tornar o seu uso inviável em análises de rotina. Como já mencionado, pode-se reduzir a passivaçao do eletrodo e aumentar a vida útil desses dispositivos acoplando o SPE em células eletroquímicas de análise por injeçao em fluxo (FIA-SPE) ou em batelada (BIA-SPE). O primeiro trabalho empregando FIA-SPE foi publicado em 1998, no qual os autores utilizaram reatores enzimáticos em linha com o SPE para determinar o frescor de peixes.34 O trabalho pioneiro utilizando BIA-SPE é mais recente (2014), no qual foi proposto um sistema inteiramente portátil, adequado para análises em campo de modo prático, robusto e reprodutível.35 Após este trabalho, o mesmo grupo de pesquisa produziu, em parceria com uma empresa, uma versao comercial do sistema BIA-SPE.36 Atualmente, esses sistemas de detecçao sao comercializados em kits para a montagem dos sistemas FIA-SPE (célula, potenciostato portátil, bomba peristáltica, tubulaçoes e injetor) e BIA-SPE (célula, potenciostato portátil e pipeta eletrônica).37 De modo alternativo, células eletroquímicas hidrodinâmicas para SPE de custo muito menor podem ser confeccionadas em laboratório com o uso de microrretífica,38 tornearia35 ou impressao 3D.39 Apesar da praticidade e rapidez destes sistemas hidrodinâmicos com SPE, existem poucos trabalhos na literatura para determinaçao de fármacos em medicamentos por FIA-SPE40-43 e BIA-SPE.43 Dessa forma, este trabalho propoe a determinaçao de CS empregando SPE em sistemas BIA e FIA com detecçao amperométrica, sendo avaliados cinco SPE de diferentes eletrodos de trabalho. A potencialidade e comparaçao do desempenho desses dois sistemas (BIA-SPE e FIA-SPE) para determinaçao de CS em formulaçoes farmacêuticas foram avaliadas em funçao dos parâmetros analíticos.
PARTE EXPERIMENTAL Reagentes e soluçoes Todos os reagentes foram de grau analítico. O padrao de citrato de sildenafila (CS) foi obtido da Sigma-Aldrichr. As soluçoes foram preparadas com água deionizada obtida do sistema de purificaçao GEHAKA OS10LXE (resistividade > 18,2 MΩ cm). O tampao Britton-Robinson (TBR) 0,040 mol L-1 foi preparado com ácido acético, ácido bórico e ácido fosfórico, todos da Dinâmica (Sao Paulo, Brasil) e o ajuste do pH desejado foi realizado com soluçao de hidróxido de sódio (Vetec) e/ou ácido clorídrico, ambos a 0,2 mol L-1. O CS foi quantificado nos medicamentos da marca referência, Viagra (Pfizerr), e de quatro formulaçoes genéricas (Eurofarmar, EMSr, Medleyr e Neo Químicar), todas com dosagem rotulada de 50 mg. Os comprimidos farmacêuticos foram adquiridos em drogarias da cidade de Dourados-MS. As soluçoes estoque de CS foram preparadas em balao volumétrico, dissolvendo uma massa adequada do padrao de CS em água deionizada com auxílio de banho ultrassônico por 10 minutos. O mesmo procedimento foi adotado na preparaçao dos medicamentos de CS, porém o pó foi obtido triturando-se 20 comprimidos de cada medicamento (do mesmo lote). As soluçoes injetadas nos sistemas BIA e FIA foram preparadas no início do dia de trabalho, diluindo-se apropriadamente a soluçao estoque do padrao (ou amostra) no eletrólito suporte. Nas análises cromatográficas as soluçoes estoque de CS foram preparadas e diluídas em metanol (grau HPLC), sendo estas injetadas neste sistema após uma filtraçao. Medidas Eletroquímicas As medidas eletroquímicas foram realizadas com potenciostato portátil Dropsensr µStat400 interfaceado a um computador contendo o software Dropview8400r. A voltametria foi utilizada nos estudos do comportamento eletroquímico em diferentes eletrodos de trabalho e eletrólitos. A amperometria foi utilizada para detecçao e determinaçao de CS nos sistemas hidrodinâmicos BIA e FIA. Para a detecçao de CS foram utilizados os SPE comerciais da Dropsensr.37 Esses dispositivos contém os três eletrodos no mesmo substrato de cerâmica, sendo o eletrodo auxiliar de grafite e o eletrodo de pseudo-referência (EPR) de prata. Foram avaliados cinco SPE por voltametria, cada um contendo um eletrodo de trabalho distinto, sendo constituídos de: Carbono (grafite) nao modificado (SPE-C); Carbono modificado com nanotubos de parede simples (SPE-SWCNT), nanotubos de parede múltipla (SPE-MWCNT), Grafeno (SPE-Gr) e Polianilina (SPE-PA). A área geométrica de todos os eletrodos de trabalho foi de 0,13 cm² (r = 2 mm). Nas medidas voltamétricas estacionárias, o SPE foi inserido em um béquer de 10 mL contendo o eletrólito suporte. Nas medidas amperométricas hidrodinâmicas, o melhor SPE selecionado para determinaçao de CS foi acomodado na mesma célula eletroquímica construída no laboratório e adaptada ora para o sistema BIA, ora para o sistema FIA. Sistemas BIA-SPE e FIA-SPE Na Fig. 1 é apresentado um esquema da célula eletroquímica hidrodinâmica, de configuraçao do tipo Wall Jet, que foi usada para os sistemas BIA-SPE e FIA-SPE. Nesta célula, o SPE é colocado em um orifício na parte inferior, contendo um anel cilíndrico de borracha (o-ring) por cima dos seus eletrodos, sendo este conjunto (SPE com o-ring) fixado por uma chapa rígida com dois parafusos. A tampa contém um orifício concêntrico ao eletrodo de trabalho do SPE, que é adequado para posicionar uma ponteira (Combitipr) de 1,0 mL da pipeta eletrônica. Assim, a extremidade inferior da Combitip possui distância sempre fixa de aproximadamente 2 mm da saída da soluçao até a superfície do eletrodo de trabalho no SPE, como já reportado.30 Esta célula com SPE é usada tanto em BIA quanto em FIA, porém cada sistema possui seus componentes específicos. Em BIA a injeçao dos padroes e amostras é realizada por um injetor manual ou eletrônico (mais reprodutível), sendo que neste trabalho as soluçoes de CS foram injetadas por uma pipeta eletrônica Eppendorfr Multipette Stream. No sistema BIA, após a injeçao da soluçao, a diluiçao do analito no eletrólito é acelerada por meio da convecçao do eletrólito suporte.32 Neste trabalho foi utilizado um agitador mecânico construído no próprio laboratório, o qual foi colocado na parte superior da célula ao lado do orifício da ponteira (detalhe em azul na Fig 1). No sistema FIA é necessário uma bomba peristáltica para transportar a soluçao do eletrólito no interior de tubos de polipropileno em direçao ao SPE, sendo as soluçoes do analito inseridas no percurso por um injetor manual (ou automático). O sistema FIA utilizado neste trabalho foi de linha única e composto basicamente por tubos de polietileno de 1,0 mm de diâmetro interno, bomba peristáltica (Gilsonr, modelo Minipuls 3) e um injetor manual comutador. Para manter a mesma distância da injeçao no sistema BIA, a parte final do tubo de polietileno usado em FIA é inserida dentro da Combitip (detalhe em vermelho na Fig 1), com a soluçao saindo exatamente na extremidade inferior desta ponteira. Deste modo, a distância entre a extremidade inferior da ponteira e o SPE, bem como o diâmetro do jato de soluçao sao sempre muito próximos em ambos os sistemas (FIA e BIA), garantindo uma comparaçao de resultados mais adequada.
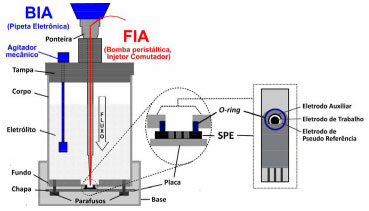 Figura 1. Esquema com os principais componentes da célula eletroquímica Wall Jet para os sistemas: BIA-SPE com suas partes específicas (em azul) do agitador mecânico e da base de encaixe da pipeta eletrônica; e FIA-SPE com as suas partes específicas (em vermelho) do tubo de polietileno inserido dentro da ponteira, cuja soluçao é bombeada por uma bomba peristáltica e a injeçao realizada por um injetor manual. Em destaque a regiao ampliada do encaixe do SPE na célula e de cada eletrodo no SPE.
A célula eletroquímica construída possui disposiçao semelhante ao primeiro sistema BIA-SPE proposto e dispensa o uso de suporte,35 permitindo o fácil posicionamento em bancadas de laboratório ou em qualquer superfície horizontal. Além disso, o material do corpo da célula é de policloreto de vinila (PVC), um polímero com alta resistência mecânica e química. Imagens e outros detalhes desta célula para os sistemas BIA e FIA podem ser consultadas no material suplementar. Análises por Cromatografia Líquida de Alta Eficiência (HPLC) Os medicamentos contendo CS foram também analisados por HPLC para a comparaçao dos métodos propostos. Os experimentos foram realizados em um cromatógrafo líquido da Shimadzu (Modelo Prominence LC 20 AD) com detector no UV com arranjo de diodos (SPD-M20A), injetor automático (SIL-10AF), bomba de pistao LC-6Adx3 e coluna C18 Shim-Pack XROD de 15 mm de comprimento e 2 mm de diâmetro interno, com temperatura controlada (forno CTO-20A) em 40 ºC. Os experimentos por HPLC foram conduzidos no modo isocrático com fase móvel contendo 100 % de metanol. Deste modo, o CS apresentou um tempo de retençao de 2,16 min e foi quantificado nas cinco amostras farmacêuticas em 290 nm. As condiçoes cromatográficas foram adaptadas de um trabalho prévio para a análise de CS.28 Os resultados obtidos por FIA-SPE e BIA-SPE para o doseamento, em triplicata, do CS nos cinco medicamentos foram comparados com HPLC-UV aplicando os testes estáticos t e F, ambos com nível de confiança de 95%.
RESULTADOS E DISCUSSAO O comportamento eletroquímico do CS foi avaliado sob SPE-C por voltametria cíclica em meio de soluçoes tampao Britton-Robinson (TBR) 0,04 mol L-1 em pH de 2 a 10. Os resultados sao apresentados na Figura 2, sendo possível observar processos de oxidaçao irreversíveis para CS, cujos potenciais de pico se tornam menos positivos com o incremento de pH. No voltamograma do pH 2 (Figura 2), o CS apresentou apenas um processo de oxidaçao nítido em torno de 1,1 V, porém de pH 4 a 7 foram observados dois processos de oxidaçao, os quais a partir de pH 8 foram tornando-se menos perceptíveis nos voltamogramas. Estes resultados corroboram com o perfil de CS observado em eletrodos de Carbono Vítreo20 e BDD,25, 28 Na literatura, um mecanismo sugerido é de que o primeiro processo anódico é correspondente à oxidaçao do anel piperazínico da molécula de sildenafila e o segundo é devido à adsorçao/dessorçao do produto gerado no primeiro.20 Para o SPE-C nao foi observado o segundo pico anódico em pH 2, provavelmente devido à sobreposiçao dos dois picos neste valor de pH. Como a corrente de pico de oxidaçao para o CS foi mais sensível em pH 2 no TBR 0,04 mol L-1, este eletrólito foi escolhido nas medidas subsequentes. Apesar do deslocamento dos potenciais de pico do CS em valores mais altos de pH proporcionarem uma melhor seletividade para detecçao deste analito, esses pHs nao foram escolhidos pelo fato destes medicamentos nao apresentarem interferentes para detecçao eletroquímica nesta faixa de potencial.
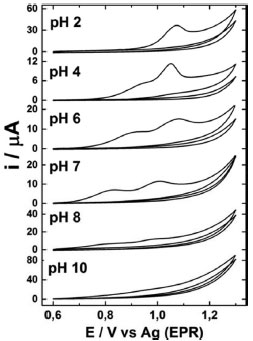 Figura 2. Voltamogramas cíclicos obtidos sob SPE-C em meio de TBR 0,04 mol L-1 (pH de 2 a 10) sem e com a adiçao de CS 75 µmol L-1. Velocidade de varredura: 50 mV s-1
Diferentes tipos de eletrodos impressos foram avaliados para detecçao de CS em funçao da melhor sensibilidade e repetibilidade das respostas eletroquímica. Este estudo foi realizado para dez medidas sucessivas de soluçao de CS 5,0 µmol L-1 em cada SPE por voltametria de onda quadrada. Os parâmetros da técnica (frequência, amplitude e incremento de potencial) foram otimizados adotando como critério a melhor sensibilidade para detecçao do CS. Na Fig. 3A é apresentado o primeiro voltamograma obtido para cada eletrodo impresso avaliado: Carbono nao modificado (SPE-C) e modificado com nanotubo de parede simples (SPE-SWCNT), nanotubo de parede múltipla (SPE-MWCNT), Grafeno (SPE-Gr) e Polianilina (SPE-PA). Com exceçao do SPE-Gr que apresentou o maior potencial de pico anódico (Epa) para a oxidaçao de sildenafila, os demais SPE proporcionaram um Epa semelhante para este composto, em aproximadamente +1,05 V. Deste modo, os SPE modificados nao promoveram nenhum efeito catalítico para o CS. Na Fig. 3A, observa-se também que a corrente de fundo obtida no SPE-Gr (> 200 µA) foi muito superior em relaçao aos outros SPE. Este comportamento do SPE-Gr pode ser justificado pelo ordenamento tridimensional do grafeno, o qual é responsável por controlar a capacitância do eletrodo. De acordo com a literatura, 44 em muitos casos as unidades de grafeno estao irregularmente empilhadas devido às aglomeraçoes nao controladas durante a síntese ou uso deste eletrodo, podendo haver um aumento da corrente capacitiva. Além disso, a fragilidade da superfície do SPE-Grafeno da Dropsensr foi observada pelo constante desprendimento de grafeno do eletrodo de trabalho, antes e durante as análises, o que provoca ainda mais variaçoes na área eletroquimicamente ativa deste eletrodo e, consequentemente, pode ter aumentado a sua corrente capacitiva.
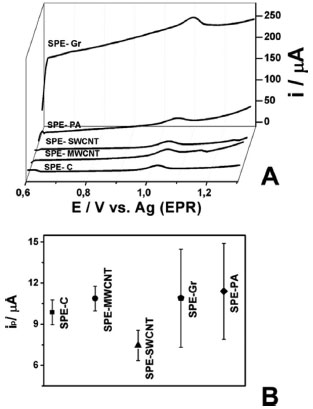 Figura 3. (A) Voltamogramas de onda quadrada da primeira varredura ob tidos em soluçao de CS 5,0 µmol L-1 nos distintos SPE: C, MWCNT, SWCNT, Gr e PA; (B) Correntes de pico médias (± DP) obtidas para dez varreduras sucessivas de CS em cada SPE. Eletrólito: TBR 0,04 mol L-1 pH 2; Frequência: 20 Hz; Amplitude: 25 mV, Incremento de Potencial: 3 mV
Na Figura 3B sao apresentados os valores de correntes de pico médias (± DP) de dez voltamogramas de onda quadrada sucessivos para cada SPE. Nesta Figura 3B é possível observar, com exceçao do SPE-SWCNT, que os eletrodos modificados apresentaram correntes de pico (ipa) levemente superiores ao eletrodo nao modificado (SPE-C). Entretanto, a repetibilidade desses sinais nos 10 voltamogamas para detecçao do CS foi muito baixa para o SPE-Gr e SPE-PA, com desvio padrao relativo (DPR) próximo a 30 % nesses eletrodos. Os sensores que apresentaram maior precisao foram SPE-C e SPE-MWCNT (DPR ≈ 9 % para ambos), sendo a ipa média apenas de 10 % menor para o SPE-C. Deste modo, o eletrodo impresso de carbono nao modificado (SPE-C) foi escolhido para as medidas amperométricas nos sistemas BIA e FIA, uma vez que este dispositivo apresenta um custo de aquisiçao em torno de 60 % mais baixo do que o SPE-MWCNT. Para a investigaçao da resposta eletroquímica da sildenafila nos sistemas hidrodinâmicos com detecçao amperométrica, uma soluçao de CS 5,0 µmol L-1 foi injetada em triplicata na célula BIA preenchida com soluçao TBR 0,04 mol L-1 pH 2. A detecçao amperométrica foi realizada aplicando um potencial constante no SPE-C em funçao do tempo, sendo avaliados os potenciais aplicados de 0,0 V até + 1,2 V (vs. EPR). O voltamograma hidrodinâmico apresentado na Figura 4 foi construído a partir dos valores médios (± DP) das correntes de pico anódicas em cada potencial aplicado. Na Figura 4 pode ser observado que o início da oxidaçao do CS na superfície do SPE-C ocorre a partir de + 0,9 V e alcança um valor máximo em + 1,2 V. Este comportamento corrobora com o observado por voltametria cíclica no mesmo eletrólito (Figura 2). Embora a maior corrente de pico anódica (ipa) ter sido obtida em + 1,2 V, neste potencial a corrente de fundo (linha de base) foi mais intensa e instável, provavelmente, devido à descarga da água na superfície do SPE-C. Assim, o CS foi detectado no potencial de + 1,1 V no SPE-C nos estudos seguintes para os sistemas BIA e FIA.
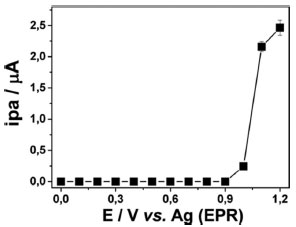 Figura 4. Voltamogramas hidrodinâmicos obtidos plotando as correntes de pico médias (± DP) para três injeçoes da soluçao de CS 5,0 µmol L-1 no sistema BIA com detecçao amperométrica em potenciais distintos. Eletrólito: TBR 0,04 mol L-1 pH 2; Volume injetado: 100 µL; Vazao: 134 µL s-1
Os parâmetros de injeçao (volume e a vazao) nos sistemas BIA e FIA foram investigados para obter as melhores respostas analíticas em funçao da sensibilidade e frequência analítica. Os estudos foram realizados injetando uma soluçao de CS 5,0 µmol L-1, em triplicada, sob cada condiçao de modo univariado, ou seja, variando o volume injetado sob uma vazao fixa e, posteriormente, variando a vazao sob um volume fixo. No estudo do volume injetado no sistema BIA, a pipeta eletrônica (Eppendorfr) acoplada na ponteira de 1,0 mL permitiu a injeçao de volumes no intervalo de 10 a 1000 µL. As correntes médias (± DP) para três injeçoes deste estudo sao apresentadas na Fig. 5A (BIA). Neste estudo observa-se que quando sao injetados volumes de 10 a 100 µL a corrente de pico é diretamente proporcional ao volume injetado na soluçao. No entanto, acima de 100 µL estes sinais sao praticamente constantes e os desvios sao maiores, provavelmente, devido à maior passivaçao da superfície do eletrodo de trabalho. Além disso, a frequência analítica é menor em volumes mais altos de injeçao, obtendo-se picos mais largos. Deste modo, o volume de 50 µL foi escolhido para a injeçao no sistema BIA. Já no sistema FIA, a magnitude do volume injetado no percurso da soluçao carregadora (eletrólito suporte) depende da alça de amostragem ("looping") que é utilizada no injetor comutador. Como também apresentado na Fig. 5A (FIA), as alturas de correntes sao diretamente proporcionais aos volumes injetados em todo o intervalo avaliado (75 até 250 µL), sendo a corrente máxima obtida no volume de 250 µL. Este comportamento é observado no FIA devido à dispersao longitudinal do CS no eletrólito durante o percurso analítico (distância do injetor até o SPE). Em outras palavras, a concentraçao no centro do volume injetado é menor quando alcança o SPE em relaçao à concentraçao inicial no injetor. Esse efeito só é eliminado em grandes volumes de injeçao, pois as alturas das correntes passam a permanecer constante com aumento do volume injetado. No entanto, alças de amostragem acima de 250 µL nao foram avaliadas devido à diminuiçao da frequência analítica e possibilidade de maior contaminaçao da superfície do eletrodo de trabalho. Dessa forma, a escolha da alça de amostragem foi baseada na maior precisao da resposta eletroquímica no sistema FIA-SPE, sendo escolhido o volume injetado de 150 µL para os experimentos posteriores.
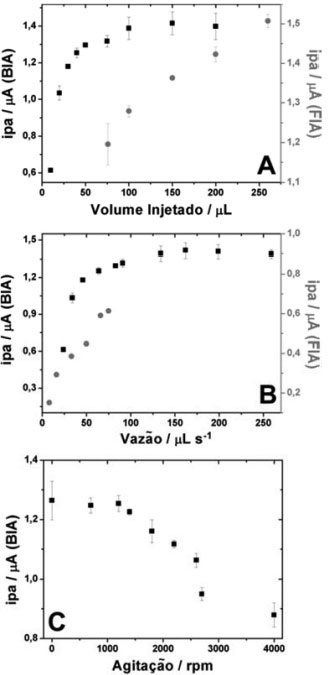 Figura 5. Correntes de pico médias e respectivos desvios (ipa ± DP) para três injeçoes de soluçao de CS 5,0 µmol L-1 nos sistemas BIA e FIA em SPE-C, variando os volumes injetados em (A), vazoes em (B) e agitaçao mecânica do eletrólito em BIA em (C). Condiçoes fixadas em: (A) Vazao de 134 µL s-1 (BIA) e 66 µL s-1 (FIA); (B) Volume injetado de 50 µL (BIA) e 75 µL (FIA); (C) Volume de 50 µL e Vazao de 100 µL s-1. Eletrólito: TBR 0,04 mol L-1 pH 2; Potencial: + 1,1 V (vs. EPR)
No sistema BIA, a pipeta eletrônica usada neste trabalho permite a injeçao das soluçoes sob dez vazoes diferentes (24 a 250 µL s-1 na ponteira de 1,0 mL). As correntes de pico médias das triplicatas (± DP) em cada vazao sao apresentadas na Fig. 5B (BIA), sendo os sinais diretamente proporcionais às velocidades de injeçao devido à diminuiçao da camada de difusao de Nernst. No entanto, no sistema BIA a precisao da coleta dos sinais de corrente foi reduzida em vazoes acima de 150 µL s-1. Esse fenômeno pode ocorrer devido à velocidade de aquisiçao do sinal nao ser suficiente para coletar as correntes do analito que sao registradas no pico (patamar de corrente), uma vez que nessas condiçoes o composto eletroativo pode passar muito rápido pela superfície do eletrodo. Assim, a vazao de 100 µL s-1 foi usada nas próximas injeçoes para o sistema BIA. No sistema FIA, a bomba peristáltica usada neste trabalho permitiu vazoes de 8 a 75 µL s-1 com os tubos utilizados (diâmetro interno de 1,0 mm). Como mostrado na Fig. 5B (FIA) entre o intervalo avaliado de 8 a 75 µL s-1, a maior corrente de pico foi obtida na maior vazao do sistema. No caso do sistema FIA, como o volume injetado ainda tem um efeito de dispersao, a altura da corrente pode ser aumentada em vazoes altas devido ao menor tempo disponível para a diluiçao da soluçao de CS na soluçao carregadora, reduzindo a dispersao no centro da zona de amostra. Além disso, há o aumento da corrente de pico devido à diminuiçao da camada de difusao de Nernst com incremento da vazao. Deste modo, as determinaçoes de CS por FIA foram realizadas na vazao máxima de 75 µL s-1. O último parâmetro investigado, apenas para o sistema BIA, foi em relaçao à agitaçao mecânica do eletrólito no interior da célula. Neste estudo, soluçoes de CS 5,0 µmol L-1 foram injetadas, em triplicata, mantendo a vazao e o volume constantes sem agitaçao. Na sequência, o agitador foi ligado na rotaçao inicial de 700 rpm e novas injeçoes da mesma soluçao, em triplicata, foram realizadas. Deste modo, prosseguiu-se o experimento realizando novo incremento na rotaçao seguido de novas triplicatas até o nível máximo de agitaçao (4000 rpm). O nível de agitaçao é proporcional à tensao aplicada pela fonte universal do motor DC (de 3 a 12 V) utilizado no sistema BIA. Como mostrado na Fig. 5C, agitaçoes até 1500 rpm aumentam a precisao das medidas em relaçao à medida sem agitaçao. Além disso, a velocidade de análise na presença de agitaçao foi bastante superior do que na ausência de agitaçao (duraçao de um pico ≈ 10 s com agitaçao a 700 rpm vs. 40 s sem agitaçao). Empiricamente, este aumento da velocidade é percebido pelo decaimento mais rápido do pico, que pode ser justificado pela remoçao acelerada das espécies eletroativas próximas à superfície do eletrodo de trabalho em funçao da convecçao gerada pelo motor DC.32 Entretanto, uma convecçao acima de 1500 rpm causa grande diminuiçao na precisao e na corrente de pico, pois a convecçao excessiva provoca uma turbulência na soluçao da célula, podendo remover parte da zona da soluçao de CS antes mesmo de sua total detecçao no eletrodo de trabalho. Outro ponto importante da agitaçao é diminuir a contaminaçao do eletrodo de trabalho devido ao menor tempo de contato direto do analito com o sensor após a detecçao.43 Assim, as determinaçoes de CS foram realizadas com uma agitaçao branda, a 700 rpm. Após a otimizaçao das condiçoes nos sistemas hidrodinâmicos com detecçao amperométrica, soluçoes de concentraçoes crescentes do padrao de CS foram injetadas em triplicata nos sistemas BIA e FIA. Deste modo, foi possível obter alguns parâmetros de confiabilidade analítica, como sensibilidade, faixa linear e limite de detecçao (LD). Na sequência deste estudo, soluçoes diluídas dos cinco medicamentos foram injetadas em triplicata, sendo o CS quantificado em cada formulaçao por meio da interpolaçao das respectivas correntes de pico nas curvas analíticas de calibraçao (externa), as quais foram obtidas pelos amperogramas dos sistemas BIA-SPE e FIA-SPE. Na Figura 6 sao apresentados os amperogramas para ambos os experimentos e as respectivas curvas de calibraçao. A partir destes resultados, foram calculadas as seguintes equaçoes de reta: i(µA) = 0,188 [CS] (µmol L-1) - 0,0131 (R = 0,998) para o sistema BIA; e i(µA) = 0,108 [CS] (µmol L-1) + 0,0462 (R = 0,999) para o sistema FIA. Os LD estimados foram de 0,0520 µmol L-1 (BIA) e 0,215 µmol L-1 (FIA). As faixas lineares apresentadas em ambos os métodos foram estreitas (de 3,00 a 21,0 µmol L-1 para o sistema BIA e de 2,50 a 20,0 µmol L-1 para FIA), sendo essas semelhantes às faixas observadas de outros trabalhos para a detecçao de CS em eletrodos impressos,26, 27 carbono vítreo21 e BDD.25 Todos estes parâmetros analíticos sao apresentados na Tabela 1.
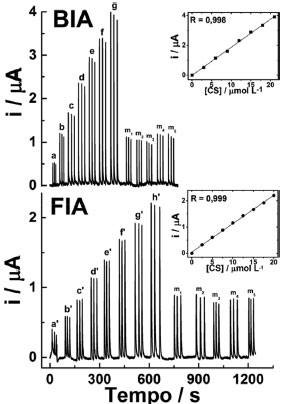 Figura 6. Injeçoes em triplicata de soluçao padrao de CS no sistema BIA (3,0 - 21,0 µmol L-1, a - g) e sistema FIA (2,5 - 20 µmol L-1, a' - h'), bem como das soluçoes diluídas das cinco amostras de medicamentos de CS (m1 a m5) em ambos os sistemas. As inserçoes representam as respectivas cur vas de calibraçao de cada sistema. Volume injetado: 50 µL (BIA) e 150 µΛ (ΦIA); vazao: 100 µL s-1 (BIA) e 75 µL s-1 (FIA); eletrólito: TBR 0,04 mol L-1 pH 2; potencial aplicado: + 1,10 V (vs. EPR); agitaçao mecânica da célula BIA: 700 rpm.
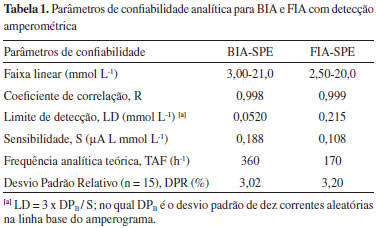
Para estimar a precisao e a frequência analítica teórica (TAF, theoretical analytical frequency), foram realizadas três injeçoes alternadas de soluçao de CS a 2,0 µmol L-1 e 15,0 µmol L-1 nos sistemas BIA e FIA. Como apresentado nos amperogramas da Figura 7, nota-se que os DPR das correntes de pico para as injeçoes de CS 2,0 µmol L-1 sao próximos tanto para o sistema BIA (DPR = 3,61 %; n = 15), quanto para o sistema FIA (DPR = 3,76 %; n = 15). O mesmo comportamento ocorreu nos DPR paras as correntes de picos referentes à soluçao de CS 15,0 µmol L-1 calculados em 3,02 e 3,20 % (n = 15) para os sistemas BIA e FIA, respectivamente. Estes resultados indicam que a passivaçao (e/ou contaminaçao) do SPE-C é mínima quando estes eletrodos sao acoplados aos sistemas BIA e FIA. Cabe destacar que a repetibilidade obtida para SPE-C pela voltametria de onda quadrada em estado estacionário (Fig. 2B) foi muito baixa para 10 medidas de CS 5,0 µmol L-1 (DPR = 9,0 %). Essa diferença entre os DPRs obtidos para os métodos hidrodinâmicos propostos e a voltametria estacionária demonstra a grande potencialidade dos sistemas FIA e BIA para aumentar a estabilidade da detecçao eletroquímica.
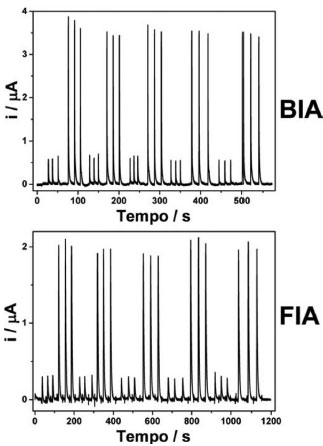 Figura 7. Amperogramas obtidos para injeçoes em triplicatas e alternadas nos sistemas BIA e FIA de soluçao de CS de 2,0, e 15,0 mmol L-1. Condiçoes de cada sistema idem a Figura 6.
Os valores das TAF foram calculados obtendo a média das larguras de pico das injeçoes de CS 15 mmol L-1 (Figura 7), estimando o número de injeçoes por hora para cada sistema. Nos dois casos, as TAF foram calculadas considerando que as injeçoes sao realizadas em sequência, desprezando o tempo para preencher a pipeta no sistema BIA e a alça de amostragem no sistema FIA. Os valores das TAF estao apresentados na Tabela 1. Na Tabela 1 também pode ser comparado o desempenho das duas formas de injeçao (BIA e FIA) com detecçao amperométrica em funçao dos parâmetros analíticos apresentados para determinaçao de CS. Nesta Tabela observa-se que o sistema BIA foi o mais sensível, provavelmente, devido às maiores vazoes permitidas pela pipeta eletrônica em relaçao à bomba peristáltica utilizada neste trabalho para o sistema FIA, bem como da menor dispersao do pacote da soluçao injetada em BIA.30 O fato da maior vazao proporcionada pela pipeta eletrônica também explica a maior frequência analítica obtida no sistema BIA. A estabilidade do sinal eletroquímico de ambos os sistemas foi semelhante para soluçoes concentradas e diluídas de CS (DPR ≈ 3 %), mostrando que cada SPE-C pode ser reutilizado para várias medidas de CS. Na literatura apenas duas publicaçoes comparam o desempenho entre BIA e FIA com detecçao amperométrica para um mesmo analito. Ferreira et al. determinaram o ciclopirox em eletrodo de carbono vítreo, 45 obtendo valores de TAF de 735 h-1 e 330 h-1 com sensibilidades de 0,091 e 0,022 (µA mmol-1 L) para os sistemas BIA e FIA, respectivamente. Stefano et al.43 empregaram um SPE modificado na eletroanálise de ciprofloxacina e alcançaram valores de TAF de 450 h-1 e 180 h-1 com sensibilidades de 0,1115 e 0,0768 (µA mmol-1 L) para os sistemas BIA e FIA, respectivamente. Deste modo, tal como observado no presente trabalho, as comparaçoes na literatura entre os dois sistemas para a análise de outros compostos, empregando diferentes células e eletrodos, também exibiram uma maior sensibilidade e frequência analítica para o sistema BIA. Cabe destacar que, na Figura 7 é observado um nível de ruído maior na detecçao amperométrica em FIA, sendo o provável motivo que elevou o valor de LD para este sistema quando comparado ao obtido pelo BIA. O ruído apresentado em FIA pode ser justificado pela pulsaçao da bomba peristáltica utilizada neste trabalho, podendo este efeito ser minimizado pela utilizaçao de um amortecedor de pulso ou de um sistema de propulsao alternativo.46 A eficiência dos métodos desenvolvidos por BIA e FIA com detecçao amperométrica foi avaliada para a determinaçao de CS em cinco amostras de medicamentos comerciais (Viagrar e genéricos). Os doseamentos de CS obtidos nestas amostras tanto pelos métodos propostos quanto por HPLC-UV sao apresentados na Tabela 2.
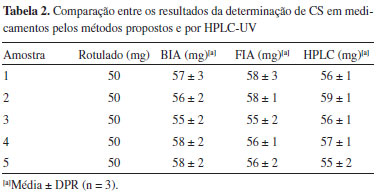
A precisao e exatidao dos resultados obtidos pelos dois métodos propostos para determinaçao de CS sao semelhantes aos apresentados por HPLC-UV. No teste F, as razoes das variâncias do conjunto das análises por cada técnica proposta em relaçao com HPLC (F = Sproposto2/SHPLC 2) foram de 1,43 e 1,28 para BIA e FIA respectivamente, sendo estes valores inferiores ao Ftabelado em um nível de confiança de 95 % (F = 2,48; a = 14). No teste t pareado, o tcalculado foi de 1,38 e 0,82 para BIA e FIA respectivamente, sendo ambos inferiores ao ttabelado também a um nível de confiança de 95 % (2,15; a = 14). Deste modo, os resultados comprovam que nao há diferença significativa entre todos os dados obtidos. Assim, os resultados confirmam que os métodos de BIA e FIA com detecçao amperométrica possuem desempenho similar ao HPLC para as determinaçoes de CS em formulaçoes farmacêuticas. Comparando os parâmetros analíticos apresentados no presente trabalho (Tabela 1), foi observado que os limites de detecçao obtidos pelos métodos BIA-SPE e FIA-SPE foram superiores a vários outros trabalhos da literatura para a determinaçao de CS com detecçao eletroquímica.18,19,21-28 Entretanto, esta característica nao se trata de um inconveniente e nem resulta em prejuízos na análise, uma vez que os métodos BIA-SPE e FIA-SPE sao propostos apenas para a determinaçao de CS em amostras de formulaçoes farmacêuticas. Em contrapartida, os métodos hidrodinâmicos apresentados neste trabalho proporcionaram uma frequência analítica muito maior frente aos demais métodos reportados para determinaçao de CS, o que representa uma grande vantagem na aplicaçao em análises de rotina deste fármaco. Além disso, a praticidade dos sistemas BIA-SPE e FIA-SPE pode ser um grande atrativo destes métodos para aplicaçao no controle de qualidade do CS pela indústria farmacêutica.
CONCLUSAO Este trabalho demonstrou dois métodos simples e rápidos para a determinaçao de CS em formulaçoes farmacêuticas empregando eletrodos impressos de carbono (grafite) acoplados aos sistemas FIA e BIA com detecçao amperométrica. O sistema BIA proporcionou uma maior sensibilidade e frequência analítica com menor consumo de reagentes (eletrólito, padrao e amostra), além de oferecer um sistema mais simples e portátil para aplicaçao do método. Os dois métodos propostos para determinaçao de CS foram comparados com o método cromatográfico (HPLC-UV) e os resultados de doseamento do fármaco mostraram-se semelhantes. A praticidade e as elevadas frequências analíticas obtidas pelos sistemas FIA-SPE e BIA-SPE para determinaçao de CS em relaçao aos demais trabalhos descritos sao grandes atrativos para análises de rotina na indústria farmacêutica, abrindo uma perspectiva para que os sistemas propostos sejam empregados para outros fármacos eletroativos.
MATERIAL SUPLEMENTAR Maiores detalhes (imagens e especificaçoes) dos componentes dos sistemas BIA-SPE e FIA-SPE utilizados neste trabalho estao disponíveis em http://quimicanova.sbq.org.br, na forma de arquivo PDF, com acesso livre.
AGRADECIMENTOS Ao CNPq (475276/2013-2 e 481683/2013-5) e à FUNDECT-MS (23/200.498/2014) pelo suporte financeiro. Rafael S. Backes agradece à CAPES pela bolsa de mestrado concedida. Este trabalho é uma colaboraçao entre projetos de pesquisa de membros da Rede Mineira de Química (RQ-MG) apoiada pela FAPEMIG (Projeto: CEX-RED-00010-14).
REFERENCIAS 1. Terrett, N. K.; Bell, A. S.; Brown, D.; Ellis, P.; Bioorg. Med. Chem. Lett. 1996, 6, 1819. 2. Hurtado, R. L.; Lasmar, M. C.; Cad. Saúde Pública 2014, 30, 891. 3. Cooper, J. D. H.; Muirhead, D. C.; Taylor, J. E.; Baker, P. R.; J. Chromatogr. B: Biomed. Sci. Appl. 1997, 701, 87. 4. Dinesh, N. D.; Vishukumar, B. K.; Nagaraja, P.; Gowda, N. M. M.; Rangappa, K. S.; J. Pharm. Biomed. Anal. 2002, 29, 743. 5. Ortiz, R. S.; Antunes, M. V.; Linden, R.; Quim. Nova 2010, 33, 389. 6. Nickum, E. A.; Flurer, C. L.; J. Chromatogr. Sci. 2015, 53, 38. 7. Ghodsi, R.; Kobarfard, F.; Tabatabai, S. A.; Iran. J. Pharm. Res. 2012, 11, 123. 8. Fidan, A. K.; Bakirdere, S.; J. AOAC Int. 2016, 99, 923. 9. Vidal, D. T. R.; Augelli, M. A.; do Lago, C. L.; Anal. Methods 2013, 5, 2041. 10. Dinesh, N. D.; Nagaraja, P.; Gowda, N. M. M.; Rangappa, K. S.; Talanta 2002, 57, 757. 11. Amin, A. S.; Moustafa, M. E.; El-Dosoky, R. M. S.; J. AOAC Int. 2009, 92, 125. 12. Altiokka, G.; Atkosar, Z.; Sener, E.; Tuncel, M.; J. Pharm. Biomed. Anal. 2001, 25, 339. 13. Los Weinert, P.; Pezza, L.; Pezza, H. R.; Quim. Nova 2008, 31, 1112. 14. Issa, Y. M.; El-Hawary, W. F.; Youssef, A. F. A.; Senosy, A. R.; Spectrochim. Acta, Part A 2010, 75, 1297. 15. Harikrishna, K.; Nagaralli, B. S.; Seetharamappa, J.; J. Food Drug Anal. 2008, 16, 11. 16. Liu, S. P.; Fan, L.; Hu, X. L.; Liu, Z. F.; Li, S.; Anal. Sci. 2006, 22, 819. 17. Berzas, J. J.; Rodriguez, J.; Castaneda, G.; Villasenor, M. J.; Anal. Chim. Acta 2000, 417, 143. 18. Sopha, H.; Hocevar, S. B.; Pihlar, B.; Ogorevc, B.; Electrochim. Acta 2012, 60, 274. 19. Tyszczuk, K.; Korolczuk, M.; Bioelectrochemistry 2010, 78, 113. 20. Ozkan, S. A.; Uslu, B.; Zuman, P.; Anal. Chim. Acta 2004, 501, 227. 21. Baranowska, I.; Koper, M.; Markowski, P.; Chem. Anal. 2008, 53, 967. 22. Stefan-van Staden, R. I.; Van Staden, J. F.; Aboul-Enein, H. Y.; J. Solid State Electrochem. 2010, 14, 997. 23. Balasoiu, S. C.; Stefan-van Staden, R. I.; van Staden, J. F.; Ion, R. M.; Radu, G. L.; Aboul-Enein, H. Y.; Electrochim. Acta 2011, 58, 290. 24. Li, Y.; Wen, T. T.; Xue, C.; Han, Q.; Wang, Y.; Hong, J. L.; Zhou, X. M.; Jiang, H.; J. Biosens. Bioelectron. 2013, 42, 287. 25. Batista, E. F.; Sartori, E. R.; Medeiros, R. A.; Rocha, R. C.; Fatibello, O.; Anal. Lett. 2010, 43, 1046. 26. Farghali, R. A.; Ahmed, R. A.; Int. J. Electrochem. Sci. 2012, 7, 13008. 27. Farghali, R. A.; Ahmed, R. A.; Int. J. Electrochem. Sci. 2015, 10, 1494. 28. Lopes, A. C. V.; Luz, R. D. S.; Damos, F. S.; dos Santos, A. S.; Franco, D. L.; dos Santos, W. T. P.; J. Braz. Chem. Soc. 2012, 23, 1800. 29. Felix, F. S.; Angnes, L.; J. Pharm. Sci. 2010, 99, 4784. 30. Quintino, M. S. M.; Angnes, L.; Electroanalysis 2004, 16, 513. 31. Ruzicka, J.; Hansen, E. H.; Anal. Chim. Acta 1975, 78, 145. 32. Wang, J.; Taha, Z.; Anal.Chem. 1991, 63, 1053. 33. Couto, R. A. S.; Lima, J.; Quinaz, M. B.; Talanta 2016, 146, 801. 34. Carsol, M. A.; Mascini, M.; Talanta 1998, 47, 335. 35. Tormin, T. F.; Cunha, R. R.; da Silva, R. A. B.; Munoz, R. A. A.; Richter, E. M.; Sens. Actuators, B 2014, 202, 93. 36. Richter, E. M.; Tormin, T. F.; Cunha, R. R.; Silva, W. P.; Perez-Junquera, A.; Fanjul-Bolado, P.; Hernandez-Santos, D.; Munoz, R. A. A.; Electroanalysis 2016, 28, 1856. 37. http://www.dropsens.com/en/accesories_pag.html, acessada em 06/04/2017 38. Caramit, R. P.; Lucca, B. G.; Ferreira, V. S.; Munoz, R. A. A.; Richter, E. M.; da Silva, R. A. B.; Electroanalysis 2015, 27, 271. 39. Dias, A. A.; Cardoso, T. M. G.; Cardoso, R. M.; Duarte, L. C.; Munoz, R. A. A.; Richter, E. M.; Coltro, W. K. T.; Sens. Actuators, B 2016, 226, 196. 40. Bergamini, M. F.; Santos, A. L.; Stradiotto, N. R.; Zanoni, M. V. B.; J. Pharm. Biomed. Anal. 2007, 43, 315. 41. Fanjul-Bolado, P.; Lamas-Ardisana, P. J.; Hernandez-Santos, D.; Costa-Garcia, A.; Anal. Chim. Acta 2009, 638, 133. 42. Stefano, J. S.; Montes, R. H. O.; Richter, E. M.; Munoz, R. A. A.; J. Braz. Chem. Soc. 2014, 25, 484. 43. Stefano, J. S.; Cordeiro, D. S.; Marra, M. C.; Richter, E. M.; Munoz, R. A. A.; Electroanalysis 2016, 28, 350. 44. Ke, Q.; Wang, J.; J. Materiomics 2016, 2, 37. 45. Ferreira, L. M. C.; Felix, F. S.; Angnes, L.; Electroanalysis 2012, 24, 961. 46. Dos Santos, W. T. P.; Ceolin, M. P.; de Albuquerque, Y. D. T.; Richter, E. M.; Quim. Nova, 2007, 30, 1754. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access





