Artigo
|
|
| Inibição à corrosão de aço-carbono em meio salino pelo heterociclo isatina veiculado em microemulsões Efficiency of the heterocycle isatin loaded in microemulsions as corrosion inhibitor for mild steel in saline medium |
|
Adna Dornelles Nicácio de Souza1; Cátia Guaraciara Fernandes Teixeira Rossi1; Tereza Neuma de Castro Dantas1; Miguel Angelo Fonseca de Souza1; Djalan França de Lima1; Fabrício Gava Menezes1; Maria Aparecida Medeiros Maciel1,2,*,#
1. Instituto de Química, Universidade Federal do Rio Grande do Norte, Campus Universitário, Lagoa Nova, 59072-970 Natal - RN, Brasil Recebido em 18/12/2016 *e-mail: mammaciel@hotmail.com Polar microemulsion systems (SME) based on saponified coconut oil (OCS) as surfactant were prepared in order to increase the solubility of the heterocycle isatin (IST) aiming at its application as corrosion inhibitor against AISI 1020 mild steel, in saline medium. The adsorptions phenomena of the tested SME systems (SME-OCS1-IST and SME-OCS2-IST) in the liquid/gas interface were evaluated by surface tension measurements which do not show significant differences in the presence of ion Cl-. The free energy values of the micellization proved the occurrence of spontaneous process. The corrosion inhibition effectiveness of SME-OCS2, SME-OCS1-IST and SME-OCS2-IST samples was evaluated in 0.5% aqueous NaCl using voltammetry linear scan method (LPR). The maximum efficiency findings were 73.2% for SME-OCS2, 88.2% for SME-OCS2-IST and 97.6% for SME-OCS1-IST. The spontaneity of the adsorption phenomena was also observed in the liquid/metal interface by analyzes of the adsorption free energy. In addition, since computational calculations have been found as a very relevant tool in the corrosion field, a theoretical study was performed in attempt to give support to the observed experimental results, in which B3LYP and 6-311++G(d,p) were applied aiming at investigation of geometry, electronic density aspects, HOMO-LUMO energy gap, as well as the binding between isatin and metal surface. INTRODUÇAO A corrosao acarreta prejuízos financeiros e operacionais significativos, além de danos ambientais e riscos operacionais. Em funçao de causar deterioraçao de equipamentos e estruturas metálicas, o fenômeno da corrosao se destaca como um dos maiores problemas das indústrias da atualidade. O aço-carbono, em funçao de suas propriedades, simples fabricaçao e baixo custo, é um dos principais tipos de aço empregados na indústria, no entanto, a exemplo de outros materiais, está sujeito à corrosao por diversos meios. Por esta razao, a demanda, em todo o mundo, por agentes inibidores de corrosao se mostra altamente atrativa para o setor industrial.1-8 Várias pesquisas vêm sendo desenvolvidas no sentido de controlar a corrosao. Dentre os métodos mais utilizados, destaca-se o uso de inibidores de corrosao por açao de películas protetoras que se adsorvem às áreas anódicas e catódicas do metal, exercendo controle sobre os processos eletroquímicos que desencadeiam a corrosao. Em funçao da eficácia de filmes protetores que se formam na interface entre o metal e o meio corrosivo, destaca-se o uso de moléculas orgânicas contendo nitrogênio, oxigênio e enxofre.9-15 Esta proteçao está vinculada às interaçoes entre heteroátomos presentes em suas estruturas com a superfície do metal, cuja natureza e carga superficial também influenciam diretamente o processo de adsorçao. A isatina (IST) é um composto orgânico heterociclo quem vem sendo amplamente utilizado em pesquisas científicas. Citando apenas um exemplo, Pinto e colaboradores desenvolveram diversos estudos com este composto objetivando incentivar o uso industrial da isatina, tendo sido co-autor de uma extensa revisao acerca da química dos derivados de IST que resultou em uma publicaçao em que se destacam diversas metodologias de síntese e aplicaçoes em diversas áreas.16 A capacidade da IST na inibiçao à corrosao de metais (alumínio e aço carbono) danificados pela açao de meios ácidos se encontra reportada em três artigos científicos.17-19 O desenvolvimento de produtos capazes de inibir a corrosao proveniente de um meio rico em ânions cloreto, em especial oriundos do ambiente marinho, tem se mostrado uma promissora fonte de pesquisa para indústrias petrolíferas, especialmente por conta das maiores reservas de petróleo estarem localizadas no mar. Um dos principais fatores associados à aplicabilidade de um inibidor de corrosao em meio aquoso neutro ou salino consiste na problemática da solubilidade. Neste contexto, os sistemas coloidais do tipo microemulsao (SME), em decorrência da sua baixa tensao interfacial, baixo custo e facilidade de obtençao, surgem como um meio alternativo para a solubilizaçao e aplicaçoes diversificadas de moléculas orgânicas.20-24 Microemulsoes podem ser definidas como sistemas termodinamicamente estáveis, isotrópicos, opticamente transparentes, de baixa viscosidade, que se formam a partir de uma solubilizaçao espontânea de dois líquidos imiscíveis (água, óleo) na presença de um tensoativo e, se necessário, um cotensoativo.20-24 Com relaçao ao uso de microemulsao do tipo O/A (sistema polar rico em água), objetivando a disponibilizaçao de compostos orgânicos para aplicaçao na inibiçao à corrosao, encontram-se os formulados SME-OCS que contém óleo de coso saponificado (OCS) como tensoativo. Este sistema padrao veiculou satisfatoriamente tiosemicarbazonas e a difenilsemicarbazida que foram avaliadas em meio salino (0,5% de NaCl) como inibidores de corrosao de aço carbono AISI 1020, com eficiências entre 84% e 92%. O tensoativo semissintético OCS foi obtido a partir do óleo de coco, cuja escolha se justifica por ser uma fonte abundante subutilizada na regiao nordeste do Brasil, que tem baixo custo e é de fácil obtençao.23,24 No presente trabalho encontra-se relatada a açao anticorrosiva do heterociclo isatina (IST) veiculado em sistemas coloidais do tipo O/A (óleo em água) contendo o tensoativo biodegradável OCS. A técnica de voltametria de varredura linear (método LPR) em aço carbono AISI-1020, no meio corrosivo salino (0,5% de NaCl), bem como estudos de adsorçao na interfaces líquido/sólido e líquido/gás, foram utilizados para os sistemas SME-OCS2, SME-OCS1-IST e SME-OCS2-IST. Cálculos computacionais foram realizados objetivando a avaliaçao teórica do inibidor IST e seu mecanismo de açao na inibiçao à corrosao.
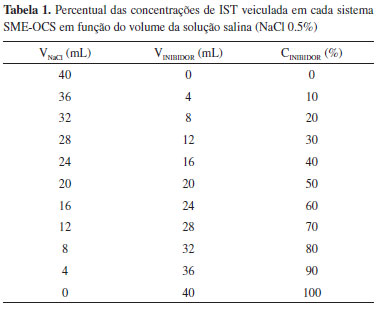
PARTE EXPERIMENTAL Obtençao do óleo de coco saponificado (OCS) O tensoativo OCS foi obtido a partir da saponificaçao do óleo de coco de acordo com metodologia previamente reportada.23 Uma soluçao contendo 20,89 g de NaOH dissolvidos em 80 mL de água destilada foi adicionada a 100 g de óleo de coco. A essa mistura foram adicionados 300 mL de álcool etílico e o sistema reacional foi mantido sob refluxo por 2 h. Após esse tempo, o álcool foi eliminado por rota evaporaçao, sendo o produto resultante seco a 40 °C. Os índices de acidez, de iodo e de saponificaçao do óleo de coco foram determinados de acordo com as metodologias apresentadas no Material Suplementar. Obtençao dos sistemas microemulsionados O sistema microemulsionado foi preparado com base na metodologia de titulaçoes e fraçoes mássicas em diagrama pseudoternário.23,24 Especificamente, utilizou-se óleo de coco saponificado (OCS) como tensoativo (T), butanol como cotensoativo (C), querosene como fase oleosa (FO) e água destilada (fase aquosa, FA). O procedimento utilizado para se obter a regiao de microemulsao baseia-se no método que envolve a determinaçao dos pontos de solubilidade máximas da matéria ativa (no caso, C/T na razao 1:1) nas fases FO e FA por meio de titulaçoes mássicas, para produzir sistema coloidal do tipo O/A (sistema rico em água). O sistema menos polar SME-OCS1 (20% de OCS, 20% de butanol, 5% de FO e 55% de FA), bem como o sistema SME-OCS2, de maior polaridade (12,5% de OCS, 12,5% de butanol, 5% de FO e 70% de FA), foram avaliados pela obtençao de diagramas pseudoternários, que possibilitaram estabelecer as composiçoes totais destes sistemas. A análise reológica e a medida de tensao superficial de cada sistema foram realizadas conforme descrito no Material Suplementar, estando de acordo com metodologia reportada. 23,24 Estudo da solubilizaçao da isatina (IST) nos sistemas microemulsionados SME-OCS As concentraçoes de IST incorporadas nos sistemas SME-OCS1 e SME-OCS2 foram determinadas via espectroscopia UV-Vis, no espectrômetro Genesys 10-UV/Vis, Thermo Electron Corporation. Os estudos foram realizados em uma faixa de comprimento de onda entre 200 nm - 400 nm, com quantificaçao de veiculaçao da IST através das absorbâncias em λ = 229 nm (SME-OCS1) e 217 nm (SME-OCS2). As absorbâncias destas microemulsoes e dos sistemas contendo IST (SME-OCS1-IST e SME-OCS2-IST) foram medidas após sucessivas diluiçoes em metanol. Todas as medidas foram realizadas em triplicata. Medidas de eficiência de inibiçao à corrosao As medidas de eficiência de inibiçao à corrosao dos sistemas isentos de IST (SME-OCS1 e SME-OCS2), bem como dos formulados SME-OCS1-IST e SME-OCS2-IST (sistemas contendo isatina), foram realizadas em meio aquoso salino (NaCl 0,5%) pela técnica de voltametria de varredura linear. Apenas para o sistema SME-OCS1 foi realizada, nesta mesma metodologia, avaliaçao preliminar.23 Os ensaios foram realizados em célula clássica de três eletrodos, com capacidade para 30 mL de soluçao, formada por um eletrodo de referência de Ag/AgCl (3,0 mol L-1 KCl), o contraeletrodo de grafite e o eletrodo de trabalho de aço carbono AISI-1020, com composiçao química 0,18% - 0,23% de carbono, 0,30% - 0,60% de manganês, 0,030% de fósforo, 0,050% de enxofre, 0,0005% - 0,003% de boro e 0,20% de cobre, com área superficial de 0,273 cm2, tendo sido polido até o espelhamento. Utilizou-se um potenciostato/galvanostato de modelo 302N da AUTOLAB PGSTAT para medidas de inibiçao à corrosao, à temperatura ambiente de 298 K. Os dados obtidos da análise de resistência polarizaçao linear (LPR) foram analisadas utilizando o software GPES da AUTOLAB, versao 4.9, obtendo-se as curvas de Tafel. Para obtençao das curvas de polarizaçao, o eletrodo de trabalho, os eletrodos de referência e contraeletrodo foram imersos em soluçao aquosa salina (NaCl 0,5) durante 15 minutos para estabelecer um potencial de circuito aberto de estado estacionário (Eocp). Após a mediçao (Eocp), potencial constante em torno de - 500 mV, as análises eletroquímicas (LPR) foram conduzidas a uma taxa de varredura de 1 mVs-1. Na sequência, os estudos de polarizaçao anódica e catódica foram conduzidos com variaçao do potencial de Eocp na faixa -500 mV a 500 mV. Nestas condiçoes experimentais, a concentraçao do inibidor variou de acordo com os valores mostrados na Tabela 1.
Os segmentos lineares anódicos e catódicos das curvas de Tafel foram extrapolados no ponto de interseçao, de acordo com os dados de potencial de corrosao (Ecorr) e de densidade de corrente de corrosao (icorr). As eficiências de inibiçao, em diferentes concentraçoes de inibidor, foram calculadas utilizando a Equaçao 1. 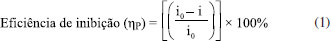 em que "i" é a densidade de corrente para as amostras analisadas, e "io" é a densidade de corrente da amostra contendo apenas NaCl (branco). Estudo computacional Os parâmetros estruturais e eletrônicos para a IST foram obtidos em fase gasosa utilizando o Programa Gaussian,25 através do método B3LYP,26 combinado com o conjunto de bases 6-311++G(d,p). As cargas atômicas foram calculadas de acordo com o método Chelpg.27 A partir do estudo computacional foi possível obter os valores teóricos de momento de dipolo (µ), assim como as energias do orbital molecular ocupado de mais alta energia (EHOMO) e do orbital molecular nao ocupado de mais baixa energia (ELUMO). A afinidade eletrônica (A) e o potencial de ionizaçao (I) foram obtidos a partir das Equaçoes 2 e 3, sendo que os mesmos foram utilizados para obtençao dos valores de eletronegatividade absoluta (χ) e dureza global (η) segundo as Equaçoes 4 e 5.28 A fraçao de elétrons transferidos (ΔN) foi calculada através da Equaçao 6, considerando as eletronegatividades absolutas do átomo de ferro e da IST sendo, respectivamente, χFe e χinh, e as durezas absolutas do metal e do inibidor como sendo χFe and χinh, respectivamente. Neste contexto, γ = (I - A)/2. Foram considerados os valores teóricos de χFe = 7 eV/mol e γFe = 0 com base na aceitaçao de que I=A para um "bulk' metálico.28 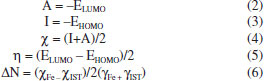
RESULTADOS E DISCUSSAO Análises fisico-químicas do óleo vegetal O tensoativo óleo de coco saponificado (OCS) foi obtido a partir da fonte vegetal óleo de coco que sofreu processo de saponificaçao de acordo com metodologia previamente descrita.23 As análises físico-químicas do óleo vegetal (Tabela 2) mostraram índices oleoquímicos compatíveis com os valores observados por Rossi e colaboradores.23

Obtençao do sistema microemulsionado a base do tensoativo OCS A hidrólise alcalina do óleo de coco resultou na formaçao do tensoativo OCS que foi utilizado para preparar a microemulsao padrao SME-OCS que contém, em proporçoes diferenciadas para cada sistema (SME-OCS1 e SME-OC2), os seguintes componentes: OCS e butanol na razao C/T =1, querosene como fase óleo e água destilada, como mostrado na Tabela 3. A partir do diagrama pseudoternário (Figura 1) do sistema padrao (SME-OCS) foram escolhidos dois pontos na regiao de Winsor IV, que possibilitaram a obtençao dos sistemas derivativos SME-OCS1 e SME-OC2.
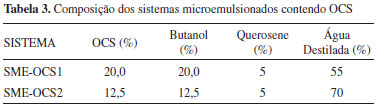
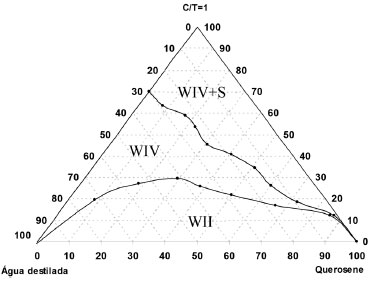 Figura 1. Diagrama pseudoternário do sistema microemulsionado SME-OCS
A justificativa para se trabalhar com uma composiçao na regiao Winsor IV consiste no fato de se ter uma maior área de microemulsao com pontos de solubilidade máximos da matéria ativa C/T (co-tensoativo/tensoativo, no caso do sistema padrao SME-OCS, o co-tensoativo utilizado foi o butanol). Para o sistema padrao SME-OCS há formaçao de regiao WIV com particulados em suspensao (WIV + S) que correspondem ao OCS nao solubilizado. Após sucessivas diluiçoes em água, ambos sistemas SME-OCS1 (40% de C/T, 5% de fase óleo e 55% de H2O) e SME-OCS2 (25% de C/T, 5% de fase óleo e 70% de H2O) se apresentaram estáveis, ou seja, nao há quebra da regiao de microemulsao WIV. Quantificaçao de isatina solubilizada nos sistemas microemulsionados A quantificaçao de IST solubilizada nos sistemas SME-OCS1 e SME-OCS2 foi determinada por espectroscopia na regiao do UV-Vis, tendo apresentado solubilidade máxima na microemulsao de menor polaridade (SME-OCS1), como mostrado na Tabela 4. Observou-se que a diferença de polaridade entre os sistemas SME-OCS1 e SME-OCS2 influencia na solubilizaçao do heterociclo isatina (IST), que após veiculaçao nestas microemulsoes foi avaliado como inibidor de corrosao.

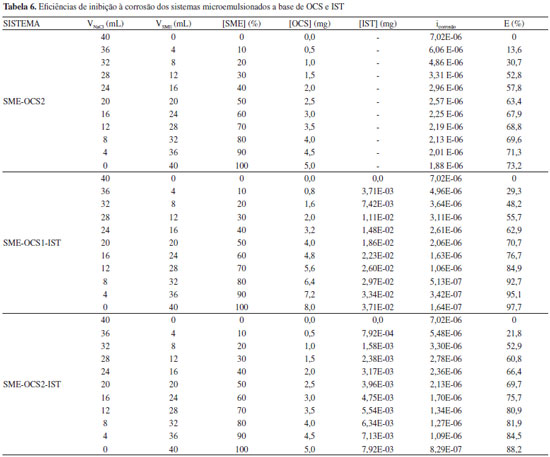
Considerando a importância da microemulsao padrao SME-OCS como sistema veiculador de compostos orgânicos23,24 e, ainda, em funçao das variaçoes de concentraçoes do tensoativo OCS, água e solubilidades máximas da IST (4,64 mg IST/mL SME-OCS1 e 0,99 mg IST/mL SME-OCS2), optou-se por avaliar a eficiência de inibiçao à corrosao da IST veiculada nos sistemas SME-OCS1-IST e SME-OCS2-IST, em percentuais significantemente reduzidos (3,71 x 10-2 mg - 7,92 9 x 10-3 mg) (Tabela 6).
Medidas de viscosidade e de tensao superficial dos sistemas microemulsionados As medidas de viscosidade dos sistemas SME-OCS1, SME-OCS2, SME-OCS1-IST e SME-OCS2-IST foram obtidas com variaçao de temperatura (25 ºC - 60 ºC). Os gráficos de tensao de cisalhamento em funçao da taxa de cisalhamento estao apresentados nas Figuras 2a-d. Observou-se que todos os sistemas apresentam viscosidade constante a uma temperatura e pressao constantes. Portanto, a viscosidade independe da taxa de cisalhamento e as microemulsoes apresentam comportamento de fluido Newtoniano.
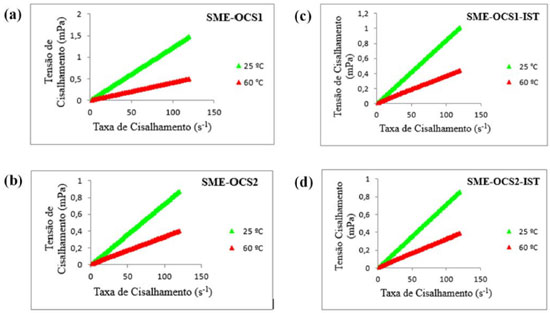 Figura 2. Comportamento reológico dos sistemas microemulsionados: (a) SME-OCS1; (b) SME-OCS2; (c) SME-OCS1-IST; (d) SME-OCS2-IST
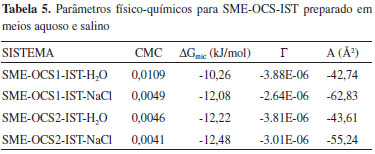
O estudo de adsorçao na interface líquido-gás e o comportamento micelar dos sistemas SME-OCS1-IST e SME-OCS2-IST foram avaliados a partir de medidas de tensao superficial. A concentraçao micelar crítica (CMC) de cada sistema foi determinada em meio neutro e salino 0,5% de NaCl. As Figuras 3a e 3b mostram as curvas de determinaçao da CMC através dos valores da tensao superficial em funçao da concentraçao do tensoativo OCS nos sistemas contendo IST (SME-OCS1-IST e SME-OCS2-IST, respectivamente). De acordo com os resultados observados sugere-se que a presença do íon (Cl-) nao interfere na formaçao das micelas.
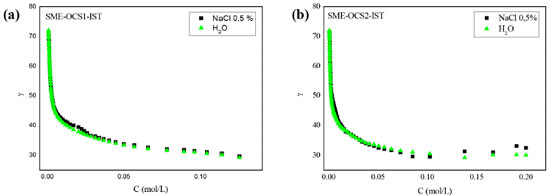 Figura 3. Curvas de determinaçao da CMC para os sistemas microemulsionados: (a) SME-OCS1-IST; (b) SME-OCS2-IST, preparados em meio aquoso salino (NaCl 0,5%)
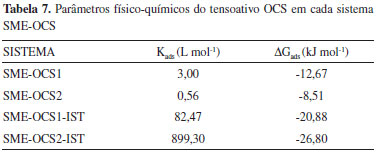
A Tabela 5 apresenta os parâmetros fisico-químicos para o fenômeno de adsorçao dos sistemas microemulsionados preparados com fase água neutra (SME-OCS1-IST-H2O e SME-OCS2-IST-H2O) e salina (SME-OCS1-IST-NaCl 0,5% e SME-OCS2-IST-NaCl 0,5%). Verificou-se que a energia livre de micelizaçao (ΔGmic) é negativa, indicando a espontaneidade da formaçao das micelas. Este resultado sugere que a adsorçao ocorre na interface líquido-gás das microgotículas de cada sistema SME, no entanto, em meio salino observa-se aumento dos valores de ΔGmic para ambos parâmetros [excesso superficial (Г) e área superficial], ou seja, a área ocupada por cada molécula torna-se maior já que os valores deste parâmetro mostraram que há uma ampla área de adsorçao na interface (Å2). O aumento dos parâmetros ΔGmic e Г para os sistemas preparados em meio salino pode estar correlacionado com as interaçoes do íon Cl- com o grupo hidrofílico do tensoativo OCS (o íon Cl- diminui a repulsao entre as cabeças polares do tensoativo) (Figura 3). Medidas da eficiência de inibiçao à corrosao O estudo da eficiência de inibiçao à corrosao em aço AISI 1020 foi realizado para os sistemas SME-OCS2 (isento de isatina), SME-OCS1-IST e SME-OCS2-IST. Em trabalhos anteriores, a eficácia de inibiçao à corrosao do tensoativo OCS livre e microemulsionado (sistema padrao SME-OCS) foram testados pelo método de curvas de polarizaçao linear (método LPR), com eficiências máximas de inibiçao 63% e 77%, respectivamente.23 Para este sistema, encontra-se reportado que derivados de carbazida, tiossemicarbazida e tiossemicarbazona, solubilizados em baixas concentraçoes, na microemulsao padrao SME-OCS, apresentaram eficiências máximas de inibiçao à corrosao significativas (83% - 94%) em meio corrosivo salino.23,24 No presente trabalho, a eficiência de inibiçao à corrosao do heterociclo isatina (IST) solubilizado em baixas concentraçoes, nos sistemas SME-OCS1 (40% de C/T) e SME-OCS2 (25% de C/T), foi avaliada utilizando-se a técnica de curvas de polarizaçao linear. Os cálculos das eficiências máximas de inibiçao à corrosao foram realizados a partir das curvas de Tafel (obtidas através de curvas LPR), que possibilitaram a obtençao dos valores das correntes (i), que por sua vez forneceram as variaçoes de inibiçoes para os sistemas SME-OCS1-IST e SME-OCS2-IST. Observou-se que o aumento na concentraçao do inibidor IST (3,71 x 10-2 mg, SME-OCS1-IST e 7,92 x 10-3 mg, SME-OCS2-IST) ocasionou diminuiçao no valor da corrente (Tabela 6), indicando que IST em maiores concentraçoes retarda mais eficazmente o processo de corrosao. O sistema SME-OCS1-IST apresentou eficácia máxima de inibiçao (97,7%) já que contém na sua composiçao, maior percentual de OCS (20%) e menor quantidade de H2O (55%), sendo também o sistema que melhor solubilizou o inibidor IST (19% de solubilizaçao). As eficiências máximas de inibiçao à corrosao do sistema padrao SME-OCS (77,0%)23 e do sistema SME-OCS2 (73,2%) avaliados para o aço carbono AISI 1020, em meio corrosivo salino, (Tabela 7) sao correlacionadas ao tensoativo OCS. A incorporaçao do heterociclo IST causa diferença significante: 97,7% para SME-OCS1-IST e 88,2% para SME-OCS2-IST, no combate à corrosao do aço carbono AISI 1020, em meio salino (Tabela 6).
A Figura 4 apresenta as curvas de Tafel obtidas para os sistemas SME-OCS contendo ou nao o inibidor IST. Observou-se deslocamento do potencial de corrosao para valores mais positivos à medida que a concentraçao de cada sistema aumentava, tendo sido possível confirmar a eficiência dos sistemas SME-OCS1-IST, SME-OCS2 e SME-OCS2-IST como inibidores de corrosao. A curva de Tafel do sistema SME-OCS1 foi avaliada previamente.23
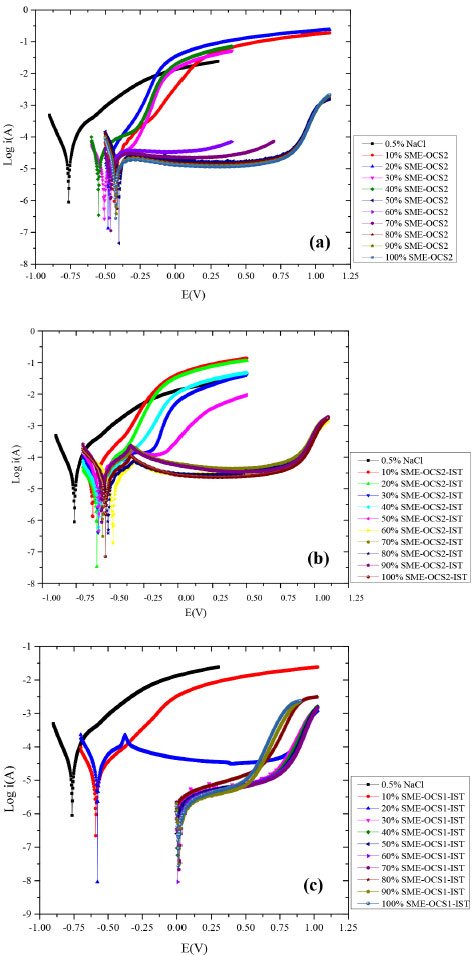 Figura 4. Curvas de Tafel: a) SME-OCS2; b) SME-OCS2-IST; c) SME-OCS1-IST
Isotermas de adsorçao Com o objetivo de avaliar o processo de adsorçao dos sistemas SME-OCS1-IST e SME-OCS2 sobre a superfície metálica foram aplicados três modelos de isotermas de adsorçao: Langmuir, Frumkin e Temkin (Equaçoes 7, 8 e 9, respectivamente). Os gráficos das isotermas foram traçados a partir da fraçao de recobrimento (θ), calculada para diferentes concentraçoes do tensoativo OCS nas microemulsoes SME-OCS1 e SME-OCS2. As Figuras 1S - 9S (Material Suplementar) apresentam os gráficos das isotermas para os sistemas SME-OCS2, SME-OCS2-IST e SME-OCS1-IST, respectivamente. 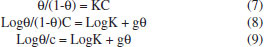 A análise das isotermas de adsorçao mostrou que, para os sistemas SME-OCS2 e SME-OCS2-IST, a isoterma de adsorçao que melhor se ajustou foi a isoterma de Langmuir, com fatores de correlaçao (R2) 0,944 e 0,950, respectivamente. No entanto, para SME-OCS1-IST, o melhor ajuste foi observado na isoterma de Frumkin (R2 = 0,987), estando de acordo com resultado previamente observado para o processo de adsorçao do sistema SME-OCS1, que também se ajusta à isoterma de adsorçao de Frumkin.23 Através da Equaçao 10 realizou-se o cálculo da energia livre do processo de adsorçao (ΔGads) para cada sistema microemulsionado, contendo ou nao IST. O valor de 55,5 refere-se à concentraçao (mol L-1) da água. A Tabela 7 mostra os valores de ΔGads e das constantes de adsorçao (K) obtidos. 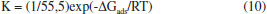 A partir das isotermas foram obtidas as constantes de adsorçao (K) correlacionadas com o tensoativo OCS presente em cada sistema microemulsionado (SME-OCS), contendo ou nao isatina (Tabela 7). De acordo com os dados da Tabela 7, observa-se que a constante de adsorçao do sistema SME-OCS2-IST (0,071) foi menor do que o valor do sistema veiculador SME-OCS2 (0,560). Resultado similar é observado para as microemulsoes SME-OCS1-IST (0,382) e SME-OCS1 (3,0). A partir dos valores de ΔGads, concluiu-se que o processo de adsorçao na interface líquido/sólido para todos os sistemas SME-OCS é espontâneo, devido aos valores negativos obtidos. A comparaçao efetuada para as energias livres de adsorçao entre os sistemas veiculadores SME-OCS1 (-12,67) e SME-OCS2 (-8,51) revelou que as microemulsoes contendo IST [SME-OCS1-IST (-7,57) e SME-OCS2-IST (-3,39)] apresentam decréscimo nos valores modulares de ΔGads. Os sistemas isentos de IST (Tabela 7) apresentaram adsorçao tipicamente física, ou seja, os efeitos entre o metal e o inibidor OCS sao relativamente fracos. No entanto, as moléculas do tensoativo OCS exercem uma barreira de proteçao no eletrodo, controlando o processo de corrosao. Apenas para o sistema SME-OCS2-IST (ΔGads = -26,8 KJ/mol) observa-se adsorçao química. Diferente do observado para o sistema SME-OCS2-IST (12,5% de OCS), a energia livre de adsorçao |20,88| para a microemulsao SME-OCS1-IST é característica de adsorçao física. A justificativa pode estar correlacionada com uma suposta competiçao entre as moléculas do tensoativo OCS e da IST na ocupaçao dos sítios livres do metal, já que no sistema SME-OCS1 o tensoativo OCS está presente em maior percentual (20% de OCS). O fato do heterociclo IST nao ser solúvel em meio salino, impossibilitou a realizaçao de testes com esta substância nao veiculada, o que dificulta um maior esclarecimento sobre sua eficiência de adsorçao. No entanto, estudos preliminares comprovam sua eficiência (94%) na inibiçao à corrosao de cobre, em meio ácido.12 A seguir encontra-se descrito um estudo computacional que foi realizado objetivando avaliar os efeitos estruturais da IST na inibiçao à corrosao. Cálculos computacionais e modelos de mecanismo de interaçao IST-metal A química teórica tem se mostrado altamente relevante no entendimento dos mecanismos de inibiçao à corrosao em diversos meios corrosivos.29,30 Neste contexto, foi realizado um estudo teórico quântico para investigaçao das interaçoes entre o inibidor IST e a superfície metálica do aço carbono AISI 1020. O método empregado foi o B3LYP combinado com o conjunto de bases 6-311++G(d,p). Inicialmente, foram otimizados os parâmetros estruturais e eletrônicos da IST, juntamente com os cálculos das distribuiçoes dos orbitais moleculares de fronteira, HOMO e LUMO, sob a estrutura do ligante IST (Figura 5 e Tabela 8). Estruturalmente, a IST é um composto planar contendo um sistema π-conjugado que compreende a molécula como um todo, que favorece seu processo de adsorçao à superfície metálica.
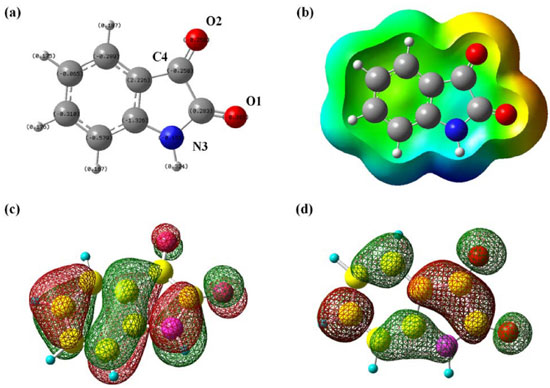 Figura 5. Resultados quânticos calculados para a IST utilizando o método DFT/B3LYP/6-311++G(d,p): (a) estrutura otimizada; (b) potencial eletrostático; (c) distribuiçao do HOMO; (d) distribuiçao do LUMO
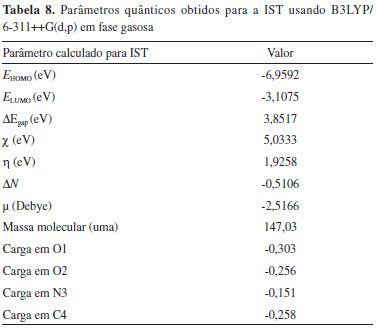
Os valores das cargas verificados para os átomos de oxigênio O1 e O2, nitrogênio N3 e do carbono C4 sao negativos (Tabela 8), estando coerente com o perfil de distribuiçao eletrônica da IST e pode ser verificado através da representaçao da superfície de potencial eletrostático (Figura 5b). A densidade eletrônica acentuada desta porçao da molécula é decorrente tanto da natureza dos átomos de oxigênio e nitrogênio, quanto dos efeitos de ressonância típicos de compostos aromáticos e heteroaromáticos, os quais geram, de forma dinâmica, espécies carregadas que interagem mais fortemente com o sítio metálico. Este efeito é potencializado especialmente quando a IST faz parte do sistema microemulsionado de menor polaridade (SME-OCS1-IST), o qual apresentou eficiência à corrosao muito mais acentuada que o sistema de maior polaridade (SME-OCS2-IST). A partir dos cálculos computacionais foi possível obter os valores das energias dos orbitais moleculares de fronteira, EHOMO e ELUMO, que se encontram distribuídos por toda a estrutura da IST (Figuras 5c e 5d), cujos valores foram -6,9592 eV e -3,1075 eV, respectivamente. Estes valores estao de acordos com aqueles encontrados teoricamente para outros inibidores de corrosao em aço carbono.28 Os valores de EHOMO obtido, assim como ΔEgap = 3,8517 eV, sao coerentes com a capacidade do ligante IST interagir com os orbitais d vazios do metal, formando complexos estáveis,28 justificando, assim, a quimiossorçao verificada experimentalmente. Por fim, a fraçao calculada de elétrons transferidos do inibidor para a superfície metálica foi 0,5106, sendo este valor também consistente com uma situaçao de doaçao efetiva de elétrons do inibidor IST para a superfície do aço carbono.
CONCLUSAO As eficiências de inibiçoes à corrosao foram avaliadas em aço carbono AISI 1020, em meio salino, para o heterociclo isatina (IST) veiculado em baixas concentraçoes (3,71 x 10-2 mg - 7,92 x 10-3 mg) em dois sistemas microemulsionados contendo o tensoativo óleo de coco saponificado (OCS). O estudo de adsorçao dos sistemas SME-OCS1-IST e SME-OCS2-IST avaliado em meio aquoso e salino (NaCl 0,5%), na interface líquido/gás, mostrou que a presença do íon (Cl-) nao ocasiona modificaçao na formaçao das micelas. De acordo com os valores observados para a energia livre de micelizaçao (ΔGmic), observou-se a ocorrência de processo espontâneo de micelizaçao. As eficiências de inibiçao à corrosao das microemulsoes SME-OCS1 e SME-OCS2 (sistemas veiculadores isentos de isatina), bem como SME-OCS1-IST e SME-OCS2-IST (sistemas contendo IST), foram avaliadas utilizando-se a técnica de voltametria de varredura linear (LPR), via método galvanostático, em que se obtém pontualmente, a linearidade de corrente. Os cálculos das eficiências máximas de inibiçao foram realizados a partir das curvas de Tafel. O decréscimo da corrente e o deslocamento do potencial de corrosao para valores mais positivos confirmam a açao inibidora destas microemulsoes. Comparativamente, o sistema SME-OCS1-IST apresentou melhor poder de inibiçao com eficiência máxima de 97,8%. Para os sistemas SME-OCS2 e SME-OCS2-IST, a isoterma de adsorçao que melhor se ajustou foi a isoterma de Langmuir, enquanto que para os sistemas SME-OCS123 e SME-OCS1-IST o melhor ajuste foi observado na isoterma de Frumkin. Os valores da energia livre de adsorçao foram negativos para todos os sistemas avaliados, indicando que o processo de adsorçao na interface líquido/sólido é espontâneo. De acordo com os valores de ΔGads observou-se que as microemulsoes isentas de isatina (SME-OCS1 e SME-OCS2) apresentam adsorçao tipicamente física e, neste caso, as moléculas do tensoativo OCS promovem uma barreira de proteçao no eletrodo, controlando desta forma o processo de corrosao. Para os sistemas com incorporaçao de IST, observou-se adsorçao mista em que SME-OCS2-IST apresenta adsorçao química e SME-OCS1-IST adsorçao física, em funçao do maior percentual do tensoativo OCS (20%). Esta diferença pode ser justificada pela reduçao da concentraçao do tensoativo OCS (12,5%) na microemulsao SME-OCS2-IST, sugerindo que no processo de adsorçao deste sistema prevalecem as características estruturais do heterociclo IST, tendo sido observado um ΔGads = -26,8 kJ/mol. Para o SME-OCS1-IST as características estruturais predominantes foram do tensoativo OCS, cujo ΔGads = -20,88 kJ/mol. Os estudos computacionais realizados suportam os resultados experimentais no que se refere à capacidade do heterociclo IST de se adsorver quimicamente à superfície do aço carbono, especificamente quando veiculado no sistema que contém menor percentual do tensoativo (SME-OCS2). Os valores de EHOMO, de ΔEgap e doaçao efetiva de elétrons do inibidor IST para a superfície metálica foram coerentes com a capacidade do ligante IST interagir com os orbitais d vazios do metal, formando complexos estáveis. Com relaçao ao aspecto da adsorçao é possível concluir que as curvas de Tafel sao limitadas a uma regiao restrita de varredura de potencial, tendo sido observado que os potenciais sao positivos. Desta forma, pode ser estimado um comportamento anódico para todos os formulados avaliados. Para continuidade desta pesquisa, portanto, pretende-se manter o meio salino e o tipo de veiculaçao (SME-OCS1-IST e SME-OCS2-IST) para avaliaçao do comportamento do inibidor IST via processo inverso, ou seja, obtém-se a linearidade de potencial, para achar a corrente. Desta forma, o estudo poderá ser aprofundado via novos estudos de LPR e Impedância Eletroquímica. De forma abrangente, a referida pesquisa está inserida em um estudo multidisciplinar, com aplicabilidade voltada para a eficácia de inibiçao à corrosao do composto orgânico IST. De fato, envolve o desenvolvimento de um novo "produto verde" que se mostrou eficaz no combate à corrosao (97,7% de inibiçao para SME-OCS1-IST e 88,2% para SME-OCS20-IST). Este composto químico (isatina, IST) é amplamente comercializado (com aplicaçoes diversas) e, no presente trabalho, por ter sido veiculado em baixas concentraçoes em um sistema biotecnológico microestruturado a base de óleo de coco saponificado (aproveitamento de matéria regional de baixo custo), poderá despertar a atençao da indústria química e, de fato, tornar-se um produto anticorrosivo 100% fabricado no país.
MATERIAL SUPLEMENTAR As análises físico-químicas do óleo de coco, as medidas de viscosidade e de tensao superficial dos sistemas microemulsionados e as isotermas de adsorçao (langmuir, Frumkim e Temkin) para os sistemas estudados estao disponíveis em http://quimicanova.sbq.org.br, na forma de arquivo PDF, com acesso livre.
AGRADECIMENTOS A CAPES pelo o apoio financeiro deste trabalho. Ao Professor Dr. Angelo da Cunha Pinto† (In memoriam) pela disponibilizaçao da amostra de isatina.
REFERENCIAS 1. Finšgar, M.; Jackson, J.; Corros. Sci. 2014, 86, 17. 2. Gutiérrez, E.; Rodríguez, J. A.; Cruz-Borbolla, J.; Alvarado-Rodríguez, J. G.; Thangarasu, P.; Corros. Sci. 2016, 108, 23. 3. Chigondo, M.; Chigando, F.; Journal of Chemistry 2016, ID 6208937, doi:10.1155/2016/6208937. DOI: http://dx.doi.org/10.1155/2016/6208937 4. Qian, B.; Hou, B.; Zheng, M.; Corros. Sci. 2013, 72, 1. 5. Malik, M. A.; Hashim, M. A.; Nabi, F.; Al-Thabaiti, S. S.; Khan, Z.; Int. J. Electrochem. Sci. 2011, 6, 1927. 6. Jawich, M. W. S.; Oweimreen, G. A.; Ali, S. A.; Corros. Sci. 2012, 65,104. 7. Prabha, S. S.; Rathish, R. J.; Dorothy, R.; Brindha, G.; Pandiarajan, M.; Al-Hashem, A.; Rajendran, S.; Eur. Chem. Bull. 2014, 3, 300. 8. Behzadnasab, M.; Mirabedini, S. M.; Kabiri, K.; Jamali, S. Corros. Sci. 2011, 53, 89. 9. Qui, L.; Xie, A.; Shen, Y.; Corros. Sci. 2005, 47, 273. 10. El-Achouri, M.; Infante, M. R.; Izquierdo, F.; Kertit, S.; Gouttaya, H. M.; Nciri, B.; Corros. Sci. 2001, 43, 19. 11. Hamid, Z. A.; Soror, T. Y.; El-Dahan, H. A.; Omar, A. M. A.; Anti-Corros. Meth. Mat. 1998, 45, 306. 12. Quartarone, G.; Bellomi, T.; Zingales, A.; Corros. Sci. 2003, 45, 715. 13. Singh, M. M.; Rastogi, R. B.; Upadhyai, B. N.; Corrosion 1994, 50, 620. 14. Abboud, Y.; Abourriche, A.; Saffaj, T.; Berrada, M.; Charrouf, M.; Bennamara, A.; Himidi, N. A.; Hannache, H.; Mat. Chem. Phys. 2007, 105, 1. 15. Finšgar, M.; Petovar, B.; Xhanari, K.; Maver, U.; Corros. Sci. 2016, 111, 370. 16. Silva, J. F. M.; Garden, S. J.; Pinto, A. C.; J. Braz. Chem. Soc. 2001, 12, 273. 17. Singh, D. D. N.; Singh, M. M.; Chaudhary, R. S.; Agarwal, C. V.; J Appl. Electrochem. 1980, 10, 587. 18. Ahamad, I.; Prasad, R.; Quraishi, M. A.; Corros. Sci. 2010, 52, 1472. 19. Ansari, K. R.; Quraishi, M. A.; Singh, A.; Corros. Sci. 2015, 95, 62. 20. Schwuger, M. J.; Schomäcker, R.; Chem. Rev. 1995, 95, 849. 21. Mendonça, C. R. B.; Bica, C. I. D.; Piatnicki, C. M. S.; Simó-Alfonso, E. F.; Ramis-Ramos, G.; Electrophoresis 2005, 26, 858. 22. Dantas T. N. C.; Silva, A. C.; Dantas Neto, A. A.; Fuel 2001, 80, 75. 23. Rossi, C. G. F. T.; Scatena Júnior, H.; Maciel, M. A. M.; Dantas, T. N. C.; Quim. Nova 2007, 30, 1128. 24. Moura, E. C. M.; Souza, A. D. N.; Rossi, C. G. F. T.; Silva, D. R.; Maciel, M. A. M.; Echevarria, A.; Bellieny, M. S. S.; Quim. Nova 2013, 36, 59. 25. Frisch, M. J.; Trucks, G. W.; Schlegel, H. B.; Scuseria, G. E.; Robb, M. A.; Cheeseman, J. R.; Montgomery, Jr., J. A.; Vreven, T.; Kudin, K. N.; Burant, J. C.; Millam, J. M.; Iyengar, S. S.; Tomasi, J.; Barone, V.; Mennucci, B.; Cossi, M.; Scalmani, G.; Rega, N. ; Petersson, G. A.; Nakatsuji, H.; Hada, M.; Ehara, M.; Toyota, K.; Fukuda, R.; Hasegawa, J.; Ishida, M.; Nakajima, T.; Honda, Y.; Kitao, O.; Nakai, H.; Klene, M.; Li, X.; Knox, J. E.; Hratchian, H. P.; Cross, J. B.; Bakken, V.; Adamo, C.; Jaramillo, J.; Gomperts, R.; Stratmann, R. E.; Yazyev, O.; Austin, A. J.; Cammi, R.; Pomelli, C.; Ochterski, J. W.; Ayala, P. Y.; Morokuma, K.; Voth, G. A.; Salvador, P.; Dannenberg, J. J.; Zakrzewski, V. G.; Dapprich, S.; Daniels, A. D.; Strain, M. C.; Farkas, O.; Malick, D. K.; Rabuck, A. D.; Raghavachari, K.; Foresman, J. B.; Ortiz, J. V.; Cui, Q.; Baboul, A. G.; Clifford, S.; Cioslowski, J.; Stefanov, B. B.; Liu, G.; Liashenko, A.; Piskorz, P.; Komaromi, I.; Martin, R. L.; Fox, D. J.; Keith, T.; Al-Laham, M. A.; Peng, C. Y.; Nanayakkara, A.; Challacombe, M.; Gill, P. M. W.; Johnson, B.; Chen, W.; Wong, M. W.; Gonzalez, C.; Pople, J. A.; Gaussian, Inc., Wallingford CT, 2004. 26. Tirado-Rives, J.; Jorgensen, W. L.; J. Chem. Theory Comput. 2008, 4, 297. 27. Breneman, C. M.; Wiberg, K. B.; J. Comput. Chem. 1990, 11, 361. 28. Daoud, D.; Douadi, T.; Hamani, H.; Chafaa, S.; Al-Noaimi, M.; Corros. Sci. 2015, 94, 21. 29. Rochdi, A.; Kassou, O.; Dkhireche, N.; Touir, R.; Bakri, M. E.; Touhami, M. E.; Sfaira, M.; Mernari, B.; Hammouti, B.; Corros. Sci. 2014, 80, 442. 30. Sastri, V.S.; Perumareddi, J. R.; Corrosion 1997, 53, 617. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access