Artigo
|
|
| Estudo químico de eflorescências salinas do sítio arqueológico Toca Exú do Jurubeba do Parque Nacional Serra da Capivara, Piauí, Brasil Chemical study of salts efflorescences of the archaeological site Toca Exú do Jurubeba of the National Park Serra da Capivara, Piauí, Brazil. |
|
Benedito Batista Farias FilhoI,*; Maria Conceiçao S. Meneses LageII; Rássius Alexandre Medeiros LimaI
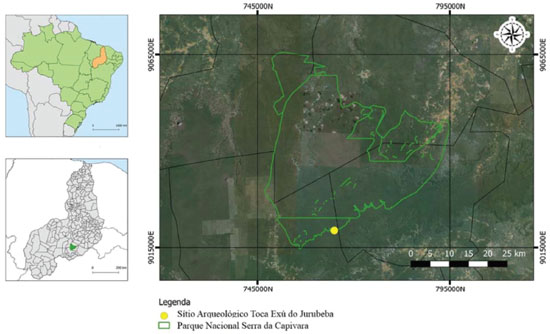
IDepartamento de Química, Universidade Federal do Piauí, 64049-550 Teresina - PI, Brasil Recebido em 07/02/2017 *e-mail: benedito.filho@hotmail.com Toca Exú do Jurubeba is part of a set of archaeological sites located in the Serra da Capivara National Park (Piauí, Brazil), a region of great world interest due to its archaeological potential, especially rock art. However, rock art is constantly threatened by both natural and anthropic factors. Among the natural salts efflorescences that are deposited on the painted graphics often even concealing them. The present study consisted of the spectroscopic analysis of different saline efflorescence samples of the Serra da Capivara National Park, using examination techniques (optical microscopy and Scanning Electron Microscopy) and analysis (Fourier Transform Infrared and Laser Induced Breakdown Spectroscopy). The analysis allowed to identify at least four different compositions of the samples as a mixture of hydrated calcium oxalate (CaC2O4 H2O) with kaolinite (Al2SiO3(OH)4), gypsum (CaSO4 2H2O), tetrahydrate calcium nitrate (Ca(NO3)2 4H2O) and aluminosilicates in the state of fossilization. The obtained results open the way for the conservation of rock art, initially in the archaeological site under study and can serve as basis for other interventions that may be developed in the region. INTRODUÇAO Os sítios arqueológicos contêm informaçoes sobre grupos humanos que habitaram no passado. Estas informaçoes sao extraídas de vestígios que conseguiram chegar até os dias atuais, cuja análise permite reconstituir o cenário vivido pelo homem pré-histórico. Dentre estes vestígios, a arte rupestre permite uma visao mais detalhista sobre o modo de vida de comunidades pretéritas, pois trata-se de um sistema de comunicaçao visual elaborado para expressar o cotidiano, o qual inclui rituais religiosos, práticas domésticas, entre outros.1 No entanto, toda essa riqueza arqueológica está ameaçada por vários problemas de conservaçao, causadas por fatores naturais e/ou antrópicos. As pinturas rupestres estao sujeitas a processos de degradaçao acelerada, o que inclui os problemas relacionados à formaçao de depósitos minerais nas paredes rochosas. Esses depósitos, também chamados de eflorescências salinas, sao agregados cristalinos de sais que apresentam forma e composiçao química variada e que se depositam sobre a superfície de uma estrutura rochosa.2,3 Sao materiais também encontrados em estruturas da construçao civil, monumentos históricos e obras de arte.4-7 A origem das eflorescências salinas sao as mais diversas, mas em geral, sao formadas pela migraçao de sais solúveis e insolúveis, presentes na regiao interna da rocha e que sao carreadas pela água para a sua superfície através de sua rede de capilaridade.8,9 Esses sais, quando expostos à temperatura do ambiente externo, cristalizam-se, formando uma estrutura que pode se apresentar de diferentes coloraçoes. Além disso, quando na superfície rochosa podem reagir com materiais do ambiente externo, como as substâncias de plantas, o que justifica a diversidade na sua composiçao química.9-11 Técnicas espectroscópicas têm sido utilizadas para caracterizaçao química de eflorescências salinas, sobretudo em obras de arte e empregam a Microscopia Eletrônica de Varredura acoplada à Espectroscopia de Energia Dispersiva (MEV/EDS),12-14 a Difraçao de Raios X (DRX)15,16 e a espectroscopia vibracional,17 além da análise térmica (DSC/TGA/DTA).18,19 O uso dessas técnicas analíticas para a caracterizaçao das eflorescências salinas direciona os restauradores e/ou conservadores a proporem procedimentos de intervençao a ser executados seja em obras de artes ou pinturas rupestres para garantir que tais patrimônios culturais cheguem a geraçoes futuras. O Parque Nacional Serra da Capivara, localizado no estado do Piauí (Brasil), tombado pela UNESCO como patrimônio cultural da humanidade em 1991, possui grande quantidade de sítios de arte rupestre em toda sua área de conservaçao ambiental.1,20,21 As pinturas rupestres têm sido alvo de estudo desde a década de 70 e têm revelado que a sua composiçao química sao óxidos minerais de ferro como a hematita, a goetita, a magnetita, entre outras.22 Trata-se de uma arte pré-histórica que apresenta riqueza de detalhes em seus desenhos, preenchimentos, e sao elaboradas em diversas cores (vermelho, amarelo, branco, preto, azul, cinza), preparadas com matéria-prima disponível no local. Dentre os sítios arqueológicos do Parque Nacional Serra da Capivara encontra-se a Toca Exú do Jurubeba (Figura 1), localizado no município de Coronel José Dias nas coordenadas geográficas UTM L 764957 e UTM N 9019386.
O sítio arqueológico em estudo é um abrigo sob rocha arenítica com dimensao de 20 metros de comprimento e 5 metros de altura e apresenta grande quantidade de pinturas rupestres em diversas tonalidades de vermelho. No entanto, o sítio está ameaçado por problemas de conservaçao, sobretudo de origem natural, devido à presença de sais brancos, que escorrem sobre o paredao rochoso e que acaba por deteriorar o seu valioso patrimônio artístico, cultural e histórico. Assim, o objetivo do presente trabalho foi o de analisar a composiçao química de eflorescências salinas presentes no sitio arqueológico Toca Exú do Jurubeba, localizado no Parque Nacional Serra da Capivara, visando desacelerar o grau de degradaçao das pinturas rupestres através de açoes preventivas e interventivas de conservaçao. Para isso, utilizou-se a espectroscopia no infravermelho com Transformada de Fourier (FTIR) e a espectroscopia de emissao em plasma induzido por laser (LIBS), além dos exames sob microscopia óptica (MO) e microscopia eletrônica de varredura (MEV). A utilizaçao dessas técnicas de análises permite avaliar as suas potencialidades para esses tipos de amostra, cujo conhecimento é de grande interesse para ciência da conservaçao em arqueologia.
PARTE EXPERIMENTAL Amostras Foram coletadas 6 micro-amostras de eflorescências salinas (SJ04.04, SJ04.06, SJ04.07, SJ05.04, SJ05.05 e SJ05.06) presentes em pontos diferentes da parede rochosa do citado sítio arqueológico Toca Exú do Jurubeba. As amostras foram retiradas de áreas distantes das pinturas rupestres priorizando os locais onde o estado de degradaçao estivesse mais avançado e tomando o cuidado para que fosse realizada uma amostragem representativa do material. Todo o processo de coleta das amostras foi realizado obedecendo às normas e regras determinadas pelas cartas patrimoniais propostas pelo ICOMOS.23 Caracterizaçao físico-química das amostras Observaçao sob microscópio óptico Uma pequena porçao das amostras de eflorescência salina foi colocada sobre uma lâmina de vidro e examinada sob a ocular de um microscópio portátil (ProScope HR CSI) com conexao USB ao computador. As imagens foram obtidas utilizando uma lente (Scalar) de aumento de 50x realizando uma observaçao minuciosa do depósito salino. Microscópio Eletrônico de Varredura O estudo morfológico das amostras foi realizado em um microscópio eletrônico de varredura (Fei Company, Quanta Feg 250) operando com tensao de 20 kV. Previamente as amostras foram fixadas em fita adesiva de carbono dupla fase e, posteriormente, realizada a metalizaçao com ouro. As leituras foram obtidas em aumentos de 5000 a 10000 vezes. Infravermelho com Transformada de Fourier As medidas por infravermelho (Agilent Technology, CARY 630 FTIR) foram realizadas no modo ATR (reflectância total atenuada), colocando-se pequenas quantidades das amostras sobre o porta-amostra do instrumento e prensadas sobre um cristal de diamante. As medidas foram realizadas no intervalo de 4000 a 400 cm-1 com resoluçao espectral de 4 cm-1 e utilizando 64 varreduras. Espectroscopia de emissao óptica em plasma induzido por laser As análises elementares foram realizadas utilizando um equipamento LIBS constituído por um policromador echelle (Mechelle 5000, Andor Technology), laser pulsado Nd:YAG (20 Hz, 1064 nm, FWHM 5,2 ns, e energia máxima do pulso de 110 mJ) e detector ICCD (iStar DH734, Andor Technology). A superfície de uma amostra de pigmento rupestre contém superfície irregular, fazendo com que, para cada medida, a localizaçao exata do plasma a ser formado seja alterada. Para minimizar esse efeito, empregou-se duas ponteiras laser de tal maneira que estas emergissem a uma certa distância da lente. A plataforma na qual a amostra se encontra é removível, e para cada amostra analisada, as ponteiras eram alinhadas até que as radiaçoes laser fossem interceptadas. As medidas foram realizadas empregando energia do laser de 20 mJ/pulso, tempo de delay de 500 ns e tempo de integraçao de 1 µs. Os sinais analíticos obtidos foram identificados utilizando-se a base de dados do NIST Atomic Spectra library. As medidas foram realizadas em triplicatas, acumulando três pulsos em locais distintos ao longo da superfície da amostra para garantir uma medida representativa.
RESULTADOS E DISCUSSAO As amostras de eflorescências salinas foram submetidas a métodos de exames e análises químicas para a sua caracterizaçao e os resultados servirem de base para etapas e trabalhos de conservaçao do sítio arqueológico Toca Exú do Jurubeba presente em uma área de grande importância mundial, o Parque Nacional Serra da Capivara. Foram elegidas as técnicas de exames mais comumente utilizadas em amostras de interesse arqueológico, como a microscopia óptica e a Microscopia Eletrônica de Varredura, que fornecem dados sobre a morfologia do material analisado. As técnicas espectroscópicas LIBS e FTIR foram escolhidas para este trabalho por ambas fornecerem sinais analíticos satisfatórios para complementaçao das análises, e o atrativo para medidas arqueológicas, que é a possibilidade de serem utilizadas sem nenhum preparo de amostra. Os exames sob microscópio óptico (Figura 2) permitiram visualizar informaçoes das eflorescências como coloraçao, tamanho e forma de partículas, bem como sua aderência ao paredao rochoso, características nao disponíveis a olho nu. Além disso, o presente estudo utilizando os exames microscópios foram fundamentais para interpretaçao inequívoca das análises por LIBS e FTIR, uma vez que este tipo de amostra possui natureza heterogênea.
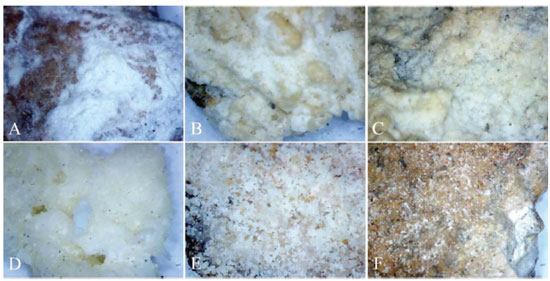 Figura 2. Exames sob microscopia óptica das amostras de eflorescência salina (A) SJ04.04, (B) SJ04.06, (C) SJ04.07, (D) SJ05.04, (E) SJ05.05 e (F) SJ05.06 com detalhes em aumento de 50x
A observaçao sob microscopia óptica das amostras permitiu revelar que os sais de eflorescências salinas já se encontram distribuídas sobre a superfície rochosa, embora ainda de forma nao-uniforme. Ao mesmo tempo, foi possível observar que cada amostra coletada possui características distintas, principalmente em relaçao à aderência na rocha. Em especial nas amostras B e C os sais se encontram incrustados sobre a superfície rochosa, com dificuldades de desagregá-las, o que leva a inferir que está em estado de fossilizaçao, enquanto que para as demais amostras (A, D, E e F) os sais estao em pequenas porçoes, fáceis de serem removidas da matriz rochosa. A amostra E apresenta uma característica distinta em relaçao às demais, com a forma de pequenas agulhas ou fibras longas distribuídas na rocha. As micrografias das amostras de eflorescência salina obtidas por MEV (Figura 3), utilizando o aumento de 10000 vezes, permitiram observar diferentes aspectos morfológicos.
 Figura 3. Micrografias das amostras de eflorescência salina (A) SJ04.04, (B) SJ04.06, (C) SJ04.07, (D) SJ05.04, (E) SJ05.05 e (F) SJ05.06 com detalhes em aumento de 10.000x
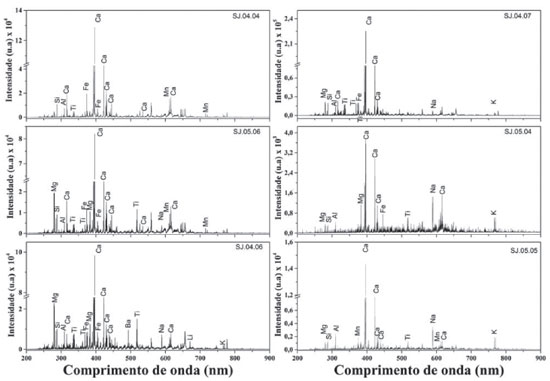
A amostra SJ04.04 revela uma morfologia de estrutura densa e compacta e muitos pontos em formato de agulha. Contrariamente, as amostras SJ04.06 (Figura 3B), SJ04.07 (Figura 3C) e SJ05.06 (Figura 3F) apresentam no formato de uma massa densa, bem como alguns graos de formato retangular e outros arredondados ao longo de sua superfície. É possível observar também nas amostras SJ05.04 (Figura 3D) e SJ05.05 (Figura 3E) um aspecto morfológico bastante semelhante na forma de várias estruturas planas retangulares que se sobrepoem e formam camadas laminares. Embora poucos detalhes foram possíveis de serem observados nas micrografias das amostras, conhecer a morfologia através de técnicas de exame permitiu fornecer informaçoes de materiais que venham estar agregados aos depósitos minerais e com isso dificultar a interpretaçao dos resultados baseados na análise qualitativa. A Figura 4 mostra os resultados da análise qualitativa das amostras com os principais sinais de emissao e seus respectivos elementos químicos que foram obtidos, realizando um exame minucioso de toda a faixa espectral obtidos por LIBS.
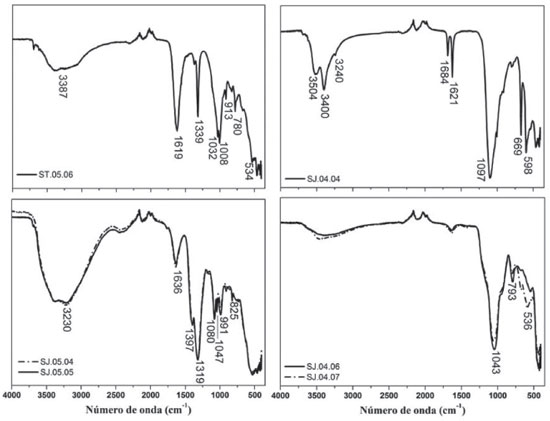
Foram selecionadas apenas as linhas de emissao mais intensas para realizar a caracterizaçao química da amostra. A linha de emissao de maior intensidade para todas as amostras refere-se ao Ca II em 396,8 nm e presentes também em 315,91 nm, 422,70 nm, 430,24 nm, 445,50 nm, 534,96 e 616,26 nm. Esse resultado pode ser responsável, em parte, pela composiçao química-mineralógica das eflorescências salinas, resultado da reaçao dos ânions solúveis que migram do interior da rocha (sulfatos, carbonatos e outros), bem como de substâncias químicas, como o ácido húmico (liberadas pelas raízes de plantas), que formam os agregados salinos. A Figura 4 mostra ainda outros componentes presentes nas amostras, uns de caráter majoritários e outros em nível de traços. Foram detectadas claramente as linhas de emissao atômica do Na I (dupleto em 588.99 e 589.59 nm), Si I (288, 17 nm), Al I (309,31 nm) e Fe II (573,73 nm; 404,59 nm e 445,49 nm)). Esses resultados estao em concordância com a composiçao de uma infinidade de eflorescências salinas já estudadas, oriundas de fontes da construçao civil,4 arquitetônica histórica,5 obras de arte e arqueológicas.5,6 Além disso, os elementos como Si e Al podem estar associados diretamente à composiçao do suporte rochoso que sao também compostos de aluminossilicatos. Elementos como Mg I (279,56 nm e 383,20 nm), Ti II (336,11 nm; 368,52 nm e 518,39 nm), K I (766,49 nm), Mn I (714,88 e 612,27 nm), Li I (670,73 nm) e Ba I (493,41 nm) podem estar associados a impurezas contidas nas amostras, uma vez que se trata de um sítio arqueológico a céu aberto e, por isso, as açoes ambientais como o vento, que arrastam materiais até as paredes rochosas e acabam se depositando, sao bastante atuantes. A caracterizaçao química utilizando a técnica LIBS foi fundamental para realizaçao do levantamento inicial dos principais elementos químicos presentes nas amostras. Assim, para a caracterizaçao completa dos depósitos minerais foi elegida a técnica FTIR, que em conjunto com o LIBS forneceu a caracterizaçao químico-mineralógica completa da amostra, permitindo assim os trabalhos de conservaçao de arte rupestre. Na Figura 5 sao apresentados os espectros FTIR das amostras de eflorescências salinas coletadas no paredao rochoso do sítio arqueológico Toca do Exú do Jurubeba. As análises espectrais FTIR revelaram que pelo menos três compostos fazem parte do conjunto de amostras analisadas e que algumas delas já estao em estado de silicificaçao, devido à presença marcante de modos vibracionais do SiO2 ou da mistura com fragmentos rochosos que vêm aderido aos depósitos de eflorescências salinas.
A amostra SJ.05.06 apresenta bandas de estiramento de Si-O em 1032 e 1008 cm-1, em 913 cm-1 é associada ao modo vibracional de deformaçao do Al-OH e em 534 cm-1 é ligada ao modo de deformaçao do Si-O-Al.24,25 Além dessas bandas foi possível observar em 1619 cm-1 o modo vibracional de estiramento da carbonila (C=O), bem como em 1339 cm-1 que é devido ao estiramento simétrico C-O-C, e a banda em 780 cm-1 que é da soma dos modos vibracionais de estiramento O-C-O e de deformaçao de C-O, [ν(O-C-O) + δ(C-O)].26 A banda larga em aproximadamente 3400 cm-1 se deve ao modo de estiramento da hidroxila de água.26 Essas informaçoes permitem identificar inequivocamente que tal amostra é composta de whewellita (CaC2O4. H2O) com a presença de caolinita [Al2Si2O5(OH)4]. O mecanismo de formaçao do oxalato de cálcio em rochas já é conhecido na literatura e ocorre pela reaçao do ácido oxálico (liberado por líquens, cogumelos e plantas radiculares) e as substâncias presentes na rocha, cujos produtos finais sao oxalatos de cálcio em diferentes formas de hidrataçao.9,10 A amostra SJ.04.04 apresentou bandas vibracionais na regiao de 3000 cm-1 (3504, 3400 e 3240 cm-1), além de 598 cm-1 que é atribuída ao estiramento de OH de água. Os modos vibracionais de deformaçao de OH ainda apareceram como bandas bem definidas em 1684 e 1621 cm-1. As assinaturas das bandas em 1097 e 669 cm-1 sao atribuídas aos modos de estiramento de S-O de íons sulfatos (SO42-).27 Todas as características espectrais, bem como a análise prévia da composiçao elementar, permitem inferir que a eflorescência salina em estudo se trata do sulfato de cálcio bihidratado (CaSO4. 2H2O). As amostras SJ.04.06 e SJ.04.07 tiveram perfis espectrais bastante semelhantes e apresentaram bandas características da caolinita, cujos modos de vibraçao em 1043 cm-1 sao atribuídos ao estiramento de Si-O, em 793 cm-1 a banda de vibraçao é característica de estiramento Si, e, em 536 cm-1, corresponde à vibraçao de deformaçao de Si-O-Al.25 Para estas amostras foi detectada apenas bandas de vibraçao de aluminossilicatos, o que indica que os sais se encontram em estado de silicificaçao. Essas amostras, como mostrado no exame sob microscópio (Figura 2), encontram-se agregadas ao suporte rochoso, o que indica que esse processo de silicificaçao ocorreu devido ao longo tempo de exposiçao às características naturais, por exemplo a radiaçao solar. Por fim, as amostras SJ.05.04 e SJ.05.05 também apresentaram composiçao química semelhante em comparaçao com as principais bandas de vibraçao no infravermelho. Pode-se observar uma banda larga e intensa ao redor de 3230 cm-1 e uma banda bem definida em 1636 cm-1 que pode ser atribuída respectivamente ao modo de estiramento e deformaçao da hidroxila da água.27-29 As demais bandas levam a entender que se trata de um sal a base de nitrato, confirmado pela presença da banda de estiramento do N-O em 1397 cm-1 e em 825 cm-1, que se refere ao estiramento N=O29,30 Além disso, outras bandas de absorçao do N-O do íon nitrato podem ser observadas em 1047 e em 1319 cm-1, que equivalem ao estiramento simétrico e assimétrico respectivamente.31 Assim, essas informaçoes em conjunto sugerem que o depósito salino para as amostras SJ.05.0 e SJ.05.05 se trata do sal de Ca(NO3)2·4H2O. A regiao do Parque Nacional Serra da Capivara contém mais de 1200 sítios arqueológicos e apesar de ser uma extensa área territorial o controle dos problemas de conservaçao vem sendo monitorados há décadas por uma equipe multidisciplinar encarregada de resolver problemas de conservaçao para a manutençao dos sítios arqueológicos. No entanto, alguns problemas pontuais, como as eflorescências salinas, ainda sao as mais difíceis de serem controladas uma vez que sao processos produzidos pela própria rocha por um processo natural. Assim, considerando que cada sítio arqueológico é um bem único dentro do contexto cultural e histórico, a produçao das eflorescências salinas dentro de um mesmo sítio arqueológico pode apresentar características químicas distintas, como foi o caso do sítio em estudo. Uma vez que as amostras foram caracterizadas físico-quimicamente, percebe-se a existência de quatro grupos distintos que auxiliarao as etapas de conservaçao e que serao utilizadas dentro do sítio em estudo, aquelas em que se encontram em estado de fossilizaçao e aquelas que ainda mantêm todas as suas características químicas originais. Para as etapas de intervençao arqueológica do sítio Exú do Jurubeba, propoe-se inicialmente a utilizaçao de retiradas mecânicas, sobretudo do grupo em que a sua composiçao química se trata de um material já em estado de silicificaçao, característica das amostras SJ.04.06 e SJ.04.07. Essa etapa é necessária porque, como apontado nos exames sob microscópio, apesar de algumas das amostras se encontrarem aderidas na rocha, elas se acumulam formando espessas camadas de sais, que podem ser removidas antes de chegarem à superfície rochosa. Uma vez concluída a limpeza mecânica, a segunda etapa consistirá de um tratamento químico, principalmente para o grupo das amostras SJ.05.06, SJ.04.04, SJ.05.04 e SJ.05.05 no sentido de solubilizar todo o material, uma vez que elas preservaram sua estrutura química. Vale a pena ressaltar todo o cuidado na escolha dos reagentes e a forma como utilizá-los nos paredoes rochosos sem que venham a provocar qualquer dano às pinturas rupestres presentes no sítio.
CONCLUSAO A análise por LIBS em conjunto com a FTIR, bem como os exames morfológicos por microscopia ótica e microscopia eletrônica de varredura foram suficientes para realizar a caracterizaçao completa das eflorescências salinas presentes no sítio arqueológico Toca Exú da Jurubeba. As técnicas mostraram potencialidades para serem aplicadas em amostras dessa natureza por dispensar o preparo de amostras e fornecer informaçoes sobre a natureza química dos depósitos minerais, importantes para os trabalhos de conservaçao de arte rupestre. Nós reportamos que as eflorescências salinas sao compostas de diferentes sais como uma mistura de oxalato de cálcio hidratado com caolinita, sulfato de cálcio e nitrato de cálcio, além de um depósito material em estado de silicificaçao. Os resultados obtidos para as amostras em estudo servirao de base para trabalhos futuros de intervençao de conservaçao no sítio arqueológico Toca Exú do Jurubeba, mas também poderao se estender como base para outros sítios arqueológicos da regiao do Parque Nacional Serra da Capivara, bem como em sítios arqueológicos que também passam pelo mesmo problema de conservaçao.
AGRADECIMENTOS Os autores agradecem ao GIAQA- Grupo de Instrumentaçao e Automaçao em Química Analítica da Unicamp pelo apoio ao desenvolvimento deste estudo. Sao gratos ainda às agências de fomento CNPq e CAPES pelo apoio financeiro.
REFERENCIAS 1. Pessis, A. M.; Guidon, N.; World Archaeology 2007, 39, 406. 2. Hennetier, L.; Almeida, J. V.; Correia, A. M. S.; Ferreira, V. M.; Br. Ceramic Trans. 2001, 100, 72. 3. Čukovska, L.; Grupče, O.; Minčeva-Šukarova, B.; Kuzmanovski, I.; J. Brazil Chem. Soc. 2009, 20, 57. 4. Lopez-Acevedo, V.; Viedma, C.; Gonzalez, V.; Iglesia, A.; J. Cryst. Growth 1997, 182, 103. 5. Backbier, L.; Rousseau, J.; Anal. Chim. Acta 1993, 283, 855. 6. Menezes, R. R.; Ferreira, H. S.; Neves, G. A.; Ferreira, H. C.; Ceramica 2006, 52, 37. 7. Madariaga, J. M.; Maguregui, M.; Vallejuelo, S. F.; Knuutinen, U.; Castro, K.; Martinez-Arkarazo, I.; Giakoumaki, A.; Pitarch, A.; J. Raman Spectrosc. 2014, 45, 1059. 8. Kramar, S.; Urosevic, M.; Pristacz, H.; Mirti, B.; J. Raman Spectrosc. 2010, 41, 1441. 9. Alberghina, M. F.; Barraco, R.; Brai, M.; Casaletto, M. P.; Ingo, G. M.; Marrale, M.; Policarpo, D.; Schillaci, T.; Tranchina, L.; Appl. Phys. A 2010, 100, 953. 10. Edwars, H. G. M.; Farwell, D. W.; Daffner, L.; Spectrochim. Acta, Part A 1996, 52, 1639. 11. Edwars, H. G. M.; Edwards, K. A. E.; Farwell, D. W.; Lewis, I. R.; Seaward, M. R. D. J.; J. Raman Spectrosc. 1994, 25, 99. 12. Aguayo, T.; Clavijo, E.; Eisner, F.; Ossa-Izquierdo, C.; Campos-Vallette, M. M.; J. Raman Spectrosc. 2011, 42, 2143. 13. Iordanidisa, A.; Garcia-Guinea, J.; Strati, A.; Gkimourtzinac, A.; Papoulidou, A.; Spectrochim. Acta, Part A 2011, 78, 874. 14. Garcia-Guinea, J.; Recio-Vazque, L.; Almendros, G.; Benavente, D.; Correcher, V.; Perez-Garcia, A.; Sanchez-Moral, S.; Fernandez-Cortes, A.; Environ. Earth Sci. 2013, 69, 1733. 15. Arroyo, F.; Villegas-Sánchez, R.; J. Cult. Heritage 2013, 14S, 109. 16. Paterakis, A. B.; Steiger, M.; Stud. Conserv. 2015, 60, 172. 17. Broggi, A.; Petrucci, E.; Bracciale, M. P.; Santarelli, M. L.; J. Raman Spectrosc. 2012, 43, 1560. 18. Dei, L.; Mauro, M.; Bitossi, G.; Thermochim. Acta 1998, 317, 133. 19. Bartl, B.; Havlínc, J.; Trejbal, J.; Durovi, M.; Thermochim. Acta 2013, 566, 292. 20. Kinoshita, A.; Mayer, E.; Mendes, V. R.; Figueiredo, A. M. G.; Baffa, O.; Radiat. Prot. Dosim. 2014, 159, 212. 21. Fontugne, M.; Shao, Q.; Frank, N.; Thil, F.; Guidon, N.; Boeda, E.; Radiocarbon 2013, 55, 1191. 22. Lage, M. C. S. M.; Revista de Geologia 1996, 9, 83. 23. Choay, F. Alegoria do Patrimônio, Unesp: Sao Paulo, 2001. 24. Alencar, W. J.; Santos, F. E. P.; Cisneros, J. C.; Silva, J. H.; Freire, P. T. C.; Viana, B. C.; Spectrochim. Acta, Part A 2015, 135, 1052. 25. Saikia, B. J.; Parthasarathy, G.; Sarmah, N. C.; Bull. Mater. Sci. 2008, 31, 775. 26. Faria, D. L. A.; Lopes, F. N.; Souza, L. A. C.; Branco, H. D. O. C.; Quim. Nova 2011, 34, 1358. 27. Tourneret, L.; Berger, F.; Mavon, C.; Chambaudet, A.; Appl. Clay Sci. 1999, 14, 299. 28. Arrizabalaga, I.; Gómez-Laserna, O.; Carrero, J. A.; Bustamante, J.; Azibar Rodríguez, A.; Arana, G.; Madariaga, J. M.; Anal. Methods 2015, 7, 1061. 29. Santos, M. L.; Florentino, A. O.; Saeki, M. J.; Aparecida, A. H.; Fook, M. V. L.; Guastaldi, A. C.; Ecletica Quim. 2005, 30, 29. 30. Vratny, F.; Appl. Spectros. 1959, 13, 59. 31. Al-Hosney, H. A.; Grassian, V. H.; Chem. Phys. 2005, 7, 1266. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access