Nota Técnica
|
|
| Papel indicador colorimétrico para detecção de formol em produtos lácteos e produtos de higiene pessoal Colorimetric indicator paper for formol detection in milk based and personal care products |
|
Guilherme B. C. Martins; Renata R. Sucupira; Paulo A. Z. Suarez*
Instituto de Química, Universidade de Brasília, 70919-970 Brasília - DF, Brasil Recebido em 19/12/2016 *e-mail: psuarez@unb.br Due to its low cost, formaldehyde was commonly used as conservative in hygienic and cosmetic products. However, formaldehyde is strongly reactive and toxic, so its use has been forbidden in several products. Recently, it was reported by different media that formaldehyde has been added illegally in milk, causing innumerous health problems. In this work we developed a colorimetric indicator paper based on Schiff 's reagent, which can be associated with a smartphone application. It was observed that the paper stabilizes the Schiff 's reagent, avoiding its decomposition during short periods. It was also possible to successfully detect the presence of formaldehyde in commercial products, such as: detergents, shampoos and conditioners. Regarding milk based products, the indicator paper is very sensitive to detect formaldehyde, having a sensibility of 0.01% (v/v). The developed indicator paper has low cost and can help the supervision of milk products, as a trial test. Also it is possible to commercialize this product to common consumer, due to its simplicity. INTRODUÇAO O formaldeído é uma molécula simples, usada durante anos em vários produtos comerciais com diversas aplicaçoes, além de ser encontrada no ar em diversos locais laborais. O principal uso do formol em produtos comerciais é como conservante e desinfetante, sendo amplamente empregado em funçao do seu baixo custo e alta eficácia. Todavia, o formol é uma molécula extremamente reativa e, portanto, agressiva e tóxica à saúde humana. Sua reatividade é tamanha que, segundo estudos relatados na literatura, 1 mg kg-1 de formol no ar é quantidade suficiente para causar irritaçoes.1 Concentraçoes maiores no ar podem causar danos à pele e ao sistema respiratório, podendo ocasionar queimaduras e danos severos aos tecidos humanos. Quando ingerido, pode causar irritaçao e lesoes internas, de modo que nao é prevista sua utilizaçao em produtos alimentícios ou que demandem ingestao. Recentemente, a Agência Internacional de Pesquisa em Câncer (IARC - The International Agency for Researchon Cancer) publicou uma nota informando que o formol é uma substância potencialmente carcinogênica,2 embora haja controvérsias em torno de que ele seja um agente cancerígeno.3 Porém, é consenso que, cancerígeno ou nao, exposiçoes constantes ou altas concentraçoes de formol sao agressivas para a saúde humana. Outros estudos também apontam que a exposiçao constante a formaldeído influencia de forma negativa o sistema hormonal e a reproduçao humana.4 Baseados nos estudos toxicológicos do formol, o órgao responsável pelo controle de produtos no Brasil, a ANVISA (Agência Nacional de Vigilância Sanitária), proibiu a comercializaçao do formol e restringiu sua utilizaçao em alguns produtos cosméticos (Resoluçao-RDC nº 35, publicada em 3 de junho de 2008; e Resoluçao-RDC nº 36, publicada em 17 de junho de 2009). A proibiçao do formol e sua restriçao também ocorrem em outros países, como, entre outros, os Estados Unidos, Inglaterra, Alemanha e Japao. O formol pode ser encontrado em diversos itens comerciais, desde produtos de limpeza, cosméticos5,6 e alimentos,7,8 incluindo bebidas alcoólicas, como, por exemplo, a cerveja.9 Também existem produtos que podem liberar formol no ar, dentre eles fumaça de cigarro,10 roupas, madeira compensada e materiais de construçao e acabamento.11 No caso de produtos que liberam formol no ar, há o risco de contaminaçao em diversos estabelecimentos, os quais necessitam ser regulados, o que seria o caso de bares, saloes de beleza, hospitais, áreas de construçao e lugares de estocagem, os quais podem possuir altas concentraçoes de formol caso o ambiente nao seja bem ventilado. No caso do Brasil, a ANVISA proíbe o uso de formol em alguns produtos de higiene pessoal. Entretanto, em alguns casos permite o uso deste como conservante, na concentraçao limite de no máximo 0,2%.12 Outro problema que tem sido amplamente discutido na mídia nos últimos anos está relacionado à adiçao criminosa de formol ao leite. Recentemente foram relatados aqui no Brasil diversos casos de adulteraçao de leite com formol, por várias empresas.13-15 O leite é utilizado diariamente, principalmente por crianças, e é consenso que a presença de formol neste alimento nao é aceitável. Portanto, é necessário o controle de formol nestes produtos de forma simples e acessível ao consumidor deste produto. É importante ressaltar que nao é permitido o uso de formol como conservante alimentar em produtos alimentícios no Brasil. Várias técnicas foram reportadas para determinaçao de formol em diversas condiçoes e amostras, de forma direta ou indireta, como, por exemplo, cromatografia líquida,16 eletroquimioluminescência,17 espectrofotometria,17,18 e fluorimetria.19 Entretanto, apesar da precisao dessas técnicas, análises laboratoriais sao pouco práticas para o uso cotidiano, principalmente se o próprio consumidor deseja ter um controle mais efetivo do que esta consumindo, seja como alimento ou produto de higiene ou beleza. Neste contexto, surge a demanda por uma forma de análise simples, com baixo custo e robusta, de fácil execuçao, que forneça resultados rápidos. Atualmente existem no mercado apenas dispositivos portáteis para detecçao qualitativa ou quantitativa de formol no ar. De fato, vários métodos foram propostos para análises portáteis, dentre eles um dispositivo que mede a concentraçao de formol no ar20 e outro em que um material nanoporoso é utilizado como indicador visual ou entao é acoplado a um dispositivo para mediçoes mais precisas.21 Ambos partem do mesmo princípio de utilizar uma detecçao colorimétrica de um aduto formado a partir do formol capturado no ar, que fica suportado em uma matriz sólida. Em outro trabalho foi feita a impregnaçao do reagente de Schiff em uma matriz sólida de sílica.22 O uso do reagente de Schiff como detector para formol já é conhecido, de modo que este é utilizado para análises qualitativas orgânicas para o reconhecimento de aldeídos. O princípio da técnica é a utilizaçao do reagente de Schiff, que reage prontamente com o formol, gerando um aduto de cor azul púrpura, facilmente distinguível a olho nu.23 O reagente de Schiff é uma soluçao incolor que contém uma molécula indicadora, a qual é produzida pela reaçao entre a p-rosanilina, um corante orgânico de cor rosácea em soluçao, com sulfito em meio ácido. Este composto é incolor e reage na presença de aldeídos, reconjugando o sistema e gerando uma nova cor em soluçao, azul púrpura. Na ausência de aldeídos o reagente de Schiff nao gera cor, permanecendo incolor. Entretanto, o efeito de diluiçao ou separaçao cromatográfica no reagente de Schiff causa sua decomposiçao, liberando a p-rosanilina livre, o que confere a cor rosácea, a qual é distinguível da cor do aduto entre o reagente de Schiff e aldeídos em funçao da tonalidade.24 É importante ressaltar que o reagente de Schiff pode ser utilizado para detecçao de aldeídos leves em produtos comerciais, de forma direta, a qual já foi relatada em outro estudo anterior do nosso grupo,24 e que inclusive foi possibilitada para aplicaçao comercial do reagente de Schiff, método este de estabilizaçao patenteado, o qual já é utilizado comercialmente.25,26 Apesar de nao ser específica para a detecçao de formol, entende-se que caso a amostra possua algum aldeído que reaja com o Reagente de Schiff, esta possivelmente, de forma similar ao formol, pode ser agressiva ao corpo humano, merecendo atençao. Em outro aspecto, o objetivo da técnica é o de ser utilizada como forma de triagem, nao sendo necessário que a técnica seja específica para a detecçao de formol. Entretanto, o uso direto do reagente de Schiff em amostras comerciais incorpora um maior custo em materiais para as dosagens, e inclusive um gasto relacionado com a quantidade, tendo em vista que o reagente de Schiff é extremamente sensível ao formol. Neste trabalho é proposto o uso de um material de baixo custo e descartável, o qual pode ser utilizado para detectar formol em diversos produtos comerciais e inclusive no ar, o qual é baseado na impregnaçao do reagente de Schiff em papel, formando papel impregnado indicador.25 Este indicador é mais versátil e barato que as outras técnicas portáveis propostas para análise de formol. O objetivo deste indicador é que seu uso seja realizado corriqueiramente e que qualquer pessoa entenda seus resultados.
PARTE EXPERIMENTAL Materiais e reagentes utilizados P-rosanilina p.a. (Vetec), metabissulfito de sódio p.a. (Synth), ácido clorídrico p.a. (Vetec) e formaldeído p.a. (Vetec) foram adquiridos de fontes comerciais com grau de pureza analítico e usados como recebidos. Os produtos comerciais testados foram obtidos em comércios locais e em todos eles foi verificada a ausência de formol, sendo eles leite integral, xampu, condicionador e detergente neutro. Síntese do reagente de Schiff A síntese foi baseada em uma metodologia descrita na literatura,25 com algumas modificaçoes. Foi dissolvido 0,2 g de p-rosanilina em 120 mL de água aquecida e deixada esfriar. Em seguida, foi dissolvido 0,5 g de bissulfito de sódio em 20 mL de água e posteriormente misturado com a soluçao de p-rosanilina. A soluçao foi agitada e em seguida foram adicionados 2 mL de ácido clorídrico e o volume foi completado até 200 mL. O frasco foi tampado e deixado em repouso por um dia. Posteriormente, a soluçao foi tratada com carvao ativado e filtrado até obter-se uma soluçao translúcida e incolor. O reagente de Schiff obtido foi armazenado em frascos âmbar tampados de modo a nao haver espaço vacante no frasco, sendo armazenado sob refrigeraçao (-4 °C). Estes cuidados no seu armazenamento sao necessários para aumentar o tempo de vida útil do reagente. Confecçao dos papéis indicadores Primeiramente, foi cortado o papel filtro em tamanhos 2x2 cm e 2x4 cm. Entao, foi preenchido o fundo de uma placa de Petri com o reagente de Schiff e, com o auxílio de uma pinça, os papéis foram embebidos na soluçao e, posteriormente, colocados para secar sobre uma superfície recoberta com um filme de polietileno. Após secarem, os papéis impregnados mantêm a sua cor inicial, sem alteraçoes. Quando secos, os papéis foram armazenados em um recipiente fechado e guardados em um freezer com temperatura inferior de -4 °C. Teste geral de detecçao de formol com os papéis impregnados em produtos lácteos e cosméticos Primeiramente, foram preparadas amostras padrao misturando quantidades conhecidas de formol em produtos comerciais (leite, xampu, detergente e condicionador para cabelos) e soluçoes aquosas do aldeído com concentraçoes conhecidas. As amostras, tanto as soluçoes aquosas quanto as de produtos comerciais, foram preparadas com as seguintes concentraçoes de formol: 0; 0,1; 0,5; 1,0,e 5,0 vol%. Entao, foi depositada uma gota de cada amostra sobre o papel indicador preparado, para observaçao da mudança de cor. Teste de detecçao de formol com os papéis impregnados em produtos lácteos Amostras de bebidas lácteas foram submetidas ao teste de detecçao de formol utilizando a matriz celulósica impregnada com o reagente de Schiff. Foram analisadas amostras comerciais de leite integral, leite desnatado, leite achocolatado e bebida láctea de frutas, com amostras isentas de formol comparadas com amostras contaminadas na proporçao de 0,01, 0,1 e 1 vol% de formol. Como referência, em todos os ensaios, uma extremidade do papel impregnado foi tratada com a amostra isenta de formol e, na outra extremidade, a amostra contaminada era colocada, sendo utilizados nestes ensaios os papéis de dimensao 2x4 cm. Teste de detecçao de formol no ar utilizando o papel indicador Para o teste de detecçao de formol no ar foi utilizada uma caixa selada, com quantidade suficiente de formol para saturar o ar dentro da caixa com a concentraçao desejada. Foi utilizada uma caixa de polietileno, com volume interno de 20 L, onde foi colocada uma placa de Petri contendo uma soluçao aquosa de formol em quantidade suficiente para saturar o ar dentro da caixa com a concentraçao desejada. Entao, foi colocada a tampa, de onde estava suspenso um papel impregnado, e foi feita vedaçao com graxa de silicone. Foram utilizadas as concentraçoes de 1, 5, 10, 25, 50 e 100 mg kg-1 de formol no ar, tendo como referência uma caixa teste isenta de formol.
RESULTADOS E DISCUSSAO Obtençao dos papéis impregnados e atividade do reagente de Schiff Para impregnar 100 papéis de 2x2 cm foram utilizados 13 mL do Regente de Schiff, os quais foram destinados para os testes com produtos comerciais. Ao final do processo de impregnaçao, os papéis permaneceram com a cor original branca. É importante ressaltar que o método de imersao utilizado é imprescindível, pois a adiçao do reagente de Schiff sobre a folha de papel por gotejamento possibilita a separaçao cromatográfica do reagente, fazendo com que o indicador se decomponha, formando a p-rosanlina, que tinge a matriz com seu tom rosáceo. Para exemplificar as cores obtidas no uso do reagente de Schiff nos testes realizados, pode-se observar a coloraçao das soluçoes contidas nos diferentes frascos mostrados na Figura 1: (a) contém a p-rosanilina; (b) contém uma mistura de cores de adutos cromóforos derivados do Reagente de Schiff misturado com p-rosanilina; (c) há apenas adutos cromóforos derivados do Reagente de Schiff; e (d) contém adutos cromóforos derivados do Reagente de Schiff em grande concentraçao. É importante observar estes padroes de cores, pois, quando um teste está isento de formol, nenhuma cor é gerada. Entretanto, mediante a degradaçao do Reagente de Schiff in loco, a cor rosácea é observada. Quando uma amostra possui formol, geralmente é formada uma cor levemente roxa, semelhante ao frasco b da Figura 1. Sendo muito alta a concentraçao de formol, a cor da p-rosanilina torna-se pouco perceptível, formando cores tendendo à cor do frasco d da Figura 1.
 Figura 1. Cores das substâncias puras e cores formadas da mistura de cro móforos e da diferença de concentraçoes dos mesmos, onde: (a) p-rosanilina; (b) uma mistura de p-rosanilina e o aduto aminosulfonado; (c) o aduto ami nossulfonado; e (d) aduto aminossulfonado em maior concentraçao. Note que a cor de b corresponde à mistura de a e c
Estabilidade e reatividade dos papéis indicadores Após secos, os papéis indicadores permanecem com a cor original do papel utilizado, que no caso era branca. Quando guardados sob refrigeraçao, sua validade se estendeu por, no mínimo, 4 meses, com sensível perda de detecçao após esse período, em funçao da decomposiçao do reagente de Schiff devido à perda do SO2 na forma de gás. Sem refrigeraçao, a estabilidade é mantida por até duas semanas. Quando nao armazenados adequadamente os papéis, estes escurecem até ficarem com a superfície completamente escura, perdendo a atividade. Os papéis indicadores foram testados inicialmente com soluçoes aquosas de formaldeído, conforme pode ser visto na Figura 2. Foi verificado que para baixas concentraçoes o papel permaneceu incolor e para concentraçoes acima de 0,5 vol% houve sempre a geraçao instantaneamente de cor violeta. Deve-se ressaltar que a intensidade da cor formada é proporcional à quantidade de analíto presente na amostra. No entanto, em testes com amostras contendo concentraçoes superiores a 5 vol%, nao se percebe a olho nu um aumento na intensidade, nao sendo mais possível distingui-la de soluçoes com concentraçoes maiores. Já na ausência do aldeído, nao se observou a formaçao de cores. Um fato que deve ser mencionado é que, quando o teste é realizado com uma amostra isenta de aldeído, pode ocorrer uma decomposiçao do reagente de Schiff, sendo liberada p-rosanilina livre que é carreada pela fase líquida ao longo do papel, gerando lentamente uma cor rosácea na borda. Esse fato se dá em funçao da separaçao cromatográfica que o reagente de Schiff sofre na presença de um eluente advindo da amostra. Porém, nos casos onde a cor rosácea é gerada, ela é facilmente distinguível da coloraçao violeta que se verifica instantaneamente na presença de aldeído, nao havendo riscos de ocorrer um resultado tipo "falso-positivo".
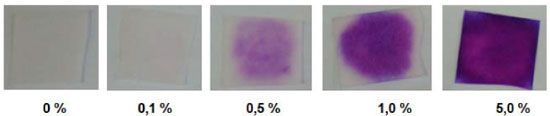 Figura 2. Ensaio realizado utilizando os papéis impregnados, com soluçoes padroes de formol em diferentes concentraçoes (vol%)
Ensaio com os produtos comerciais Quanto às amostras de xampu e detergente, que podem ser vistas respectivamente nas Figuras 3 e 4, observa-se que nas amostras isentas de formol surgiu uma cor rosácea. Já nas amostras contendo 0,1 vol% de formol, foi possível observar uma diferença de tonalidade em comparaçao com as amostras isentas de formol, porém a cor fica claramente distinguível apenas em 0,5 vol%, sendo que a cor formada é violeta. Em ambos os casos é possível observar uma variaçao da tonalidade em funçao da concentraçao até 1 vol%, porém acima de 5 vol% a cor violeta formada torna-se indistinguível. Nesses testes, verificou-se que, quando gotejadas, devido à sua alta viscosidade, as amostras nao sao rapidamente absorvidas pelo papel, como verificado no caso das soluçoes aquosas, mas este fato nao prejudicou a análise. Já nas amostras de condicionador de cabelo (Figura 5), que possui um aspecto cremoso, sua adiçao direta no papel nao é eficiente, sendo necessária a sua diluiçao prévia com água para se conseguir uma viscosidade menor que permite a absorçao mínima pelo papel de modo a formar a cor púrpura. Esses resultados sugerem que, para aplicaçao da técnica a cosméticos com texturas consistentes, se faz necessária a diluiçao da amostra.
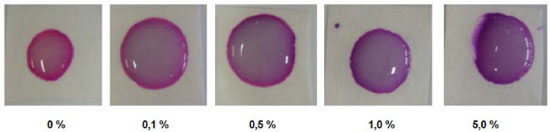 Figura 3. Ensaio realizado utilizando os papéis impregnados, com soluçoes padrao de detergente em diferentes concentraçoes (vol%)
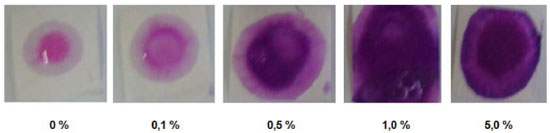 Figura 4. Ensaio realizado utilizando os papéis impregnados, com soluçoes padrao de xampu em diferentes concentraçoes (vol%)
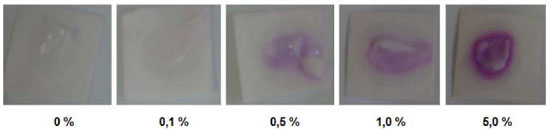 Figura 5. Ensaio realizado utilizando os papéis impregnados, com soluçoes padrao de condicionador em diferentes concentraçoes (vol%)
Nos testes com as amostras de leite, foram observadas cores mais intensas em relaçao às obtidas quando outros produtos foram analisados (veja Figura 6). No teste com a amostra de leite isenta de formol, é possível observar com clareza uma cor rosa formada, relativa à p-rosanilina livre gerada em razao da decomposiçao do reagente de Schiff. Deve-se destacar que no caso das amostras de leite foi possível identificar a contaminaçao a partir de concentraçoes de 0,1 vol%, sendo gerada uma cor violeta muito intensa. No entanto, devido à forte intensidade da cor formada, nao é possível distinguir-se das amostras com concentraçoes de formol superiores.
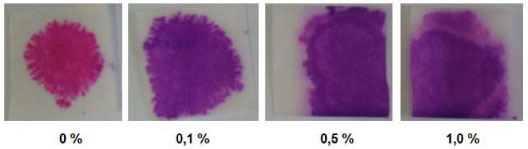 Figura 6. Ensaio realizado utilizando os papéis impregnados com soluçoes padrao de leite integral em diferentes concentraçoes (vol%)
Ensaio com os produtos lácteos Uma vez observado que amostras contendo leite sao mais adequadas para o teste, em funçao da intensa coloraçao das amostras quando em contato com o reagente de Schiff, os testes para averiguar a sensibilidade e robustez do método foram aprofundados. Para tal, foram avaliados diversos produtos lácteos, tais como o leite integral, leite desnatado, leite achocolatado e bebida láctea de frutas. Nesses testes, sobre um mesmo papel impregnado, foi pingado o padrao isento de formol em uma extremidade e, na outra extremidade, o padrao com quantidade conhecida de formol. Foram utilizadas contaminaçoes de formol de 0,01, 0,1 e 1 vol%. Nas amostras de leite integral, que podem ser observadas na Figura 7, como esperado, observa-se claramente a diferença entre uma amostra contaminada e nao contaminada com formol. Surpreendentemente, a contaminaçao com 0,01 vol% de formol apresenta cor claramente distinta do leite isento de formol. Essa amostra indica que um padrao colorimétrico pode ser utilizado como referência, em conjunto com a análise, a fim de certificar os resultados obtidos.
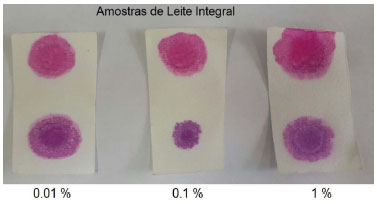 Figura 7. Ensaio realizado utilizando os papéis impregnados com soluçoes leite integral/formol em diferentes concentraçoes de formol em vol%. Na extremidade superior encontram-se os padroes isentos de formol e, nas extremidades inferiores dos papéis, as amostras contaminadas com formol em diferentes concentraçoes
Nas amostras de leite desnatado (Figura 8), observa-se o mesmo comportamento do leite integral, mostrando que nao há diferença significativa entre os produtos em relaçao ao teste de detecçao de formol em questao. É visível também a diferença de cores na presença e ausência de formol, mesmo à concentraçao de 0,01 vol%.
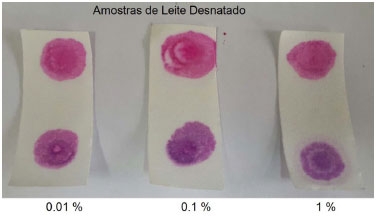 Figura 8. Ensaio realizado utilizando os papéis impregnados com soluçoes leite desnatado/formol em diferentes concentraçoes de formol em vol%. Na extremidade superior encontram-se os padroes isentos de formol e, nas extremidades inferiores dos papéis, as amostras contaminadas com formol em diferentes concentraçoes
Nas amostras de leite achocolatado, na Figura 9, o resultado colorimétrico foi mais discreto em relaçao aos testes anteriores. Ainda é possível observar as cores características das amostras de leite. Entretanto, apenas no halo gerado em torno da área marrom do achocolatado. É importante salientar que a amostra de achocolatado possui cor marrom escura, que gera a mancha central no meio das manchas. Nas bordas da mancha marrom, é possível observar claramente a diferença de cores nas amostras testadas contendo contaminaçao com formol de 0,1 e 1 vol%. Entretanto, no teste com a amostra contaminada com 0,01 vol% de formol, a diferença de cor ficou pouco perceptível, dificultando a interpretaçao do resultado.
 Figura 9. Ensaio realizado utilizando os papéis impregnados com soluçoes leite achocolatado/formol em diferentes concentraçoes de formol (vol%). Na extremidade superior encontram-se os padroes isentos de formol e, nas extremidades inferiores dos papéis, as amostras contaminadas com formol em diferentes concentraçoes
Nos resultados das análises das amostras de bebida láctea de frutas, que podem ser vistas na Figura 10, observa-se um padrao semelhante ao exposto no caso do leite achocolatado, em que a bebida láctea de frutas possui uma tonalidade laranja, que dá origem à mancha laranja central observada nos papéis. Entretanto, ao contrário do exemplo anterior, a distinçao entre as cores de amostras nao contaminadas e contaminadas é perceptível, formando claramente uma cor roxa nas amostras contaminadas, mesmo a 0,01 vol%, sendo distinguível do padrao isento de formol de coloraçao rosácea.
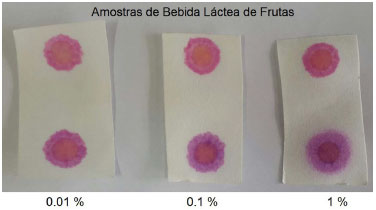 Figura 10. Ensaio realizado utilizando os papéis impregnados com soluçoes bebida láctea de frutas/formol em diferentes concentraçoes de formol em vol%. Na extremidade superior encontram-se os padroes isentos de formol e, nas extremidades inferiores dos papéis, as amostras contaminadas com formol em diferentes concentraçoes
Teste de formol no ar Nos testes realizados com papel indicador em caixas contendo ar com concentraçoes de formaldeído de 0 a 100 mg/kg, foi observado que o papel é sensível à presença do aldeído. Na caixa isenta de formol, o papel indicador permaneceu sem alteraçoes de cor por uma semana. No entanto, para tempos maiores foi verificado o escurecimento do papel, semelhante ao ocorrido quando o mesmo nao é armazenado sob refrigeraçao. Já nas caixas contendo ar com formol foi verificada a formaçao de coloraçao violeta no período de 1 a 2 h, mesmo para concentraçoes de 1 mg/kg. Foi verificado, também, que a intensidade de coloraçao do papel é proporcional tanto à quantidade de formol no ar quanto ao tempo de exposiçao, indicando que existe um controle cinético na absorçao do formol pelo papel indicador. Assim, apesar da eficiência do papel para detectar a presença de formol no ar, nao foi possível estimar um valor de forma quantitativa ou semi-quantitativa da concentraçao, visto que a intensidade da cor varia tanto em funçao do tempo como da concentraçao. Todavia, quando exposto à luz do sol ou a fontes de calor, foi observado que o papel adquire uma cor rosácea, devido à decomposiçao do reagente de Schiff, indicando que o teste nao é adequado para análises em ambientes com essas condiçoes, sendo necessários alguns ajustes para uma aplicaçao direta nessas situaçoes.
CONCLUSAO Todos os diferentes tipos de amostras de produtos comerciais, contaminadas ou nao com formaldeído, quando submetidas ao teste com o papel impregnado, mostraram resultados satisfatórios, confirmando a robustez do método. A versatilidade do papel indicador também permitiu a detecçao de formol no ar, mesmo a baixas concentraçoes. Entretanto, faz-se necessário um maior desenvolvimento do produto para tal aplicaçao. O papel impregnado com o reagente permite a identificaçao colorimétrica de formol em diversos produtos comerciais cosméticos e alimentícios em diferentes concentraçoes, inclusive abaixo de 1 vol% de formol nas amostras. Nenhum dos produtos utilizados gerou interferência na análise, e nao foram necessários pré-tratamentos das amostras, exceto para amostras com aspecto cremoso, confirmando a robustez do método. A mais importante aplicaçao do papel impregnado é na detecçao de formol em leites e derivados de leites, em que as cores podem ser distinguidas facilmente para contaminaçoes de até 0,01 vol% de formol, podendo haver o auxílio de um padrao colorimétrico para a interpretaçao da análise. Conclui-se que foi desenvolvido um produto simples, baseado em materiais renováveis, que atende demandas da populaçao, visando à saúde pública, sendo este um teste simples que pode ser aplicado na triagem de amostras, facilitando atividades de fiscalizaçao ou mesmo sanando dúvidas da populaçao quanto ao uso dos seus produtos diários.
AGRADECIMENTOS Os autores agradecem aos diversos órgaos que têm financiado as pesquisas em combustíveis do LMC-UnB, tais como FAPDF, CNPq, CAPES e FINEP. PAZS, RRS e GBCM. Agradecem ao CNPq e à CAPES pelas bolsas de pesquisa. Finalmente, os autores agradecem aos diversos programas do CDT/UnB que colaboraram com diversas açoes envolvidas no desenvolvimento desta tecnologia de análise e com a sua comercializaçao.
REFERENCIAS 1. Arts, E.; Muijser, H.; Kuper, F.; Woutersen A.; Regul. Toxicol. Pharmacol. 2008, 52, 189. 2. Zhang, L.; Steinmaus, C.; Eastmond, A.; Xin, K.; Smith, T.; Mutat. Res. 2009, 681, 150. 3. Casanova, M.; Heck, H. d’A.; Regul. Toxicol. Pharmacol. 2004, 40, 92. 4. Duong, A.; Steinmaius, C.; McHale, M.; Vaughan, P.; Zhang, L.; Mutat. Res. 2011, 728, 118. 5. Doi, T.; Kajimura, K.; Taguchi, S.; J. Health Sci. 2010, 56, 116. 6. Lefebvre, A.; Meuling, A.; Engel, R.; Coroama, M. C.; Pape, G. R. W.; Nohynek, G. J. ; Regul. Toxicol. Pharmacol. 2012, 63, 171. 7. Weng, X.; Chon, H.; Jiang, H.; Li, D.; Food Chem. 2009, 114, 1079. 8. Wang, S.; Cui, X.; Fang, G.; Food Chem. 2007, 103, 1487. 9. Wang, T.; Gao, X.; Tong, J.; Chen, L.; Food Chem. 2012, 131, 1577. 10. Dales, R.; Liu, L.; Wheeler, J.; Gilbert, L.; Can. Med. Assoc. J. 2008, 179, 145. 11. Bohm, M.; Salem, M.; Srba, J.; J. Hazard. Mater. 2012, 221 - 222, 68. 12. http://www.anvisa.gov.br/cosmeticos/alisantes/escova_progressiva.htm, acessado em Maio de 2017. 13. https://cienciaalimentos.wordpress.com/2013/05/08/materia-e-nota-tcnica-leite-operao-leite-compenado-investiga-fraude-em-leite-transportado-no-rio-grande-do-sul/, acessado em Maio de 2017. 14. http://g1.globo.com/economia/noticia/2014/04/parmalat-e-lider-anunciam-recall-de-300-mil-caixas-de-leite-com-formol.html, acessado em Maio de 2017. 15. http://www.asbra.com.br/noticia/formol-e-encontrado-em-quatro-marcas-de-leite-no-rio-grande-do-sul, acessado em Maio de 2017. 16. Larsen, A.; Jentoft, A.; Greibrokk, T.; Sci. Total Environ. 1992, 120, 261. 17. Cui, X.; Fang, G.; Jiang, L.; Wang, S.; Anal. Chim. Acta 2007, 590, 253. 18. Mohamed, A.; Mubarak, T.; Marestani, H.; Fawy, F.; Talanta 2008, 74, 578. 19. Oliveira, S.; Sousa, T.; Andrade, B.; Talanta. 2007, 73, 561. 20. Mariano, S.; Wang, W.; Brunelle, G.; Bigay, Y.; Tran thi, T-H, Procedia Eng. 2010, 5, 1184. 21. Maruo, Y.; Nakamura, J.; Anal. Chim. Acta 2011, 702, 247. 22. Maruo, Y.; Nakamura, J.; Uchiyama, M.; Higuchi, M.; Izumi, K.; Sensor. Actuator. B. 2008, 129, 544. 23. Robins, H.; Abrams, D.; Pincock, A.; Can. J. Chem. 1980, 58, 339. 24. Martins, C.; Dissertaçao de mestrado, Universidade de Brasília, Brasil, 2012. 25. Suarez, Z.; Martins, C.; INPI nº BR 10 2012 012197 2, 2012. 26. Martins, C.; Montenegro, A.; Suarez, Z.; Quim. Nova 2015, 38, 280. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access





