Educação
|
|
| Cloração mecanoquímica da acetanilida Mechanochemical chlorination of acetanilide |
|
Silvio CunhaI,II,*; Thiago FontesI,II; Daniel Moreira AraújoI,II; Valéria Belli RiattoI,II,#
IInstituto de Química, Universidade Federal da Bahia, Campus de Ondina, 40170-115 Salvador - BA, Brasil Recebido em 06/07/2017 *e-mail: silviodc@ufba.br We described herein a solvent-free synthesis of 4-chloroacetanilide both under hand grinding and mechanical grinding of stoichiometric amounts of acetanilide with trichloroisocyanuric acid. The synthetic approach was developed in the context of undergraduate organic chemistry and is the greener preparation of this compound already described. INTRODUÇÃO A formação experimental em química orgânica vem consolidando a prática da Química Verde (QV) nos cursos da graduação,1 onde os estudantes podem associar o aprendizado das técnicas e transformações tradicionais aos novos aspectos do fazer químico, com ênfase em sustentabilidade.2 Para isto, é necessário o desenvolvimento de experimentos que contemplem, por exemplo, a realização de reação na ausência de solventes3,4 ou empregando o mais verde deles, a água,5,6 bem como o uso de biomassa como material de partida/reagente7 ou aparelhos e técnicas modernas como o uso de micro-ondas,8 e até mesmo técnicas clássicas modernizadas. Neste último aspecto, a mecanoquímica é a nova fronteira da metodologia sintética.9 A mecanoquímica baseia-se na utilização de energia mecânica para promover quebra e formação de ligações devido à alta pressão e aumento da temperatura pelo atrito, geralmente na ausência de solvente, sendo empregada em reações de formação de ligações carbono-carbono, carbono-heteroátomo, oxidação, redução, condensação, acoplamento e na síntese de organometálicos.10 Sua origem remonta a tempos pré-históricos, desde a obtenção do fogo por fricção, evoluindo para a preparação de alimentos pelo processo de moagem e, em química, na realização de reação através da moagem manual com pistilo e almofariz.11 Com o desenvolvimento de equipamentos dedicados para laboratórios, sua aplicação em rotas sintéticas sofisticadas se tornou mais confiável devido ao controle da energia transferida aos reagentes e, assim, maior reprodutibilidade.9 No desenvolvimento de síntese de substância orgânica como experimento didático inserida no contexto da QV, o emprego da mecanoquímica é ainda relativamente escasso, destacando-se a adição de anilinas a naftoquinonas em fase sólida, como descrito por Martinez e colaboradores.12 Apesar dos avanços recentes na elaboração de experimentos inseridos num contexto atual,3-8,12 o treinamento prático do profissional da Química na graduação ainda é majoritariamente centrado em reações entre líquidos ou de um líquido com um sólido, sempre mediadas por solvente. A experiência do graduando no emprego de misturas sólidas em química orgânica é restrita à formação de solução sólida de KBr e substâncias orgânicas na obtenção de pastilhas para análise por infravermelho. Intencionando contribuir para reverter ao menos em parte este cenário, descrevemos aqui a cloração mecanoquímica da acetanilida por meio da moagem manual e em moinho de bolas planetário, para que as novas gerações possam ser introduzidas aos aspectos clássicos e modernos da mecanoquímica orgânica. Cloração da acetanilida A acetanilida é uma molécula camaleônica no ensino de química orgânica experimental, tanto na sua síntese quanto na obtenção de derivados.3 Para ampliar mais ainda o potencial da acetanilida como molécula didática, investigamos sua cloração sob a perspectiva da QV. Embora o cloro gasoso não seja adequado para ser empregado em reações de cloração em aulas experimentais, existem diversos outros reagentes de cloração, como ácido clorossufônico (ClSO3H), tetracloreto de estanho (SnCl4), ácido cloro-succínico, ácido tricloroisocianúrico 1 (ATCI, Esquema 1), Pd(OAc)/CuCl2, dentre outros.13,14 Destas fontes de cloro, o ATCI destaca-se por ser um reagente de baixo custo, de fácil acesso e ambientalmente seguro, já que é um desinfetante de uso doméstico e industrial. Sua estrutura heterocíclica fornece três átomos de cloro, tornando-o altamente vantajoso do ponto de vista de economia atômica, quando comparado a outros reagentes de cloração, razão da multiplicidade de aplicações em síntese orgânica como agente de cloração e/ou oxidação.15 O uso do ATCI tem como vantagem adicional gerar como subproduto o ácido issocianúrico, que não tóxico e é biodegradável.16
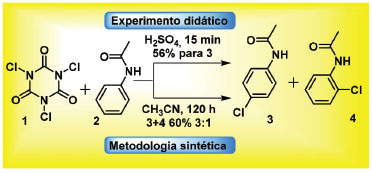 Esquema 1. Monocloração da acetanilida com o ATCI com finalidades didática17 e preparativa15
Bastos e colaboradores descreveram o experimento didático da monocloração da acetanilida empregando o ATCI em ácido sulfúrico como solvente, como intermediário na síntese da para-cloroanilina.17 Há a formação da mistura dos isômeros orto e para, mas o isômero para precipita preferencialmente, Esquema 1. Investigando o potencial sintético do ATCI, Mendonça e Mattos conseguiram realizar a mesma transformação, eliminando o inconveniente uso do ácido sulfúrico como solvente da reação, substituindo-o por acetonitrila.13 Apesar deste avanço, o experimento em meio neutro parece não ser diretamente transponível para o cenário de uma aula, pois o tempo de reação passa de 15 minutos em H2SO4, para 5 dias em CH3CN, e ainda há formação de misturas dos isômeros. Em função das características ambientalmente corretas do ATCI, que o tornam um reagente muito apropriado para aulas experimentais de química orgânica verde, e da recorrência da acetanilida como molécula pedagógica,3 o desenvolvimento de um experimento de cloração da acetanilida com o ATCI foi aqui investigado empregando mecanoquímica. Nesta abordagem, os resultados da reação sem solvente podem ser diretamente comparados com aqueles relatados com o uso de solvente, no experimento de graduação previamente descrito.17 Empregamos tanto equipamento dedicado para laboratório quanto moagem manual, de forma a tornar o experimento executável em qualquer laboratório de ensino que não disponha do equipamento, Figura 1. Com o moinho de bolas planetário18 se tornou necessário investigar algumas varáveis inerentes à mecanoquímica. Dessa forma, para definir as condições exequíveis numa aula, variou-se a rotação do moinho de esferas (350 e 500 rpm) e o tempo reacional (30, 60 e 90 min) e também a escala da reação (de 1 a 5 mmol). Como o ATCI ataca o aço inox, o estudo foi conduzido em vaso reacional revestido com ágata.
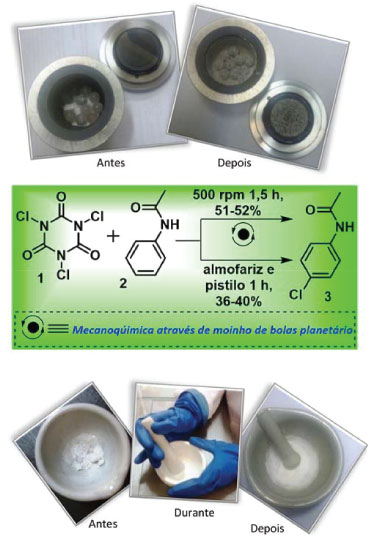 Figura 1. Síntese da 4-cloroacetanilida via mecanoquímica e comparação dos aspectos dos sólidos na moagem com moinho de bolas planetário (acima) e na moagem manual (abaixo)
Em função do ATCI ter a capacidade de transferir até três átomos de cloro, a proporção estequiométrica na reação da monocloração de 1 com 2 é 1:3, Esquema 2. Todavia, a proporção empregada dos reagentes 1 e 2 é 1:2,2 no experimento tradicional de graduação com H2SO4 como solvente, rendendo 3 em 56%.17 No procedimento aqui proposto, a proporção é 1:3,3, mais próxima da estequiométrica como preconiza a QV. A condição mecanoquímica que apresentou resultados reprodutíveis foi 500 rpm, 10 esferas de 10 mm e 90 minutos de reação, sendo obtido sempre a 4-cloacetanilida em 36% de rendimento na escala reacional de 5 mmol da acetanilida, Esquema 2. Como o rendimento obtido com a proporção 1:3,3 foi relativamente pequeno, quando comparado ao que emprega H2SO4 como solvente (56%), buscamos melhorar o rendimento aumentando o volume do solvente extrator (AcOEt) de 20 para 30 mL. Nestas condições, a 4-cloroacetanilida foi obtida com 52% de rendimento. A diminuição do número de esferas para 5 não afeta significativamente o rendimento (51%).
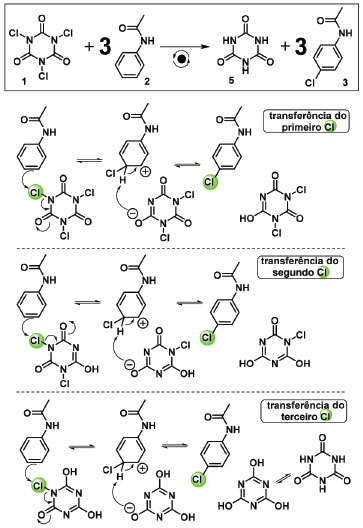 Esquema 2. Equação balanceada da síntese da 4-cloroacetanilida e possível mecanismo de reação da monocloração da acetanilida com o ATCI
A melhor condição reacional no moinho de bolas planetário foi aplicada na aula prática em uma turma de 12 estudantes, e os mesmos estudantes também realizaram a síntese empregando moagem manual na mesma escala de reação e proporção entre o ATCI e a acetanilida. Na Figura 1 são apresentados os aspectos dos sólidos antes e depois da reação nas duas modalidades de moagem investigadas. Na moagem manual, a cada dez minutos os dois componentes da equipe se alternam no processo de fricção. O rendimento da moagem manual foi inferior ao da moagem no moinho de bolas planetário, o que pode estar associado à irregularidade da força e velocidade de fricção, que varia muito entre os estudantes. Os rendimentos foram entre 40-36% dependendo do volume de solvente extratror (20 ou 30 mL) e do procedimento de recristalização (ver experimental). Destacamos que, mesmo com esta limitação no rendimento, ambas as formas de moagens são aplicáveis com sucesso na aula. Uma proposta didática dos aspectos mecanísticos da substituição eletrofílica aromática promovida pelo ATCI foi elegantemente elaborada por Vasconcellos e Lima Junior, baseados em cálculos teóricos.19 Para as reações em meio neutro, como é o caso da aqui executada no estado sólido, a formação preferencial do produto para-substituído, empregando anéis aromáticos com grupos doadores de elétrons, é explicada em função da menor energia entre os reagentes e os complexos σ do ataque na posição para, quando comparados aos correspondentes complexos σ dos ataques em orto e meta. Adicionalmente, a seletividade ao ataque na posição para em detrimento da orto pode estar também associada ao volume do eletrófilo ATCI, levando a um sinergismo de efeitos. Uma proposta das etapas para monocloração é apresentado no Esquema 2.
CONCLUSÃO Desenvolvemos a primeira síntese via mecanoquímica da 4-cloroacetanilida como uma alternativa eficaz para aula experimenal de química orgânica verde. Este experimento amplia o espectro de aplicações do ATCI e da acetanilida e insere a mecanoquímica com e sem aparelho dedicado na formação dos profissionais da Química.20,21 Em comparação com a proposta didática anterior,17 a aqui descrita tem também as vantagens de empregar quantidades praticamente estequiométricas dos reagentes e eliminar o uso do ácido sulfúrico como solvente com rendimentos adequados, demonstrando que é possível tornar as aulas experimentais mais próximas dos princípios da Química Verde.
PARTE EXPERIMENTAL A acetanilida foi preparada e purificada pelos estudantes a partir da acetilação da anilina em aula experimental realizada previamente e foi novamente recristalizada em água. O ATCI utilizado da marca Q-Clor® (em pastilhas) foi comprado numa loja de produtos para piscinas e empregado como obtido, após pulverização manual em gral e pistilo. Os pontos de fusão foram determinados em um aparelho de placa aquecida Microquímica MQAPF 301 e não foram corrigidos. Os espectros na região do infravermelho foram obtidos na forma de disco de KBr em um aparelho SHIMADZU IR Affinity-1. O equipamento mecanoquímico empregado foi o moinho de bolas planetário Restch, modelo PM100, reator de 50 mL revestido com ágata e esferas de 10 mm de ágata. Síntese mecanoquímica da 4-cloroacetanilida via moagem automática Em reator de ágata de 50 mL do moinho planetário, adicionar 10 esferas de ágata de 10 mm de diâmetro e 0,68 g (5 mmol) de acetanilida 2 e 0,34 g (1,5 mmol) de ácido tricloroisocianúrico 1 previamente pulverizado. Fechar o reator e fixar no moinho. Ajustar a rotação para 500 rpm e o tempo para 90 minutos, com mudança de sentido de giro da rotação após 45 minutos e repouso de 1 minuto. Ao término retirar o reator do moinho, abrir a tampa e adicionar 10 mL de acetato de etila. Com auxílio de uma espátula, desprender o sólido das paredes do reator da tampa e das esferas. Verter a suspensão e as esferas para um béquer; lavar o reator com mais duas porções de 10 mL de acetato de etila e transferir para o béquer. Acoplar um funil de vidro de colo curto a uma ampola de separação. Com movimentos circulares suaves, agitar levemente o béquer e transferir a suspensão e as esferas para o funil de vidro. Retirar o funil de vidro de colo curto com as esferas. Extrair a suspensão uma vez com 10 mL de solução saturada de NaHCO3 e duas vezes com 10 mL de água. Separar as fases e evaporar o solvente orgânico num rotaevaporador. Para recristalizar o sólido impuro, adicionar 20 ml de água e aquecer numa manta de aquecimento até ebulição. Adicionar pequenas porções de etanol até completa solubilização a quente. Resfriar a solução amarela ao ar e depois em banho de gelo e filtrar o sólido branco num funil de Buchner. Secar ao ar por uma semana, p.f. 176,6-177,4 ºC (Lit.22 178 ºC). Determinar o rendimento e obter o espectro na região do infravermelho. Calcular o fator E e comparar com a síntese com ácido sulfúrico como solvente.17,24 Síntese mecanoquímica da 4-cloroacetanilida via moagem manual Em um almofariz de porcelana adicionar 0,68 g (5 mmol) de acetanilida 2 e 0,35 g (1,5 mmol) do ácido tricloroisocianúrico 2 previamente pulverizado. Com auxílio de um pistilo de porcelana, macerar os reagentes com movimentos circulares até o tempo total de 60 minutos (procedimento realizado em dupla com revezamento a cada 10 minutos). Após 20 minutos, raspar com uma espátula metálica a mistura de sólidos aderida às paredes do almofariz e continuar a moagem. Ao término, adicionar 10 mL de acetato de etila no almofariz. Com auxílio de uma espátula, desprender o sólido das paredes do almofariz e do pistilo e verter a suspensão para uma ampola de separação previamente acoplada a um funil de vidro de colo curto. Repetir a lavagem com duas porções de 10 mL de acetato de etila. Extrair as fases orgânicas reunidas na ampola uma vez com 10 mL solução saturada de NaHCO3 e duas vezes com 10 mL de água. Separar as fases e evaporar o solvente orgânico num rotaevaporador. Para recristalizar o sólido impuro, adicionar 20 mL de água e aquecer numa manta de aquecimento até ebulição.Adicionar pequenas porções de etanol até completa solubilização a quente. Resfriar a solução amarela ao ar e depois em banho de gelo e filtrar o sólido branco num funil de Buchner. Secar ao ar por uma semana, p.f. 175,1-176,4 ºC (Lit.22 178 ºC). Determinar o rendimento e obter o espectro na região do infravermelho. Calcular o fator E e comparar com a síntese com ácido sulfúrico como solvente.17,24
MATERIAL SUPLEMENTAR Fotos das etapas das reações mecanoquímicas e espectro na região do infravermelho estão disponíveis em http://quimicanova.sbq.org.br, na forma de arquivo PDF, com acesso livre.
AGRADECIMENTOS Os autores agradecem o suporte financeiro do Conselho Nacional de Desenvolvimento Científico e Tecnológico - CNPq, Coordenação de Aperfeiçoamento de Pessoal de Nível Superior - CAPES, e Fundação de Amparo à Pesquisa do Estado da Bahia - FAPESB. Também agradecemos as bolsas de doutorado da CAPES a T. F. H. Silva e D. M. Araújo, e ao CNPq a bolsa de produtividade em pesquisa de S. Cunha.
REFERÊNCIAS 1. Corrêa, A. G.; Zuin, V. G.; Química Verde: Fundamentos e Aplicações, EdUFSCar: São Carlos, 2009; Pinto, C. P.; Silva, B. V.; A Química Perto de Você: Experimentos de Química Orgânica, Sociedade Brasileira de Química: São Paulo, 2012; Corrêa, A. G.; de Oliveira, K. T.; Paixão, M. W.; Brocksom, T. J.; Química Orgânica Experimental: Uma Abordagem de Química Verde, Editora Campus-Elsevier: São Paulo, 2016. 2. Corrêa, A. G.; Zuin, V. G.; Ferreira, V. F.; Vazquez, P. G.; Pure Appl. Chem. 2013, 85, 1643; Zandonai, D. P.; Saqueto, K. C.; Abreu, S. C. S. R.; Lopes, A. P.; Zuin, V. G.; Rev. Virtual Quim. 2014, 6, 73. 3. Cunha, S.; Costa, O. B. S.; Santana, L. L. B.; Lopes, W. A.; Quim. Nova 2015, 38, 874. 4. Esteb, J. J.; Stockton, M. B.; J. Chem. Educ. 2003, 80, 1446; Aktoudianakis, E.; Chan, E.; Edward, A. R.; Jarosz, I.; Lee, V.; Mui, L.; Thatipamala, S. S.; Dicks, A. P.; J. Chem. Educ. 2009, 86, 730; Esteb, J. J.; Gligorich, K. M.; O'Reilly, S. A.; Richter, J. M.; J. Chem. Educ. 2004, 81, 1794; Palleros, D. R.; J. Chem. Educ. 2004, 81, 1345; Leung, S. H.; Angel, S. A.; J. Chem. Educ. 2004, 81, 1492; Goldstein, S. W.; Cross, A. V.; J. Chem. Educ. 2015, 92, 1214. 5. da Silva, F. M.; Jones Jr, J.; Quim. Nova 2001, 24, 646. 6. Hino, K. N.; Omori, A. T.; Quim. Nova 2015, 38,156; Morsch, L. A.; Deak, L.; Tiburzi, D.; Schuster, H.; Meyer, B.; J. Chem. Educ. 2014, 91, 611; Cunha, S.; Marques, M. F.; Rocha, V.; Quim. Nova 2013, 36, 1453; Cunha, S.; Santana, L. L. B.; Quim. Nova 2012, 35, 642; da Silva, B. N. M.; Bastos, R. S.; Silva B. V.; Pinto, A. C.; Quim. Nova 2010, 33, 2279. 7. Omori, A. T.; Portas, V. B.; Oliveira, C. S.; Quim. Nova 2012, 35, 435; Cunha, S.; Lustosa, D. M.; Conceição, N. D.; Fascio, M.; Magalhães, V.; Quim. Nova 2012, 35, 638; Ferreira, V. F.; Rocha, D. R.; Silva, F. C.; Quim. Nova 2009, 32, 623. 8. Soares, P.; Fernandes, C.; Chavarria, D.; Borges, F.; J. Chem. Educ. 2015, 92, 575; Cunha, S.; Santos Filho, R. F.; Riatto, V. B.; Dourado, G. A. A.; Quim. Nova 2013, 36, 190; Konrath, E. L.; Piedade, M.; Eifler-Lima, V.; Quim. Nova 2012, 35, 1887; Teixeira, E. F.; dos Santos, A. B.; Bastos, R. S.; Pinto A. C.; Kümmerle, A. E.; Coelho, R. R.; Quim. Nova 2010, 33, 1603; Zovinka, E. P.; Stock, A. E.; J. Chem. Educ. 2010, 87, 350. 9. Hernández, J. G.; Bolm, C.; J. Org. Chem. 2017, 82, 2733; Do, J.-L.; Loots, L; Friščić, T.; ACS Cent. Sci. 2017, 3, 13; Tan, D.; Loots, L.; Friščić, T.; Chem. Commun. 2016, 52, 7760; Wang, G.-W.; Chem. Soc. Rev. 2013, 42, 7668. 10. Wixtrom, A.; Buhler, J.; Abdel-Fattah, T.; J. Chem. Educ. 2014, 91, 1232; Berry, D. E.; Carrie, P.; Fawkes, K. L.; Rebner, B.; Xing, Y.; J. Chem. Educ. 2010, 87, 533. 11. Takacs, L.; Chem. Soc. Rev. 2013, 42, 7649. 12. Martinez, S. T.; Silva, B. V.; Pinto, A. C.; Ferreira, V. F.; da Silva, F. C.; Quim. Nova 2012, 35, 858. 13. Mendonça, G. F.; de Mattos, M. C. S.; Quim. Nova 2008, 31, 798. 14. Mishra, A. K.; Nagarajaiah, H.; Moorthy, J. N.; Eur. J. Org. Chem. 2015, 12, 2733. 15. Cunha, A. C.; da Paixão, F. M.; de Souza, M. C. B. V.; Ferreira, V. F.; Quim. Nova 2006, 29, 520; Tilstam, U.; Weinmann , H.; Org. Proc. Res. Dev. 2002, 6, 384; Wengert, M.; Sanseverino, A. M.; de Mattos, M. C. S.; J. Braz. Chem. Soc. 2002, 13, 700. 16. Huthmacher, K.; Most, D.; Cyanuric Acid and Cyanuric Chloride, Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH: Weinheim, 2005. 17. Bastos, R. S.; da Cunha, A. S.; da Silva, L. C.; de Oliveira, C. C. P.; Rezende, C. M; C.Pinto, A. C.; Quim. Nova 2008, 31, 172. 18. Tilstam, U.; Weinmann, H.; Org. Process Res. Dev. 2002, 6, 384; Wengert, M.; Sanseverino, A. M.; de Mattos, M. C. S.; J. Braz. Chem. Soc. 2002, 13, 700. 19. Para representar a moagem realizada em moinho de bolas planetário e diferenciar das outras modalidades de moagem, estamos sugerindo o símbolo descrito na Figura 2: um disco preenchido circundado por duas setas curvas, onde o disco representa a moagem por moinho de bolas e as duas setas curvas representam, cada uma, um dos movimentos que ocorre no moinho planetário, o movimento em torno do próprio eixo do vaso reacional e o movimento deste em torno do centro do aparelho. 20. Cunha, S.; Santana, L. L. B.; J. Braz. Chem. Soc. 2017, 28, 1137. 21. Para uma proposta de construção de moinho, ver:de Paula, L. D.; Alves, A. C.; Alves, H. C. S.; Ribeiro, E. A.; Madurro, A. G. B.; Madurro, J. M.; Quim. Nova 2014, 37, 736. 22. Vasconcellos, M. L. A. A.; Lima Junior, C. G.; Quim. Nova 2009, 32, 244. 23. Margetić, D.; Štrukil, V.; Mechanochemical Organic Synthesis, Elsevier: Amsterdam, 2016. 24. Quando empregamos a mistura água:etanol 70:30 como indicado na referência 17, o rendimento foi sempre ligeiramente inferior. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access





