Educação
|
|
| EXTRAÇÃO DO R-(+)-LIMONENO A PARTIR DAS CASCAS DE LARANJA: AVALIAÇÃO E OTIMIZAÇÃO DA VERDURA DOS PROCESSOS DE EXTRAÇÃO TRADICIONAIS EXTRACTION OF R-(+)-LIMONENE FROM ORANGE PEELS: ASSESSEMENT AND OTIMIZATION OF THE GREENNESS OF TRADITIONAL EXTRACTION PROCESSES |
|
Tânia C. M. PiresI; Maria Gabriela T. C. Ribeiro*,I; Adélio A. S. C. MachadoII
I. LAQV/REQUINTE, Departamento de Química e Bioquímica, Faculdade de Ciências da Universidade do Porto, Rua do Campo Alegre 687, Porto 4169-007, Portugal Recebido em 29/07/2017 *e-mail: gribeiro@fc.up.pt This article reports a study, performed in educational context, to increase the greenness of the extraction of R-(+)-limonene from orange peels. Protocols from the literature were evaluated with the green star (GS)metric and new protocols, based in them, were designed to increase the overall greenness. These were tested in the laboratory and their greenness was assessed by traditional greenness metrics and metrics inspired in the industrial activity. Results showed that the steam distillation technique presents the largest overall greenness when evaluated by the GS, because organic solvents are not involved, but mass and energy metrics indicate that the extractions by solvent techniques are greener. This conflict denotes the complexity of the concept of chemical greenness and the need of using several types of metrics when greenness evaluation is at stake. The results show that the inclusion of experiments on the R-(+)-limonene extraction in the educational laboratory is efficient to show the difficulties of assessing the greenness of chemistry and of implementing Green Chemistry. INTRODUÇAO A escassez de recursos naturais e a ameaça de problemas ambientais, tanto a elevada produçao de resíduos, muitos dos quais tóxicos, como os efeitos dos poluentes decorrentes da atividade humana, requerem modalidades inovadoras de implementaçao da química com menos impactos sobre o ambiente. 1,2 Como consequência, nos últimos anos, observa-se um interesse crescente no uso de matérias-primas renováveis que possam ser uma alternativa aos recursos fósseis convencionais, contribuindo para a criaçao de um novo paradigma na indústria química, a bioindústria. 1,3 A bioindústria inova relativamente à indústria convencional através da utilizaçao de biomassa e respetivos resíduos como matéria-prima renovável, que é convertida em produtos comercializáveis através de tecnologias sustentáveis e de baixo impacto ambiental, em alternativa aos derivados de petróleo. 1 A biomassa, sendo disponível em larga quantidade e renovável, merece presentemente muita e diversificada atençao como matéria-prima para a indústria química. 1-6 O termo bioindústria engloba as instalaçoes da indústria química que usam biomassa como matéria-prima, havendo presentemente muito interesse em desenvolver e implementar um conceito mais amplo, de natureza sistémica, o de biorrefinaria. A biorrefinaria, analogamente a uma refinaria de petróleo que inclua instalaçoes de indústria petroquímica, que produz vários combustíveis e substâncias a partir do petróleo, é um agrupamento de instalaçoes de processos de conversao de biomassa em biocombustíveis, produtos químicos e energia, permitindo um maior aproveitamento da biomassa. 1,7 Um exemplo de biorrefinaria é a produçao de bioetanol, que pode ser usado quer como combustível, quer como reagente de base ("platform") no fabrico de outros produtos químicos. 1,3 Atualmente, procura-se desenvolver biorrefinarias que utilizem a biomassa nos resíduos produzidos na cadeia de fornecimento de alimentos como matéria-prima, para minimizar a competiçao com a indústria alimentar pela biomassa virgem. 7 Um exemplo refere-se à biomassa das cascas dos citrinos, resíduos resultantes do processamento de laranjas para a produçao de sumos, que apresenta elevado potencial para o desenvolvimento de biorefinarias. 8-10 Entre os produtos químicos que se podem obter da biomassa, sao importantes os óleos essenciais, amplamente utilizados em vários domínios da atividade industrial. Por exemplo, devido às suas características em nível sensorial, mas também pela sua açao antibacteriana e fungicida, sao usados nas indústrias da cosmética, perfumaria, alimentar e farmacêutica. 11-14 Os resíduos resultantes do processamento de laranjas permitem a obtençao de um óleo essencial e do seu principal componente, R-(+)-limoneno (a seguir designado, mais simplesmente, por limoneno), bem como de outros produtos, nomeadamente bioetanol e nanocelulose. 15 Os citrinos representam um importante papel na indústria alimentar, principalmente na produçao de sumos. Mundialmente, estima-se que a produçao de citrinos ronde os 94,8 milhoes de toneladas por ano, sendo o Brasil o líder mundial. A nível global, estima-se que 31,2 milhoes de toneladas de citrinos sao processadas industrialmente por ano, produzindo 15,6 milhoes de toneladas de resíduos. 1 Os principais componentes dos resíduos húmidos das cascas de citrinos sao água (80% em peso), açucares, celulose e hemicelulose, pectina e limoneno. 1 Os óleos essenciais dos citrinos sao removidos das cascas antes de estas serem depositadas no ambiente, destacando-se o óleo de laranja. 1,15,16 As principais utilizaçoes do óleo de laranja sao a aromatizaçao de bebidas e produtos de confeitaria, a utilizaçao como fragrância em perfumes, sabonetes e produtos para o lar, e a sua purificaçao para obtençao do seu principal componente com elevado grau de pureza, o limoneno. Este, presente em percentagem entre 90 e 95%, é usado em larga escala em variadas aplicaçoes:17-19 como reagente de base da indústria química para a síntese de compostos com estruturas semelhantes como, por exemplo, carveol, carvona, α-terpineol, álcool perílico e ácido perílico;1 no fabrico de borracha e tintas, e como agente dispersante para óleos,20 componente de óleos essenciais artificiais21 e solvente para resinas. 20 Estudos recentes exploraram a produçao de poliamidas e poliuretanos renováveis a partir do limoneno. 22 No entanto, a maior utilizaçao do limoneno, que tem incentivado o crescimento da sua extraçao, é como agente de limpeza, tanto em nível industrial como doméstico, uma vez que é ambientalmente seguro e mais eficaz que as os agentes de limpeza tradicionais. Assim, além de usado na produçao de produtos de limpeza domésticos, é empregado como agente de limpeza nas indústrias petrolífera, automóvel, de pavimentaçao e eletrónica. 23 O limoneno tem um forte poder inseticida sendo, por isso, também bastante usado no fabrico de produtos com essa funçao. 24-26 Como solvente, devido à sua baixa toxicidade, o limoneno pode substituir uma grande variedade de substâncias como, por exemplo, aguarrás mineral ("white spirits"), butanona, tolueno, xileno, éteres de glicol e solventes orgânicos clorados e fluorados, tal como os CFC's, cujo uso foi proibido. 18 O limoneno tem também aplicaçoes na indústria farmacêutica, nao só como solvente na síntese de compostos químicos, mas também como princípio ativo, uma vez que exibe baixa toxicidade para a saúde humana. É um solvente do colesterol e, como tal, tem sido utilizado na dissoluçao de cálculos biliares contendo colesterol, bem como na neutralizaçao da azia (ácido gástrico); e exibe também atividade quimopreventiva contra vários tipos de cancro. 27-29 O elevado valor comercial do óleo de laranja (e do limoneno, seu principal componente) devido à ampla aplicaçao industrial e ao interesse da utilizaçao de biomassa como matéria-prima renovável, sugerem que o estudo comparativo dos processos da sua extraçao das cascas de laranja será interessante no contexto do ensino da Química Verde (QV),30,31 parecendo especialmente adequado para a prática de métricas de avaliaçao da verdura química, dada a variedade de técnicas alternativas usadas. As três principais técnicas de extraçao industrial das fragrâncias naturais e óleos essenciais sao: (i) destilaçao por arrastamento de vapor, técnica que consiste na utilizaçao do vapor de água para destilar os componentes do óleo essencial a uma temperatura inferior a 100 ºC (após a condensaçao da fase de vapor, o óleo separa-se da fase aquosa, uma vez que sao imiscíveis, o que facilita a sua remoçao); (ii) separaçao mecânica, em que o óleo é removido da casca por processos mecânicos como prensagem, raspagem ou perfuraçao da casca; e (iii) extraçao com solventes, que consiste na extraçao das fragrâncias voláteis dos materiais naturais utilizando solventes nao polares, e.g. tolueno, hexano e éter de petróleo. 21 O óleo de laranja é obtido industrialmente por extraçao mecânica da casca de laranja, sendo a prensagem das cascas para a extraçao do óleo frequentemente combinada com a produçao de sumo. Uma revisao bibliográfica na literatura educacional sobre os processos de extraçao do óleo de laranja/limoneno usados em aulas laboratoriais32-36 para obtençao do óleo e sua caracterizaçao, no contexto do isolamento de produtos naturais, mostrou que, para além da utilizaçao das técnicas clássicas de hidrodestilaçao ou destilaçao por arrastamento de vapor e extraçao com solvente, foram propostos outros processos: extraçao a microescala;37 extraçao do limoneno no contexto da síntese de outros produtos (e.g. (-)-carvona38 e α-terpineol39), que o usam como reagente estequiométrico; bem como, no contexto da QV, isolamento do limoneno utilizando dióxido de carbono líquido como solvente, para ser utilizado no laboratório de química analítica. 40 Por outro lado, na revista Green Chemistry foram publicadas propostas de novos procedimentos de extraçao do óleo de laranja: o uso de líquidos iónicos como solventes de extraçao;11 a utilizaçao de solventes mais benignos na extraçao, como o dióxido de carbono líquido,41 óleo alimentar e polímeros (polietilenoglicol e polipropilenoglicol);42 e o uso de processos hidrotérmicos com micro-ondas de baixa temperatura. 7 Estes estudos mostram preocupaçao em obter processos mais verdes para a extraçao do óleo de laranja,11,40-42 mas nao incluem qualquer referência à importância da avaliaçao e análise da verdura dos processos tradicionais e alternativos. O Brasil lidera mundialmente a produçao de laranjas e de suco de laranja1,16 e é um grande produtor de óleos essenciais, nomeadamente de óleos de citrinos. Neste contexto, faz sentido incluir a extraçao do óleo de laranja e sua purificaçao nos programas das disciplinas experimentais de Química no Brasil. 39 Por outro lado, o estudo laboratorial dos diversos processos tradicionais de extraçao do óleo de laranja permite promover a introduçao da QV nos laboratórios de ensino pré-universitários e universitários, mediante a análise da verdura química com diversos tipos de métricas. Assim sendo, é aliciante tratar este tema em contexto educacional com vista a contribuir para o desenvolvimento de competências verdes dos alunos, cada vez mais importantes para o seu futuro profissional,43,44 no quadro presente em que se procura promover um desenvolvimento mais sustentável. Por estas razoes, o presente trabalho teve como objetivo global investigar a verdura dos processos vigentes de extraçao do óleo de laranja, tendo em vista a sua aplicaçao no laboratório educacional. Em suma, mais concretamente, os objetivos específicos deste trabalho foram: 1) avaliar a verdura química de diferentes protocolos publicados para extraçao do óleo de laranja, com vista a identificar quais sao os processos tradicionais mais verdes; e 2) investigar a sua otimizaçao, utilizando intensivamente métricas de verdura tradicionais, bem como outras de "inspiraçao industrial", para realizar uma avaliaçao multidimensional da verdura.
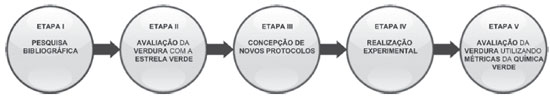
METODOLOGIA O trabalho desenvolveu-se em cinco etapas, apresentadas a seguir (ver a Figura 1).
Etapa I - Pesquisa bibliográfica A pesquisa bibliográfica de protocolos experimentais referentes à extraçao do óleo essencial de laranja e/ou do limoneno a partir da casca de laranja foi realizada no Journal of Chemical Education, na Química Nova e em livros de experiências de Química Orgânica. Os protocolos encontrados foram de dois tipos: os que partiam das cascas de laranja como matéria-prima, que utilizavam dois processos de extraçao diferentes, destilaçao por arrastamento de vapor (Figura 2, Processo 1, seis protocolos)26,32,34,38,39,45,46 e extraçao com solvente orgânico a frio (Figura 2, Processo 2, três protocolos). 33,46,47 Por outro lado, foram encontrados protocolos que faziam apenas a purificaçao de óleo de laranja comercial para obtençao do limoneno (Figura 2, Processo 3, dois protocolos). 48
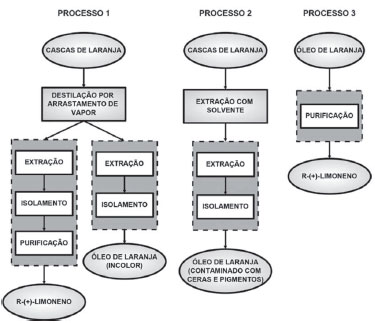 Figura 2. Esquema resumo dos diferentes tipos de processos nos protocolos da bibliografia (os retângulos representam operaçoes; as elipses, materiais; os retângulos a tracejado, envolvem as fases de cada um dos processos)
Etapa II - Avaliaçao da verdura dos protocolos da literatura com a métrica estrela verde Os protocolos referentes aos Processos 1 e 2 foram analisados considerando separadamente três fases: (i) extraçao do óleo essencial - remoçao deste da casca das laranjas; (ii) isolamento - separaçao do óleo da água e/ou dos solventes utilizados; e (iii) purificaçao (quando incluída) - obtençao do limoneno com pureza aumentada. No caso dos protocolos que partem do óleo de laranja comercial só existe esta última fase. Mais informaçao sobre as diversas fases é fornecida na Parte experimental. Para todos os protocolos de cada processo foi efetuada a análise da verdura do processo global e de cada fase. Esta avaliaçao individualizada das fases, realizada com a métrica holística estrela verde (EV)49-51 (ver a secçao Métricas), teve como objetivo esclarecer a forma como cada fase afeta a verdura global. Etapa III - Conceçao de novos protocolos Após a análise da verdura, verificou-se que todos os protocolos do processo 2 apresentavam uma verdura muito limitada, pelo que se optou por desenhar novos protocolos e testar novos solventes na extraçao do óleo de laranja para tentar melhorar a verdura. Etapa IV - Realizaçao experimental dos protocolos selecionados Nesta etapa realizou-se experimentalmente a extraçao do óleo de laranja utilizando o protocolo avaliado como o mais verde para o processo 1, bem como os protocolos desenhados no trabalho para aumentar a verdura do processo 2. Para o processo 3 selecionou-se o protocolo mais verde, purificando-se uma amostra de óleo de laranja comercial (Sigma-Aldrich, ref. W282537), a seguir designada, para simplificar, por amostra comercial. Etapa V - Avaliaçao da verdura utilizando métricas da Química Verde Nesta etapa procedeu-se a avaliaçao da verdura dos protocolos realizados experimentalmente utilizando nao só a EV, mas também métricas quantitativas de massa, energia e tempo, descritas a seguir.
MÉTRICAS As métricas usadas sao apresentadas na Tabela 1, na qual se incluem as expressoes para o seu cálculo.

A literatura tem usado11,12,21,37 o termo rendimento para indicar a percentagem de bioproduto útil extraído da biomassa (neste caso percentagem em peso de óleo essencial extraído de um material natural), mas este rendimento nao coincide com a definiçao de rendimento tradicional para as reaçoes químicas. Recentemente, foi proposto o termo eficiência material (ME, do inglês "Material Efficiency") para designar a referida grandeza em estudos da extraçao de produtos químicos da biomassa,52,53 mas aqui propôe-se o termo eficiência material de biomassa (BME, do inglês "Biomass Material Eficiency") para explicitar a particularidade de a eficiência material se referir à biomassa. Quando vários produtos sao extraídos da biomassa em paralelo, a grandeza é definida para o seu conjunto, isto é, dividindo a massa total dos produtos úteis extraídos pela massa de biomassa de partida. O fator E é uma métrica da quantidade de resíduos produzidos, definida como a razao entre a massa total de resíduos e a massa de produto obtido (o seu valor ideal é zero, que ocorre se nao houver produçao de quaisquer resíduos). 52,54 A água é geralmente ignorada neste cálculo, o que foi seguido neste trabalho. O fator E, sendo uma métrica normalizada pelo produto, pode ser expresso como uma soma de parcelas referentes aos diversos tipos de resíduos. 55 No caso presente, haverá uma parcela, o fator EBIO, referente a resíduos de biomassa, e outra, o fator ENBIO, referente aos outros resíduos, sendo fator E = fator EBIO + fator ENBIO. A métrica BME está relacionada com a métrica parcial de quantidade de resíduos provenientes da biomassa, sendo BME = 1/(Fator EBIO + 1). Esta expressao é útil para verificar a correçao dos valores calculados para as duas métricas (ver Tabelas 6S, 8S e 10S do Material Suplementar). As métricas intensidade de energia (EI), intensidade de tempo (TI) e "throughput"56 (ou "velocidade" de produçao, melhor taxa de produçao, a quantidade de massa de produto obtido por unidade de tempo) sao métricas de utilizaçao industrial, habitualmente ausentes no ensino, mas foram usadas neste trabalho para trazerem para o contexto educacional questoes centrais como a utilizaçao de energia e a importância que a duraçao dos processos têm do ponto de vista da economia do processo industrial, devido à sua influência nos custos de produçao. Assim, é importante chamar a atençao dos estudantes para essas variáveis. EI é a razao entre a energia utilizada e a massa do produto obtido e TI a razao entre o tempo utilizado e esta mesma massa. Como na indústria se procura maximizar a velocidade de obtençao do produto (throughput), um dos fatores mais importantes para o custo de produçao,57,58 para o seu cálculo exige-se o conhecimento do tempo das operaçoes. Para permitir a obtençao destas métricas, as experiências incluíram a mediçao das energias e tempos ao longo dos procedimentos laboratoriais. Para a avaliaçao da verdura química utilizou-se a métrica EV,49-51 construída com base nos perigos das substâncias envolvidas, mais precisamente a sua versao revista51 que utiliza as frases de perigo do Sistema Global Harmonizado de Classificaçao e Rotulagem de Químicos. 59 A EV é uma métrica holística da verdura química, de natureza gráfica, que cobre todos os princípios da QV aplicáveis em cada situaçao sob estudo (experiência, operaçao, síntese, etc. ), permitindo comparaçoes visuais fáceis da verdura. Desde que os procedimentos sejam descritos com suficiente detalhe na literatura, a EV nao exige a sua realizaçao laboratorial prévia para avaliar a verdura química e por isso é útil, quando há várias alternativas, para a seleçao do procedimento mais verde para posterior realizaçao experimental.
PARTE EXPERIMENTAL Avaliaçao da verdura dos protocolos de literatura Os protocolos encontrados na literatura sao resumidos na Tabela 2. As EV construídas para todos os protocolos sao apresentadas na Figura 2S do Material Suplementar; no "Catálogo digital de verdura de atividades laboratoriais para o ensino da Química Verde"60 proporciona-se informaçao detalhada sobre a realizaçao da avaliaçao, que inclui a construçao das EV para as diferentes fases integrantes de cada protocolo (extraçao, isolamento e purificaçao), bem como para o processo global. Na Tabela 2, para cada protocolo, sao indicadas duas referências: a primeira refere-se à peça bibliográfica onde foi obtido o protocolo avaliado e a segunda à página da net do referido Catálogo60 em que descreve a avaliaçao da verdura com a EV e onde se pode consultar detalhes (descriçao do protocolo, EV para cada fase e global, bem como as tabelas de apoio à sua construçao).
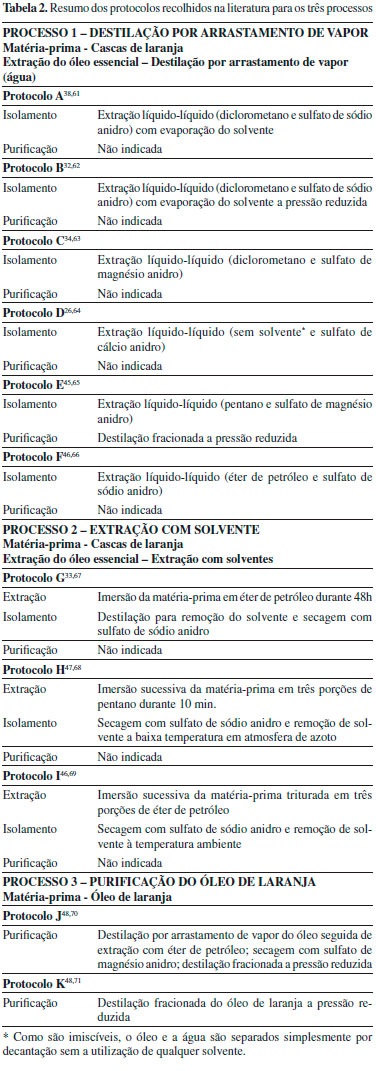
Os resultados globais da avaliaçao dos protocolos com a EV (traduzidos pelo Indice de Preenchimento da Estrela, IPE),51 usados a seguir na seleçao de protocolos, apresentam-se na Tabela 3.
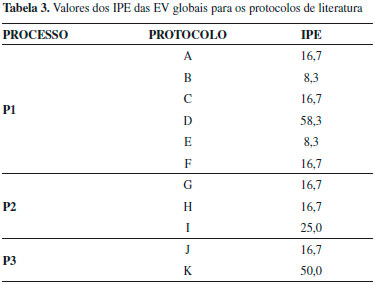
Processo 1 - Destilaçao por arrastamento de vapor A partir da análise das EV dos seis protocolos encontrados na literatura para este processo verificou-se que o protocolo mais verde é o D26,64 (ver a Tabela 3 e Figura 2S do Material Suplementar). A verdura da fase de extraçao é igual e elevada para todos os protocolos avaliados (IPE = 83,3), uma vez que a operaçao de extraçao é sempre a mesma. No caso do isolamento, a verdura varia entre IPE=8,3 (Protocolo B,32,62 Tabela 2) e IPE=66,7 (Protocolo D26). Como a pontuaçao de cada um dos princípios nas EV globais corresponde à menor pontuaçao no conjunto das EV de extraçao e isolamento (e no caso do protocolo E,45,65 Tabela 2, também de purificaçao), a fase com menor verdura química será a determinante da verdura global. O protocolo D, com maior verdura na fase de isolamento, apresenta a maior verdura global e foi o selecionado para a realizaçao experimental (ver a Figura 3, que apresenta as EV obtidas para os protocolos selecionados para execuçao laboratorial, permitindo a comparaçao das respetivas verduras).
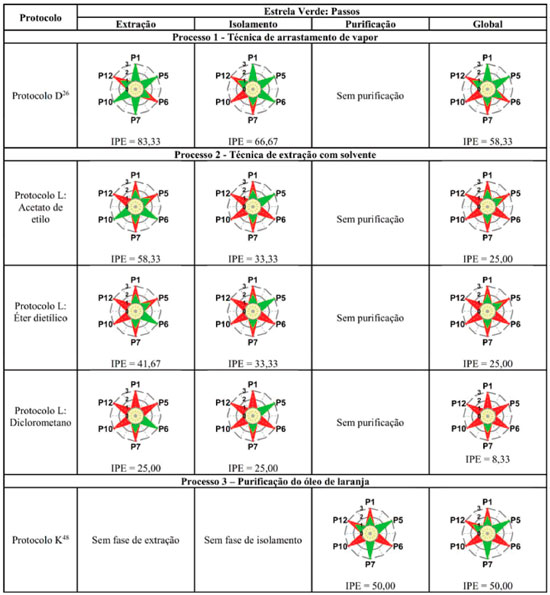 Figura 3. Comparaçao entre as EV dos protocolos escolhidos para realizaçao experimental para cada processo; os protocolos L foram desenvolvidos neste trabalho, ver texto
Processo 2 - Extraçao com um solvente orgânico A avaliaçao global dos três protocolos da literatura (G, H e I, Tabela 2) indicou como mais verde o protocolo I46,69 (ver a Tabela 3 e Figura 2S do material suplementar); a verdura da fase de extraçao é igual para todos os protocolos avaliados (IPE = 25,0), mas na fase de isolamento o protocolo I apresenta a maior verdura pelo fato de o isolamento ocorrer à temperatura ambiente (IPE = 41,7). Nenhum destes protocolos foi selecionado para realizaçao experimental atendendo a que os solventes utilizados na extraçao, o éter de petróleo e o pentano, envolvem variados perigos para a saúde humana (ver adiante). Por isso, para implementaçao laboratorial, foram concebidos outros protocolos com solventes mais benignos, que serao apresentados na secçao seguinte. Processo 3 - Purificaçao do óleo de laranja A avaliaçao dos protocolos J48.70 e K48,71 (Tabela 2) mostra que o protocolo K48,71 (ver a Tabela 3 e a Figura 2S do Material Suplementar) apresenta a maior verdura química, sendo respetivamente IPE = 50,0 e IPE = 16,7 para as EV dos dois protocolos. Assim, foi selecionado para realizaçao experimental o protocolo K (Figura 3). Conceçao de novos protocolos para a extraçao com solvente orgânico Para este processo, em alternativa aos solventes orgânicos referidos nos protocolos de literatura, procuraram-se outros com características semelhantes que pudessem substituí-los: acetato de etilo (AcEt), éter dietílico (Et2O) e diclorometano (DCM), este último usado nos protocolos A, B e C. Na Tabela 4 apresentam-se os perigos dos solventes, quer dos usados nos protocolos, quer dos substituintes considerados para serem usados na extraçao.
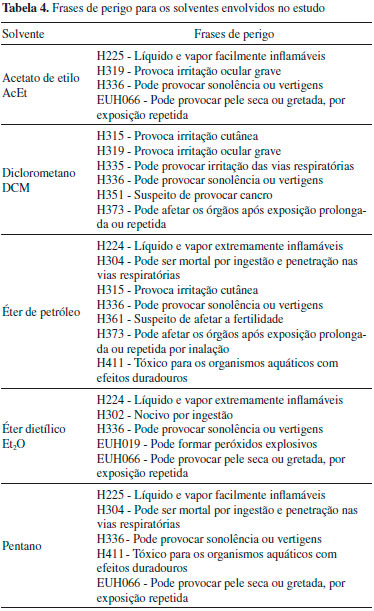
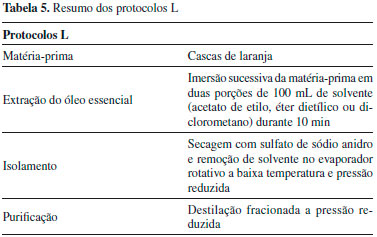
Como solventes de substituiçao para a fase de isolamento foram escolhidos o AcEt e o Et2O, por apresentarem menor potencial de risco para a saúde humana (Tabela 4). Como estes solventes nao sao usados em nenhum protocolo de literatura de extraçao do limoneno, utilizou-se ainda o DCM, sugerido nos protocolos A-C do processo 1 (Tabela 2) como solvente adequado para o limoneno. Embora este solvente apresente também perigos elevados para a saúde (Tabela 4), foi usado para se avaliar comparativamente com os referidos acima. O procedimento da fase de extraçao dos novos protocolos (L), resumido na Tabela 5 (ver detalhes na secçao 3.2.2.1 do Material Suplementar), é similar ao dos protocolos I,46,69 Tabela 2, constituído por imersao sucessiva do epicarpo das cascas de laranja em duas porçoes de 100 mL do solvente escolhido (AcEt, Et2O ou DCM), mas o isolamento é realizado por evaporaçao do solvente, num evaporador rotativo a pressao reduzida, o que prejudica a pontuaçao da EV para o sexto princípio relativamente aos protocolos indicados na literatura, mas evita contaminar a atmosfera com os solventes.
Realizaçao experimental de protocolos Os protocolos listados na Figura 3, selecionados da literatura mediante avaliaçao preliminar da verdura com a EV ou concebidos a partir destes com vista a melhorar a verdura, foram realizados experimentalmente, conforme descrito sucintamente a seguir (ver detalhes na secçao 3 do Material Suplementar). O trabalho experimental envolveu mediçoes nao habituais nos laboratórios educacionais, como mediçoes do tempo gasto nas operaçoes e da energia utilizada. Processo 1 - Destilaçao por arrastamento de vapor Ao longo do trabalho experimental baseado no protocolo D26 foram introduzidas alteraçoes em nível da escala, montagem ou parte da casca de laranja utilizada, com o objetivo de obter maior quantidade de óleo de laranja no menor tempo possível. Na Figura 4 (parte de cima, Processo 1) apresenta-se o roadmap que sintetiza as alteraçoes introduzidas no protocolo D original, os seus objetivos e as melhorias que se foram obtendo. Destas sucessivas alteraçoes resultaram quatro variantes de procedimento, D1-D4. No Material Suplementar, secçao 3.2.1, apresentam-se descriçoes pormenorizadas dos procedimentos experimentais e da caracterizaçao do limoneno obtido.
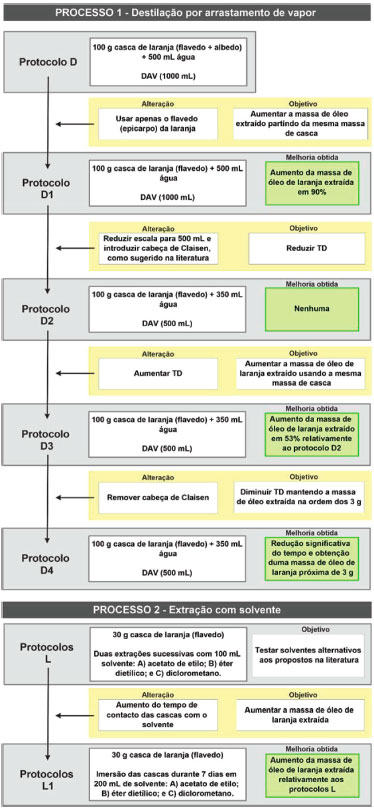 Figura 4. Roadmap que sintetiza o trabalho experimental realizado para os processos 1 e 2 (DAV (X mL), destilaçao por arrastamento de vapor em balao de X mL; TD, tempo de destilaçao)
Na comparaçao do aspeto dos óleos de laranja obtidos pelo protocolo D4 com o da amostra comercial (Figura 5S, secçao 3.2.1.2 do Material Suplementar), verificou-se que o óleo obtido era incolor e límpido, indicando ausência de qualquer tipo de pigmento corado ou cera, enquanto o comercial apresentava um tom amarelo pálido (sintoma de contaminaçao, possivelmente devida ao seu processo industrial de obtençao ser a prensagem a frio21). O óleo de laranja obtido foi caracterizado por 1H RMN e por cromatografia gasosa e comparado com o 1H RMN obtido para a amostra comercial. A análise dos espectros de 1H RMN (Figuras 6S e 7S, secçao 3.2.1.2 do Material Suplementar) permitiu concluir que o óleo de laranja obtido, assim como o comercial, sao compostos essencialmente por R-(+)-limoneno. Nenhum dos outros constituintes do óleo apresenta desvios significativos no espetro, confundindo-se mesmo com o ruido, indicando que estao presentes em pequenas quantidades, tal como esperado. A análise por cromatografia gasosa permitiu estimar que a percentagem de limoneno presente no óleo obtido e na amostra comercial ronda os 93% e 95%, respetivamente, valores que se encontram entre os limites indicados na literatura, 90-95%. 21 Com o objetivo de aumentar quantidade de óleo obtida atendeu-se à morfologia da laranja, mais precisamente ao modo como o óleo essencial está distribuído no fruto. A laranja é constituída por três camadas, o flavedo ou epicarpo, o albedo ou mesocarpo e o endocarpo. A casca da laranja contém duas camadas: o epicarpo, camada rica em pigmentos onde estao contidas as glândulas de óleo, e o albedo, composto de células esponjosas de forma irregular e cor branca, separadas por grandes bolhas de ar. O óleo essencial está contido no interior de glândulas próprias (diâmetro de 0,4 a 0,6 mm), situadas imediatamente após a epiderme do fruto, no epicarpo, pelo que se aumenta a eficiência da operaçao se se fizer a extraçao a partir apenas do epicarpo da casca. Com esta base, introduziu-se uma alteraçao no protocolo D, utilizando apenas o epicarpo de cascas de laranja como matéria-prima (protocolo D1), que permitiu um aumento de 90% na massa de limoneno obtido, mantendo-se o odor e aspeto do produto. Para se investigar se seria possível diminuir o tempo necessário à destilaçao por arrastamento de vapor, reduziu-se a escala do balao, de 1000 mL para 500 mL, e introduziu-se uma cabeça de Claisen na montagem (protocolo D2). A reduçao da escala permitiu diminuir a quantidade de água usada. No entanto, verificou-se que a quantidade de destilado era aproximadamente metade da obtida nos casos anteriores no mesmo intervalo de tempo. Por isso, nao foi possível interromper a destilaçao mais cedo, sendo necessário manter o mesmo tempo. A massa de óleo obtida foi semelhante à obtida no procedimento D1. Em face destes resultados, prolongou-se o tempo de destilaçao para obter uma quantidade de destilado semelhante à dos protocolos anteriores, D1 e D2 (protocolo D3). Verificou-se ser necessário mais de 5 horas para cumprir esse objetivo, tendo a massa de óleo obtida aumentado (53%) relativamente ao protocolo D2. Por fim, decidiu-se remover a cabeça de Claisen para investigar se, à escala de 500 mL, se conseguia extrair uma massa de óleo da ordem dos 3 g em 3 ½ horas em vez das mais de 5 horas necessárias no procedimento D3, objetivo que foi alcançado (protocolo D4). No entanto, experiências adicionais mostraram nao ser possível diminuir mais o tempo de destilaçao, uma vez que a quantidade de óleo obtida diminuía bastante. Processo 2 - Extraçao com um solvente orgânico O trabalho experimental baseado nos protocolos L conduziu a resultados insatisfatórios com os três solventes alternativos (AcEt, Et2O e DCM), porque a quantidade de óleo extraída foi muito pequena. Assim, decidiu aumentar-se o tempo de contacto da matéria-prima com o solvente para sete dias (geralmente o tempo que decorre entre as aulas de laboratório), em vez das extraçoes sucessivas utilizadas nos protocolos L (protocolos L1). Na Figura 4 (parte inferior, Processo 2) apresenta-se o roadmap que sintetiza a alteraçao nos protocolos, bem como os resultados obtidos (descriçoes pormenorizadas dos procedimentos sao incluídas no Material Suplementar, secçao 3.2.2). Com os protocolos L1 consegue-se extrair óleo de laranja no caso dos três solventes testados, embora as quantidades variassem bastante de solvente para solvente, sendo o DCM o solvente mais eficiente em termos de quantidade de óleo extraída. Os resultados sao apresentados e discutidos em pormenor na secçao seguinte. A comparaçao dos aspetos do óleo de laranja obtido por este processo, da amostra comercial e do óleo obtido por destilaçao por arrastamento de vapor, processo 1 (Figura 9S, secçao 3.2.2.2 do Material Suplementar), mostrou que o óleo extraído com DCM apresenta um tom amarelo mais forte do que comercial, indicando uma maior contaminaçao por pigmentos. O respetivo espectro de 1H RMN (Figura 10S, secçao 3.2.2.2 do Material Suplementar) evidenciou que o óleo continha substâncias ausentes nas amostras comercial e no óleo obtido no processo 1, possivelmente pigmentos responsáveis pela coloraçao. Verificou-se ainda a presença de DCM, uma vez que é difícil extrair todo o DCM sem evaporar também óleo. Em suma, a qualidade do óleo essencial obtido por extraçao com DCM é inferior à obtida por destilaçao por arrastamento de vapor, provavelmente devido à contaminaçao. Processo 3 - Purificaçao do óleo de laranja A amostra comercial foi purificada seguindo o protocolo K, com uma reduçao para microescala (balao de 10 mL), mas o espectro de 1H RMN do óleo purificado nao mostrou alteraçao relativamente ao do óleo nao purificado. No entanto a análise por cromatografia gasosa permitiu verificar que a percentagem de limoneno aumentou de 95% para 98% com a purificaçao. Na secçao 3.2.3 do Material Suplementar incluem-se detalhes do procedimento, bem como uma imagem da montagem usada (Figura 11S) e os espetros de 1H RMN do óleo comercial (Figura 6S) e do limoneno obtido após purificaçao deste (Figura 12S).
RESULTADOS E DISCUSSAO Avaliaçao com a Estrela Verde As EV dos protocolos de destilaçao por arrastamento de vapor e extraçao com solventes realizados experimentalmente (processos 1 e 2, respetivamente), apresentadas na Figura 3, mostram que o protocolo D (processo 1), que nao requer solventes orgânicos, é o mais verde (IPE = 58,3). Os protocolos L, seguidos no processo 2, apresentam uma verdura mais baixa, que varia com o solvente usado no isolamento. Quando se usa AcEt ou Et2O a verdura é reduzida (IPE=25,0), mas com DCM é ainda mais reduzida (IPE = 8,3). Por outro lado, o protocolo K, relativo à purificaçao do óleo de laranja (processo 3), apresenta verdura (IPE = 50,0) próxima da do protocolo D (IPE = 58,3), porque nao utiliza solventes, já que consiste numa destilaçao fracionada a pressao reduzida. Os protocolos D1-D4 apresentam a mesma EV que o protocolo D e os protocolos L1 (AcEt, Et2O, DCM) a mesma EV que os protocolos L correspondentes, pois as alteraçoes introduzidas nao afetam os parâmetros avaliados pela EV. O protocolo L com DCM apresenta menor verdura do que os protocolos da literatura porque, conforme já referido, o solvente é separado num evaporador rotativo à pressao reduzida, o que implica, porém, menor impacto sobre o ambiente. Esta situaçao exemplifica como as interaçoes entre as diversas dimensoes da verdura podem ser importantes, requerendo soluçoes de compromisso na otimizaçao desta. Avaliaçao com métricas de massa Na Figura 5 apresentam-se os valores obtidos para as métricas fator E, BME e throughtput para todos os protocolos realizados (os dados experimentais usados nos cálculos constam das Tabelas 6S e 8S, secçao 3.2.1.3, e 10S, secçao 3.2.2.3, do Material Suplementar).
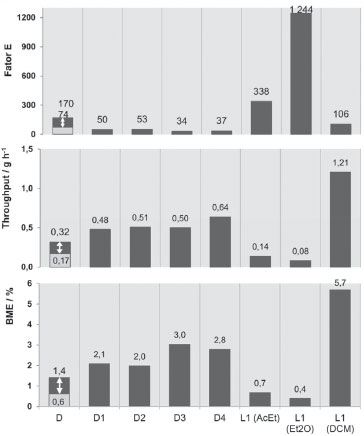 Figura 5. Valores de BME, throughtput e fator E para o processo 1 (destilaçao por arrastamento de vapor): D-D4; e processo 2 (extraçao com solventes): L1); para o protocolo D apresenta-se o intervalo de valores obtidos em quatro experiências ()
No caso da destilaçao por arrastamento de vapor (processo 1), os valores da BME para os protocolos D1-D4 sao cerca de duas a cinco vezes superiores, para o throughtput duas a quatro vezes superiores e para o fator E cerca de metade a um quinto inferiores aos obtidos para o protocolo D (Figura 5). Este facto deve-se ao uso, como matéria-prima, do epicarpo da casca de laranja em vez de toda a casca. Segundo a literatura,12,21 a percentagem de óleo essencial extraída de materiais naturais varia entre cerca de 0,01% e 5%, dependendo do processo de isolamento e do material natural. Os valores obtidos para essa percentagem (aqui designada por BME) nos diferentes procedimentos do processo 1 variam de 0,61% a 3,04% (Tabela 6S e 8S, no Material Suplementar, secçao 3.2.1.3), portanto dentro do intervalo indicado. Quanto ao fator E, o protocolo D apresenta o valor mais elevado (entre 74 e 170) de todos os protocolos do processo 1, por se ter usado como matéria-prima toda a casca de laranja e nao apenas o epicarpo, como nos protocolos D1-D4, sendo a massa de limoneno obtida muito mais baixa. Como os procedimentos D e D1 foram realizados em balao de 1000 mL, foi necessária uma maior quantidade de água relativamente aos procedimentos D2-D4, em que se utilizou um balao de 500 mL, o que explica que o fator E para estes últimos seja inferior ao de D1. Para o caso da extraçao com solventes (processo 2, protocolos L1), quando se usou DCM, como reportado na literatura,32,34,38 o valor obtido para a BME foi 5,7%, bastante superior ao encontrado para os outros dois solventes, AcEt ou Et2O, 0,7% e 0,4%, respetivamente. Em consequência, a utilizaçao destes solventes para a extraçao nao parece viável, apesar de serem menos perigosos para a saúde humana. Os solventes sao recuperados após extraçao no evaporador rotativo e a massa de solvente recuperado nao constitui um resíduo e, portanto, nao é considerada no cálculo do fator E (ver a Figura 6, onde se mostram os intervalos de valores das massas das substâcias em jogo). Se o solvente nao fosse recuperado, os valores do fator E aumentavam (ver valores nas Tabelas 9S e 10S do Material Suplementar, secçao 3.2.2.3). O volume de solvente recuperado variou com a volatilidade do solvente, constituindo 15,0%, 42,5% e 77,4% do volume/massa inicial, repetivamente para o Et2O, DCM e AcEt. Quanto mais volátil o solvente, menor a massa recuperada, devido provavelmente a perdas para a atmosfera, o que revela dois problemas quanto à verdura: perdas de solvente para reutilizaçao e contaminaçao da atmosfera. O AcEt, solvente menos volátil, permite obter a menor massa de resíduos (incluindo perdas por volatilizaçao), já que se consegue recuperar a maior percentagem do solvente inicial. Por outro lado, o DCM conduz à maior massa de resíduos, embora a recuperaçao tenha sido superior à do Et2O. Isto deve-se ao facto do DCM ter uma densidade bastante superior à do Et2O, respetivamente 1,33 g cm-3 e 0,71 g cm-3. Como se usaram volumes iniciais de solvente iguais, e nao massas, as diferentes densidades vao ter peso significativo nas massas de resíduos. Este caso mostra como a densidade dos solventes pode influenciar os valores do fator E, isto é, a verdura química - um aspeto que, tanto quanto os autores sabem, nunca foi discutido na literatura.
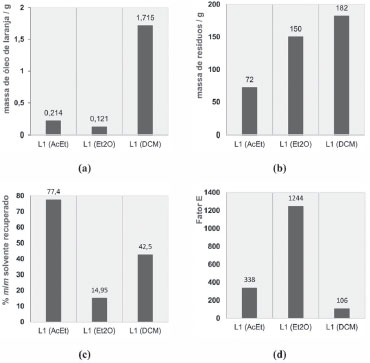 Figura 6. Valores obtidos no processo 2 (Extraçao com solvente) para (a) massa de óleo de laranja, (b) massa de resíduos, (c) percentagem massa/massa de solvente recuperado e (d) fator E
O protocolo L1 realizado com DCM é o que apresenta o menor valor de fator E, embora produza a maior massa de resíduos (Figura 6), porque a massa de óleo de laranja extraído foi muito superior. No entanto, os valores de throughput obtidos para este processo sao muito baixos, devido ao elevado tempo de imersao das cascas de laranja no solvente para nao prejudicar a quantidade de óleo extraída. A comparaçao dos resultados para os processos 1 e 2 mostra que o protocolo L1, em que se realiza a extraçao com DCM, é o que apresenta menor valor para o fator E, o que se deve principalmente ao maior valor de BME. No entanto, a massa de óleo extraída foi baixa comparativamente com a quantidade de biomassa utilizada em ambos os processos (o valor máximo de BME nao atingiu os 6%), o que é de esperar face à baixa quantidade relativa de óleo na casca de laranja. Para para a purificaçao da amostra comercial (processo 3) o rendimento obtido foi de 79 ± 2% (n=4). O valor determinado para o fator E foi muito baixo 0,27 ± 0,03 (n=4), o que resulta de nao se usarem substâncias auxiliares. Avaliaçao com métricas de tempo e de energia Nas operaçoes de trituraçao das cascas de laranja e de destilaçao (processo 1) e de evaporaçao do solvente no evaporador rotativo (processo 2), a mediçao de energias e tempo permitiu o cálculo das respetivas métricas de intensidade, sendo os resultados apresentados na Figura 7.
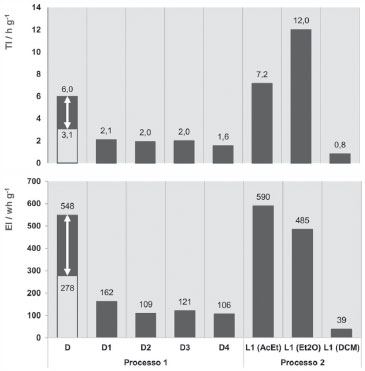 Figura 7. Valores da Intensidade de Energia (EI) e Intensidade de Tempo (TI) para o processo 1 (destilaçao por arrastamento de vapor): D-D4; e processo 2 (extraçao com solventes): L1(Solvente); para o protocolo D apresenta-se o intervalo de valores obtidos em quatro experiências ()
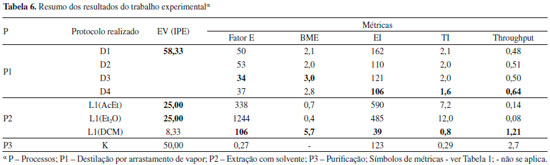
No processo 1 (destilaçao por arrastamento de vapor), os protocolos D2-D4 apresentam os menores valores para a EI, logo, menor utilizaçao de energia por grama de limoneno extraído. O protocolo D apresenta um valor de EI superior aos dos restantes (Figura 7), devido principalmente à pequena quantidade de limoneno obtido relativamente aos outros protocolos, já que a energia utilizada é semelhante para todos (Tabela 5S e 7S do Material Suplementar, secçao 3.2.1.3). Pela mesma razao, no que se refere a TI, o protocolo D apresenta também um valor total superior aos restantes. No processo 2 (extraçao com solventes), a utilizaçao de energia ocorre durante a separaçao no evaporador rotativo. Os procedimentos em que se usa AcEt ou Et2O apresentam um valor de EI bastante superior ao do DCM (Figura 7), o que se deve principalmente à maior massa de óleo extraída neste último caso (Figura 5). O AcEt é o solvente que envolve maior utilizaçao de energia, por ser o menos volátil e, consequentemente, o mais difícil de remover por evaporaçao, daí que o valor obtido para o EI seja superior ao obtido para o Et2O, embora a massa de óleo extraída seja superior. Comparando os dois processos, verifica-se que o menor valor de EI foi obtido para o processo 2 com DCM, o que se deve essencialmente à maior massa de óleo obtida por grama de matéria-prima. Para o processo 3, referente à purificaçao da amostra comercial, obteve-se os valores EI = 123 ± 20 Wh g-1 (n=4) e TI = 17,7 ± 0,9 min g-1 (n=4). Tanto quanto se explorou a literatura, esta nao contém valores destas grandezas com que estes possam ser cotejados. Comparaçao dos processos de extraçao Na Tabela 6 apresenta-se um resumo dos resultados discutidos em detalhe acima. O negrito ou cor assinalam os melhores resultados obtidos para cada caso, evidenciando contradiçoes entre as métricas quando se fazem comparaçoes entre protocolos do mesmo tipo, por exemplo, D3 apresenta as melhores métricas de massa mas D4 as melhores métricas de energia e tempo. As causas e implicaçoes destes conflitos serao evidenciadas na discussao a seguir.
A importância da gestao do tempo na prática industrial implica que seja importante maximizar a taxa de extraçao do óleo de laranja/limoneno por unidade de tempo, de forma a obter a maior quantidade de óleo por grama de epicarpo de casca de laranja no menor tempo possível. Os resultados experimentais mostram que os protocolos mais eficazes para realizar a extraçao do óleo a partir da casca de laranja sao: o protocolo D4, para o processo de extraçao por destilaçao por arrastamento de vapor; e o protocolo L1 (DCM), para a extraçao com solventes (ver Tabela 6). O melhor valor de BME (5,7%) foi conseguido com o protocolo L1 (DCM), que apresenta também o melhor valor de throughput; no entanto, a destilaçao por arrastamento de vapor (D4, processo 1), devido ao menor tempo exigido na extraçao do óleo, pode executar-se em uma aula laboratorial (no processo de extraçao com solvente sao necessárias duas aulas, entre as quais as cascas ficam a extrair). Por outro lado, a gestao dos custos com a energia é também importante. Embora a extraçao com DCM, protocolo L1(DCM), apresente os melhores valores para EI e TI, outros aspetos desencorajam o uso deste procedimento: por um lado, os perigos do DCM para a saúde humana sao elevados (em especial, H351 - suspeito de provocar cancro); por outro, o óleo extraído apresenta uma qualidade inferior à do obtido por destilaçao, exibindo contaminaçao com substâncias presentes na casca. Embora o fator E para a extraçao com DCM seja o mais baixo (ver a Tabela 6), os resíduos apresentam perigos elevados para a saúde. 67-69 Este caso exemplifica uma situaçao vulgar quando se procura aumentar a verdura de um processo químico: sendo a verdura um conceito de natureza multidimensional, a procura do seu aumento em uma dimensao pode implicar diminuiçao em outra (ou outras), pelo que sao requeridos compromissos nem sempre fáceis ou mesmo exequíveis. Após este balanço, considerando que a água consumida na refrigeraçao pode ser reutilizada, o processo mais verde parece ser afinal a destilaçao por arrastamento de vapor, por apresentar menores riscos no manuseamento das substâncias e menor fator E, embora as métricas de massa sejam menos favoráveis que as da extraçao com DCM. Discussao sumativa A análise dos protocolos disponíveis na literatura para realizar a extraçao do limoneno das cascas de laranja e de outros obtidos pela sua alteraçao com vista a incrementar a verdura, realizada com a métrica EV, revelou que o uso de solventes orgânicos prejudica significativamente a verdura, devido aos perigos para a saúde humana e o ambiente associados genericamente aos solventes propostos ou usados (pentano, hexano, éter de petróleo e DCM). Aquela avaliaçao sugere que a destilaçao por arrastamento de vapor, que nao utiliza qualquer solvente orgânico, permite procedimentos mais verdes. No entanto, a avaliaçao de verdura dos protocolos realizada com outras métricas de diferentes tipos conduziu a resultados que, embora em parte conflituosos entre si, poem em causa esta conclusao. Quando se aborda a metrificaçao da verdura em postura holística, nao é invulgar encontrar situaçoes em que diferentes métricas de verdura proporcionam resultados em conflito, o que evidencia a complexidade do conceito de verdura química e as dificuldades de concretizar a QV. O presente caso é um exemplo rico das dificuldades de lidar com tais situaçoes que permite mostrar a importância da análise da verdura química ser realizada em paralelo com diversos tipos de métricas quantitativas, quer métricas de verdura "clássicas" (BME e fator E), quer outras mais ligadas a aspetos económicos da atividade industrial (throughput, EI e TI), bem como com métricas holísticas (como a EV). Na realidade, só o uso paralelo de diferentes métricas permite captar informaçao sobre diferentes coordenadas da verdura e obter uma visao mais global e realista das situaçoes em estudo, o que possibilita a identificaçao de soluçoes de compromisso melhor fundamentadas em atividades de otimizaçao da verdura. 56 Este tema merece mais atençao do que a que lhe tem sido dada na literatura da QV, em especial a de natureza pedagógica, tendo este trabalho conduzido a resultados que ilustram bem a importância da multidimensionalidade das métricas e a necessidade de o assunto ser incluído no ensino da QV.
CONCLUSAO A análise e otimizaçao da verdura dos protocolos de extraçao do óleo de laranja a partir das cascas encontrados na literatura educacional (destilaçao por arrastamento de vapor e extraçao com solvente) conduziu a um conjunto de resultados que permitem um bom aproveitamento para impulsionar o progresso da QV no contexto educacional, em especial no que diz respeito ao aprofundamento do conceito de verdura química - fazendo sentir a sua complexidade e as dificuldades da sua avaliaçao por meio de métricas. O uso da metodologia adotada aqui para a realizaçao experimental da extraçao de óleos essenciais constitui uma base para conceber atividades diversas para o ensino médio (anos terminais) e universitário, que incentivem um conhecimento aprofundado da verdura química, o que será bastante formativo na abordagem da QV. Em particular, fazer sentir aos alunos quanto a verdura química e a própria QV envolvem uma multiplicidade de dimensoes com relaçoes intrincadas, que implicam a consideraçao de uma grande variedade de aspetos para vencer as barreiras a ultrapassar quando se pretende reformatar a prática da química para obter QV, o que exige a adoçao de raciocínio sistémico - sem prejuízo da racionalidade cartesiana vigente na ciência, mas sim em paralelo com esta.
MATERIAL SUPLEMENTAR Detalhes sobre procedimentos experimentais e as Figuras 1S-12S e Tabelas 1S-12S estao disponíveis em http://www.quimicanova.sbq.org.br, em formato PDF, com acesso livre.
AGRADECIMENTOS O trabalho de MGTCR e TCMP recebeu apoio financeiro da Uniao Europeia (fundos FEDER POCI/01/0145/FEDER/007265) e de fundos nacionais (FCT/MEC, Fundaçao para a Ciência e Tecnologia e Ministério da Educaçao e Ciência) no âmbito do Acordo de Parceria PT2020 UID/QUI/50006/2013.
REFERENCIAS 1. Lin, C. S. K. ; Pfaltzgraff, L. A. ; Herrero-Davila, L. ; Mubofu, E. B. ; Abderrahim, S. ; Clark, J. H. ; Koutinas, A. A. ; Kopsahelis, N. ; Stamatelatou, K. ; Dickson, F. ; Thankappan, S. ; Mohamed, Z. ; Brocklesby, R. ; Luque, R. ; Energy Environ. Sci. 2013, 6, 426. 2. Clark, J. H. ; Pfaltzgraff, L. A. ; Budarin, V. L. ; Hunt, A. J. ; Gronnow, M. ; Matharu, A. S. ; Macquarrie, D. J. ; Sherwood, J. R. ; Pure Appl. Chem. 2013, 85, 1625. 3. Gallezot, P. ; Chem. Soc. Rev. 2012, 41, 1538. 4. Coelho, M. A. Z. ; Ribeiro, B. D. ; White Biotechnology for Sustainable Chemistry. RSC: Cambridge, 2016. 5. Sanders, J. ; Scott, E. ; Weusthuis, R. ; Mooibroek, H. ; Macromol. Biosci. 2007, 7, 105. 6. Christensen, C. H. ; Rass-Hansen, J. ; Marsde, C. C. ; Taarning, E. ; Egeblad, K. ; ChemSusChem 2008, 1, 283. 7. Pfaltzgraff, L. A. ; De bruyn, M. ; Cooper, E. C. ; Budarin, V. ; Clark, J. H. ; Green Chem. 2013, 15, 307. 8. López, J. A. S. ; Li, O. ; P. Thompson, I. P. ; Crit. Rev. Biotechnol. 2010, 30, 63. 9. Boukroufa, M; Boutekedjiret, C. ; Petigny, L. ; Njara Rakotomanomana,N. ; Chemat, F. ; Ultrason. Sonochem. 2015, 24, 72. 10. González-Rivera, J. ; Spepi, A. ; Ferrari, C. ; Duce, C. ; Longo, I. ; Falconieri, D. ; Piras, A. ; Tinè, M. R. . ; Green Chem. 2016, 18, 6482. 11. Bica, K. ; Gaertner, P. ; Rogers, R. D. ; Green Chem. 2011, 13, 1997. 12. Sterrett, F. S. ; J. Chem. Educ. 1962, 39, 203. 13. Barros, F. M. C. d. ; Zambarda, E. d. O. ; Heinzmann, B. M. ; Mallmann, C. A. ; Quim. Nova 2009, 32, 861. 14. Alcântara, J. M. ; Yamaguchi, K. K. d. L. ; Junior, V. F. d. V. ; Lima, E. S. ; Quim. Nova 2010, 33, 141. 15. Tsukamoto, J. ; Durán, N. ; Tasic, L. ; J. Braz. Chem. Soc. 2013, 24, 1537. 16. Bizzo, H. R. ; Hovell, M. C. ; Rezende, C. M. ; Quim. Nova 2009, 32, 588. 17. Sterrett, F. S. ; J. Chem. Educ. 1962, 39, 246. 18. http://www.floridachemical.com/whatisd-limonene.htm, acessada em outubro de 2017. 19. Mattos, M. C. S. d. ; Bernini, R. B. ; J. Braz. Chem. Soc. 2007, 18, 1068. 20. Júnior, M. R. M. ; Pastore, G. M. ; Quim. Nova 2007, 30, 382. 21. Surburg, H. ; Panten, J. ; Common Fragrance and Flavor Materials: Preparation, Properties and Uses, 5th ed. , Wiley-VCH Verlag GmbH & Co. , 2006. 22. Firdaus, M. ; Meier, M. A. R. ; Green Chem. 2013, 15, 370. 23. http://www.floridachemical.com/App%20Page%20Combined.pdf, acessada em outubro de 2017. 24. Júnior, C. V. ; Quim. Nova 2003, 26, 390. 25. Baser, K. H. C. ; Demirci, F. In Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley and Sons, Inc. , 2011; pp 1-37. 26. Beatty, J. H. ; J. Chem. Educ. 1986, 63, 768. 27. Shahidi, F. ; Zhong, Y. , In Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley and Sons, Inc. , 2012; pp 1-17. 28. Sun, J. ; Altern Med Rev 2007, 12, 259. 29 Figueiredo, I. M. ; Santos, L. V. d. ; Costa, W. F. d. ; Carvalho, J. E. d. ; Silva, C. C. d. ; Sacoman, J. L. ; Kohnb, L. K. ; Sarragiotto, M. H. ; J. Braz. Chem. Soc. 2006, 17, 954. 30. Lenardao, E. J. ; Freitag, R. A; Dabdoub; M. J. ; Batista, A. C. F. ; Silveira, C. C. ; Quim. Nova 2003, 26, 123. 31. Machado, A. A. S. C. ; Quim. Nova 2011, 34, 535. 32. Greenberg, F. H. ; J. Chem. Educ. 1968, 45, 537. 33. Griffin, R. W. ; J. Chem. Educ. 1974, 51, 601. 34. Glidewell, C. ; J. Chem. Educ. 1991, 68, 267. 35. Logan, J. L. ; Rumbaugh, C. E. ; J. Chem. Educ. 2012, 89, 613. 36. Epstein, J. L. ; Castaldi, M. ; Patel, G. ; Telidecki, P. ; Karakkatt, K. ; J. Chem. Educ. 2015, 92, 954. 37. Garner, C. M. ; Garibaldi, C. ; J. Chem. Educ. 1994, 71, A146. 38. Rothenberger, O. S. ; Krasnoff, S. B. ; Rollins, R. B. ; J. Chem. Educ. 1980, 57, 741. 39. Baptistella, L. H. B. ; Imamura, P. M. ; Melo, L. V. d. ; Castello, C. ; Quim. Nova 2009, 32, 1069. 40. Buckley, H. L. ; Beck, A. R. ; Mulvihill, M. J. ; Douskey, M. C. ; J. Chem. Educ. 2013, 90, 771. 41. McKenzie, L. C. ; Thompson, J. E. ; Sullivan, R. ; Hutchison, J. E. ; Green Chem. 2004, 6, 355. 42. Kulkarni, P. S. ; Brazinha, C. ; Afonso, C. A. M. ; Crespo, J. G. ; Green Chem. 2010, 12, 1990. 43. http://www.cedefop.europa.eu/files/3057_en.pdf, acessada em outubro de 2017. 44. Haack, J. A. ; Hutchison, J. E. ; ACS Sustainable Chem. Eng. 2016, 4, 5889. 45. Bergstrom, W. ; Howells, M. , Advanced Chemistry Laboratory Experiments. University of Minnesota, 1988. 46. http://resources.schoolscience.co.uk/ICI/periodictable/downloads/smellpracs.pdf, acessada em outubro de 2017. 47. Smith, D. C. ; Forland, S. ; Bachanos, E. ; Matejka, M. ; Barrett, V. ; Chem. Educator 2001, 6, 28. 48. Afonso, C. A. M. ; Simao, D. P. ; Ferreira, L. P. ; Serra, M. E. d. S. ; Raposo, M. M. M. ; 100 Experiências de Química Orgânica. IST Press, 2011. 49. Ribeiro, M. G. T. C. ; Costa, D. A. ; Machado, A. A. S. C. ; Quim. Nova 2010, 33, 759. 50. Ribeiro, M. G. T. C. ; Costa, D. A. ; Machado, A. A. S. C. ; Green Chem. Lett. Rev. 2010, 3, 149. 51. Ribeiro, M. G. T. C. ; Yunes, S. F. ; Machado, A. A. S. C. ; J. Chem. Educ. 2014, 91, 1901. 52. Sheldon, R. A. ; Green Chem. 2007, 9, 1273. 53. Sheldon, R. A. ; Green Chem. 2017, 19, 18. 54. Sheldon, R. A. ; Chem. Ind. 1992, 23, 903. 55. Machado, A. A. S. C. ; Introduçao às métricas da Química Verde: uma visao sistémica. Editora UFSC, 2014. 56. Machado, A. A. S. C. ; Quim. Nova 2011, 34, 1291. 57. Zhang, T. Y. ; Chem. Rev. 2006, 106, 2583. 58. Butters, M. ; Catterick, D. ; Craig, A. ; Curzons, A. ; Dale, D. ; Gillmore, A. ; Green, S. P. ; Marziano, I. ; Sherlock, J. -P. ; White, W. ; Chem. Rev. 2006, 106, 3002. 59. http://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=CELEX:32008R1272:EN:NOT, acessada em outubro de 2017. 60. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1, acessada em outubro de 2017. 61. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/A, acessada em outubro de 2017. 62. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/B, acessada em outubro de 2017. 63. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/C, acessada em outubro de 2017. 64. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/D, acessada em outubro de 2017. 65. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/E, acessada em outubro de 2017. 66. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/F, acessada em outubro de 2017. 67. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/G, acessada em outubro de 2017. 68. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/H, acessada em outubro de 2017. 69. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/I, acessada em outubro de 2017. 70. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/J, acessada em outubro de 2017. 71. http://educa.fc.up.pt/catalogo/pt/separacoes/1/1/K, acessada em outubro de 2017. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access