Artigo
|
|
| Imobilização de complexo de rutênio contendo base de Schiff na unidade metalo-orgânica UiO-67 Immobilization of ruthenium Schiff base complex in the metal-organic framework UiO-67 |
|
Herculys B. Jorge; Cleiser T. P. da Silva; Helena S. Nakatani; Andrelson W. Rinaldi; Vagner R. De Souza*
Departamento de Química, Universidade Estadual de Maringá, 87020-900 Maringá - PR, Brasil
Recebido em 28/01/2018 *e-mail: vrsouza2@uem.br Zirconium-based metal-organic framework, UiO-67, was synthesized and used as support for the immobilization of the [RuCl2(ENAPY)] (ENAPY = N,N'-bis(7-metyl-2-pyridylmethylene)-1,2-diiminoethane)). The immobilized system exhibited violet-blue color. The {UiO-67/[RuCl2(ENAPY)]} was characterized by cyclic voltammetry, X-ray diffraction, UV-Vis, FTIR and X-ray photoelectron spectroscopy. The electrochemistry of the immobilized system is characterized by a reversible pair of waves at +0.40 V (vs NHE), ascribed to the Ru3+/2+ redox process. The electronic spectrum of the immobilized system is characterized by bands at 520 and 380 nm ascribed to a ligand-to-metal charge-transfer transitions {Ru2+(dπ) → ENAPY(pπ*)}. The IR bands of immobilized complex {1630 cm-1 (νasC=C), 1590 cm-1 (νasC=N), 1450 cm-1 (νsC=C), 1340 cm-1 (νsC=C)} are weak in comparison with the neat complex due to their low concentration in MOF cages. X-ray diffractogram of the immobilized system indicated that the crystallinity and morphology of UiO-67 was preserved during inclusion of ruthenium complex. The XPS spectra of UiO-67 and UiO-67/ruthenium complex shows a signal at 462 eV that can be ascribed to Ru 3p3/2 and at 400 eV ascribed to N 1s core level of the ruthenium Schiff base complex immobilized into MOF. INTRODUÇAO Com base em princípios elementares da química de coordenaçao e no aproveitamento adequado das características eletrônicas e estéricas dos íons metálicos e ligantes, foram projetadas estruturas moleculares relativamente complexas classificadas como polímeros de coordenaçao ou metal organic framewoks (MOF).1 Na construçao de polímeros baseados em compostos de coordenaçao, o acoplamento interunidades pode ser efetuado por meio de ligantes ou complexos de ponte capazes de formar estruturas mono, bi ou tridimensionais.2 Sistemas lineares ou unidimensionais podem ser desenvolvidos com sais de cobalto(II) e ligantes 4,4'-bipiridina, em soluçao aquosa.3 Sistemas bidimensionais sao obtidos pela polimetalaçao de estruturas planares com propriedades multiponte como as meso-tetrapiridilporfirinas de cobre.4 Finalmente, sistemas tridimensionais podem ser obtidos pela polimetalaçao de complexos baseados no tris(bipiridina)rutênio(II), [Ru(bpy)3]2+, e sistemas poli-imínicos substituídos com grupos coordenantes.5 As vantagens de sistemas tridimensionais estao associadas ao desenvolvimento de materiais com elevada porosidade, com poros uniformes e ordenados em escala molecular, bem como na estabilidade dessas estruturas após a remoçao da maior parte das moléculas do solvente presentes nos poros desse material.6 Considerando o potencial inesgotável dos compostos de coordenaçao na construçao de estruturas metalo-orgânicas (MOFs), Cavka e colaboradores7 reportaram a síntese de uma nova classe de polímeros de coordenaçao tridimensional baseada em óxido de zircônio (IV) conectado por moléculas de ácidos dicarboxílicos. Como os primeiros derivados desta classe foram obtidos na Universidade de Oslo, as novas estruturas metalo-orgânicas foram designadas de UiO, em homenagem à instituiçao de pesquisa. Dentre as MOFs do tipo UiO, destacamos a UiO-67 que é constituída por clusters octaédricos de [Zr6O4(OH)4] ligados a doze moléculas de ácido 4,4'-bisfenildicarboxílico (BPDC), formando uma estrutura supramolecular organizada, simétrica e tridimensional, com cavidades octaédricas de diâmetro ~20 Å e cavidades tetraédricas de diâmetro de ~12 Å.8 Essa rede cristalina é mantida mesmo quando a MOF é submetida à temperatura de 300 °C, como mostra o estudo de estabilidade térmica desenvolvido por Cavka e colaboradores.7 Segundo os autores, o aquecimento da amostra no intervalo de temperatura 250 – 300 °C faz com que o cluster Zr6O4(OH)4 perca duas moléculas de água e seja convertido em Zr6O6. O cluster Zr6O6, formado pela desidrataçao do precursor, continua conectado às moléculas de ácido 4,4'-bisfenildicarboxílico preservando a porosidade da estrutura metalo-orgânica. A área superficial da UiO-67 pode variar de 500 a 2000 m2 g-1, dependendo do método de ativaçao e do solvente utilizado na preparaçao da MOF, visto que a metodologia aplicada pode provocar imperfeiçoes estruturais associadas à ausência de molécula de ácido 4,4'-bisfenildicarboxílico na esfera de coordenaçao do centro metálico,9,10 conforme representado na Figura 1.
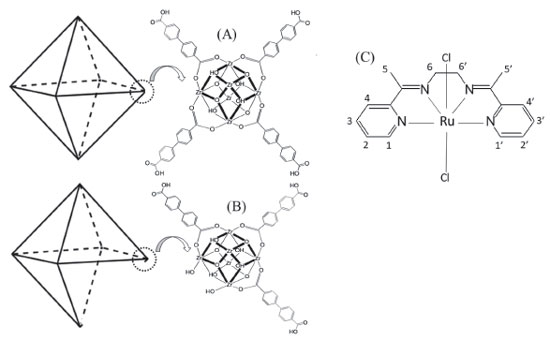 Figura 1. Representaçao do cluster [Zr6O4(OH)4] ligado a moléculas de ácido 4,4'-bisfenildicarboxílico (BPDC), sendo (A) estrutura da MOF UiO-67 sem defeito; (B) com defeito estrutural provocado pela vacância da molécula do ácido 4,4'-bisfenildicarboxílico; (C) do complexo de rutênio [RuCl2(ENAPY)] contendo a numeraçao para átomos de hidrogênio para auxiliar na interpretaçao do espectro de RMN 1H (material suplementar)
A manutençao da estrutura cristalina com alta porosidade, aliada às características geométricas das cavidades e aos efeitos entrópicos, sao atrativos para a aplicaçao da UiO-67 e estruturas análogas no reconhecimento molecular,11 adsorçao/dessorçao de gases,12 catálise13 e funcionalizaçao dos microambientes com compostos fotoquimicamente ativos,14 possibilitando a derivaçao de novos sensores, catalisadores e fotodispositivos. No contexto da funcionalizaçao de microambientes, a imobilizaçao de complexos metálicos nas cavidades ou na superfície das MOFs permite que reaçoes químicas ou fotoquímicas possam se dar nos sítios ativos das moléculas confinadas nos espaços interlamelares, aumentando a seletividade e eficiência dos processos reacionais ou catalíticos.15 Na área fotofísica, espécies excitadas podem ser geradas com um tempo de vida (ou de emissao) bem maior, quando confinadas nas cavidades das matrizes.16 Essa abordagem amplia consideravelmente o espectro de utilizaçao e de interesse dos sistemas, visto que os íons metálicos constituem centros de reatividade substitucional, redox ou fotoquímica e, quando colocados em ambientes apropriados, proporcionam atividade catalítica e de sensoriamento analítico.17 Recentemente, Chen e colaboradores18 reportaram a aplicaçao de nanopartículas de UiO-67 modificadas com o íon complexo [Ru(bpy)3]2+ para a detecçao precoce de tumores utilizando diagnóstico por imagem fluorescente, que permite a visualizaçao de células sem alterar sua morfologia ou integridade dos componentes celulares. Além disso, Chen e colaboradores18 mostraram que as nanopartículas de UiO-67 modificadas com o íon complexo de rutênio sao fotossensíveis e induzem a morte células tumorais humanas do tipo A549 (câncer de pulmao) pela geraçao de moléculas de oxigênio singlete. A combinaçao da estrutura das unidades metalo-orgânicas, em particular da MOF UiO-67, com as características espectroscópicas e eletroquímicas dos complexos de rutênio apresenta-se como uma opçao para a detecçao e determinaçao de moléculas gasosas de interesse ambiental. Contudo, antes de explorar a especificidade da matriz (MOF), somada à característica eletrônica do centro metálico, é necessário estudar as interaçoes existentes entre o centro metálico e a cavidade da MOF. Assim, o objetivo desse trabalho é imobilizar o complexo [RuCl2(ENAPY)], sendo ENAPY = N,N'-bis(7-metil-2-piridilmetileno)-1,2-diiminoetano, na estrutura metalo-orgânica UiO-67 e, por meio de técnicas espectroscópicas e eletroquímica, avaliar a influência da MOF nas características estrutural, eletrônica e redox do complexo de rutênio. As estruturas do complexo e da MOF UiO-67 estao representadas na Figura 1.
PARTE EXPERIMENTAL Os reagentes cloreto de rutênio hidratado (Aldrich), 2-acetilpiridina (Aldrich), etilenodiamina (Aldrich), cloreto de zircônio (Merck), ácido 4,4'-bifenildicarboxílico (BPDC, Merck), etanol (Merck), acetonitrila (Merck), dimetilformamida (Merck) e diclorometano (Merck) foram de grau analítico e utilizados sem purificaçao prévia na síntese dos compostos. O complexo de rutênio e a MOF UiO-67 foram sintetizados conforme procedimentos descritos na literatura.8,19 Para o complexo de rutênio, o resultado de análise elementar é coerente com a fórmula [RuCl2C16H18N4] - experimental (calculado): C: 43,79 (43,84); H: 4,19 (4,15); N: 12,72 (12,78)%. Modificaçao da MOF UiO-67 pelo complexo de rutênio Inicialmente foram preparadas as soluçoes: (A): 10 mg do complexo de rutênio dissolvidos em 5 ml de diclorometano; (B): 30 mg da MOF UIO-67 adicionados a 5 ml de diclorometano. A mistura foi submetida à agitaçao (agitador tipo vortex) por 5 minutos. Em seguida, misturou-se as soluçoes A e B, deixando em agitaçao mecânica por 3 dias. Posteriormente, centrifugou-se a mistura reacional por 15 minutos em 2000 rpm. O sólido obtido foi ressuspendido em 5 mL de CH2Cl2 e centrifugado por mais 15 minutos a 2000 rpm. Esse processo foi realizado três vezes. Por fim, o sólido foi ressuspendido em 5 mL de acetona e centrifugado (esse processo foi realizado duas vezes). Caracterizaçao Espectro de RMN de 1H do complexo de rutênio, dissolvido em CDCl3, foi obtido à temperatura ambiente em um espectrômetro Varian Inova operando a 300 MHz. Os teores de C, H, N foram determinados no equipamento Perkin Elmer CHN-2000. Os difratogramas de raios X foram obtidos em um difratômetro AXS D8 Advance – Bruker, utilizando radiaçao Cu-Ka (λ = 1,541 Å) com ângulo de difraçao (2θ) na faixa de 5 a 40° em passo de 0,04°. Espectros de refletância difusa dos compostos sólidos foram obtidos em espectrofotômetro Lambda-1050 PerkinElmer. As análises de UV-Vis foram realizadas em soluçoes aquosas e acetonitrila em cubetas de quartzo e obtidas em um espectrofotômetro UV-VIS Cary 50 Scan Varian. Espectros FTIR foram obtidos em espectrômetro Nicolet iZ10, Thermo Fisher Scientific, em pastilha de KBr na regiao de 4000 a 400 cm-1. A composiçao dos elementos que constituem o sistema MOF-complexo de rutênio foi analisada por espectroscopia fotoeletrônica de raios X, XPS, utilizando equipamento VG Microtech, anodo de Mg (risca Ka), analisador semi-hemisférico de 150 mm e 9 channeltrons, pressao de trabalho de 1 x 10-9 mBar, CAE = 50 eV e resoluçao energética de 0,80 eV. Voltamogramas cíclicos foram obtidos em potenciostato Metrohm Autolab, modelo PGSTAT101, utilizando soluçao de acetonitrila contendo 0,10 mol L-1 de perclorato de lítio como eletrólito suporte. A célula eletroquímica foi composta por: eletrodo de trabalho: platina; eletrodo de referência: Ag/AgNO3 0,01 mol L-1 e perclorato de lítio 0,10 mol L-1; eletrodo auxiliar: fio de platina.
RESULTADOS E DISCUSSAO Caracterizaçao dos precursores Ressonância Magnética Nuclear de 1H A composiçao da esfera de coordenaçao ao redor do íon rutênio(II) foi inferida pela análise do espectro de RMN de 1H do complexo dissolvido em clorofórmio deuterado (Figura 1S). No espectro foram observados dois sinais dubletos [δ = 8,65 ppm; d = 8,04 ppm] e dois sinais tripletos [δ = 7,84 ppm; d = 7,48 ppm], que foram atribuídos aos prótons aromáticos dos anéis piridínicos do ligante ENAPY coordenado ao centro metálico. Os prótons dos grupos CH3 foram associados ao sinal de ressonância com valor de deslocamento químico igual a 2,75 ppm. Verificou-se, também, um singleto em δ 2,60 ppm que foi atribuído aos prótons dos grupos CH2. A partir dos valores de integraçao dos sinais de ressonância, determinou-se a relaçao estequiométrica entre o ligante ENAPY e o centro metálico que, neste caso, foi de 1:1. O padrao dos sinais de ressonância observado é coerente com a existência de um composto simétrico e, dentre os isômeros possíveis para esse sistema,20 pode-se concluir que o ligante ENAPY coordenou-se ao centro metálico através dos quatro átomos de nitrogênio disponíveis: dois dos grupos imina e dois dos anéis piridínicos. Essas ligaçoes perfazem as interaçoes no plano equatorial do complexo, que tem os dois anéis piridínicos e as duas iminas em posiçoes vicinais entre si. As posiçoes axiais do complexo sao ocupadas por íons cloreto. As atribuiçoes foram corroboradas por dados cristalográficos descritos na literatura.19 Difratometria de raios X: método do pó A difratometria de raios X foi utilizada para a identificaçao e caracterizaçao do sólido obtido da reaçao de cloreto de zircônio e ácido 4,4'-bisfenildicarboxilico (BPDC). O difratograma do sólido, Figura 2S, foi comparado com os dados descritos na literatura21 e o padrao de difraçao obtido foi característico da estrutura metalo-orgânica UiO-67. A estrutura da MOF é mantida pelas ligaçoes de ponte do zircônio com o ácido 4,4'-bisfenildicarboxílico, pela formaçao de ligaçoes com o oxigênio central na unidade Zr3O (classificadas como µ3-O), além das ligaçoes metal-OH localizadas no triangulo Zr3 (classificadas como µ3-OH). A estrutura desse cluster é estável, resultando em um sólido cristalino, de estrutura cúbica de face centrada e grupo espacial Fm3m, cuja organizaçao do reticulo cristalino resulta em cavidades octaédricas de diâmetro ~20 Å e interstícios tetraédricos de diâmetro de ~12 Å.8 Caracterizaçao do sistema MOF UiO-67/[RuCl2(ENAPY)] O indicativo da imobilizaçao do complexo de rutênio na MOF UiO-67 foi dado pela mudança de coloraçao da UiO-67. A MOF inicialmente branca adquiriu coloraçao azul. Dois dias após a síntese, o sistema UiO-67/complexo de cor azul mudou de coloraçao, passando a apresentar a cor vermelha. Essa alteraçao de coloraçao é justificada pelo comportamento do complexo de rutênio na presença de água. A reaçao do cloreto de rutênio com o ligante imínico ENAPY, em etanol e presença de cloreto de lítio, leva à formaçao do complexo [RuCl2(ENAPY)] que dissolvido em solventes orgânicos gera soluçoes de cor azul. Na presença de água, ocorre a troca dos ligantes axiais (de íons Cl- por moléculas de água) levando à formaçao do aquocomplexo de rutênio [Ru(ENAPY)(H2O)2]Cl2, de coloraçao vermelha, como pode ser observado na Figura 2. O processo de aquaçao do complexo de rutênio já está descrito na literatura22 e, por isso, optamos por nao reproduzi-lo aqui. Dessa forma, os dados espectroscópicos e eletroquímicos apresentados a seguir correspondem ao sistema UiO-67/[Ru(ENAPY)(H2O)2]Cl2.
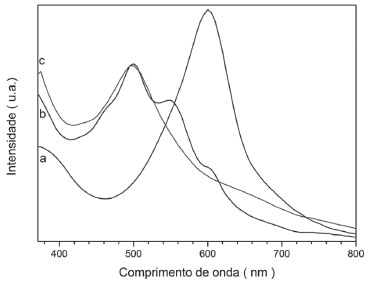 Figura 2. Espectros eletrônicos do complexo de rutênio em: (a) acetonitrila {[RuCl2(ENAPY)]}; (b) acetonitrila contendo 5% v/v de água destilada após 5 minutos {[RuCl(H2O)(ENAPY)]+ intermediário, nao isolado}; (c)acetonitrila contendo 5% v/v de água destilada após 20 minutos {[Ru(ENAPY)(H2O)2]2+}, à temperatura ambiente
Além disso, a análise de XPS comprovou a inserçao do complexo na unidade MOF UIO-67, que é constituída de 1,0% de Zircônio; 68,7% de Carbono; 3,0% de Oxigênio; 26,8% de Nitrogênio e 0,4% de Rutênio em massa do sistema. Na Figura 3 o pico em 400 eV foi atribuído à transiçao de elétrons envolvendo orbitais 1s e 2s dos átomos de nitrogênio, bem como o pico em 462 eV foi associado à transiçao eletrônica centrada no rutênio (3p2/3 ® 4d3/2 (ou 4d5/2)).23
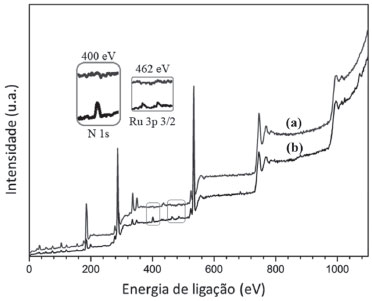 Figura 3. Espectros de XPS da MOF UiO-67 (a), e da MOF UiO-67 modificada com complexo de rutênio (b). Em destaque os sinais referentes as transiçoes eletrônicas envolvendo orbitais 1s do N e 3p2/3 do Ru(II)
Espectros eletrônicos na regiao do UV-Visível O espectro eletrônico do complexo imobilizado na MOF UiO-67 obtido por refletância difusa, Figura 4b, apresentou uma banda em λ = 520 nm e um ombro em λ = 380 nm atribuídos aos processos de transferência de carga metal – ligante {MLCT, Ru(t2g6) → π*(ENAPY)}.22,24 Comparando-se os espectros do complexo em soluçao (Figura 4c) e imobilizado na MOF (Figura 4b), nota-se um deslocamento batocrômico da banda MLCT (λsoluçao = 500 ;nm; λimobilizado = 520 nm). Este deslocamento pode ser justificado pelas interaçoes do complexo de rutênio com as cavidades da matriz via ligaçoes de hidrogênio das moléculas de água coordenadas axialmente ao centro metálico com as hidroxilas presentes no cluster de zircônio {Zr–µ3–OH.....H2O–RuII–H2O..... OH–µ3–Zr}. As ligaçoes de hidrogênio aproximam a base de Schiff coordenada ao rutênio dos ligantes 4,4'-bisfenildicarboxilicos (BPDC) que conectam os clusters de zircônio, favorecendo as interaçoes das nuvens eletrônicas dos anéis aromáticos desses ligantes. As interaçoes π -π dos ligantes ENAPY – BPDC, por efeito indutivo de corrente de anel, diminuem a densidade eletrônica ao redor do centro metálico, estabilizando os níveis dπ do rutênio(II) e, consequentemente, deslocando a banda MLCT do complexo de rutênio.
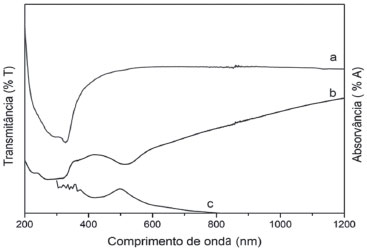 Figura 4. Espectros eletrônicos na regiao do UV-Visível dos compostos: (a) MOF UiO-67 (modo refletância difusa); (b) MOF UiO-67 modificada com complexo de rutênio (modo refletância difusa); (c) complexo de rutênio em soluçao aquosa
Voltametria Cíclica A matriz UiO-67 nao apresentou processos redox associados aos clusters de zircônio, tampouco às moléculas de solventes inclusas nas cavidades da estrutura metalo-orgânica, como mostrado na Figura 5a, o que está de acordo com o comportamento eletroquímico dessa classe de MOF conforme dados da literatura.25
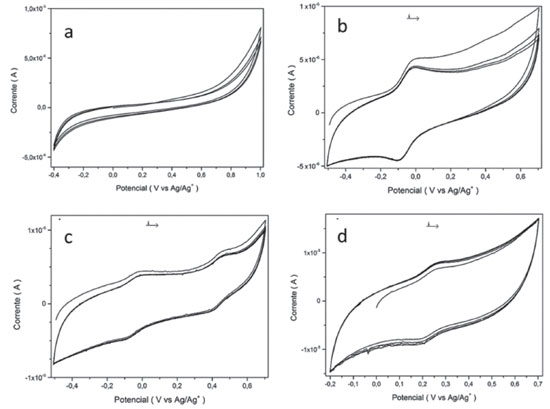 Figura 5. Voltamogramas cíclicos de: (a) MOF UiO-67; (b) complexo de rutênio em acetonitrila; (c) complexo de rutênio em acetonitrila contento água destilada; (d) MOF UiO-67 modificada com complexo de rutênio. Solvente acetonitrila contendo 0,10 mol L-1 de LiClO4, eletrodo de trabalho: platina; eletrodo de referência: Ag/AgNO3 0,01 mol L-1 + LiClO4 0,10 mol L-1; eletrodo auxiliar: fio de platina, sentido de varredura anódico, velocidade de varredura 100 mV s-1
No voltamograma cíclico do complexo de rutênio, em acetonitrila – Figura 5b, verificou-se um par de ondas reversível e monoeletrônico com valor de E½ = -0,05 V (vs Ag/Ag+) atribuído ao processo redox RuII – RuIII. Assim como nos complexos polipiridínicos de rutênio,26 o processo de oxidaçao do [RuCl2(ENAPY)] é centrado no metal e leva à formaçao da espécie [RuIIICl2(ENAPY)]+1, de configuraçao dπ(t2g5). Ao adicionar água à soluçao do complexo dissolvido em acetonitrila (0,5 mL de água em 5 mL de acetonitrila), Figura 5c, verificou-se dois pares de ondas reversíveis com valores de E½ = -0,05 V e E½ = +0,45 V (vs Ag/Ag+) atribuídos aos processos redox RuII – RuIII das espécies [RuCl2(ENAPY)] e [Ru (H2O)2(ENAPY)]2+, respectivamente. A substituiçao dos ligantes axiais (de Cl- por H2O) fez com que o potencial de oxidaçao do centro metálico deslocasse em aproximadamente 400 mV no sentido positivo, que pode ser justificado pelo acréscimo de carga positiva sobre o complexo em funçao da troca de um ligante σ/π-doador (íon cloreto, classificado como ligante de campo fraco) por outro ligante com caráter σ-doador (molécula de água, classificada como ligante de campo moderado). No voltamograma cíclico do sistema UiO-67/complexo de rutênio, Figura 5d, observou-se apenas um par de ondas reversível com valor de E½ = 0,25 V (vs Ag/Ag+) atribuído à oxidaçao/reduçao do centro metálico {Ru2+ (t2g6) Como mencionado anteriormente, o complexo de rutênio incorporado na matriz UiO-67 é o [Ru (H2O)2(ENAPY)]2+, haja vista a tendência de aquaçao do complexo precursor. Contudo, quando comparamos os valores de potencial de oxidaçao do aquocomplexo em soluçao (E½ = 0,45 V) e imobilizado (E½ = 0,25 V) notamos um deslocamento de 200 mV, o que é coerente com o comportamento espectroscópico e reflete a estabilizaçao dos níveis dπ do metal no aquocomplexo induzida pelas interaçoes do complexo de rutênio com as cavidades da matriz via ligaçoes de hidrogênio das moléculas de água coordenadas axialmente ao centro metálico com as hidroxilas presentes no cluster de zircônio {Zr–µ3–OH....H2O–RuII–H2O.....OH–µ3–Zr}. Espectros vibracionais na regiao do Infravermelho (FTIR) Como mencionado, a UiO-67 é constituída por clusters octaédricos de [Zr6O4(OH)4] ligados a moléculas de ácido 4,4'-bisfenildicarboxílico, formando uma estrutura supramolecular organizada, simétrica e tridimensional com cavidades octaédricas e tetraédricas.8 O cluster de zircônio é estabilizado por grupos carboxílicos na conformaçao eclipsada (syn-syn), por átomos de oxigênio e grupos hidroxilas ligados aos íons de zircônio(IV), formando as interaçoes do tipo µ3-O e e µ3-OH, como ilustrado na Figura 1. O espectro vibracional da MOF UiO-67, Figura 6b, é caracterizado por uma banda intensa e alargada na regiao de 3500 cm-1 atribuída aos estiramentos assimétricos das ligaçoes O-H de moléculas de água adsorvidas na MOF somados aos estiramentos assimétricos dos fragmentos hidroxilas µ3-OH da estrutura metal-orgânica. Em 1670 cm-1 e 1630 cm-1 foram observadas bandas relativamente intensas atribuídas aos estiramentos assimétricos em fase e fora de fase dos grupos COO- dos ácidos 4,4'-bisfenildicarboxílicos coordenados aos centros metálicos, respectivamente. A presença dos ácidos 4,4'-bisfenildicarboxílicos ligados aos íons de Zr(IV) também foi corroborada pelas bandas observadas em 1540 cm-1 associada ao estiramento assimétrico das ligaçoes C=C dos anéis aromáticos (νasC=Canel), 1425 cm-1 atribuída ao estiramento simétrico dos fragmentos carboxílicos (νsCOO-), 1350 cm-1 atribuída ao estiramento simétrico das ligaçoes C=C dos anéis aromáticos e 735 cm-1 associada às deformaçoes angulares das ligaçoes C=C e COO-. Duas bandas de intensidade relativamente fraca foram observadas em 620 cm-1 e 530 cm-1 atribuídas aos estiramentos assimétrico e simétrico, respectivamente, das ligaçoes Zr-OC=O. As bandas observadas em 680 cm-1 e 440 cm-1 foram associadas aos estiramentos dos átomos de oxigênio e dos grupos hidroxilas ligados aos íons de zircônio(IV), formando as interaçoes do tipo µ3-O e µ3-OH, respectivamente.
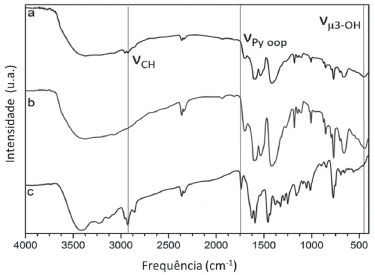 Figura 6. Espectros vibracionais na regiao do infravermelho dos compostos: (a) MOF UiO-67 modificada com complexo de rutênio; (b) MOF UiO-67; (c) complexo de rutênio, obtidos em pastilha de KBr
A imobilizaçao do complexo de rutênio na MOF UiO-67 nao alterou significativamente os modos vibracionais na unidade metalo-orgânica, como podemos observar no espectro vibracional do sistema UiO-67/complexo de rutênio, Figura 6a. Nesse caso, observamos um conjunto de bandas de intensidade relativamente fraca na regiao de 2900 cm-1 atribuído aos estiramentos assimétricos das ligaçoes C-H dos fragmentos CH2 e CH3 da base de Schiff coordenada ao rutênio. Verificamos também a ausência da banda em 1730 cm-1 (presente no espectro vibracional do complexo puro, Figura 6c) característica da deformaçao fora do plano do anel piridínico da base de Schiff. Além disso, notamos um deslocamento de 18 cm-1 da banda associada ao estiramento do fragmento µ3-OH da estrutura metalo-orgânica após a imobilizaçao do complexo de rutênio (νµ3-OH = 440 cm-1 para UiO-67; νµ3-OH = 458 cm-1 para UiO-67/complexo). A partir dessas observaçoes podemos inferir que interaçao do complexo de rutênio com a UiO-67 ocorreu próxima aos fragmentos µ3-OH, cuja localizaçao está destacada na Figura 1. As dimensoes desses microambientes tendem a dificultar os movimentos de deformaçao fora do plano dos anéis piridínicos da base de Schiff (νpy-oop), o que justifica o desaparecimento da banda atribuída a esse modo vibracional. Finalmente, os dados vibracionais aliados ao difratograma de raios-X de pó indicaram que as características estruturais da MOF nao foram alteradas pela presença do complexo de rutênios nos microambientes da UiO-67. Difratometria de raios X: método do pó No difratograma do complexo de rutênio, Figura 7c, verificou-se a ausência de picos de difraçao, revelando a característica amorfa desse derivado metálico. Para a matriz UiO-67 foram obtidos dois difratogramas: o primeiro logo após a síntese da MOF, Figura 7b', e o segundo após o processo de secagem da amostra, Figura 7b. O difratograma obtido da MOF UiO-67 logo após a síntese apresentou apenas dois picos de difraçao com valores de 2θ = 5,7° e 6,6° correspondentes aos planos [111] e [200] da estrutura metalo-orgânica, revelando baixo grau de cristalinidade do pó. Por outro lado, o difratograma da MOF UiO-67 obtido após o processo de secagem apresentou picos de difraçao melhores definidos, indicando elevado grau de cristalinidade da amostra. A atribuiçao dos picos de difraçao do pó da matriz UiO-67 está apresentada na Figura 2S, por isso optamos por nao reproduzir nessa etapa.
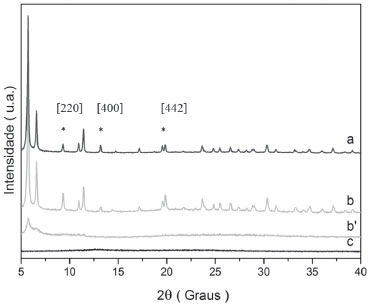 Figura 7. Difratogramas de raio-X método do pó dos compostos: (a) MOF UiO-67 modificada com complexo de rutênio; (b) MOF UiO-67 após etapa de secagem; (b')MOF UiO-67 antes da etapa de secagem; (c) complexo de rutênio
A imobilizaçao do complexo de rutênio na UiO-67 nao alterou significativamente os picos de difraçao da MOF, como podemos observar no difratograma da Figura 7a, mostrando que o arranjo cristalino da MOF é preservado. No entanto, a intensidade relativa dos picos de difraçao com valores de 2θ = 9,2°, 13,5° e 20° foram alteradas após a inclusao do complexo na matriz (intensidade de pico antes da inclusao: I9,2 = 30,4; I13,5 = 24,3; I20 = 26,7; intensidade de pico após a inclusao: I9,2 = 44,7; I13,5 = 42,6; I20 = 41,3). Essa alteraçao de intensidade dos picos sugere que o complexo de rutênio está inserido na MOF e promove uma readequaçao dos microambientes da estrutura cristalina correspondentes aos planos [220], [400] e [442]. Método Brunauer-Emmett-Teller O método BET forneceu as áreas superficiais dos sólidos UiO-67 e UiO-67 modificada com o complexo de rutênio. A MOF UIO-67 apresentou uma área superficial de aproximadamente 1900 m2 por grama de composto, o que é coerente com os dados descritos na literatura para os derivados UiO.8-10 Já a MOF modificada com o complexo de rutênio apresentou valor de aproximadamente 1400 m2 por grama de composto. Com a inserçao do complexo na MOF houve um decréscimo de área disponível na estrutura cristalina e porosa da UiO-67, revelando que o derivado de rutênio está inserido nos microambientes da matriz e compete com as moléculas de N2 pelo espaço disponível na amostra de UiO-67.
CONCLUSAO A imobilizaçao do complexo de rutênio com a unidade MOF UiO-67 ocorreu de forma espontânea e foi direcionada por ligaçoes de hidrogênio das moléculas de água coordenadas axialmente ao centro metálico com as hidroxilas presentes no cluster de zircônio. As ligaçoes intermoleculares aproximaram a base de Schiff coordenada ao rutênio dos ligantes 4,4'-bisfenildicarboxilicos (BPDC) que conectam os clusters de zircônio, favorecendo as interaçoes das nuvens eletrônicas dos anéis aromáticos desses ligantes que, por efeito indutivo de corrente de anel, diminuiram a densidade eletrônica ao redor do centro metálico, estabilizando os níveis dπ do rutênio(II). A imobilizaçao do complexo de rutênio na estrutura da UiO-67 promoveu uma readequaçao dos microambientes da estrutura cristalina, a qual diminuiu a capacidade de absorçao e armazenamento de gás nos microambientes da MOF.
MATERIAL SUPLEMENTAR Estao disponíveis em http://quimicanova.sbq.org.br, com acesso livre, o espectro de RMN 1H do complexo [RuCl2(L)] obtido em clorofórmio deuterado (Figura 1S) e o difratograma de raios-X, método do pó, do composto precursor UiO-67 contendo os índices de Miller para planos da estrutura cúbica da MOF (Figura 2S).
AGRADECIMENTOS Os autores agradecem à Fundaçao Araucária/Paraná e ao CNPq pelo suporte financeiro na execuçao do projeto de grupo.
REFERENCIAS 1. Batten, S. R.; Champness, N. R.; Chen, X.-M.; Garcia-Martinez, J.; Kitagawa, S.; Öhrstrom, L.; O'Keeffe, M.; Suh, M. P.; Reedijk, J.; Pure Appl. Chem. 2013, 85, 1715; Oar-Arteta, L.; Wezendonk, T.; Sun, X.; Kapteijn, F.; Gascon, J.; Mater. Chem. Front. 2017, 1, 1709; Semino, R.; Moreton, J. C.; Ramsahye, N. A.; Cohen, S. M.; Maurin, G.; Chem. Sci. (2018), doi.: 10.1039/c7sc04152g. 2. Kaskel, S.; The Chemistry of Metal Organic Frameworks: Synthesis, Characterization, and Applications, vol. 1, 1th ed., Wiley: New York, 2016. 3. Leong, W. L.; Vittal, J. J.; Chem. Rev. 2011, 111, 688. 4. Sinelshchikova, A. A.; Nefedov, S. E.; Enakieva, Y. Y.; Gorbunova, Y. G.; Tsivadze, A. Y.; Kadish, K. M.; Chen, P.; Bessmertnykh-Lemeune, A.; Stern, C.; Guikard, R.; Inorg. Chem. 2013, 52, 999. 5. Easun, T. L.; Jia, J.; Calladine, J. A.; Blackmore, D. L.; Stapleton, C. S.; Vuong, K. Q.; Champness, N. R.; George, M. W.; Inorg. Chem. 2014, 53, 2606; Tian, J.; Xu, Z.-Y.; Zhang, D.-W.; Wang, H.; Xie, S.-H.; Xu, D.-W.; Ren, Y.-H.; Wang, H.; Liu, Y.; Li, Z.-T.; Nature Commun. 2016, 7, 11580. 6. Yap, M. H.; Fow, K. L.; Chen, G. Z.; Green Energy Environ. 2017, 2, 218. 7. Cavka, J. H.; Jakobsen, S.; Olsbye, U.; Guillou, N.; Lamberti, C.; Bordiga, S.; Lillerud, K. P.; J. Am. Chem. Soc. 2008, 130, 13850. 8. Katz, M. J.; Brown, Z. J.; Colon, Y. J.; Siu, P. W.; Scheidt, K. A.; Snurr, R. Q.; Hupp, J. T.; Farha, O. K.; Chem. Commun. 2013, 49, 9449. 9. Lawrence, M. C.; Schneider, C.; Katz, M. J.; Chem. Commun. 2016, 52, 4971. 10. Gutov, O. V.; Hevia, M. G.; Escudero-Adan, E. C.; Shafir, A.; Inorg. Chem. 2015, 54, 8396. 11. Dalapati, R.; Biswas, S.; Sens. Actuators, B 2017, 239, 759. 12. Hu, J. B.; Liu, Y.; Liu, J.; Gu, C.K.; Wu, D. W.; Microporous Mesoporous Mater. 2018, 256, 25; Ahmad, M. Z.; Navarro, M.; Lhotka, M.; Zornoza, B.; Tellez, C.; Fila, V.; Coronas, J.; Sep. Purif. Technol. 2018, 192, 465. 13. Liang, H. X.; Jiao, X. L.; Li, C.; Chen, D. R.; J. Mater. Chem. A 2018, 6, 334. Shaabani, A.; Mohammadian, R.; Hooshmand, S. E.; Hashemzadeh, A.; Amini, M. M.; Chem. Select 2017, 2, 11906. 14. Larsen, R. W.; Mayers, J. M.; Wajtas, L.; Dalton Trans. 2017, 46, 12711; Zhao, J.; Wang, Q.; Sun, C. Y.; Zheng, T. T.; Yan, L. K.; Li, M. T.; Shao, K. Z.; Wang, X. L.; Su, Z. M.; J. Mater. Chem. A 2017, 5, 12498. Larsen, R.W.; Wojtas, L.; J. Solid State Chem. 2017, 247, 77; Guan, B. Y.; Yu, X. Y.; Wu, H. B.; Lou, X. W.; Adv. Mater. 2017, 29, 1703614; Downes, C. A.; Marinescu, S. C.; ChemSusChem 2017, 10, 4374; Chaudhari, A. K.; Ryder, M. R.; Tan, J.-C.; Nanoscale 2016, 8, 6851. 15. Takashima, Y.; Fukuhara, Y.; Sato, Y.; Tsuruoka, T.; Akamatsu, K.; Eur. J. Inorg. Chem. 2017, 45, 5344; Shu, X.; Yu, Y.; Jiang, Y.; Luan, Y.; Ramella, D.; Appl. Organomet. Chem. 2017, 31, 3862; Pourkhosravani, M.; Dehghanpour, S.; Farzaneh, F.; Sohrabi, S.; React. Kinet., Mech. Catal. 2017, 122, 961; Tang, L.; Shi, J. F.; Wang, X.L.; Zhang, S. H.; Wu, H.; Sun, H. F.; Jiang, Z. Y.; Nanotechnology 2017, 28, 275601. 16. Zhang, W. X.; Li, B.; Ma, H. P.; Zhang, L. M.; Guan, Y. L.; Zhang, Y. H.; Zhang, X. D.; Jing, P. T.; Yue, S. M.; ACS Appl. Mater. Interfaces 2017, 8, 21465; Chen, R.; Zhang, J.; Chelora, J.; Xiong, Y.; Kershaw, S. V.; Li, K. F.; Lo, P. K.; Cheah, K. W.; Rogach, A. L.; Zapien, J. A.; ACS Appl. Mater. Interfaces 2017, 9, 5699; Bennett, T. D.; Cheetham, A. K.; Acc. Chem. Res. 2014, 47, 1555. 17. Rogge, S. M. J.; Bavykina, A.; Hajek, J.; Garcia, H.; Olivos-Suarez, A. I.; Sepulveda-Escribano, A.; Vimont, A.; Clet, G.; Bazin, P.; Kapteijn, F.; Daturi, M.; Ramos-Fernandez, E. V.; Llabrés-Xamena, F. X.; van Speybroeck, V.; Gascom, J.; Chem. Soc. Rev. 2017, 46, 3134; Campbell, M. G.; Dinca, M.; Sensors 2017, 17, 1108; Lin, R.-B.; Liu, S.-Y.; Ye, J.-W.; Li, X.-Y.; Zhang, J.-P.; Adv. Sci. 2016, 3, 1500434. 18. Chen, R.; Zhang, J.; Chelora, J.; Xiong, Y.; Kershaw, S. V.; Li, K. F.; Lo, P.-K.; Cheah, K. W.; Rogach, A. L.; Zapien, J. A.; Lee, C.-S.; ACS Appl. Mater. Interfaces 2017, 9, 5699. 19. Pal, S.; Pal, S.; Polyhedron 2003, 22, 867. 20. Da Silva, A. P.; Gauze, G. F.; Matias, T. A.; de Souza, V. R.; Rozada, T. C.; Basso, E.; Tetrahedron Lett. 2011, 52, 5043. 21. David, J.; Trolliard, G.; Volkringer, C.; Loiseau, T.; Maitre A.; RSC Adv. 2015, 5, 51650. 22. de Souza, V. R.; Nunes, G. S.; Rocha, R. C.; Toma, H. E.; Inorg. Chim. Acta 2003, 348, 50. 23. Handbook of X-ray data, Zschornack, G., org.; Springer-Verlag, Berlin, 2007. 24. De Souza, V. R.; Ferreira, A. M. C.; Toma, H. E.; Dalton Trans. 2003, 458. 25. Morozan, A; Jaouen, F ; Energy Environ. Sci. 2017, 5, 9269 26. Juris, A.; Balzani, V.; Barigelletti, F.; Belser, P.; von Zelewsky, A.; Coord. Chem. Rev. 1988, 84, 85. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access






 Ru3+ (t2g5)}.
Ru3+ (t2g5)}.