Artigo
|
|
| Efeito da concentração dos íons Eu3+ e Bi3+ nas propriedades fotoluminescente da matriz de YVO4 Concentration effect of the Eu3+ and Bi3+ in the photoluminescence properties of YVO4 matrix |
|
Marcela G. MatosI; Emerson H. de FariaI; Katia J. CiuffiI; Lucas A. RochaI; Eduardo J. NassarI,*; Marc VerelstII
I. Universidade de Franca, Av. Dr. Armando Salles Oliveira, 201, Pq. Universitário, 4404-600 Franca - SP, Brasil Recebido em: 29/01/2018 *e-mail: eduardo.nassar@unifran.edu.br Inorganic matrices have been extensively studied for several applications, mainly doped with lanthanoid ions presenting special spectroscopic properties. The radiation emission can be affected by several factors, such as; matrix, synthesis methodology, activating ions and sensitizers, and concentrations. Thus, in this work the matrix of yttrium vanadate doped with Eu3+ ions as activator and Bi3+ ions as sensitizer was prepared by the non-hydrolytic sol-gel methodology. Europium (III) and Bismuth (III) ions concentrations were varied in 1, 3 and 5% in mol with respect to the Y3+ ion and the samples were heat treated at 1000 °C. The X-ray diffraction analyzes showed a single phase of the yttrium vanadate matrix, indicating the non-influence of the dopant ions on the crystalline structure. The dopants concentrations presented influences on the spectroscopic properties of the emitting ion, the intensity parameters (Ω2 e Ω4), increased as a function of the increase of Bi3+ concentration, affecting the covalence of the bond and the rigidity of the system. The increase of Eu3+ concentration directly affected its environment, decreasing the symmetry and increasing the quantum efficiency. Finally, increasing the dopant ions promoted the decreasing the crystallite size. INTRODUÇAO Atualmente a aplicaçao dos elementos lantanóides tem sido vasta, englobando craqueamento de petróleo, catalisador automotivo, imas permanentes, lasers, ligas, eletrônica, iluminaçao, concentradores solares, bio-análises, imageamento, visao noturna, comunicaçao, entre outros.1 Diante de tantas aplicaçoes, as propriedades luminescentes sao de suma importância, a utilizaçao em pequenas quantidades como ativadores ou dopantes em matrizes hospedeiras, preservam suas características espectroscópicas, tais como: tempo de vida na ordem de milissegundos, finas bandas de emissao e grande deslocamento Stokes.2,3 Em 1962, Judd4 e Ofelt5 estudaram independentemente os mecanismos de dipolo elétrico forçado atuantes nas transiçoes f-f possibilitam as transiçoes de estados de mesma paridade. Os parâmetros de intensidade fenomenológicos de Judd-Ofelt (Ωl, sendo λ = 2, 4 e 6) estudados trazem informaçoes sobre a covalência da ligaçao química, qualidade e propriedades mecânicas do ambiente ao redor do íon, podendo ser calculados a partir dos espectros de absorçao ou emissao dos íons lantanóides, utilizando os cálculos propostos por Judd-Ofelt.6 A inserçao de íons metálicos (Bi3+, Pb2+, Ba2+, Li+) em matrizes hospedeiras tem sido uma estratégia para sensibilizar os íons Ln3+, intensificando a emissao desses através de transferência de energia.7 O íon Bi3+ é um metal de configuraçao 6s2 muito empregado como sensibilizador em matrizes hospedeiras, pois apresenta intensa e larga banda de absorçao na regiao do UV, característica da transiçao 1S0 → 3P0, a qual pode transferir energia para os estados excitados dos ativadores (íons Ln3+) com níveis de menor energia, resultando na amplificaçao da luminescência,8-16 a importância do uso do íon Bi3+ tem sido mostrado na literatura como bom sensibilizador para a matriz YVO4.17-22 O processo sol-gel é conhecido por ser uma metodologia utilizada no preparo de diversas matrizes hospedeiras contendo os íons Ln3+,23 sendo a rota sol-gel nao-hidrolítica importante para a formaçao dos óxidos inorgânicos, empregando solventes orgânicos e sais metálicos como precursores. Esta rota promove a formaçao de partículas inorgânicas de diversas formas e tamanhos influenciada pela escolha do solvente que atua como doador de oxigênio.24 Uma variedade de redes hospedeiras podem ser obtidas por essa metodologia.20,25-44 Diante disso, o objetivo deste trabalho foi obter por meio do processo sol gel rota nao-hidrolítica a matriz de YVO4 dopadas com o íon ativador Eu3+ e Bi3+ como sensibilizador, ambos em diferentes concentraçoes com o intuito de promover a intensificaçao da emissao do íon Eu3+. As caracterizaçoes foram realizadas através da difraçao de raios X para identificaçao da fase cristalina formada e fotoluminescência do íon Eu3+ avaliando as propriedades espectroscópicas.
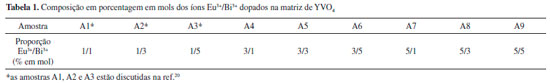
EXPERIMENTAL Preparo dos precursores Os precursores metálicos utilizados na preparaçao da matriz de YVO4, YCl3, EuCl3 e VOCl4 foram obtidos conforme descrito por Matos et al.20,28,33,38 Os respectivos óxidos foram calcinados à 900 ºC e dissolvidos em HCl para a formaçao dos respectivos cloretos. As massas necessárias foram pesadas para a obtençao da soluçao de concentraçao de 0,1 mol L-1, o pH da soluçao foi ajustado entre 4 e 5. Após total dissoluçao e sob aquecimento, foi adicionado lentamente álcool etílico até obtençao da soluçao etanólica. Preparo da matriz via sol gel O processo Sol Gel rota nao hidrolítica vem sendo utilizado em nosso grupo de pesquisa Sol Gel - UNIFRAN, a partir do método publicado por Acosta et al.,45 modificaçoes foram sendo realizadas para adaptaçao do método.20,28,29,33,35,36,38,46 A matriz de vanadato de ítrio apresenta fórmula genérica ABO4 com íons Y3+ pertencentes ao sítio A e íons V5+ ao sítio B, as porcentagens dos precursores em mols dos íons Eu3+ e Bi3+ foram em substituiçao ao sítio A (Y3+) e estao descritas na Tabela 1, o solvente utilizado para todas as sínteses foi o álcool etílico PA.
Os sólidos obtidos após secagem em estufa a 100 °C apresentaram caráter bastante higroscópico, necessitando de serem armazenadas em dessecador sob vácuo, as amostras sofreram tratamento térmico à 1000 ºC por 4 h. Caracterizaçoes Difraçao de raios X (DRX) Os difratogramas de raios X por meio do método do pó, foram realizados em um difratômetro RIGAKU MiniFlex II operando à 30 kV e 15 mA utilizando um monocromador da radiaçao CuKa (λ = 1,5405 Å), variando o ângulo de obtençao entre 10 - 70°. Todas as amostras foram processadas com passo de 0,05°/10 s. Espectroscopia fotoluminescente (FL) Os espectros foram obtidos a partir das amostras no estado sólido, acondicionados em capilares, à temperatura ambiente, sob excitaçao contínua com lâmpada de Xe (450 W). O espectrofluorímetro utilizado foi Horiba Jobin Yvon Fluorolog3 equipado com monocromadores duplo (excitaçao e emissao) e fotomultiplicadora R 928 Hammatsu. A emissao coletada a 90° do feixe de excitaçao. As fendas de excitaçao e emissao utilizadas foram posicionadas, respectivamente, em 2,0 e 1,0 nm com tempo de integraçao igual a 0,5 ms e passo de 0,5 nm. O filtro de emissao utilizado foi G1227 (100% de transmitância, para λ > 450 nm). As curvas de decaimento radiativo foram obtidas utilizando-se um acessório de fosforimetria equipado com uma lâmpada pulsada de Xe (5 J/pulso).
RESULTADOS E DISCUSSAO As Figuras 1 e 2 apresentam os difratogramas de raios X para as amostras A4 à A9, tratadas à 1000 ºC para as amostras A1, 2 e 3 nao estao apresentados, os difratogramas constam na literatura.20
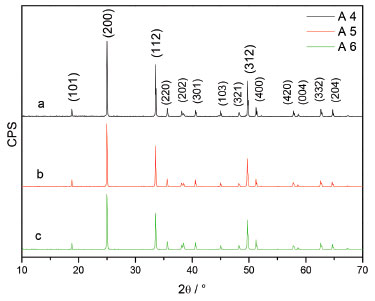 Figura 1. DRX da matriz YVO4 dopado com 3% de íon Eu3+ variando a concentraçao do íon Bi3+, a) 1%, b) 3% e c) 5%
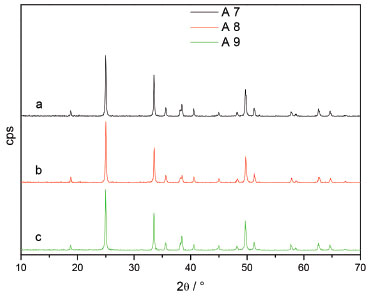 Figura 2. DRX da matriz YVO4 dopado com 5% de íon Eu3+ variando a concentraçao do íon Bi3+, a) 1%, b) 3% e c) 5%
Os picos observados nos difratogramas estao em conformidade com os da matriz de YVO4, nenhum pico relacionados aos óxidos de ítrio III, európio III, bismuto III e vanádio V estao presente nas Figuras 1 e 2. A Tabela 2 apresenta os índices de Miller para os três principais picos e suas respectivas porcentagem com relaçao a intensidade.
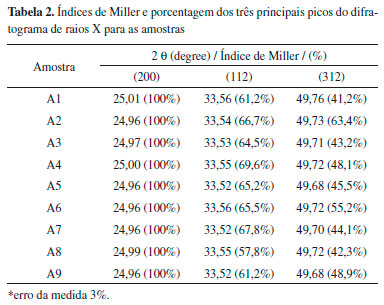
Com exceçao das amostras A2 e 6, todas as outras apresentaram porcentagens de intensidades dos picos com índice de Miller (112) e (312) em relaçao ao pico (200), em concordância com o padrao de difraçao JCPDS 72-274, os quais foram atribuídos à fase tetragonal de corpo centrada, com grupo espacial I41/amd (D4h). As amostras A2 e 6 apresentaram porcentagens dos picos em 2q = 33,5 e 49,7º muito próximas, semelhante ao padrao JCPDS 17-341, pertencendo ao mesmo grupo espacial. Os íons usado como dopantes na matriz YVO4 na substituiçao dos íons Y3+ apresentam raios iônicos próximos, afetando pouco a simetria do íon. O íon Y3+ ocupa um sítio de simetria D2d na forma de um bisdisfenoide circundado por oito ligantes O2- sem centro de inversao.12,47 Os íons Eu3+ e Bi3+ substituem os sítios dos íons Y3+ devido a similaridade dos raios iônicos entre eles 1,0920,30 (Eu3+), 1,2020 (Bi3+) e 0,88 Å,22 (Y3+), contudo distorçoes do sítio de simetria do íon Y3+ devem acontecer. A substituiçao dos íons V5+ é praticamente impossível devido à grande diferença entre os raios iônicos (V5+ raio 0,36 Å).48 A intensidade relativa dos picos dos difratogramas indica o crescimento preferencial no plano (200) da estrutura, que pode estar relacionado à inserçao de espécies mais volumosas no sítio A, ocasionando na distorçao da estrutura.49 O tamanho dos cristalitos podem ser estimados através da equaçao de Scherrer (Eq. 1),30,50 usando a largura a meia altura dos picos de reflecçao obtidos no DRX.  em que L é o tamanho médio dos cristalitos, λ comprimento de onda da radiaçao de raios X (0,154056 nm), K é uma constante relacionada a forma do cristalito e pode ser considerado igual a unidade, e β é a largura a meia altura dos picos em radiano. A Tabela 3 apresenta o tamanho médio dos cristalitos para as amostras obtidos a partir do difratogramas de raios X.
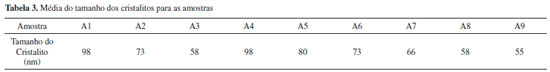
O tamanho médio dos cristalitos apresentou um comportamento semelhante para as amostras em funçao do aumento da porcentagem do íon Bi3+, para as amostras contendo porcentagens fixas de íon Eu3+ o tamanho do cristalito diminui com o aumento da concentraçao do íon Bi3+, fato que pode estar relacionado com a migraçao dos dopantes para a superfície ou regioes de contorno das partículas impedindo o seu crescimento.51,52 A Figura 3 mostra a dependência do tamanho do cristalito em funçao do aumento da concentraçao do íon Bi3+.
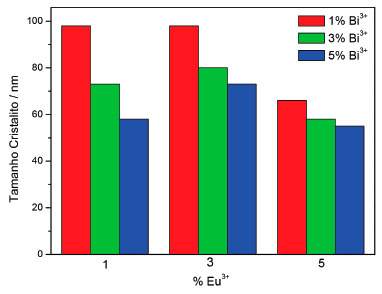 Figura 3. Tamanho do cristalito em funçao da concentraçao do íon Eu3+ e Bi3+
As amostras A7, 8 e 9 contendo a concentraçao fixa de 5% do íon Eu3+ apresentaram os menores valores de tamanho de cristalito, podendo ser atribuído a porcentagem final dos dopantes serem maior que as demais amostras. Saltarelli et al.30 obteve tamanho de cristalito ao redor de 28 nm para amostras preparadas na presença de catalisador e 55 nm na ausência, utilizando como precursor o cloreto de ítrio III e tratamento térmico de 800 ºC para obtençao da matriz. A mesma autora em 201527 sintetizou o YVO4 substituindo o precursor cloreto de ítrio III por alcóxido de ítrio III, obtendo cristalitos de 15 nm e 24 nm, para as amostras com e sem catalisador. Matos et al.28 preparando a matriz de vanadato de ítrio dopado com íon európio III e tratado à 1000 ºC obteve crsitalito na ordem de 50 nm. Todas as amostras foram preparadas com porcentagens fixa do íon Eu3+ em 1% em relaçao ao íon Y3+. Esses trabalhos mostraram que a metodologia, condiçoes de síntese, precursores, concentraçao e tipo de dopante influenciam no tamanho dos cristalitos. Fotoluminescência (FL) As Figuras 4 e 5 mostram os espectros de excitaçao para as amostras A4, 5, 6, 7, 8 e 9, da matriz YVO4:Eu3+:Bi3+ variando as concentraçoes dos dopantes e fixando o comprimento de onda de emissao em 618 nm. Os espectros para as amostras A1, 2 e 3 estao disponíveis na literatura.20
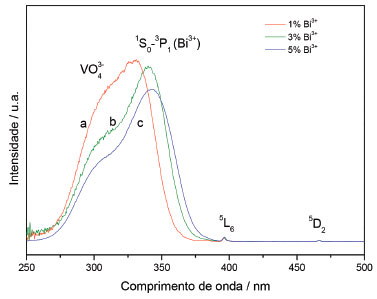 Figura 4. Espectro de excitaçao para matriz de YVO4 dopada com 3% do íon Eu3+ com variaçao da concentraçao do íon Bi3+ em 1% (a), 3% (b) e 5% (c)
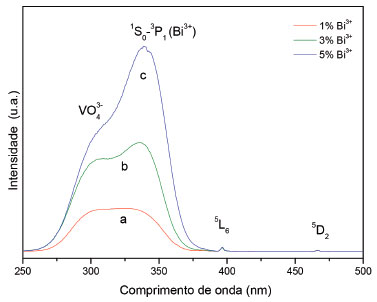 Figura 5. Espectro de excitaçao da matriz de YVO4 dopada com 5% de íons Eu3+ com variaçao da concentraçao de íons Bi3+ em 1% (a), 3% (b) e 5% (c)
A Tabela 4 apresenta os valores de comprimento de onda relativos as bandas de transferência de carga (BTC) atribuídas ao ânion vanadato e ao íon bismuto III para as amostras.
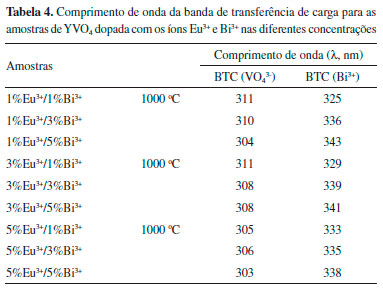
Os espectros de excitaçao dos sólidos foram obtidos à temperatura ambiente e sao apresentados nas Figuras 4 e 5, independente da concentraçao dos íons ativadores e sensibilizadores, observou-se considerável predominância da BTC em menores comprimento de onda entre 275 à 375 nm, em relaçao às bandas relativas as transiçoes f-f do íon Eu3+. Os espectros apresentam perfis semelhantes diferenciando dos máximos de excitaçao, como mostra a Tabela 4. Esses máximos sao atribuídos a transferência de carga O2- → V5+ do ânion VO43-.28,48,53 A energia desta banda está relacionada às transiçoes do nível do estado fundamental 1A2 (1T1) para os estados excitados 1A1 (1D) e 1B1 (1D) do ânion VO43-, de acordo com a teoria do orbital molecular,19 a transferência de energia ocorre mais facilmente do grupo VO43- para os íons Eu3+, devido à diferença de raio iônico entre V5+: 0,36 Å e Eu3+: 1,09 Å. O processo de excitaçao da espécie aniônica VO43- ocorre por processo de transiçao permitida.48 O comprimento de onda da BTC pode ser influenciado pelo número de coordenaçao, carga aniônica, grau de covalência e polarizabilidade da ligaçao química,53 a alta energia da BTC indica uma maior interaçao metal-ligante. Assim, com o aumento da concentraçao dos dopantes Eu3+ e Bi3+ observa-se um deslocamento para comprimentos de ondas maiores, menor energia, diminunido assim a interaçao metal-ligante, fato que pode estar relacionado às diferenças de raios iônicos Y3+ (0,88 Å), substituido por Eu3+ (1,09 Å) e Bi3+ (1,20 Å). Os íons Eu3+ incorporados na matriz de YVO4 estao substituindo os íons Y3+ no retículo devido a similaridade dos raios iônicos e o número de coordenaçao igual a 8.54 A literatura tem descrito a preparaçao da matriz YVO4 dopada com íons Eu3+ obtida pelo metodologia sol-gel hidrolítica e nao-hidrolítica,28,27,30 os quais apresentam bandas de transferência de carga no intervalo de 308 à 324 nm, uma banda simétrica. Nas amostras após a adiçao do íon Bi3+ a larga banda na regiao de menor comprimento de onda aparece assimétrica composto de pelo menos duas outras bandas (Tabela 4), as quais podem ser atribuídas ao ânion VO43- (λ = 303 à 311 nm)20 e ao íon Bi3+ (λ = 325 à 340 nm).8 As transiçoes f-f do íon Eu3+ presentes na regiao de baixa energia, entre os comprimento de onda de 380 até 500 nm, apresentaram menor intensidade em relaçao à BTC. As transiçoes 7F0 → 5L6 (396 nm) e 7F0 → 5D2 (467 nm) dentro da configuraçao 4f6 do íon Eu3+ foram observadas nos espectros de excitaçao de todas as amostras. As Figuras 6 e 7 apresentam os espectros de emissao do íon Eu3+ na matriz obtidos sob excitaçao monitorada no máximo da BTC e no nível 5L6 do íon Eu3+ para as amostras contendo 3 e 5% do íon Eu3+, os espectros da amostra contendo 1% já foram apresentados na literatura.20
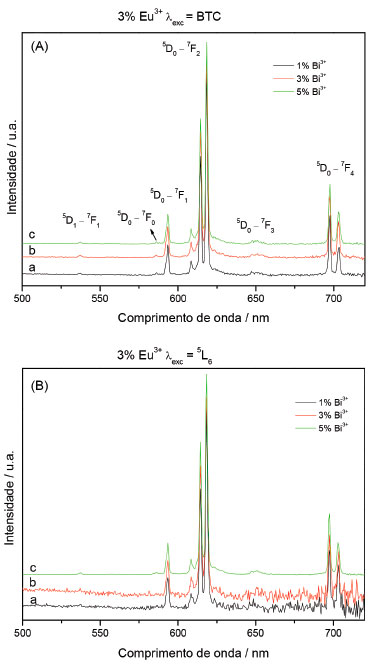 Figura 6. Espectros de emissao da matriz de YVO4 dopada com 3% do íon Eu3+ com variaçao da concentraçao do íon Bi3+ em 1% (a), 3% (b) e 5% (c), λexc = BTC (A) e 5L6 (B)
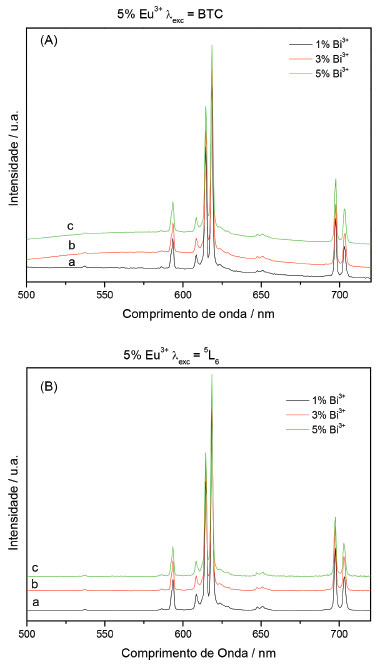 Figura 7. Espectros de emissao da matriz de YVO4 dopada com 5% do íon Eu3+ com variaçao da concentraçao do íon Bi3+ em 1% (a), 3% (b) e 5% (c), λexc = BTC (A) e 5L6 (B)
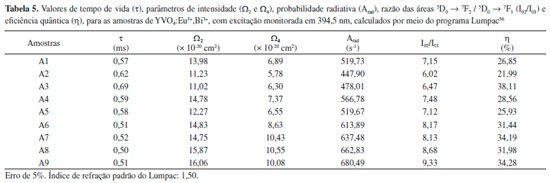
Os espectros de emissao das amostras apresentaram perfis semelhantes, independentemente da concentraçao dos dopantes e do comprimento de onda de excitaçao. As finas bandas sao caracterísitcas das transiçoes do íon Eu3+ relativas ao estado excitado 5D0 para o fundamental 7FJ (J = 0, 1, 2, 3 e 4), bandas na regiao de comprimento de onda ao redor de 530 nm, atribuídas às transiçoes 5D1 → 7F1, sao observadas para todas as amostras. Os difratogramas de raios X nao indicaram fases diferentes e nem a formaçao de óxido, apenas a fase do vanadato de ítrio, mesmo com a variaçao da porcentagem dos íons dopantes Eu3+ e Bi3+. Assim, os íons dopantes nao influenciaram a estrutura da matriz, independente do porcentagem utilizada. A similaridade nos espectros de emissao, quando excitados na BTC ou diretamente no nível 5L6 do próprio íon Eu3+ vem confirmar essas observaçoes do DRX. As larguras a meia alturas das bandas relativas as transiçoes 5D0 → 7F1 e 5D0 → 7F2 foram em torno de 2,0 nm, com erro de 0,1 nm, indicando o nao desdobramento dos estados energéticos do íon emissor, fato que deveria ocorrer se houvesse a existência de mais de um sítio emissor, portanto, a confirmaçao de um único sítio de simetria pode ser observado através dos espectros de emissao. A banda correspondente à transiçao de caráter dipolo-elétrico (DE) 5D0 → 7F2, centralizada em 618,5 nm, apresentou-se mais intensa em relaçao à transiçao de caráter dipolo-magnético (DM) 5D0 → 7F1, indicando que o íon Eu3+ ocupa um sítio sem centro de inversao de simetria. A transiçao 5D0 → 7F2 é conhecida como hipersensível, nos espectros obtidos nao foram observadas quaisquer alteraçoes da mesma, indicando que o íon Eu3+ ocupa o mesmo sítio de simetria na matriz, provavelmente com grupo pontual D2d.55 A presença da banda relativa à transiçao 5D0 → 7F0, centralizada em 588 nm, sugere que o íon Eu3+ ocupa um sítio sem centro de inversao de simetria. O perfil simétrico desta banda indica somente uma componente, confirmando que a emissao do íon Eu3+ ocorre a partir de um único sítio na matriz. Esses estados energéticos nao sofrem influência do campo cristalino (2J + 1), sendo observado somente uma banda no espectro de emissao. A Tabela 5 apresenta os parâmetros espectroscópicos das amostras contendo diferentes concentraçoes dos íons Eu3+ e Bi3+. Os tempos de vida do estado excitado (nível 5D0, monitorados na transiçao 5D0 → 7F2) foram obtidos por ajustes matemáticos dos decaimentos experimentais, as taxas de decaimento radiativo e as eficiências quânticas do nível 5D0 foram calculadas a partir dos espectros de emissao e dos tempos de vida, tendo a transiçao 5D0 → 7F1 (permitida por dipolo-magnético) como referência. Para obtençao dos parâmetros de intensidade de Judd-Ofelt utilizou-se o programa Lumpac.56
As curvas de tempo de vida de emissao (Figura 8) apresentaram decaimento nonoexponencial, indicando que o íon Eu3+ ocupa somente um sítio de simetria, confirmando a observaçao relativa a banda da transiçao 5D0 → 7F0. Os valores do tempo de vida sao similares para as diferentes comprimento de onda de excitaçao e das porcentagens dos íons Eu3+ e Bi3+, indicando que os relativamente baixos tempos de vida podem estar sendo influenciados pela ressonância entre os níveis de energia do íon Eu3+ e a banda de transferência de carga do íon Bi3+,20 além da energia de fônon da matriz, responsável pelos decaimentos nao radiativos. O tempo de vida do íon Eu3+ dopado na matriz de YVO4 obtido via sol-gel apresentam valores na ordem de 1,0 ms28,30,57 o decrescimo ocorre após a adiçao do dopante Bi3+.20 Comparando com outras matrizes, como Nb2O5 tratada a 900 ºC25 e o Y3Al5O12 tratada a 800 ºC,42 ambas obtida pela metodologia nao-hidrolítica os valores de tempo de vida foram da ordem de 1,0 e 2,0 ms, respectivamente. As energias de fônon dessas matrizes sao: óxido de nióbio (Nb2O5) 900 cm-1, óxido de ítrio e alumínio (YAG) 840 cm-1 e a do vanadato de ítrio (YVO4) 890 cm-1, portanto, a maior contribuiçao para o decréscimo do tempo de vida pode estar relacionado ao aumento da porcentagem dos íons dopantes promovendo supressao da luminescência por concentraçao.
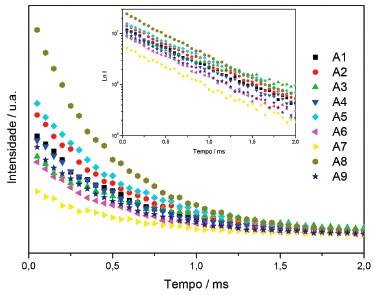 Figura 8. Curvas de decaimento da luminescência para as amostras excitadas no nível 5L6, fixando o comprimento de emissao no nível 7F2
A mudança no ambiente químico ao redor do íon Eu3+ pode afetar a intensidade das bandas relativas as transiçoes do estado excitado 5D0 para o fundamental 7FJ (J = 0, 2, 3 e 4), com exceçao da transiçao de dipolo magnético 5D0 → 7F1, portanto, essa transiçao pode ser utilizada como padrao para medidas de intensidades relativas das outras bandas do espectro de emissao.58,59 Assim, pequenas alteraçoes nessa razao poderá indicar mudanças na simetria do íon Eu3+. A Figura 9 mostra as razoes de intensidades relativas das bandas correspondentes às transiçoes 5Do → 7F2 / 5Do → 7F1 em funçao das concentraçoes dos íons Eu3+ e Bi3+.
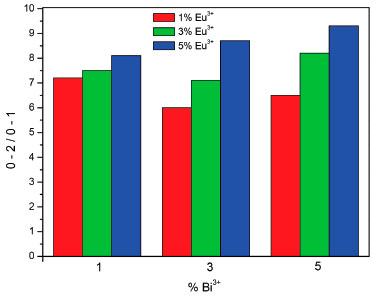 Figura 9. Razao das intensidades relativas das transiçoes 5D0 → 7F2 / 5D0 → 7F1 em funçao das concentraçoes dos íons Eu3+ e Bi3+
A Figura 9 apresenta comportamento semelhantes quando a concentraçao do íon Bi3+ e fixada, o aumento da concentraçao do íon Eu3+ provoca um aumento na razao das intensidades relativas 5D0 → 7F2 / 5D0 → 7F1 para todas as concentraçoes de Bi3+, indicando que a quantidade de íons dopantes podem estar distorcendo o ambiente químico devido aos pequenos aumentos dos raios iônicos dos dopantes Eu3+ (1,09 Å) e Bi3+ (1,20 Å) com relaçao ao íon Y3+ (0,88 Å), promovendo uma diminuiçao na simetria do íon Eu3+. O aumento mais acentuado na razao das bandas foi observado para as amostras contendo 3 e 5% do íon Bi3+ devido ao maior raio iônico deste íon, o qual pode estar influenciando a simetria ao redor do íon emissor Eu3+, produzindo subgrupos pontuais. O aumento na concentraçao do íon Bi3+ afeta diretamente o ambiente do íon Eu3+. Os parâmetros de intensidade das transiçoes f - f dos íons de terras raras, Ω2 e 4, tem sido instrumento de estudo para obtençao de informaçoes sobre o ambiente químico do íon Eu3+, tais como microssimetria, covalência da ligaçao e rigidez do retículo sob a influência das transiçoes vibrônicas.40,60-64 As Figuras 10 e 11 apresentam a dependência dos parâmetros de intensidade Ω2 e 4 em funçao das concentraçoes dos íons Eu3+ e Bi3+.
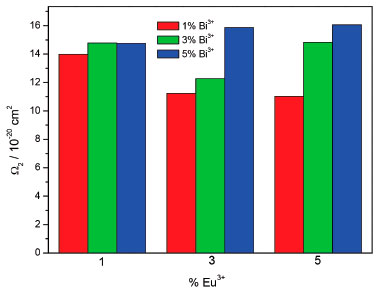 Figura 10. Parâmetro de intensidade (Ω2) em funçao das concentraçoes dos íons Eu3+ e Bi3+
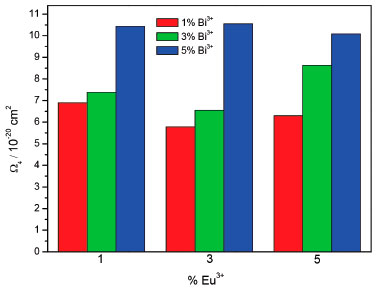 Figura 11. Parâmetro de intensidade (Ω4) em funçao das concentraçoes dos íons Eu3+ e Bi3+
O parâmetro de intensidade Ω2 mostra mudanças na microssimetria do íon Eu3+ e a covalência da ligaçao em funçao da concentraçao dos íons dopantes,65 maiores valores para o Ω2 indica uma maior covalência da ligaçao química e uma menor simetria para o íon, fato esse também observado através da alta razao das bandas referentes as transiçoes 5D0 → 7F2 / 5D0 → 7F1 que indicou ambiente de baixa simetria para o íon Eu3+. Observa-se que para a concentraçao constante do íon Eu3+ e variaçao da concentraçao do íon Bi3+ os valores de Ω2 aumenta, isso pode ser atribuído a maior distorçao da simetria devido ao maior raio iônico do Bi3+. A Figura 11 mostra a dependência do parâmetros Ω4 com a concentraçao dos dopantes em relaçao a rigidez estrutural da matriz e a influência direta das transiçoes vibrônicas,62,63 os baixos valores do Ω4 podem indicar uma maior rigidez no ambiente químico dos sistemas.66 O comportanto é similar ao observado para o Ω2, para uma concentraçao fixa do íon Eu3+ e variaçao da concentraçao do íon Bi3+ ocorre um aumento no parâmetro Ω4, podendo estar indicando uma diminuiçao na rigidez do sistema dependente do dopante Bi3+. Esses sistemas estudados apresentaram valores de Ω2 maiores que Ω4, sugerindo que o íon nao ocupa um ambiente químico com centro de simetria, confirmado pela presença da banda correspondente a transiçao 5D0 → 7F0,67,68 a literatura tem mostrado sistemas semelhantes a esse.20,32 Sistemas que apresentam Ω4 maior que Ω2 indicam que o íon Eu3+ está ocupando sítio de alta simetria, como observados para sistemas como o YAG que apresenta sítio com centro de inversao.40,65,69,70 A eficiência quântica (η) do estado excitado 5D0 poder ser determinada pela razao do coeficiente de emissao radiativa (Arad) pela total (AT), onde AT = Arad + Anrad.64,71,72 A Figura 12 apresenta a dependência da eficiência quântica em funçao das concentraçoes dos íons dopantes.
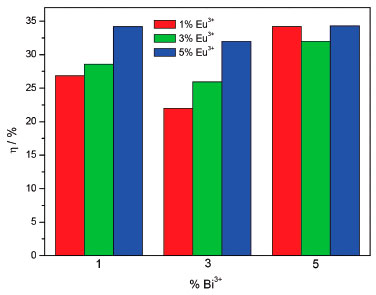 Figura 12. Eficiência quântica (η) em funçao das concentraçoes dos íons Eu3+ e Bi3+
A eficiência quântica para concentraçoes fixas do íon Bi3+ mostrou-se dependente da concentraçao do íon Eu3+, com o aumento, mais ativadores estao dispostos na rede cristalina podendo ser sensibilizados pela transferência de energia do íon Bi3+ para o íon Eu3+. O aumento da eficiência quântica é dependente da emissao espontânea radiativa (Arad), na Tabela 5 nota-se que as concentraçoes que obtiveram maiores η também apresentaram maiores Arad.
CONCLUSAO A metodologia sol-gel nao-hidrolítica tem apresentado em diversos trabalhos na literatura sua eficácia na preparaçao de matrizes hospedeiras para íons lantanóides, produzindo fases puras com características para aplicaçoes como emissores de radiaçao nos diversos campos do conhecimento. Neste trabalho, o estudo da incorporaçao de íons sensibilizadores (Bi3+) para produzir um aumento de emissao dos íons ativadores (Eu3+), mostrou a dependência da concentraçao desses íons nas propriedades espectroscópicas dessa matriz. Os parâmetros de intensidade Ω2 e Ω4 dependem da concentraçao do íon Bi3+, quando a concentraçao do íon Eu3+ se mantém fixa, o aumento da concentraçao do íon Bi3+, com raio iônico de 1,20 Å, provoca a diminuiçao do tamanho do cristalito, reduzindo a distância interatômica favorecendo um maior recobrimento dos orbitais e por consequência aumentando a covalência da ligaçao e a rigidez do sistema. A eficiência quântica e a simetria do íon Eu3+ mostraram serem dependentes das concentraçoes dos íons, a concentraçao fixa do íon Bi3+ e variaçao do íon Eu3+ mostrou um aumento na razao das bandas referentes as transiçoes 5D0 → 7F2 / 5D0 → 7F1 relacionadas a diminuiçao da simetria.
AGRADECIMENTOS Os autores agradecem às agências brasileiras de fomento, CNPq (304348/2013-9) e CAPES, à FAPESP nos processos 2011/20313-8 (M.G.M), 2011/09823-4, 2012/11673-3, e 2011/51858-0 (E.J.N.). Ao Prof. Dr. M. L. A. Silva da Universidade de Franca pelos dados de difraçao de raios X, e finalmente ao CEMES-CNRS pelo desenvolvimento de parte deste trabalho.
REFERENCIAS 1. Eliseeva, S. V.; Bünzli, J.-C. G.; New J. Chem. 2011, 35, 1165. 2. Wei, Q.; Chen, D.; Opt. Laser Technol. 2009, 41, 783. 3. Biju, S.; Reddy, M. L. P.; Freire, R. O.; Inorg. Chem. Commun. 2007, 10, 393. 4. Judd, B. R.; Phys. Rev. 1962, 127, 750. 5. Ofelt, G. S.; J. Chem. Phys. 1962, 37, 511. 6. Malta, O. L.; Carlos, L. D.; Quim. Nova 2003, 26, 889. 7. Natarajan, V.; Dhobale, A. R.; Lu, C.-H.; J. Lumin. 2009, 129, 290. 8. Chen, L.; Zheng, H.; Cheng, J.; Song, P.; Yang, G.; Zhang, G.; Wu, C.; J. Lumin. 2008, 128, 2027. 9. Park, W. J.; Jung, M. K.; Im, S. J.; Yoon, D. H.; Colloids Surf. Physicochem. Eng. Asp. 2008, 313-314, 373. 10. Park, J. Y.; Jung, H. C.; Raju, G. S. R.; Moon, B. K.; Jeong, J. H.; Kim, J. H.; Solid State Sci. 2010, 12, 719. 11. Park, J. Y.; Jung, H. C.; Raju, G. S. R.; Moon, B. K.; Jeong, J. H.; Son, S.-M.; Kim, J. H.; Mater. Res. Bull. 2010, 45, 572. 12. Ningthoujam, R. S.; Singh, L. R.; Sudarsan, V.; Singh, S. D.; J. Alloys Compd. 2009, 484, 782. 13. Xia, Z.; Chen, D.; Yang, M.; Ying, T.; J. Phys. Chem. Solids 2010, 71, 175. 14. Mu, Z.; Hu, Y.; Chen, L.; Wang, X.; J. Lumin. 2011, 131, 1687. 15. Hong, J.-H.; Zhang, Z.-G.; Cong, C.-J.; Zhang, K.-L.; J. Non-Cryst. Solids 2007, 353, 2431. 16. Nguyen, H.-D.; Mho, S.; Yeo, I.-H.; J. Lumin. 2009, 129, 1754. 17. Takeshita, S.; Isobe, T.; Niikura, S.; J. Lumin. 2008, 128, 1515. 18. Takeshita, S.; Isobe, T.; Sawayama, T.; Niikura, S.; J. Lumin. 2009, 129, 1067. 19. He, Y.; Zhao, M.; Song, Y.; Zhao, G.; Ai, X.; J. Lumin. 2011, 131, 1144. 20. Matos, M. G.; Rocha, L. A.; Nassar, E. J.; Verelst, M.; Opt. Mater. 2016, 62, 12. 21. Sun, J.; Xian, J.; Xia, Z.; Du, H.; J. Lumin. 2010, 130, 1818. 22. Park, W. J.; Jung, M. K.; Yoon, D. H.; Sens. Actuators, B 2007, 126, 324. 23. Sanchez, C.; Rozes, L.; Ribot, F.; Laberty-Robert, C.; Grosso, D.; Sassoye, C.; Boissiere, C.; Nicole, L.; C. R. Chim. 2010, 13, 3. 24. Bilecka, I.; Niederberger, M.; Electrochimica Acta. 2010, 55, 7717. 25. Matias, C. R.; Nassar, E. J.; Dexpert-Ghys, J.; Verelst, M.; Rocha, L. A.; J. Braz. Chem. Soc. 2015, 26, 2558. 26. Pereira, P. F. S.; Nogueira, I. C.; Longo, E.; Nassar, E. J.; Rosa, I. L. V.; Cavalcante, L. S.; J. Rare Earths 2015, 33, 113. 27. Saltarelli, M.; Matos, M. G.; de Faria, E. H.; Ciuffi, K. J.; Rocha, L. A.; Nassar, E. J.; J. Sol-Gel Sci. Technol. 2015, 73, 283. 28. Matos, M. G.; de Faria, E. H.; Rocha, L. A.; Calefi, P. S.; Ciuffi, K. J.; Nassar, E. J.; Sarmento, V. H. V.; J. Lumin. 2014, 147, 190. 29. Pereira, P. F. S.; Matos, M. G.; Ferreira, C. M. A.; De Faria, E. H.; Calefi, P. S.; Rocha, L. A.; Ciuffi, K. J.; Nassar, E. J.; J. Lumin. 2014, 146, 394. 30. Saltarelli, M.; Luz, P. P.; Matos, M. G.; de Faria, E. H.; Ciuffi, K. J.; Calefi, P. S.; Rocha, L. A.; Nassar, E. J.; J. Fluoresc. 2012, 22, 899. 31. Silva, G. M.; de Faria, E. H.; Nassar, E. J.; Ciuffi, K. J.; Calefi, P. S.; Quim. Nova 2012, 35, 473. 32. Pereira, P. F. S.; de Moura, A. P.; Nogueira, I. C.; Lima, M. V.; Longo, E.; de Sousa Filho, P. C.; Serra, O. A.; Nassar, E. J.; Rosa, I. L. V.; J. Alloys Compds. 2012, 526, 11. 33. Matos, M. G.; Calefi, P. S.; Ciuffi, K. J.; Nassar, E. J.; Inorg. Chim. Acta 2011, 375, 63. 34. Alfenas, C. dos S.; Ricci, G. P.; de Faria, E. H.; Saltarelli, M.; de Lima, O. J.; da Rocha, Z. N.; Nassar, E. J.; Calefi, P. S.; Montanari, L. B.; Martins, C. H. G.; Ciuffi, K. J.; J. Mol. Catal. A: Chem. 2011, 338, 65. 35. Ricci; G. P.; Rocha; Z. N.; Nakagaki; S.; Castro, K. A. D. F.; Crotti, A. E. M.; Calefi, P. S.; Nassar; E. J.; Ciuffi, K. J.; Appl. Catal., A 2010, 389, 147. 36. Pereira, P. F. S.; Matos, M. G.; Avila, L. R.; Nassor, E. C. O.; Cestari, A.; Ciuffi, K. J.; Calefi, P. S.; Nassar, E. J.; J. Lumin. 2010, 130, 488. 37. Cestari, A.; Avila, L. R.; Nassor, E. C. O.; Pereira, P. F. S.; Calefi, P. S.; Ciuffi, K. J.; Nakagaki, S.; Gomes, A. C. P.; Nassar, E. J.; Mater. Res. 2009, 12, 139. 38. Matos, M. G.; Pereira, P. F. S.; Calefi, P. S.; Ciuffi, K. J.; Nassar, E. J.; J. Lumin. 2009, 129, 1120. 39. Cestari, A.; Bandeira, L. C.; Calefi, P. S.; Nassar, E. J.; Ciuffi, K. J.; J. Alloys Compds. 2009, 472, 299. 40. Nassar, E. J.; Pereira, P. F. S.; Nassor, E. C. O.; Avila, L. R.; Ciuffi, K. J.; Calefi, P. S.; J. Mater. Sci. 2007, 42, 2244. 41. Ciuffi, K. J.; Caetano, B. L.; Rocha, L. A.; Molina, E. F.; Rocha, Z. N.; Ricci, G. P.; de Lima, O. J.; Calefi, P. S.; Nassar, E. J.; Appl. Catal., A 2006, 311, 122. 42. Nassar, E. J.; Avila, L. R.; Pereira, P. F. S.; Mello, C.; de Lima, O. J.; Ciuffi, K. J.; Carlos, L. D.; J. Lumin. 2005, 111, 159. 43. Nassar, E. J.; Avila, L. R.; Pereira, P. F. S.; de Lima, O. J.; Rocha, L. A.; Mello, C.; Ciuffi, K. J.; Quim. Nova 2005, 28, 238. 44. Ciuffi, K. J.; de Lima, O. J.; Sacco, H. C.; Nassar, E. J.; J. Non-Cryst. Solids 2002, 304, 126. 45. Acosta, S.; Corriu, R. J. P.; Leclercq, D.; Lefèvre, P.; Mutin, P. H.; Vioux, A.; J. Non-Cryst. Solids 1994, 170, 234. 46. de Lima, O. J.; Papacıdero, A. T.; Rocha, L. A.; Sacco, H. C.; Nassar, E. J.; Ciuffi, K. J.; Bueno, L. A.; Messaddeq, Y.; Ribeiro, S. J. L.; Mater. Charact. 2003, 50, 101. 47. Rambabu, U.; Munirathnam, N. R.; Chatterjee, S.; Reddy, B. S.; Han, S.-D.; Ceram. Int. 2013, 39, 4801. 48. Zhou, Y.H.; Lin, J.; Opt. Mater. 2005, 27, 1426. 49. de Sousa Filho P. C.; Serra, O. A.; J. Phys. Chem. C 2011, 115, 636. 50. Li, J.; Chem, Y.; Yin, Y.; Yao, F.; Yao, K.; Biomaterials 2007, 28, 781. 51. Vijatovic, M. M.; Stojanovic, B. D.; Bobic, J. D.; Ramoska, T.; Bowen. P.; Ceram. Int. 2010, 36, 1817. 52. Cassia-Santos, M. R.; Mendes, S. B.; Gurgel, M. F. C.; Figueiredo, A. T.; Godinho Jr. M.; Braz, C. E. M.; Longo, E.; Cerâmica 2014, 60, 259. 53. Cavalli, E.; Angiuli, F.; Belletti, A.; Boutinaud, P.; Opt. Mater. 2014, 36, 1642. 54. Fan, B.; Qi, S.; Zhao, W.; Opt. Mater. 2018, 76, 329. 55. Oliveira, H. H. S.; Cebim, M. A.; Da Silva, A. A.; Davolos, M. R.; J. Alloys Compd. 2009, 488, 619. 56. Basu B. B. J.; Vasantharajan, N.; J. Lumin. 2008, 128, 1701. 57. Dutra, J. D. L.; Bispo, T. D.; Freire, R. O.; J. Comput. Chem. 2014, 35, 772. 58. de Souza, R.F.; Railsback, B.; Terræ Didatica 2012, 8, 73. 59. Ishizaka, T.; Nozaki, R.; Kurokawa, Y.; J. Phys. Chem. Solids. 2002, 63, 613. 60. Nassar, E.J.; Serra, O.A.; Souza-Aguiar, E.F.; Quim. Nova 1998, 21, 121. 61. da Silva, A.A.; Davolos, M.R.; Opt. Mater. 2011, 33, 1226. 62. Jorgensen, C.K;. Reisfeld, R.; J. Less-Common Met. 1983, 93, 107. 63. Babu, A. B.; Jamalaiah, B. C.; Suhasini, T.; Rao, T. S.; Moorthy, L. R.; Solid State Sci. 2011, 13, 574. 64. Walsh, B. M. In Advances in Spectroscopy for Lasers and Sensing; Di Bartolo, B., Forte, O., eds.; Springer: Netherlands, 2006, p. 403 e 433. 65. de Sá, G. F.; Malta, O. L.; Donegá, C. de M.; Simas, A. M.; Longo, R. L.; Santa-Cruz, P. A.; da Silva Jr., E. F.; Coord. Chem. Rev. 2000, 196, 165. 66. Sá Ferreira, R. A.; Nobre, S. S.; Granadeiro, C. M.; Nogueira, H. I. S.; Carlos, L. D.; Malta, O. L.; J. Lumin. 2006, 121, 561. 67. Santos, J. G.; Dutra, J. D. L.; Alves, S.; De Sá, G. F.; Da Costa, N. B.; Freire, R. O.; J. Braz. Chem. Soc. 2013, 24, 236. 68. Kodaira, C. A.; Brito, H. F.; Felinto, M. C. F. C.; J. Solid State Chem. 2003, 171, 401. 69. Kodaira, C.A.; Brito, H. F.; Malta, O. L.; Serra, O. A.; J. Lumin. 2003, 101, 11. 70. Reisfeld, R.; Jorgensen, C. K.; Handbook on the Physics and Chemistry of Rare Earth, North Holland, Amsterdam, 1984. 71. Ferreira, C. M. A.; Freiria, G. S.; de Faria, E. H.; Rocha, L. A.; Ciuffi, K. J.; Nassar, E. J.; J. Lumin. 2016, 170, 686. 72. Lourenço, A. V. S.; Kodaira, C. A.; Souza, E. R.; Felinto, M. C. F. C.; Malta, O. L.; Brito, H. F.; Opt. Mater. 2011, 33, 1548. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access