Artigo
|
|
| Predição de toxicidade dos estabilizantes usuais em propelentes à base de nitrocelulose e de seus principais produtos de degradação Prediction of toxicity of the usual stabilizers in nitrocellulose based propellants and their main degradation products |
|
Rodrigo L. B. RodriguesI; Jakler NicheleI; Tanos C. C. FrançaI,II,*; Letivan G. Mendonça FilhoI,#
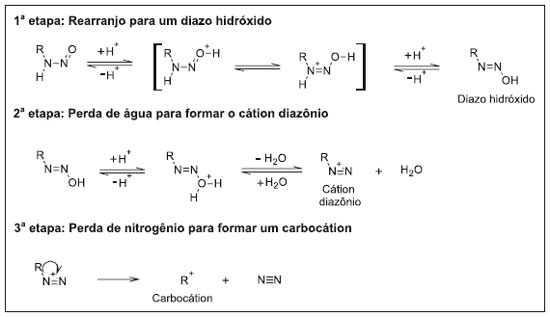
I. Seção de Engenharia Química, Instituto Militar de Engenharia, 22290-270 Rio de Janeiro - RJ, Brasil Recebido em: 27/02/2018 *e-mail: tanosfranca@gmail.com This work aims to establish a hierarchy of risks of the stabilizers used in nitrocellulose-based propellants concerning to toxicity, carcinogenicity and mutagenicity. Four stabilizers - diphenylamine, ethyl centralite, akardite-II and 2-nitrodiphenylamine - and their products of degradation were investigated. The prediction of the toxicity was based on the analysis of their structures with the software Lazar, using the OpenTox framework. Our results provide a quantitative reference of the risks involved in the manufacturing and disposal of propellants due to the use of such stabilizers. INTRODUÇAO Propelentes sao substâncias químicas puras ou misturas utilizadas com a finalidade de mover objetos. Podem ser gases, líquidos ou sólidos e sua açao pode ou nao envolver uma reaçao química. Exemplos de propelentes sao o hidrogênio, o hélio, a gasolina, combustíveis de foguetes e as pólvoras utilizadas em muniçoes. Estas últimas geralmente contêm a nitrocelulose (NC) como principal componente de suas formulaçoes, cuja instabilidade demanda a utilizaçao de estabilizantes.1 Os estabilizantes sao substâncias utilizadas nas formulaçoes de propelentes com a finalidade de retardar o processo de degradaçao natural da NC, prolongando o tempo de vida dos propelentes à base de NC, quando em condiçoes adequadas de armazenamento.1 No processo de interaçao química entre os estabilizantes e os vapores nitrosos oriundos da degradaçao da NC, é gerada uma grande variedade de compostos nitrosados, dentre os quais se destacam as N-nitroso-aminas e as N-nitroso-amidas. Tais substâncias tóxicas sao as principais responsáveis pelos riscos à saúde dos profissionais que manipulam pólvoras e propelentes, assim como, pela contaminaçao do ambiente. Há relatos na literatura sobre o risco desses compostos serem carcinogênicos, mutagênicos e prejudiciais à reproduçao (abreviados aqui como CMR).1-5 Os estabilizantes utilizados comercialmente hoje em dia na composiçao de propelentes a base de NC sao todos análogos da ureia e de aminas secundárias, sendo a difenilamina (DPA), a etil centralite (EC), a akardite II (AK-II) e a 2-nitrodifenilamina (2-NDPA) os mais comuns. Alternativas menos tóxicas a esses compostos, já foram apontadas na literatura, como os ésteres e éteres aromáticos propostos por Krumlinde6 ou os estabilizantes à base de óleo epoxidado, conhecidos como Lankroflex E2307 (óleo de soja epoxidado), Lankroflex L (óleo de linhaça epoxidado), e Lankroflex ED6 (uma mistura epoxidada de ácidos graxos C14-C22 e 2-etil-hexil ésteres).1,7 Recentemente, surgiram também possibilidades de substituiçao dos estabilizantes por compostos naturais, chamados de "green stabilizers", sendo a α-ionona apontada como o "green stabilizer" mais promissor dentre outros compostos de origem natural como a Vitamina E e a Curcumina.8 Embora algumas das alternativas acima tenham se mostrado promissoras, ainda nao há registros de um estabilizante comercial que nao seja um análogo da ureia e de aminas secundárias. Revisao bibliográfica e estado da arte As N-nitroso-aminas e as N-nitroso-amidas oriundas da interaçao entre os estabilizantes comerciais e os vapores nitrosos gerados na degradaçao da NC, estao associadas ao aparecimento de carcinomas em diversos órgaos, variando o órgao afetado com o composto administrado. Identificou-se, por exemplo, a ocorrência de tumores de fígado em ratos pela açao da N-nitroso-dimetilamina (DMN). Já a N-nitroso-metil-ureia, foi capaz de provocar lesoes hemorrágicas seguidas de carcinomas no estômago, intestino e pâncreas de cobaias.9,10 A Figura 1 ilustra o processo de decomposiçao de N-nitroso-aminas primárias formadas na degradaçao da NC. Iniciando por mecanismos do tipo SN1 ou SN2, as espécies resultantes sofrem rearranjo para diazo-hidróxidos. Em seguida, sofrem eliminaçao de água, gerando cátions diazônio R-N2+, que após perderem o N2, geram carbocátions (R+). Estes últimos, por serem eletrófilos, sao capazes de alquilar nucleófilos do DNA (nas posiçoes N7 e O6 da guanina e N1 da adenina) ou formar diazoalcanos, catalisando alteraçoes de sítios específicos da dupla hélice do DNA, que podem provocar mutaçoes.11,12
As alquil-aminas secundárias ou as aminas aromáticas secundárias, como a difenilamina (DPA), geram N-nitroso-aminas com potencial de serem CMR14 (vide Figuras 1S e 2S do material suplementar). Todavia estas nao se decompoem espontaneamente como as N-nitroso-aminas derivadas de aminas primárias. A reaçao cessa com a formaçao de N-nitroso-amina (Figura 2), porque estas substâncias sao bases muito fracas e insolúveis em ácidos diluídos.
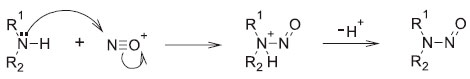 Figura 2. Mecanismo da nitrosaçao de aminas secundárias13 (R1 e R2 = radical alquil ou aril)
As alquil-aminas terciárias nao apresentam hidrogênio ligado ao átomo de nitrogênio. Possivelmente, o átomo de hidrogênio ligado ao átomo de carbono adjacente ao nitrogênio é eliminado para formaçao de produtos complexos.13 Já as aril-aminas terciárias sofrem a nitrosaçao do anel aromático via uma reaçao de substituiçao eletrofílica, conforme ilustrado na Figura 3.
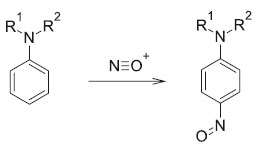 Figura 3. Nitrosaçao de amina terciária aromática13
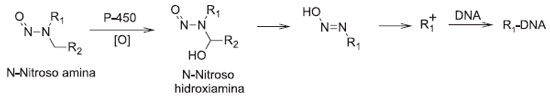
As N-alquil-nitrosaminas possuem um mecanismo mutagênico comum, iniciado por uma ativaçao metabólica pelas enzimas do citocromo P450, que tornam esses compostos mais polares e hidrossolúveis, através da hidroxilaçao do carbono adjacente ao grupo N-nitroso (Figura 4). As únicas N-nitroso aminas que nao passam por essa rota metabólica sao aquelas que nao possuem hidrogênio em carbono α, tais como a N-nitroso-metil-tercbutilamina, a N-nitroso-etil-tercbutilamina e a N-nitroso-dibenzilamina. Possivelmente, por essa razao, elas nao sao carcinogênicas.11
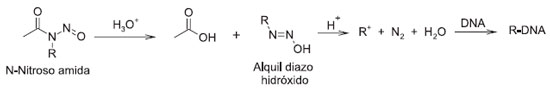
As N-nitroso-amidas, que sao os produtos da degradaçao da EC e da AK-II (vide Figuras S3 e S4 do material suplementar), se hidrolisam de maneira similar ao que ocorre na decomposiçao das N-nitroso-hidroxiaminas (Figura 4) e nessa decomposiçao também sao formados diazo-alcanos capazes de interagir com o DNA (Figura 5).
Os danos provocados nas bases de DNA pelas N-nitroso-aminas e N-nitroso-amidas podem levar a lesoes citotóxicas e mutagênicas.12 As lesoes citotóxicas bloqueiam a replicaçao levando à morte celular, enquanto as lesoes mutagênicas provocam erros de codificaçao e causam mutaçoes no DNA, que sao consideradas como um mecanismo importante de carcinogênese. Comparando as estruturas e atividades cancerígenas conhecidas de vários compostos N-nitrosados, pode-se afirmar que as N-nitroso dialquil aminas produzem tumores em órgaos distantes de sua introduçao, onde provavelmente existe a capacidade de hidroxilar o carbono do composto nitrosado. Já as N-nitroso amidas apenas induzem a formaçao de tumores no local do seu contato, provavelmente, devido à menor solubilidade em meio aquoso, o que faz com que estes compostos nao sejam transportados para longe do local de sua aplicaçao. Consequentemente, os diazoalcanos responsáveis pelo câncer serao produzidos no local do contato com a pele. Isso acontece também no caso de estabilizantes da família da ureia, como a AK-II e a EC.11 O desenvolvimento da mutagenicidade em bactérias foi investigado a partir de cinco N-nitrosaminas15 - N-nitroso-dimetilamina (NDMA), N-nitroso-dietilamina (NDEA), N-nitroso-di-n-propilamina (NDPrA), N-nitrosopirrolidina (NPYR) e N-nitroso-difenilamina (NNDPA) - durante processos oxidativos envolvendo fotólise UV, ozônio e radicais OH. Durante a fotólise UV, a mutagenicidade foi detectada apenas no caso da NNDPA. Os produtos de oxidaçao de NDMA, NDEA e NDPrA nao apresentaram mutagenicidade significativa nas cepas utilizadas. Em contrapartida, as oxidaçoes de NNDPA e NPYR por radicais hidroxílicos indicaram a formaçao de espécies mutagênicas. Dessa maneira, a associaçao entre a contaminaçao causada pela manipulaçao direta da DPA e a exposiçao ao sol aumenta os riscos de ocorrência de cânceres de pele.12 A literatura registra também que o potencial cancerígeno depende das cadeias laterais e aumenta da seguinte forma para as N-nitroso aminas: N, N-diaril-N-NO < N-aril-N-NO < N,N-dialquil-N-NO.16 Portanto, as N-nitroso-alquil-anilinas, produzidas a partir da EC, seriam mais tóxicas que as N-nitroso-DPAs, derivadas da DPA ou da 2-NDPA. De forma geral, o uso dos estabilizantes EC, AK-II, DPA e 2-NDPA em quase todas as composiçoes de propelentes em todo o mundo faz com que esses materiais sejam considerados tóxicos, muito tóxicos, cancerígenos ou mutagênicos. No entanto, para uma informaçao mais precisa e quantitativa a respeito dos riscos associados a cada um deles, é necessário avaliar seus potenciais CMR, bem como os de seus produtos de degradaçao. A investigaçao conduzida no presente trabalho é inédita na literatura e permite estabelecer uma hierarquia de riscos desses estabilizantes. Com essa informaçao, equipes de segurança do trabalho e de avaliaçao de risco ambiental podem ter dados mais confiáveis referentes à fabricaçao, à manipulaçao e às operaçoes de descarte de propelentes.
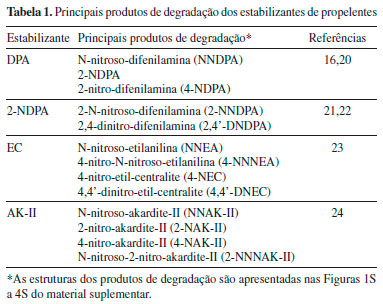
PARTE EXPERIMENTAL Os principais produtos de degradaçao dos quatro estabilizantes investigados no presente trabalho - DPA, EC, AK-II, 2-NDPA - e que sao os mais utilizados em propelentes à base de NC, estao listados na Tabela 1. A partir das estruturas destes compostos é possível prever seus riscos toxicológicos utilizando o software Lazar (Lazy Structure-activity Relationships) disponível em https://lazar.in-silico.de/predict.17,18 Este software gera previsoes para uma variedade de propriedades tóxicas com base em compostos reportados com estruturas semelhantes, sendo estruturado na OpenTox,19 a principal plataforma global aberta para toxicologia preditiva, disponível em http://www.opentox.net. O usuário tem a opçao de desenhar ou inserir a representaçao química com os caracteres Smiles (Simplified Molecular Input Line Entry Specification), que será a entrada de dados para a prediçao no Lazar.17,18
O software Lazar17,18 fornece seus resultados com base nas opçoes de escolha do usuário, que seriam os valores preditivos da toxicidade aguda para o peixe Fathead Minnow25 e para o crustáceo planctônico Daphnia Magna,26 que sao organismos bioindicadores, bem como a estimativa de permeabilidade à barreira hematoencefálica27 (BHE) e os valores de toxicidade frente à bactéria Salmonela Typhimurium.28 Além disso, o Lazar17,18 também apresenta nos resultados da prediçao, os compostos similares utilizados como referência de suas aproximaçoes, sendo confiável se a estrutura investigada estiver dentro do domínio de aplicabilidade do OpenTox.17,18 Os cálculos associados à toxidade correspondem às probabilidades de ocorrência do risco toxicológico, sendo positivos para penetraçao na BHE, carcinogenicidade e mutagenicidade ou negativos para nao penetraçao na BHE, nao carcinogenicidade e nao mutagenicidade. Ao invés de se trabalhar com nível de confiança, os resultados podem ser interpretados como probabilidades reais variando de 0 a 1. Uma previsao confiável tem uma alta probabilidade para a classe prevista e uma baixa probabilidade para a outra. As previsoes nao confiáveis, ou seja, nao conclusivas possuem valores semelhantes para ambas às classes e sao causadas por muitas atividades contraditórias de compostos similares. As similaridades sao calculadas a partir do método de Tanimoto-Jaccard.29,30 O Lazar17,18 faz previsoes de toxicologia baseadas em algoritmos estatísticos através da análise de fragmentos estruturais em um conjunto de moléculas com estruturas similares, capturando apenas os fragmentos relevantes para o end point ou limite tóxico sob investigaçao.31 Um estudo comparativo com outros aplicativos computacionais revelou que o Lazar apresentou as piores estatísticas entre os modelos para carcinogenicidade em hamsters, entretanto, foi o mais preciso para a prediçao da mutagenicidade.32
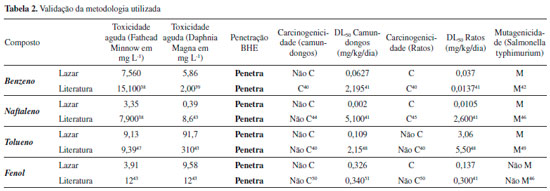
RESULTADOS E DISCUSSAO Validaçao da metodologia Para validar a metodologia utilizada foi feita uma pesquisa na literatura de alguns resultados já reportados e, no caso de valores numéricos, como a DL50, os resultados pesquisados foram comparados com os fornecidos pelo Lazar17,18 (Tabela 2). Os resultados qualitativos, como a carcinogenicidade e a mutagenicidade, também foram comparados com os resultados pesquisados na literatura. Todos os compostos analisados nesta validaçao tem boa penetraçao na BHE porque sao lipossolúveis.33 A DL50 nao foi incluída na Tabela 2 porque os resultados na literatura também serao valores estimados com outros modelos preditivos. Pode-se afirmar que a Tabela 2 mostra uma congruência da maioria dos dados preditos com a literatura, especialmente, para a prediçao da mutagenicidade e carcinogenicidade.
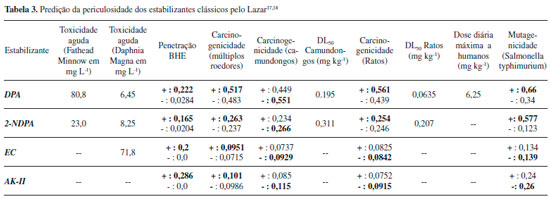
Ainda sobre a validaçao de resultados foi reportada uma pesquisa envolvendo prediçoes de mutagenicidade com os dados de 3.895 estruturas e seus resultados foram confirmados com a utilizaçao deste aplicativo computacional. Com base nesse trabalho a mutagenicidade com a Salmonella poderia ser prevista com precisao de 85% para compostos no domínio do banco de dados das substâncias com potencial carcinogênico. A precisao para outras carcinogenicidades variaram entre 78 e 95% para estruturas dentro do domínio de aplicabilidade.17 Em outro reporte similar foram utilizados 1.544 compostos químicos potencialmente carcinogênicos a ratos e o aplicativo computacional atingiu 78% de especificidade.34 Em outro exemplo, o uso deste aplicativo computacional foi bem sucedido em três casos ligados a produtos químicos relacionados à reciclagem em um aterro industrial da Itália. O primeiro caso é uma avaliaçao de ensaios in vitro para a investigaçao da toxicidade de um lixiviado. O segundo exemplo analisa qualitativamente o potencial carcinogênico de alguns compostos perfluorados, usando modelos QSAR e células in vitro. Finalmente, uma avaliaçao QSAR de diferentes produtos químicos foi demonstrada, a fim de se validar como modelos in silico seriam utilizados, como ferramenta, para preencher as lacunas existentes na literatura, sobre o perfil toxicológico dos compostos investigados.35 Em síntese, a falta de dados de algumas substâncias deste trabalho evidencia a escassez de material publicado sobre o assunto e fortalece a necessidade de mais estudos sobre a toxicidade de materiais energéticos para se preencher esta lacuna na literatura científica, com também, o uso de aplicativos computacionais de prediçao toxicológica. Foram encontradas algumas referências que já utilizam dados de toxicologia preditiva.36,37 Análise de toxicidade dos estabilizantes Os resultados da análise de toxicidade dos estabilizantes DPA, EC, AK-II e 2-NDPA, através do Lazar,17,18 sao apresentados na Tabela 3 expressos na forma de probabilidades de ocorrência do risco e de dados adicionais, como, por exemplo, a dose letal para ratos e camundongos. Os dados apresentados permitem inferir que todos os estabilizantes tendem a ter uma boa penetraçao na BHE, o que implica em uma boa difusao pelo corpo humano. A DPA é, provavelmente, o estabilizante mais tóxico seguido da 2-NDPA, que é um de seus derivados. Ambos apresentaram potencial mutagênico. Entre a EC e a AK-II, pode-se inferir que, possivelmente, nao sao carcinogênicos nem mutagênicos.
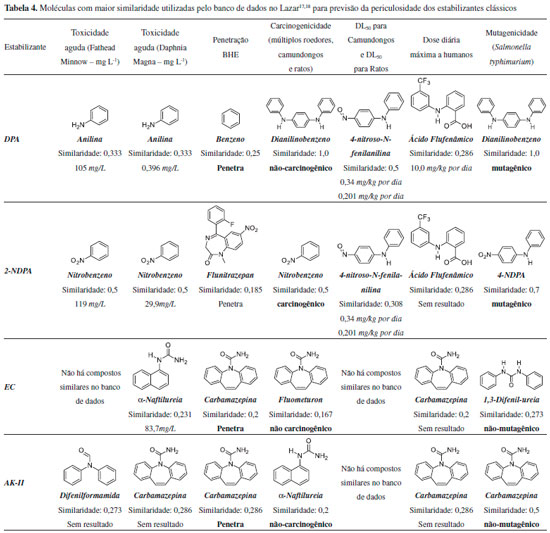
A Tabela 4 apresenta as moléculas utilizadas pelo Lazar17,18 para determinar os valores de probabilidade propostos na Tabela 3, de acordo com as atividades tóxicas conhecidas, indicando a sua similaridade com a estrutura do estabilizante investigado. Adicionalmente, a Tabela 5 apresenta os resultados similares para os principais produtos de degradaçao de cada estabilizante investigado.
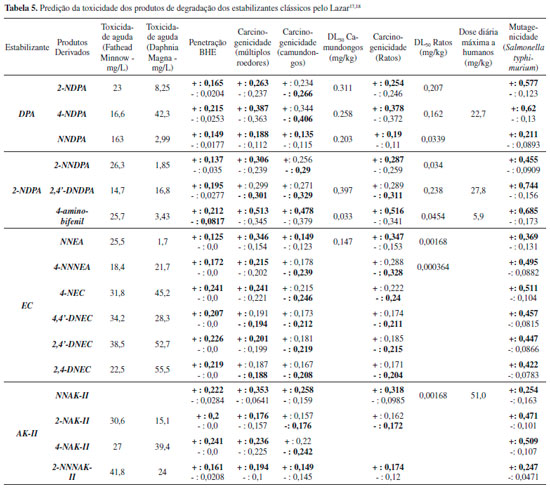
A análise da Tabela 5 mostra que os produtos derivados da degradaçao da DPA apresentaram potencial de serem tóxicos e mutagênicos, podendo ser hierarquizados quanto à mutagenicidade na seguinte ordem: 4-NDPA > 2-NDPA > NNDPA e quanto à toxicidade na seguinte ordem: NNDPA > 4-NDPA > 2-NDPA, todos com boa penetraçao na BHE. Já os produtos derivados da degradaçao da 2-NDPA apresentaram grande potencial mutagênico na seguinte ordem: 2,4'-DNDPA > 4-amino-bifenil > 2-NNDPA, e alta toxicidade na ordem inversa. Os produtos derivados da degradaçao da EC apresentaram os melhores resultados para penetraçao na BHE em comparaçao com os demais estabilizantes. O potencial mutagênico desses produtos foi hierarquizado na seguinte ordem: 4-NNEA ~ 4-NEC > 4,4'-DNEC ~ 2,4'-DNEC ~ 2,4-DNEC > NEA. Foram também preditas as altíssimas toxicidades da 4-NNNEA e da 4-NEA respectivamente. Os produtos derivados da degradaçao da AK-II e da NNAK-II apresentaram potencial carcinogênico e alta toxicidade quando comparados aos demais produtos desta família. O potencial mutagênico observado para esses compostos segue a seguinte ordem: 4-NAK-II > 2-NAK-II > 2-NNAK-II > NNAK-II.
CONCLUSAO Com base nos resultados obtidos, pode-se afirmar que, dentre os quatro estabilizantes investigados a DPA e a 2-NDPA apresentam grande potencial mutagênico, sendo a DPA a mais tóxica seguida pela 2-NDPA. Além disso, os quatro estabilizantes investigados apresentaram índices que sugerem grande capacidade de penetraçao na BHE, possuindo desta forma capacidade de transporte e de difusao pela corrente sanguínea no organismo humano. Com base na diferença entre as probabilidades encontradas, os produtos de degradaçao dos quatro estabilizantes clássicos, foram hierarquizados quanto ao potencial mutagênico, estabelecendo a seguinte ordem: 2,4'-DNDPA > 4-amino-bifenil > 4-NDPA > 2-NDPA > 4-NEC ~ 4-NNEA ~ 4-NAK-II. Como consequência desse resultado, os quatro estabilizantes foram ordenados quanto ao potencial mutagênico de seus produtos de degradaçao em: 2-NDPA > DPA > EC > AK-II. Com relaçao ao potencial carcinogênico, todos os produtos apresentaram probabilidades próximas impossibilitando uma análise comparativa confiável. A única exceçao foi a NNAK-II, derivada da AK-II, que apresentou este risco em potencial. Sobre a toxicidade, com base nas probabilidades da DL50 em ratos e camundongos, foi possível propor a seguinte ordem decrescente de toxicidade para os produtos de degradaçao: 4-NNNEA > 4-NEA ~ NNAK-II > 2-NNDPA ~ NNDPA > 4-amino-bifenil > 4-NDPA > 2-NDPA > 2,4'-NDPA e, consequente mente, a seguinte ordem de toxicidade: EC > AK-II > 2-NDPA > DPA para os estabilizantes clássicos com relaçao aos seus produtos da degradaçao. Por fim, foi possível observar que o maior potencial mutagênico está associado ao produto da degradaçao que contêm grupos nitro em sua estrutura, enquanto que a toxicidade está relacionada à presença do grupo nitroso.
AGRADECIMENTOS Os autores agradecem ao IME pela infraestrutura, e às agências de fomento CNPq (Processo 306156/2015-6) e FAPERJ (Grant no E-02/202.961/2017) pelo suporte financeiro. Este projeto também foi financiado pelo "excellence project FIM". MATERIAL SUPLEMENTAR Os produtos de degradaçao da DPA, 2-NDPA, EC e AK-II estao esquematizados no Material Suplementar, disponível de forma gratuita em http://quimicanova.sbq.org.br em formato PDF.
REFERENCIAS 1. Fryš, O.; Bajerová, P.; Eisner, A.; Skládal, J.; Ventura, K.; Propellants, Explos., Pyrotech. 2011, 36, 347. 2. Toxicological Profile for N-nitrosodiphenylamine, Agency for Toxic Substances and Disease Registry, 2017. 3. Drzyzga, O.; Jannsen, S.; Blotevogel, K. H.; Ecotoxicol. Environ. Saf. 1995, 31, 149. 4. Goodall, C. M.; Lijinsky, W.; Tomatis, L.; Wenyon, C. E. M.; Toxicol. Appl. Pharmacol. 1970, 17, 426. 5. Böhnlein-Mauß, J.; Kröber, H.; Propellants, Explos., Pyrotech. 2017, 42, 54. 6. Krumlinde, P.; Ek, S.; Tunestål, E. & Hafstrand, A.; Propellants, Explos., Pyrotech. 2017, 42, 78. 7. Fryš, O.; Bajerová, P.; Eisner, A. & Skládal, J.; Cent. Eur. J. Energ. Mater. 2010,7, 253. 8. Dobson, R.; Dejeaifve, A.; Monseur, L.; Fonder, N.; 7th Nitrocelluose Symposium, Montreal, Canadá, 2016. 9. Magee, P. N.; Barnes, J. M.; Br. J. Cancer 1956, 10, 114. 10. Low, H.; Archives of Environmental Health - An International Journal 1974, 29, 256. 11. Araujo, M. E.; Cyrne, L.; Marinho, H. S.; Norberto, F.; Bol. Soc. Port. Quim. 2000, 79, 30. 12. Nieminuszczy, J.; Grzesiuk, E.; Acta Biochim. Pol. 2007, 54, 459. 13. Vollhardt, K. P. C.; Schore, N. E.; Organic Chemistry Structure and Function, 6th ed., Bookman: Porto Alegre, 2013. 14. Drzyzga, O.; Chemosphere 2003, 53, 809. 15. Mestankova, H.; Schirmer, K.; Canonica, S.; von Gunten, U.; Water Res. 2014, 66, 399. 16. Lussier, L. S.; Gagnon, H.; Bohn, M. A.; Propellants, Explos., Pyrotech. 2000, 25, 117. 17. Helma, C.; Mol. Divers. 2006, 10, 147. 18. Maunz, A.; Gütlein, M.; Rautenberg, M.; Vorgrimmler, D.; Gebele, D.; Helma, C.; Front Pharmacol. 2013; 4, 1. 19. Willighagen, E. L.; Jeliazkova, N.; Hardy, B.; Grafström, R. C.; Spjuth, O.; BMC Res. Notes 2011, 4, 487. 20. Bohn, M. A.; J. Therm. Anal. Calorim. 2001, 65, 103. 21. Andrade, J.; Iha K, Rocco, J. A. F. F.; Franco, G. P.; Moreira, E. D.; Suárez-Iha, M. E. V.; Eclet. Quim. 2007, 32, 7. 22. Yucel, A.; Inal, E. K.; Akay, M. A.; Cent. Eur. J. Energy Mater. 2011, 8, 183. 23. Lussier, L. S.; Gagnon, H.; Bergeron, E.; Bohn, M. A.; Symp. Chem. Problems Connected Stab. Explos. 2004, 12, 183. 24. Lussier, L. S.; Bergeron, E.; Gagnon, H.; Propellants, Explos., Pyrotech. 2006, 31, 253. 25. Russom, C. L.; Bradbury, S. P.; Broderius, S. J.; Hammermeister, D. E.; Drummond, R. A.; Environ. Toxicol. Chem. 1997, 16, 948. 26. Antczak, P. Jo H. J; Woo, S.; Scanlan, L.; Poynton, H.; Loguinov. A.; Chan, S.; Falciani, F.; Vulpe, C.; Environ. Sci. Technol. 2013, 47, 11747. 27. Muehlbacher, M.; Spitzer, G. M.; Liedl, K. R.; Kornhuber, J.; J. Comput. Aided Mol. Des. 2011, 25, 1095. 28. Voltolini, A. M.; Horn, R. C.; Rocha, J. A. V.; Resumos da XIV Salao de Iniciaçao Científica - UFRGS, Porto Alegre, Brasil, 2002. 29. Swamidass, S. J.; Chen, J.; Bruand, J.; Phung, P.; Ralaivola, L.; Baldi, P.; Bioinformatics 2005, 21(Suppl. 1), i359. 30. Fligner, M. A.; Verducci, J. S.; Blower, P. E.; Technometrics 2002, 44, 110. 31. Gatnik, M. F.; Worth, A. P.; Review of software tools for toxicity prediction, available at https://publications.europa.eu/en/publication-detail/-/publication/fb675f8d-8758-4451-83c6-638a153e1635/language-en, acessada em junho 2018. 32. Rybacka, A.; Rudén, C.; Andersson, P. L.; Basic Clin. Pharmacol. Toxicol. 2014, 115, 77. 33. Ruppenthal, J. E.; Toxicologia, Rede e-Tec-Brasil: Colégio Técnico Industrial de Santa Maria, Universidade Federal de Santa Maria: Santa Maria, 2013. 34. http://www.antares-life.eu/files/ANTARES_D14.pdf, acessada em junho 2018. 35. Baderna, D.; Golbamaki, N.; Maggioni, S.; Vaccari, M.; Colacci, A.; Benfenati, E. Em Global Risk-Based Management of Chemical Additives II; Baderna, D., ed.; Springer-Verlag: Berlin Heidelberg, 2012, p. 171. 36. http://always-on-target.com/wp-content/uploads/2017/07/5.56mm-CQT-SDS.pdf, acessada em junho 2018. 37. https://echa.europa.eu/documents/10162/18584504/afa_dehp-0005-02-aa_en.pdf/d355aac7-3d27-4f02-827f-bf105c272542, acessada em junho 2018. 38. DeGraeve, G. M.; Elder, R. G.; Woods, D. C.; Bergman, H. L.; Arch. Environ. Contam. Toxicol. 1982, 11, 487. 39. Bulich, A. A.; Greene, M. W.; Isenberg, D. L.; Aquatic Toxicology and Hazard Assessment 1981, 737, 338. 40. Huff, J. E.; Haseman, J. K.; DeMarini, D. M.; Eustis, S.; Maronpot, R. R.; Peters, A. C.; Persing, R. L.; Chrisp, C. E.; Jacobs, A. C.; Environ. Health Perspect. 1989, 82, 125. 41. Bingham, E.; Cohrssen B. Em Patty's Toxicology, 6 Volume Set; Bingham, E., Cohrssen B., eds;. John Wiley & Sons: New Jersey, 2012. 42. Kalf, G. F.; Snyder, C. A.; Rev. Toxicol. 1987, 18, 141. 43. LeBlanc, G. A.; Bull. Environ. Contam. Toxicol. 1980, 24, 684. 44. La Voie, E. J.; Dolan, S.; Little, P.; Wang, C. X.; Sugie, S.; Rivenson, A.; Food Chem. Toxicol. 1988, 26, 625. 45. Toxicology and carcinogenesis studies of naphthalene (Cas nº. 91-20-3) in f344/n rats., U. S. Department of Health and Human Services, 2000. 46. Narbonne, J.-F.; Cassand, P.; Alzieu, P.; Grolier, P.; Mrlina, G.; Calmon, J. P.; Mutat. Res. Lett. 1987, 191, 21. 47. Marchini, S.; Tosato, M. L.; Norberg-King, T. J.; Hammermeister, D. E.; Hoglund, M. D.; Environ. Toxicol. Chem. 1992, 11, 187. 48. Ostergaard, G.; Em The Nordic Expert Group for Criteria Documentation of Health Risks from Chemicals: I25. Toluene, Marklund, S., ed.; National Institute for Working Life: Stockholm, 2000. 49. Mohtashamipur, E., Norpoth, K., Woelke, U.; Huber, P.; Arch. Toxicol. 1985, 58, 106. 50. https://ntp.niehs.nih.gov/ntp/htdocs/lt_rpts/tr203.pdf, acessada em junho 2018. 51. Nomiyama, K.; Minai, M.; Suzuki, T.; Kita, H.;Ind. Health 1967, 5, 143. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access