Artigo
|
|
| Estudo da cinética de oxidação de biodiesel B100 obtido de óleo de soja e gordura de porco: determinação da energia de ativação Study of oxidation kinetics of B100 biodiesel from soybean and pig fat: activation energy determination |
|
Diego Galvan; Juliane R. Orives; Rodolfo L. Coppo; Cezar Henrique F. Rodrigues; Kelly Roberta Spacino; Jurandir P. Pinto; Dionísio Borsato*
Departamento de Química, Universidade Estadual de Londrina, CP 10.011, 86057-970 Londrina - PR, Brasil Recebido em 09/05/2013 *e-mail: dborsato@uel.br The quality of biodiesel is extremely important for its commercialization and use; oxidation of biodiesel is a critical factor because it decreases the fuel storage time. A commercial biodiesel was mixed with synthetic antioxidants, according to a simplex-centroid experimental mixture design, and its stability was evaluated through induction period and activation energy. In all trials, addition of antioxidants increased activation energy in the mixtures containing tertiary butylhydroquinone (TBHQ). When a mixture containing 50% TBHQ and 50% butylated hydroxyanisole was used, synergistic effect was observed, and the major activation energy obtained was 104.43 kJ mol-1. INTRODUÇÃO Com a finalidade de inibir ou retardar a oxidação do biodiesel são empregados compostos químicos conhecidos como antioxidantes. O uso de antioxidantes e seus mecanismos funcionais têm sido amplamente estudados e podem ser classificados em primários, sinergistas, removedores de oxigênio, biológicos, agentes quelantes e antioxidantes mistos.1,2 Os principais e mais conhecidos antioxidantes são os compostos fenólicos sintéticos, tais como butil-hidroxianisol (BHA), butil-hidroxitolueno (BHT), terc-butil-hidroquinona (TBHQ) e propil galato (PG). A estrutura fenólica destes compostos permite a doação de um próton a um radical livre, regenerando a molécula do acilglicerol e interrompendo o mecanismo de oxidação por radicais livres. Dessa maneira, os derivados fenólicos transformam-se em radicais livres, que podem se estabilizar sem promover ou propagar reações de oxidação.3 De acordo com Ramalho e Jorge,3 o BHA é um antioxidante mais efetivo na supressão da oxidação em gorduras animais que em óleos vegetais. Apresenta pouca estabilidade frente a elevadas temperaturas, mas é particularmente efetivo no controle de oxidação de ácidos graxos de cadeia curta, como aqueles contidos em óleo de coco e palma.2 O BHT tem propriedades similares ao BHA sendo que o BHA e o TBHQ são sinergistas entre si.3 O sinergismo apresentado por estes antioxidantes tem sido estudado e os resultados têm demonstrado que, em alguns casos, dependendo da temperatura de ensaio, a mistura é mais eficiente que o antioxidante utilizado isoladamente.3,4 Uma das formas de se avaliar o sinergismo entre antioxidantes é pelo emprego dos delineamentos de misturas propostos por Scheffé,5 sendo o simplex-centroide muito utilizado porque ele permite avaliar a influência dos componentes individuais bem como as suas misturas, permitindo com isso explorar toda a região experimental.4,6-8 Na formulação de um produto muitas vezes a proporção dos ingredientes na mistura, bem como os níveis mínimos/máximos, não são independentes uns dos outros. Experimentos de mistura são tipicamente realizados todas as vezes que a resposta é função das proporções das variáveis e não das quantidades absolutas. Nestes casos, delineamentos especiais para mistura são críticos para o emprego bem sucedido de experimentos envolvendo formulações.4,5,9 Além disso, esses delineamentos geram equações preditivas que permitem a aplicação de algoritmos matemáticos que possibilitam determinar as condições ótimas de uma formulação ou de um processo industrial, mesmo aqueles que envolvem mais de uma variável dependente e ainda com restrições.10-12 O objetivo do trabalho foi determinar a energia de ativação durante o processo de oxidação de biodiesel B100, a partir de diferentes temperaturas, utilizando o delineamento simplex-centroide para avaliar estatisticamente o efeito dos antioxidantes sintéticos utilizados.
PARTE EXPERIMENTAL Biodiesel Utilizou-se biodiesel B100 (Biopar Bioenergia do Paraná - Rolândia - PR, Brasil), isento de antioxidantes, obtido por transesterificação de uma mistura composta de 90% de óleo de soja e 10% de gordura de porco com metóxido de sódio como catalisador. Análise cromatográfica Foi utilizado um cromatógrafo gasoso modelo GC-17A com detector de ionização de chama (Shimadzu), com coluna DB1 (J&W Scientific) - 100% polimetilsiloxano com 30 m de comprimento x 0,25 mm de diâmetro interno x 0,25 µm de espessura de filme. As temperaturas do injetor split e do detector foram mantidas a 340 ºC. A rampa de aquecimento da coluna foi mantida inicialmente a 50 ºC por 2 min e, na sequência, aquecida à razão de 10 ºC min-1 até 180 ºC, mantendo-a nessa temperatura por 2 min, a seguir, aquecida a razão de 15 ºC min-1 até 340 ºC, permanecendo nessa temperatura por 10 min. A vazão do gás de arraste, N2, foi de 1,5 mL min-1 e o volume de injeção de 2,0 mL com razão de split 10. Os dados foram coletados por meio do software CLASS-CR10 Shimadzu. Análise de conformidade As análises foram realizadas em triplicata, segundo a norma ASTM D9313 para ponto de fulgor, ASTM D66414 para índice de acidez, ASTM D405215 para massa específica e ASTM 658416 para teor de glicerina livre e total e mono, di e triglicerídeos. O teor de álcool pela EN 1411017 e de ésteres pela EN 14103.18 Delineamento experimental para mistura (Statistica, 2009)19 Foi utilizado o planejamento simplex-centroide para três componentes, com duas repetições no ponto central, com 2q-1 combinações de misturas sendo q é o número de componentes com soma igual a 1 ou 100%.20 Antioxidantes Foram utilizados o butil-hidroxianisol (BHA) Synth 98,5%, butil-hidroxitolueno (BHT) Synth 99,0% e terc-butil-hidroquinona (TBHQ) Acros 97,0%, todos grau P.A., que foram adicionados diretamente ao biodiesel antes da avaliação da estabilidade oxidativa, nas quantidades estabelecidas pelo delineamento de mistura, não ultrapassando o total de 6,0 x 10-3 mol L-1, aproximadamente 0,1% m/m.8 Teste de estabilidade à oxidação Para todos os ensaios foi utilizado o método acelerado Rancimat (Metrohm, Suíça; Modelo: 873) de acordo com a norma oficial EN 14112.21 As amostras do controle e do ponto central do delineamento utilizado foram realizadas em triplicatas e nos demais pontos em duplicata. Os ensaios foram realizados nas temperaturas de 110, 115, 120 e 125 ºC. Cinética de oxidação do biodiesel Os dados de condutividade obtidos pelo Rancimat, para cada ensaio, foram ajustados considerando-se uma cinética de ordem 122 e os parâmetros constante de velocidade (k) para cada temperatura considerada e energia de ativação (Ea) foram calculados para cada ponto do delineamento. Modelo matemático A função utilizada foi do tipo:
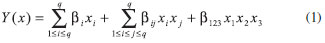
na qual Y representa a função resposta energia de ativação; x1, x2 e x3 são as variáveis independentes e correspondem à porcentagem de TBHQ, BHT e BHA na mistura, respectivamente, e β os parâmetros.9,19 Análise estatística Os coeficientes da regressão, a análise de variância e a otimização das condições foram determinados por meio do software Statistica v.9.0.19
RESULTADOS E DISCUSSÃO Caracterização do biodiesel De acordo com a análise cromatográfica (Figura 1), foi observado que o biodiesel consistia basicamente de ésteres metílicos com composição variando do C12:0 até C24:0.
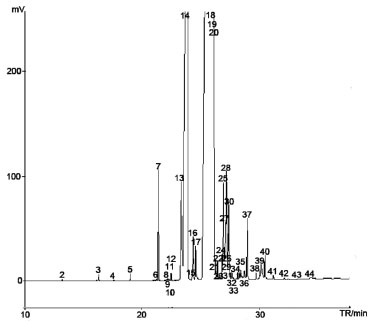 Figura 1. Perfil cromatográfico do biodiesel B100 utilizado
A análise do cromatograma mostrou que o biodiesel utilizado apresentou um teor de ésteres de 98,98% m/m estando em acordo com a EN 14103,18 cuja porcentagem mínima de ésteres exigida deve ser 96,50% m/m.23 Observou-se a presença de ésteres insaturados, como o oleato e linoleato de metila aparecendo em maior quantidade (63,68% m/m), os quais são susceptíveis a reações de oxidação aceleradas pela exposição ao oxigênio e altas temperaturas, que podem gerar compostos poliméricos, que são prejudiciais ao funcionamento do motor.7,24 Na Tabela 1 são apresentados os principais parâmetros de conformidade do biodiesel B100 utilizado, sendo que todos apresentaram valores de acordo com a legislação vigente.25
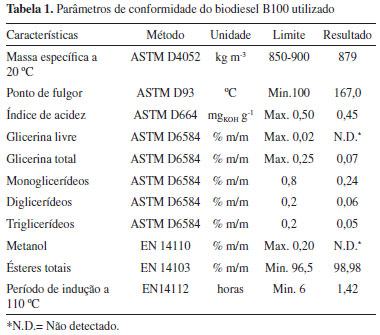
Os teores de mono, di e triglicerídeos presentes somaram juntos 0,35% e o teor de glicerina total verificado foi de 0,07%, valor inferior ao da legislação brasileira, que prevê um teor máximo de glicerina total de 0,25%, enquanto que a glicerina livre não foi detectada.25 A determinação da glicerina residual serve como parâmetro para avaliar a eficiência do processo de purificação do biodiesel, pois quando apresenta elevado teor de glicerina tem sérios problemas de armazenamento quando misturado ao diesel, causando separação nos tanques de estocagem e formação de depósitos que podem entupir os bicos injetores do motor além de aumentar as emissões de aldeídos.26 Para assegurar a qualidade do biodiesel é necessário estabelecer padrões de qualidade, objetivando fixar teores limites dos contaminantes que não venham prejudicar a qualidade das emissões da queima, bem como o desempenho, a integridade do motor e a segurança no transporte e manuseio. Devem ser monitoradas também possíveis degradações do produto durante o processo de estocagem.26 O valor médio do período de indução para a amostra do biodiesel B100 sem antioxidante, que foi usado como controle, foi de 1,42 h (Tabela 1). O alto teor de ésteres de ácidos graxos insaturados, presentes na composição do biodiesel devido ao uso de óleo de soja como matéria prima (90%), torna-o sensível à degradação oxidativa, conduzindo a valores baixos de período de indução. Porém, o valor obtido é superior ao relatado para o biodiesel somente de soja, 0,16 h e 1,36 h,27,28 indicando que o uso da gordura de porco influência no aumento da estabilidade a oxidação. No entanto, ainda há necessidade de adição de antioxidantes nesse biodiesel para atender às especificações cujo valor mínimo do período de indução é de 6 h.25 Na Tabela 2 pode-se notar que após a adição de antioxidantes definidos pelo delineamento simplex centroide ao biodiesel, todos os ensaios apresentaram um aumento no período de indução quando comparados ao controle, e que seus valores diminuem com o aumento da temperatura.
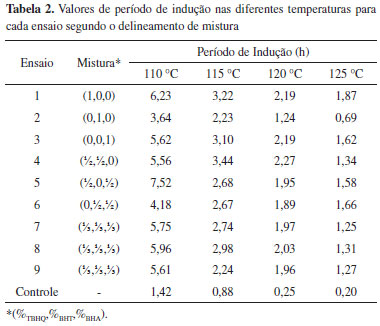
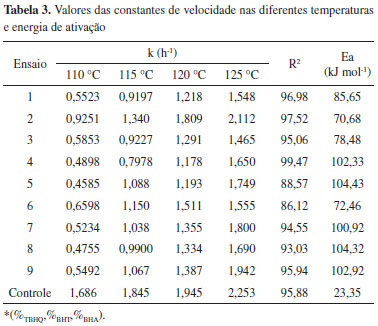
As amostras do biodiesel B100 utilizado, contendo antioxidantes, bem como o controle, foram submetidas ao teste acelerado de estabilidade oxidativa utilizando o Rancimat, nas temperaturas de 110, 115, 120 e 125 ºC. Os valores ajustados do logaritmo neperiano da condutividade elétrica vs tempo podem ser utilizados como método indireto para o cálculo tanto da ordem de reação quanto da constante de velocidade. Justifica-se o uso desta técnica pelo fato do produto da reação de oxidação alterar a condutividade no aparelho Rancimat.22 Este método foi utilizado para cada ensaio e os valores das constantes de velocidade foram determinados. A Tabela 3 apresenta os valores das constantes de velocidade nas diferentes temperaturas e a energia de ativação para o controle e os demais tratamentos.
A equação de Arrhenius é útil porque expressa a relação quantitativa entre a temperatura, a constante de velocidade e a energia de ativação. Uma das principais aplicações é a determinação da energia de ativação de uma reação, partindo-se de dados cinéticos experimentais a diferentes temperaturas e a melhor maneira de efetuarmos esta determinação é graficamente.29,30 A partir da lei de Arrhenius, um gráfico de ln k versus T-1 fornece uma linha reta. A Figura 2 mostra este gráfico para o controle e os demais tratamentos definidos pelo delineamento simplex-centroide, nas diferentes temperaturas aplicadas ao Rancimat.
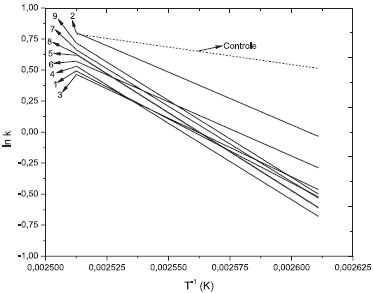 Figura 2. Gráfico de ln k versus T-1 do controle e demais tratamentos contendo antioxidantes em diferentes temperaturas
O fato da Ea ser dada pelo coeficiente angular significa que quanto mais elevada a energia de ativação, mais forte será a dependência entre a constante de velocidade e a temperatura, isto é, mais inclinada será a reta no gráfico.29,31 Na Figura 2 podemos observar que a amostra controle apresenta a menor inclinação, indicando que ela é mais susceptível a oxidação quando comparada com os demais tratamentos contendo antioxidantes. Já a mistura contendo 50% de TBHQ e BHA (ensaio 5) apresenta uma reta com a maior inclinação. De acordo com Levenspiel,29 a influência da temperatura nas reações é determinada pela energia de ativação e pelo nível de temperatura. Reações com valores elevados de Ea são mais dependentes da temperatura e reações com valores baixos de Ea são relativamente independentes da temperatura. Portanto, reações de oxidação do biodiesel B100 obtido predominantemente de óleo de soja ocorrem à temperatura ambiente e são muito sensíveis à variação de temperatura.32 Observa-se na Tabela 3 que os menores valores de Ea foram obtidos nos três primeiros ensaios onde os antioxidantes aparecem isoladamente. As vantagens do TBHQ, quando comparadas com as do BHT e BHA, devem-se aos dois grupos hidroxílicos presentes em sua molécula e ainda a apresentarem certo impedimento estérico. Considerando os valores experimentais obtidos para todos os ensaios contendo misturas com TBHQ, podemos observar um efeito sinérgico quando comparado com os valores da Ea obtida quando se utilizou os antioxidantes isoladamente. Isto implica que o efeito conjunto da mistura é maior que a soma dos efeitos individuais obtidos quando os antioxidantes são usados separadamente. Tal efeito sinérgico não foi observado na mistura contendo BHT com BHA. Porém, a presença dos antioxidantes nas amostras de biodiesel B100, quando comparadas com a amostra controle, aumentou de 3 a 4,5 vezes a energia de ativação e, consequentemente, a estabilidade do biocombustível utilizado. A Tabela 3 mostra ainda que a maior energia de ativação foi obtida no ensaio 5 composto por uma mistura de TBHQ e BHA. Xin et al.33 apresentou um estudo cinético da estabilidade oxidativa de biodiesel obtido de óleo de cártamo em mistura com propilgalato, a uma concentração na ordem de 100 ppm, utilizando o método Rancimat. Os autores encontraram uma Ea de 97,02 kJ mol-1, valor intermediário aos encontrados para os tratamentos com antioxidantes TBHQ, BHT e BHA. No entanto, essa constatação deve ser feita com restrições, uma vez que os antioxidantes são diferentes, a concentração de propilgalato utilizada é menor que a concentração dos antioxidantes empregados no presente estudo e a matéria prima utilizada formada por uma mistura de 90% de óleo de soja com 10% de gordura de porco. De acordo com Levenspiel,29 reações com valores variando entre 40 e 400 kJ mol-1 são consideradas de baixa e alta energia de ativação, respectivamente. Portanto, o biodiesel empregado apresentou pouca estabilidade química, mesmo em presença de antioxidantes, porque os valores obtidos da energia de ativação foram baixos. Aos valores da energia de ativação (Tabela 3) foi aplicado o delineamento de mistura simplex-centroide. Na equação canônica (2), ajustada aos dados experimentais, a variável dependente Y representa a energia de ativação (Ea) e x1, x2 e x3 representam as variáveis independentes TBHQ, BHT e BHA respectivamente. Os termos com asteriscos são significativos em nível de 5%. Em adição, todos os termos, exceto o binário da mistura de BHT e BHA apresentaram coeficientes positivos, indicando que eles influenciam positivamente a Ea do biodiesel B100 em presença de antioxidantes. Os termos significativos apresentaram baixos valores de p, variando de 0,04% para o termo linear de TBHQ (x1) até 0,86% para a interação binária entre o TBHQ e o BHA (x1x3), indicando com isso uma grande influência dos antioxidantes utilizados no comportamento da Ea do biodiesel B100 estudado.
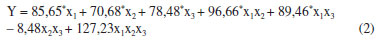
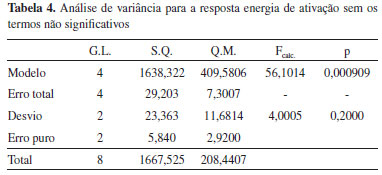
A análise de variância (Tabela 4) mostrou que o modelo proposto é significativo em nível de 5%, apresentando um elevado valor de R2 ajustado, indicando que ele consegue explicar 97% da variância e, além disso, a falta de ajuste, sem os termos de interação ternária (x1x2x3) e binária (x2x3), foi não significativa (p = 20%), indicando que o modelo pode ser usado para fins preditivos.
A região de combinação ternária entre as variáveis independentes TBHQ, BHT e BHA pode ser observada por meio das curvas de nível apresentadas na Figura 3. Ela mostra as regiões de contorno da superfície de resposta para a variável dependente, energia de ativação, obtidas pelo modelo matemático. Ela também mostra que uma maior estabilidade pode ser alcançada utilizando-se uma mistura contendo os antioxidantes TBHQ e BHA.
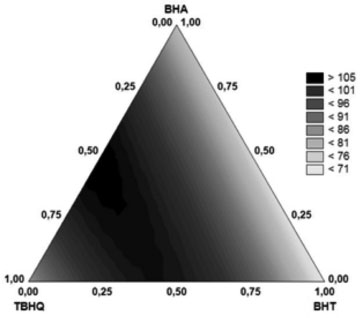 Figura 3. Região de combinação entre as variáveis TBHQ, BHT e BHA obtida pelo modelo matemático (eq. 2) para a energia de ativação
A Figura 4 mostra a otimização da equação preditiva que representa a energia de ativação do biodiesel B100 em presença dos antioxidantes sintéticos. Podemos observar que o valor máximo de 104,43 kJ mol-1 pode ser obtido quando se usa uma mistura contendo 50% de TBHQ e BHA.
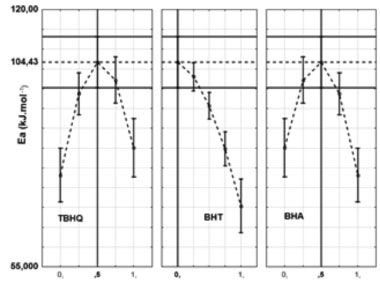 Figura 4. Otimização da energia de ativação do biodiesel B100 em mistura com antioxidantes
A condição ótima mostrada na Figura 4 foi validada experimentalmente, em triplicata, obtendo-se um valor médio de 102,72 kJ mol-1 para a energia de ativação. O teste de Tukey aplicado à média mostrou que não há diferença significativa entre o valor estimado pelo modelo (Ea = 104,43 kJ mol-1) e o valor médio obtido (p = 22,52%). Além disso, o teste de Levene's mostrou que a condição de homogeneidade da variância pode ser aceita, pois o valor de p foi igual 25,51%.
CONCLUSÃO O biodiesel empregado apresentou baixa estabilidade química, pois se observou baixas energias de ativação tanto para o controle quanto para os ensaios contendo os antioxidantes. Porém, a adição de antioxidantes aumentou a energia de ativação em todos os experimentos e naqueles contendo misturas com TBHQ foi observado um efeito sinérgico, quando comparado com os valores da energia de ativação obtida ao se utilizar os antioxidantes isoladamente. A otimização da equação preditiva que representa a energia de ativação do biodiesel B100 em presença dos antioxidantes sintéticos mostrou que o valor máximo de 104,43 kJ mol-1 pode ser obtido quando se emprega uma mistura contendo 50% de TBHQ e 50% de BHA. O delineamento experimental de mistura simplex centroide é uma ferramenta estatística adequada para avaliar a energia de ativação e o efeito sinérgico entre os antioxidantes sintéticos utilizados em um biodiesel B100 obtido a partir de uma mistura de óleo de soja e gordura de porco.
AGRADECIMENTOS A UEL e ao CNPq e CAPES pela concessão de bolsas.
REFERÊNCIAS 1. Jain, S.; Sharma, M. P.; Renewable Sustainable Energy Rev. 2010, 14, 667. 2. Santos, A. N.; Cordeiro, A. M. T. M.; Damasceno, S. S.; Aguiar, R. T.; Rosenhain, R.; Carvalho Filho, J. R.; Santos, I. M. G.; Maia, A. S.; Souza, A. G.; Fuel 2012, 97, 638. 3. Ramalho, V. C.; Jorge N.; Quim. Nova 2006, 29, 755. 4. Borsato, D.; Dall'Antonia, L. H.; Guedes, C. L. B.; Maia, E. C. R.; Freitas, H. R.; Moreira, I.; Spacino, K. R.; Quim. Nova 2010, 33, 1726. 5. Scheffé, H.; J. R. Stat. Soc. B 1963, 25, 235. 6. Hill, T.; Lewicki, P.; Statistics: Methods and Applications, 1st ed., StatSoft Inc: Tulsa, 2006. 7. Maia, E. C. R.; Borsato, D.; Moreira, I.; Spacino, K. R.; Rodrigues, P. R. P.; Gallina, A. L.; Fuel Process. Technol. 2011, 92, 1750. 8. Cini, J .R. M.; Borsato, D.; Guedes, C. L. B.; Silva, H. C.; Coppo, R. L. Quim. Nova 2013, 36, 79. 9. Cornell, J. A.; Experiments with mixtures - designs, models and the analysis of mixture data, 2nd ed., John Wiley and Sons Inc: New York, 2002. 10. Derringer, G.; Suich, R.; J. Qual. Technol. 1980, 12, 214. 11. Chen, J. S.; Lee, C. M.; Crapo, C.; J. Food Sci. 1993, 58, 535. 12. Gacula, M. C.; Design and analysis of sensory optimization, Food & Nutrition Press: Thumbull, 1993. 13. ASTM International; ASTM D93 - 10a Standard Test Methods for Flash Point by Pensky-Martens Closed Cup Tester, 2001. 14. ASTM International; ASTM D664 - 11 Standard Test Method for Acid Number of Petroleum Products by Potentiometric Titration, 2001. 15. ASTM International; ASTM D4052 - 09 Standard Test Method for Density, Relative Density, and API Gravity of Liquids by Digital Density Meter, 2002. 16. ASTM International; ASTM D6584 - 10 Standard Test Method for Determination of Total Monoglyceride, Total Diglyceride, Total Triglyceride, and Free and Total Glycerin in B-100 Biodiesel Methyl Esters by Gas Chromatography, 2003. 17. EN 14110:2003; Fat and oil derivatives. Fatty Acid Methyl Esters (FAME). Determination of methanol content, 2003. 18. EN 14103:2003; Fat and oil derivatives. Fatty Acid Methyl Esters (FAME). Determination of ester and linolenic acid methyl esters content, 2003. 19. Statistica for Windows Software. v.9.0, Tulsa, OK, USA, 2009. 20. Calado, V.; Montgomery, D. C.; Planejamento de Experimentos usando o Statistica. E-papers Serviços Editoriais Ltda, Rio de Janeiro, 2003. 21. EN 14112:2003; Fat and oil derivatives. Fatty Acid Methyl Esters (FAME). Determination of oxidation stability (accelerated oxidation test), 2003. 22. Matos, L. A. C.; Brugnera, A. B.; Banczek E. P.; Rodrigues, P. R. P. Em Materials and Processes for Energy: Communicating Current Research and Technological Developments; Méndez-Vilas, A., ed.; Formatex Research Center: Badajoz, 2013. 23. Karaosmanoglu, F.; Becker, U. G.; Energy Sources 1996, 18, 637. 24. Ferrari, R. A.; Oliveira, V. S.; Scabio, A.; Quim. Nova 2005, 28, 19. 25. Brasil, Agência Nacional do Petróleo, Gás Natural e Biocombustíveis; Resolução nº14, de maio de 2012, estabelece a especificação para a comercialização de biodiesel que poderá ser adicionado ao óleo diesel. Diário Oficial da União, Brasília, 18/05/2012. 26. Lôbo, I. P.; Ferreira, S. L. C.; Cruz, R. S.; Quim. Nova 2009, 32, 1596. 27. Domingos, A. K.; Saad, E. B.; Vechiato, W. W. D.; Wilhein, H. M; Ramos, L. P.; J. Braz. Chem. Soc. 2007, 18, 416. 28. Ryu, K.; Bioresour. Technol. 2010, 101, S78. 29. Levenspiel, O.; Chemical reaction engineering, 3rd ed., John Wiley and Sons Inc: New York, 1999. 30. Russel, J. B.; Química Geral, 2nd ed., Makron Books: São Paulo, 1994. 31. Atkins, P.; Paula, J.; Atkins' Physical Chemistry, 8th ed., Oxford Press: New York, 2006. 32. Borsato, D.; Maia, E. C. R.; Dall'Antonia, L. H.; Silva, H. C.; Pereira, J. L.; Quim. Nova 2012, 35, 733. 33. Xin, J.; Imahara, H.; Saka, S.; Fuel 2009, 88, 282. |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access





