Revisão
|
|
| O potencial da Xantona Natural α-mangostina no desenvolvimento de novos agentes anti-infecciosos: uma revisão The potential of Natural Xanthone α-Mangostin in the development of novel antiinfective agents: a review |
|
Douglas Chaves de Alcântara PintoI; Gabriela Alves de SouzaI; Paulo Pitasse-SantosI; Afonso Santine M. M. VelezI; Debora Decote-RicardoII; Debora Regina Lopes dos SantosII; Leonardo Freire-de-LimaIII; Célio G. Freire-de-LimaIII ; Marco Edilson Freire de LimaI,*
I. Departamento de Química Orgânica, Instituto de Química, Universidade Federal Rural do Rio de Janeiro, 23890-000 Seropédica - RJ, Brasil Recebido em 20/05/2022 *e-mail: marcoedilson@gmail.com The mangosteen (Garcinia mangostana, Linn.) is a tropical fruit cultivated in the tropical forests of Southeast Asian countries. It is recognized as the queen of fruits due to its unique color, aroma, and flavor. It has been used for centuries in Southeastern Asian traditional medicine for the treatment of various diseases. Many functional molecules with high medicinal value are obtained from the pericarp of mangosteen fruit, whose major constituent is xanthone α-mangostin. Several studies have been carried out over the last decades to further investigate and understand the pharmacological properties associated with the plant and its main chemical constituents, belonging to the class of xanthones. In addition, numerous in vitro and in vivo studies related to mangosteen have been published, indicating its importance and its potential application in medicinal chemistry. Prenylated xanthones, which include α-mangostin, are secondary metabolites particularly common in plants belonging to the Clusiaceae family. These substances have been intensively investigated for their potential as biologically active agents. This article describes a critical analysis of published data related to the properties of α-mangostin, aiming to provide a more detailed view of its potential as a chemotherapeutic agent for the prevention and treatment of infectious diseases. INTRODUÇÃO Os produtos naturais (PNs) são reconhecidos historicamente por sua grande importância e contribuição na descoberta e desenvolvimento de novos medicamentos, sendo uma fonte extremamente relevante para a busca de novas alternativas terapêuticas, prevenção e tratamento de diversas doenças. PNs têm como principais características elevadas diversidade e complexidade estruturais, agregando grandes vantagens ao processo de descoberta de novas substâncias potencialmente bioativas.1,2 Para suprir as funções biológicas essenciais durante a evolução, os PNs passaram por otimização de suas estruturas, permitindo o controle dos mais diversos mecanismos de defesa endógenos, bem como propiciando mecanismos de competição com outros organismos. Isso explicaria a grande relevância nos estudos e aplicação destas substâncias para o tratamento de doenças infecciosas e do câncer. A sua longa utilização na medicina tradicional, por diferentes povos pertencentes a culturas distintas, é uma fonte de informações valiosas sobre o perfil de eficácia e segurança dos produtos de origem natural. Além disso, os efeitos adversos, observados para fármacos de origem sintética, devido principalmente ao seu uso em maior escala, despertaram crescente interesse por PNs derivados de plantas.3,4 Outro ponto relevante é que os produtos químicos de origem natural, mesmo aqueles de origem vegetal, que são os mais estudados, ainda estão longe de serem investigados de forma exaustiva.5 Geralmente, as substâncias naturais apresentam massa molecular elevada, maior número de átomos de Carbono sp3 e átomos de Oxigênio, e um menor número de átomos de Nitrogênio e Halogênios. Devido às suas características estruturais, os PNs possuem, em geral, maior número de doadores e aceptores de ligação de hidrogênio, um ponto de grande relevância para as interações destes com os diferentes tipos de receptores biológicos. Além disso, os produtos de origem natural, normalmente, detêm um menor coeficiente de partição, o que indica uma maior hidrofobicidade. Eles podem ainda apresentar maior rigidez molecular, em relação aos compostos de origem sintética.6 Essas características e circunstâncias revitalizaram o interesse dos pesquisadores na descoberta de medicamentos com base em produtos obtidos de fontes naturais. Para o aproveitamento mais racional de todo esse potencial, é de fundamental importância a adoção de uma abordagem interdisciplinar: aliar conhecimento etnofarmacológico a outras importantes áreas do conhecimento, como a botânica, a fitoquímica, a química computacional, as estratégias biotecnológicas e sintéticas, além de testes farmacológicos, tanto in vitro, quanto in vivo. O trabalho coordenado entre as diferentes áreas é crucial para o sucesso das pesquisas na área da química medicinal de produtos naturais.7 Nesta revisão serão discutidos os aspectos químicos e de atividade biológica da xantona natural α-mangostina, presente no pericarpo dos frutos do mangostão e que possui promissora aplicabilidade no desenvolvimento de novos agentes anti-infecciosos.
A QUÍMICA DA XANTONA NATURAL α-MANGOSTINA Xantonas As xantonas são estruturas de origem natural, presentes como metabólitos secundários em famílias de plantas superiores, mas também em fungos, líquens e bactérias.8 Entre as plantas superiores, as xantonas são encontradas em um número limitado de famílias, como a Glusiaceae ou Guttifrae, Moraceae, Polygalaceae e Gentianaceae. Em sua maioria, apresentam-se como compostos polihidroxilados, sendo também encontrados na forma de éteres mono ou polimetílicos, e glicosilados.9 As características estruturais dos compostos desta classe, aliadas ao seu alto potencial como agentes terapêuticos, tem despertado grande interesse na área da Química Medicinal, com ênfase tanto na área dos produtos de origem natural, como também de derivados sintéticos.10 Nesse contexto, as xantonas são consideradas estruturas privilegiadas,11 visto serem capazes de interagir com múltiplos alvos moleculares e, assim, desencadeando a ação farmacológica pretendida. Seu esqueleto base, o sistema xantônico (Figura 1), pode apresentar substituintes diversos, dando origem a diferentes tipos de xantonas, de acordo com a via biossintética ou proposta sintética para obtenção dessas substâncias, as quais, apresentam uma variada gama de atividades biológicas já descritas na literatura.12,13
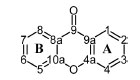 Figura 1. Numeração dos átomos de carbono presentes no núcleo xantônico básico
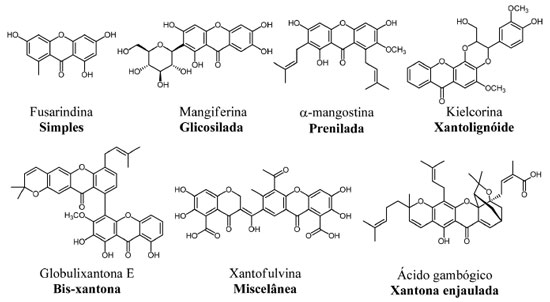
A classe das xantonas abrange uma importante série de heterociclos oxigenados, bastante estudados quimicamente, sendo classificadas e subdivididas de acordo com a natureza de seus substituintes. As xantonas podem ser classificadas em seis grandes grupos: xantonas oxigenadas simples, xantonas glicosiladas, xantonas preniladas, xantolignóides, bis-xantonas e xantonas miscelâneas (ou que não se enquadram em nenhuma das classes anteriores).9 Adicionalmente, dentro das xantonas isoladas de espécies de Garcinia, temos as chamadas xantonas enjauladas (do inglês: caged xanthones). Na Figura 2 estão representados exemplos de cada uma das classes de xantonas supracitadas, que foram descritas quanto à sua atividade biológica.
A metilxantona fusarindina, uma representante das xantonas classificadas como simples, é obtida a partir de uma cepa de Penicillium sp. isolada de Murraya paniculata, possui atividade antibacteriana. Xantonas simples podem apresentar funcionalidades como hidroxila, metoxila, metila, dentre outras; e tem sido isolada, tanto de plantas, quanto de fungos. Na grande maioria das vezes as xantonas metiladas são mais frequentes em fungos e líquens, ao passo que as hidroxiladas e metoxiladas estão presentes com mais frequência em plantas.14 A classe das xantonas glicosiladas, está dividida em dois grupos: xantonas O-glicosiladas e xantonas C-glicosiladas. A maioria se apresenta na forma tetra oxigenada e as famílias Gentianaceae e Polygalaceae são algumas das fontes principais para obtenção desses tipos estruturais de xantonas.15 Um exemplo de xantona C-glicosilada, é a mangiferina (Figura 2), assim como seu isômero isomangiferina e homomangiferina, largamente encontradas em angiospermas e pteridófitas. A mangiferina foi isolada pela primeira vez das cascas do tronco, folhas e frutos de Mangifera indica L (Anacardiaceae), onde é encontrada em abundância.16,17 A existência de um substituinte C-glicosídeo presente no núcleo da molécula pode em algumas situações promover interações moderadas com transportadores presentes na membrana das células, podendo, dessa forma, contribuir para o aumento de sua absorção no meio biológico, elevando sua biodisponibilidade.18 Uma outra classe estrutural de xantonas, também bastante estudada, é a classe das xantonas preniladas, que são caracterizadas por apresentar em sua estrutura um substituinte lipofílico com cinco átomos de carbonos, a prenila. Um composto alvo de várias investigações nos últimos anos, e que representa bem essa classe de xantonas, é a α-mangostina, isolada dos frutos de Garcinia mangostana Linn.19 Os xantonolignóides são uma classe de compostos que apresentam um lignóide, grupo fenilpropânico, ligado ao seu núcleo. Em muitas rotas biossintéticas esse grupo fenilpropânico se liga ao anel xantônico intermediado pelo álcool coniferil. Um importante exemplar desta classe, chamado de kielcorina, pode ser isolado da planta Kielmeyera variabilis e possui atividade anti-inflamatória in vitro.20 As bis-xantonas são originadas quando dois núcleos xantônicos se unem formando dímeros. Estruturalmente, esses compostos são os mais complexos dentre os constituintes das xantonas naturais, sendo mais frequentemente isolados a partir de fungos e líquens e menos comuns em espécies de plantas. A globulixantona E é um dos poucos exemplares provenientes de uma planta, essa bis-xantona foi isolada da raiz de Symphonia globulifera, uma árvore encontrada em florestas africanas e América Latina. No Brasil, esta planta é encontrada na floresta amazônica, onde é popularmente conhecida como Ananim, cujo extrato é utilizado como tônico. Estudos in vitro mostraram que globulixantona E é ativa contra bactérias Staphylococcus aureus, Bacillus subtilis e Vibrio anguillarium (Gram-positivas), mas inativa contra Escherichia coli (Gram-negativa).21 Na classe das miscelâneas estão as xantonas que geralmente são obtidas a partir de fungos, como por exemplo a xantofulvina, isolada de Penicillium sp.22 Essa xantona possui propriedades inibitórias interessantes contra semaforinas, proteínas que atuam como reguladoras durante o desenvolvimento neural do sistema nervoso central e periférico. A expressão de semaforinas em mamíferos, ocasionada por algum tipo de lesão neural, pode resultar em perda da capacidade de regeneração dos axônios dos neurônios.23 O gênero Garcinia contém xantonas enjauladas (do inglês: caged xanthones), que ocorrem principalmente em algumas espécies, como G. morella, G. hanburyi, G. bracteata, G. gaudichaudii e G. scortechinii. Todas essas espécies são amplamente distribuídas no Sudeste Asiático.24 As xantonas enjauladas apresentam uma característica incomum em sua estrutura, com a formação de uma "gaiola" tricíclica sobre o anel C. Além disso, as substituições no anel A e oxidações periféricas podem gerar uma gama de substâncias naturais potencialmente ativas. Esse núcleo enjaulado está associado a um variado perfil de bioatividade, como efeitos antiviral e antibacteriano, por exemplo. O ácido gambógico Figura 2, um dos representantes desta família, tem seus efeitos antiproliferativos, contra linhagens de células tumorais, descritos na literatura.25,26 O ácido gambógico foi, inclusive, avaliado na China em ensaios clínicos para o tratamento de alguns tipos de cânceres, como o de pulmão, de cólon e de rins. Outro dado relevante e descrito em diversos estudos é o fato de que as xantonas enjauladas apresentam baixos efeitos de citotoxicidade, o que representa um ponto favorável à sua aplicabilidade em Química Medicinal.27 A xantona prenilada α-mangostina Garcinia mangostana Linn é uma planta pertencente ao gênero Guttifera, syn. família Clusiaceae, que contém árvores frutíferas bem conhecidas, com cerca de 35 gêneros e até 800 espécies, sendo boa parte de seus frutos comestíveis.28 A α-mangostina pode ser obtida a partir de Garcinia mangostana Linn., sendo extraída das cascas de seus frutos, conhecidos como mangostão (Figura 3A). Já foram isoladas pelo menos 68 xantonas a partir de G. mangostana. Na realidade, as xantonas preniladas são os principais compostos presentes na fruta, possuindo um variado perfil de atividade biológica. Dentre essas xantonas, destaca-se a α-mangostina (Figura 3B), que é o seu componente majoritário, e devido a isso, um dos mais estudados. A planta é nativa do sudeste asiático, de regiões como Tailândia, Malásia, Filipinas, Sri Lanka e Indonésia, tendo se adaptado muito bem às condições de cultivo no Brasil. O primeiro isolamento da α-mangostina foi reportado por Schmid, em 1885.29 Nesse trabalho surgiu, pela primeira vez, o termo "xantona", derivado da palavra xanthos (que no grego significa amarelo), fazendo referência à coloração amarela intensa exibida por esse produto natural (Figura 3C).
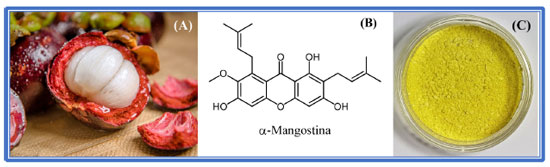 Figura 3. (A) Fruto de Garcinia mangostana, o mangostão;30 (B) Estrutura de seu principal componente, a xantona prenilada α-mangostina, isolada do pericarpo (de cor púrpura) dos frutos; (C) Cristais de α-mangostina, isolados em nosso laboratório
Vários produtos podem ser obtidos e comercializados a partir da polpa do fruto mangostão e também de seu pericarpo, o que demonstra o seu grande potencial de aproveitamento. Desse modo, desperta-se cada vez mais o interesse das indústrias alimentícias e de suplementos, sendo o mangostão detentor de um enorme e crescente potencial comercial.31 Segundo a FAO (Food and Agriculture Organization) estima-se que a produção de resíduos agroindústriais e perdas, que ocorrem durante o ciclo de abastecimento da cadeia alimentar, esteja entre 25 a 30% do total produzido. Porém, é sabido que muitos dos subprodutos gerados na indústria alimentícia ainda contém quantidades apreciáveis de nutrientes, minerais, vitaminas, fibras, além de uma série de substâncias com propriedades bioativas essenciais à saúde.32 Nesse contexto, o mangostão, cada vez mais conhecido por suas qualidades peculiares, tem ganhado destaque e reconhecimento internacional. O fruto é exportado para muitos países desenvolvidos, justamente por se caracterizar como uma fonte extremamente rica em nutrientes e substâncias bioativas, com potencial para combate e prevenção contra envelhecimento precoce e doenças degenerativas, como Alzheimer, câncer e arteriosclerose.33 Os países que lideram a produção mundial de mangostão são Índia, Indonésia e China. Dados recentes demonstram que a Índia é responsável por cerca de 45,89% da produção global, tendo produzido, aproximadamente, 25,6 milhões de toneladas de mangostão em 2019. O Brasil, como o oitavo produtor mundial do fruto, contribuiu com 3,58% da produção mundial em 2020, o que equivale a cerca de 2 milhões de toneladas.34 A introdução da Garcinia mangostana no Brasil é recente, tendo ocorrido em 1935, na Bahia e, em 1942 no Pará. Atualmente a G. manostana é cultivada, principalmente, nesses dois Estados e, em menor escala, nos Estados do Espírito Santo e São Paulo.35 O mangostão é conhecido como a "rainha das frutas", devido ao seus inigualáveis sabor e aroma. Os frutos possuem coloração púrpura-avermelhado, contrastando com uma polpa branca, suculenta e saborosa.36 O pericarpo do fruto tem sido bastante utilizado na medicina tradicional, empregado no tratamento de doenças, como infecções dermatológicas, dores abdominais, diarreias, disenterias, úlcera crônica, e na cicatrização de feridas. Atualmente, o extrato do fruto é comercializado como alimento ou bebida, e até mesmo utilizado como suplemento antidiabético. Cabe ainda destacar o interesse crescente observado nos últimos anos na pesquisa relacionada à α-mangostina, seja na investigação de suas atividades biológicas, ou ainda no planejamento, síntese e avaliação de novos derivados.10,37 A α-mangostina possui um amplo espectro de atividades biológicas, com grande número de trabalhos, descritos na literatura, demonstrando importantes perfis de atividades associados à xantona natural. Muitas evidências in vitro e in vivo revelaram que a α-mangostina é detentora de extensas propriedades farmacológicas, tais como: ação antialérgica, antioxidante, anti-inflamatória, imunomodulatória, anticâncer, antibacteriana, antimalárica, antifúngica, antiparasitária, antiviral, antiobesidade, bem como propriedades neuroprotetoras para a doença de Alzheimer, hepatoprotetoras e cardioprotetoras.38-40 Devido ao variado perfil de atividades biológicas, houve nos últimos anos um considerável aumento no interesse em pesquisas relacionadas à α-mangostina, seja no aprofundamento da investigação de suas atividades biológicas ou, ainda, na avaliação de novos derivados e análogos (Figura 4).41 O crescente interesse despertado em diferentes grupos de pesquisa se dá justamente pelo fato desta substância natural apresentar uma versatilidade sintética e estrutural extremamente favorável ao planejamento e execução de variadas modificações sintéticas, o que permite, a princípio, modular o perfil farmacocinético e farmacodinâmico das novas substâncias sintetizadas, que passam a ter o potencial de se tornarem novos candidatos a fármacos para diferentes aplicações.42,43
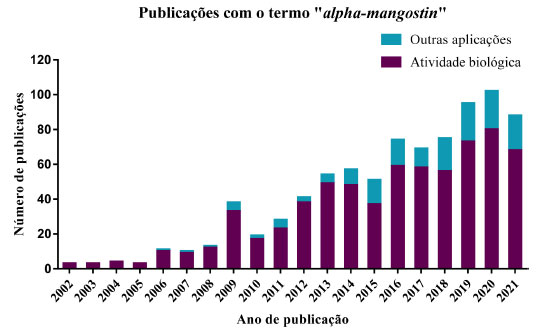 Figura 4. Gráfico de trabalhos publicados envolvendo estudos com a xantona natural α-mangostina41
Biossíntese de xantonas As rotas biossintéticas das xantonas têm sido estudadas desde a descoberta da presença dessas substâncias em fontes naturais. A etapa fundamental na via biossintética de xantonas é a formação do próprio esqueleto tricíclico xantônico, os intermediários-chave podem ser poli-hidroxibenzofenonas.44 Um dos primeiros trabalhos investigativos, na elaboração de uma proposta de via biossintética para as xantonas, foi realizado por Fujita e Inoue, em 1980. Nesse estudo, os autores utilizaram como ferramenta a marcação com isótopo de carbono 14C, vários compostos foram marcados e administrados às partes aéreas da planta Anemarrhena asphodeloides bunge (Liliaceae), que produz mangiferina. Nesse trabalho a fenilalanina, o ácido para-cumárico, o ácido para-hidroxibenzóico e o ácido protocatecuico foram marcados isotopicamente. No entanto, apenas a fenilalanina e o ácido para-cumárico demostraram capacidade para se incorporarem no esqueleto xantônico. Esse resultado sugeriu que esses dois compostos poderiam ser os precursores diretos para a biossíntese da mangiferina.45 Dessa forma, a fenilalanina, biossintetizada pela rota do chiquimato, sofre uma β-oxidação, com perda de dois átomos de carbono, dando origem ao ácido meta-hidroxibenzóico. Ele, ao reagir com três unidades de acetato, leva à formação do intermediário chiquimato-acetato que, por sua vez, cicliza e dá origem ao intermediário 2,3',4,6-tetraidroxibenzofenona, precursor-chave na formação do esqueleto xantônico (Esquema 1). Experimentos realizados com Gentiana lutea, utilizando fenilalanina marcada com 14C, forneceram xantonas contendo o marcador no anel B. Por outro lado, quando tratadas com acetato marcado com 14C, foram produzidas xantonas em que o marcador estava presente no anel A. Assim, após análises, a incorporação da fenilalanina foi observada, confirmando a importância deste precursor na biossíntese de xantonas.46,47
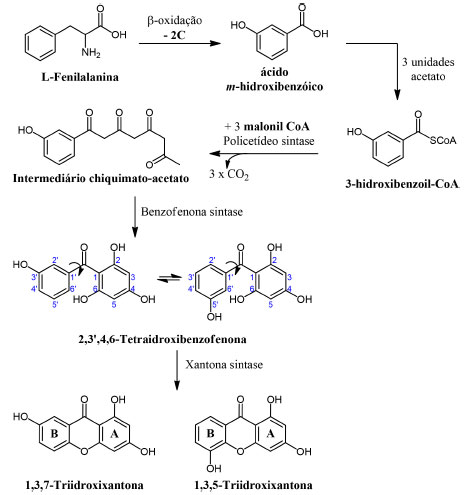 Esquema 1. Via biossintética para formação de xantonas
Para ocorrer a reação de ciclização, levando à formação completa do sistema xantônico a partir da benzofenona (2,3',4,6-tetraidroxibenzofenona), é necessário que uma reação de acoplamento oxidativo fenólico aconteça, para formar o anel heterocíclico central das xantonas.48 Um dos primeiros estudos mecanísticos de ciclização deste anel foi realizado por Beerhus, em 1996, utilizando uma linhagem celular de Centaurium erythraea.49,50 Outro experimento importante foi realizado com Hypericum androsaemum, onde os genes responsáveis pela expressão da enzima bezofenona sintase foram clonados. Essa estratégia, empregando engenharia genética, permitiu que uma mutação específica ocorresse em uma cavidade do sítio ativo da proteína, originando a fenilpirona-sintase, uma nova variante de policetídeo-sintase.51,52 As policetídeo-sintases do tipo III estão intimamente envolvidas na construção de uma diversidade de PNs. Com a variação dos substratos iniciais é possível promover alterações no número de extensões nas cadeias desses compostos, bem como na forma e no modo de ciclização intramolecular que vai ocorrer.53 Os resultados desses estudos foram fundamentais para a compreensão e elucidação dos mecanismos de ciclização em sistemas xantônicos. Esse processo de ciclização ocorre inicialmente com a transferência de dois elétrons, seguida de desprotonação, produzindo assim, um radical fenóxido, que é estabilizado por ressonância. O radical fenóxido formado, que dependendo da espécie vegetal estará funcionalizado em posições distintas do anel B da benzofenona intermediária, sofre ciclização, levando à formação do núcleo tricíclico xantônico, através de um ataque eletrofílico regiosseletivo (Esquema 2).54
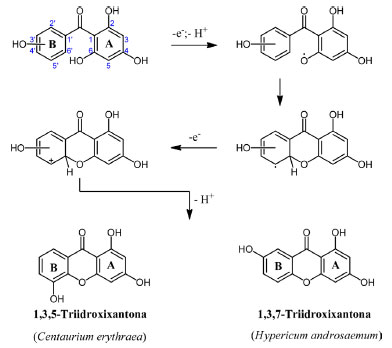 Esquema 2. Mecanismo de acoplamento regiosseletivo para 2, 3', 4, 6-tetraidroxibenzofenona
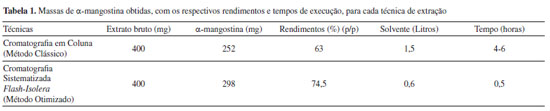
Isolamento e purificação da α-mangostina a partir da matriz vegetal Ao se imaginar a utilização de metabólitos especiais de origem vegetal como fármacos, ou mesmo como matérias-primas para a preparação destes, impõe-se como limitações os fatos da maioria deles serem biossintetizados em pequenas quantidades; serem de difícil isolamento; e não serem obtidos a partir de fontes renováveis. Em relação a essas características, a xantona natural α-mangostina é uma das raras exceções.55 A α-mangostina ocorre em maiores proporções no extrato obtido a partir do pericarpo dos frutos de G. mangostana, compondo cerca de 60 a 70% da massa do extrato bruto. A metodologia clássica envolve a extração do pericarpo dos frutos de G. mangostana com solventes de média polaridade, como diclorometano ou acetato de etila, seguida por separação em coluna aberta, empacotada com sílica gel.56 Em nosso grupo, o isolamento da α-mangostina foi realizado através da adaptação de metodologias previamente descritas. A extração da matriz vegetal foi realizada utilizando-se acetato de etila e para a purificação foi utilizado o equipamento Isolera-Flash System (Biotage AB, Uppsala, Sweden) com o objetivo de se otimizar o processo de separação da α-mangostina. Inicialmente, o pericarpo dos frutos de G. mangostana (440 g) foram secos em estufa com circulação de ar a 45 oC por 36 h, gerando 210 g de matéria seca, indicando a perda de 53% de água e demais componentes voláteis. As cascas secas dos frutos foram então trituradas em liquidificador semi-industrial e armazenadas à temperatura ambiente. Cerca de 10 g do pó das cascas do mangostão foram extraídos em aparelhagem de Soxhlet, usando como solvente o acetato de etila. Após remoção do excesso de solvente, o extrato bruto foi obtido na forma de um material viscoso, que cristalizou, após repouso de 48 h à temperatura ambiente, com massa igual a 1,14 g. Posteriormente, 400 mg deste extrato bruto foi purificado por cromatografia líquida em coluna aberta, usando como eluente a mistura hexano/acetato de etila em proporções variáveis de 5 a 30% do solvente mais polar, com incrementos de 5%. Assim, foi possível a separação dos componentes majoritários contidos na matriz vegetal, a saber, as xantonas α-mangostina e gartanina. As massas obtidas para cada xantona foram 252 mg e 60 mg, respectivamente. A estratégia de otimização da metodologia de extração da α-mangostina, utilizando o equipamento Isolera-Flash System, teve como objetivos principais a redução no tempo de aquisição dos constituintes majoritários de interesse, presentes na matriz vegetal. Assim, diminui-se também a demanda por solventes orgânicos, utilizados em larga escala nos métodos clássicos de purificação. Por fim, o produto natural pôde ser obtido com alto rendimento e elevado teor de pureza. As vantagens da utilização do equipamento automatizado, como o Isolera-Flash System, devem-se à possibilidade de se trabalhar com um gradiente de solvente de maneira mais controlada, bem como com um sistema de detecção e recolhimento das frações mais eficiente. Com isso, observou-se uma redução significativa de tempo e de uso de solventes, promovendo-se o desenvolvimento de uma química mais sustentável e menos agressiva ao meio ambiente. Na Tabela 1, a seguir, estão os resultados comparativos de ambas as metodologias utilizadas.
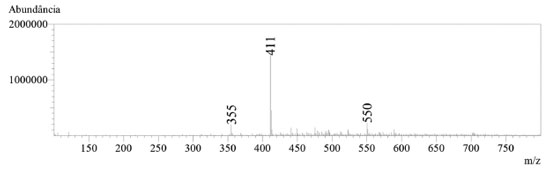
A pureza do produto natural, α-mangostina, foi avaliada por cromatografia líquida de alta eficiência (CLAE), acoplada à espectrometria de massas. A análise foi realizada em um equipamento Shimadzu LCMS 2020, utilizando-se coluna Kromasil C18 150 × 4.6 mm × 5 µm (AkzoNobel) e sistema binário composto por água contendo 0,1% ácido fórmico (A) e acetonitrila contendo 0,1% ácido fórmico (B). O monitoramento da análise foi realizado por medida da absorção no ultravioleta (UV) utilizando detector de arranjo de diodos (DAD) na faixa de 200 - 400 nm e espectrômetro de massas com método de ionização por electrospray no modo positivo (ESI+). Na Figura 5, é possível notar no cromatograma obtido por DAD (245 nm) um único pico majoritário (tR = 7,75 min.), com pureza acima de 99% e perfil da curva UV condizente com o reportado para a α-mangostina.31 Na Figura 6 é mostrado o espectro de massas (ESI+) para o produto obtido, de modo que foi observado sinal de m/z 411, condizente com o valor de m/z 411,2 calculado para C24H27O6+, referente ao íon molecular adicionado de um próton [M+H]+.
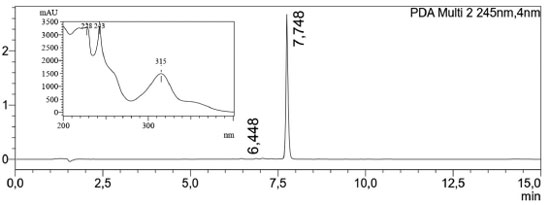 Figura 5. LCMS-PDA (200-400 nm) α-mangostina. Condições: t = 0 min, 50% B; t = 5 min, 95% B; t = 12 min, 95% B; t = 13 min, 50% B
Síntese total da α-mangostina Apesar do extenso número de trabalhos disponíveis na literatura, envolvendo estudos das diversas atividades biológicas exibidas pela α-mangostina, são raros os trabalhos descrevendo rotas para a síntese total desta xantona natural. Esse fato se deve, principalmente, à elevada acessibilidade do produto natural nas matrizes vegetais de onde o mesmo é extraído, além da facilidade da sua extração e purificação em quantidades adequadas aos ensaios. Cabe também ressaltar que a principal fonte de extração da α-mangostina, o pericarpo dos frutos do mangostão, é um material de descarte, se configurando assim como uma fonte de baixo custo, renovável e abundante. O primeiro trabalho descrevendo a síntese total da α-mangostina foi realizado pelo grupo de Nishiyama e colaboradores, em 2002, através de uma estratégia convergente, tendo como precursores dos dois fragmentos aromáticos, o 2,4-diidroxibenzaldeído (1, Esquema 3, entrada 1a) e o 1,3,5-triidroxibenzeno (floroglucinol, 2, Esquema 3, entrada 1b). Os dois precursores foram submetidos, cada um deles, a uma sequência sintética de oito etapas, tendo sido transformados, respectivamente, nos intermediários 3 e 4, adequadamente funcionalizados, para serem posteriormente unidos através da sequência convergente, mostrada no Esquema 3, entrada 2. O acoplamento dos fragmentos 3 e 4 foi realizado através da adição do ânion gerado pelo tratamento do brometo aromático com n-BuLi, o qual, uma vez formado, se adiciona à carbonila aldeídica presente em 3. O álcool 5 (Esquema 3, entrada 2), após oxidação e desproteção das hidroxilas fenólicas benziladas, gerou a cetona intermediária 6, a qual ciclizou, através do seu tratamento com PPh3/CCl4, em THF, gerando o anel heterocíclico central, característico do esqueleto xantônico. A desproteção da hidroxila fenólica, protegida na forma do éter metóxi-metílico (MOM), forneceu então a α-mangostina, em rendimento de 7,6% após as quatro etapas finais de síntese.57
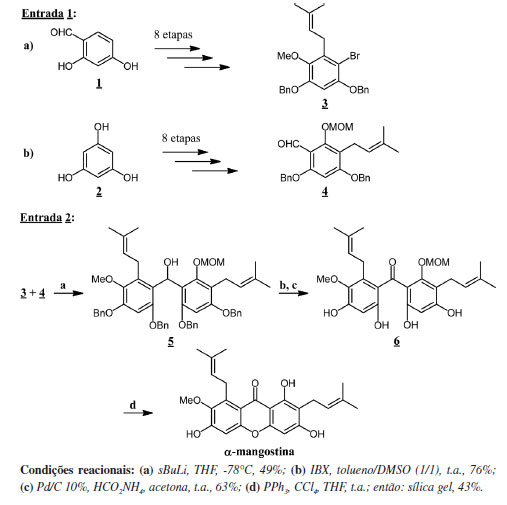 Esquema 3. Abordagem descrita por Nishiyama e colaboradores para a síntese total da α-mangostina57
Posteriormente, em 2013, Wang e colaboradores descreveram uma abordagem sintética mais concisa, baseada numa reação de acilação de Friedel-Crafts entre o cloreto do ácido 2,4,5-trimetóxibenzóico (7) e o 1,3,5-trimetóxibenzeno (8), mas que na etapa de introdução das duas prenilas se inspirou na abordagem original, descrita pelo grupo de Nishiyama (Esquema 4). Na abordagem de Wang, a α-mangostina foi obtida em mistura com a β-mangostina, numa proporção de 61,3% e 24,8%, respectivamente.58
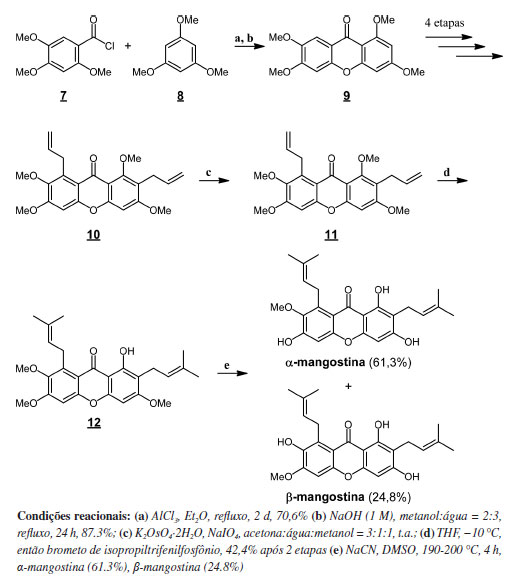 Esquema 4. Abordagem de Wang para a síntese de α- e β-mangostina58
ATIVIDADES BIOLÓGICAS DA α-MANGOSTINA Como vivemos numa atmosfera oxidante, os radicais livres de oxigênio, bem como outras espécies oxidantes relacionadas, são onipresentes no organismo humano, bem como nos demais organismos aeróbicos. A chamadas espécies reativas de oxigênio (ERO's) possuem tempo de meia-vida curto, estando envolvidas em diferentes tipos de reações de oxirredução, as quais, potencialmente, podem gerar danos celulares através de modificações oxidativas em biomacromoléculas, dentre as quais proteínas e ácidos nucléicos. Além desses dois substratos, os lipídios são também alvos preferenciais destas ERO's. De fato, apesar da ocorrência de vários sistemas enzimáticos e não enzimáticos que visam manter a homeostase, através do controle das concentrações intracelulares de ERO's, em algumas situações pode ocorrer a formação excessiva dessas espécies, levando ao acúmulo de produtos que comprometem a função e a estrutura, tanto celular quanto tissular. Esses eventos, normalmente, levam à degeneração, e até mesmo à morte celular com a consequente degradação de tecidos. Estas alterações são observadas tanto na gênese quanto na progressão de várias patologias, e mesmo durante o processo normal de envelhecimento. Desta forma, os eventos oxidativos são o pano de fundo de diferentes enfermidades, estando eles associados à fisiopatologia delas. Destacam-se nesse cenário as doenças cardiovasculares, as doenças neurodegenerativas, os diferentes tipos de cânceres, além dos processos inflamatórios, associados aos mais variados tipos de infecção, causadas por diferentes tipos de agentes etiológicos (como vírus, protozoários, bactérias e fungos).59 A formação de radicais de oxigênio está associada ao metabolismo redox celular, que tem início com a redução monovalente do oxigênio molecular por proteínas de transferência de elétrons ou redutores endógenos, produzindo o radical superóxido O2•−. Sob condições fisiológicas, < 0,2% do oxigênio total consumido pelas mitocôndrias é reduzido monovalentemente a O2•−. No entanto, como as taxas de consumo de oxigênio mitocondrial são grandes, os fluxos de O2•− podem ser significativos.60 Outras espécies de ROS's de importância, formados em diferentes microambientes, são o radical hidroxila (•OH), a espécie oxidante mais poderosa produzida no meio biológico, além de radicais peroxila (ROO•). Estudos teóricos demonstram que a α-mangostina é capaz de neutralizar tanto radicais •OH, quanto •OOH, através de dois caminhos distintos, a transferência de átomos de hidrogênio (TAH) e a formação de adutos radicalares (FAR) (Esquema 5). Os autores demonstraram ainda o favorecimento dessas reações da α-mangostina em meio aquoso, quando comparadas à sua ocorrência em a meios apolares. Outro ponto ressaltado nesse estudo foi que a eficácia da α-mangostina como sequestrante do radical •OOH é semelhante à dos carotenos, superior à da alicina, da melatonina e da N-acetilcisteína amida, e inferior à do ácido 2-propenossulfénico.61 Esses resultados evidenciam a α-mangostina como um excelente agente sequestrador de radicais livres no meio biológico. Dessa forma, as ações terapêuticas desta xantona natural, além de poderem estar associadas à sua capacidade de interagir com diferentes tipos de receptores biológicos específicos, podem ser, principalmente, associadas com sua pronunciada capacidade antioxidante.
 Esquema 5. Mecanismos de inativação de ERO's pela ação da α-mangostina (MGT)61
α-MANGOSTINA COMO AGENTE ANTI-INFECCIOSO Os PNs são fontes históricas, tanto de matéria-prima como de inspiração para a descoberta e o desenvolvimento de novos fármacos.61 Nesse contexto, a xantona prenilada α-mangostina coloca-se como uma molécula extremamente promissora, devido ao seu perfil estrutural, à sua abundância e acessibilidade do material vegetal onde ocorre, além da facilidade de sua extração.62 A α-mangostina apresenta uma grande variedade de atividades biológicas associadas a ela, sendo que aqui destacamos o seu potencial como agente anti-infecciosos, devido, principalmente, à demanda crescente de novas alternativas terapêuticas para o tratamento dos diferentes tipos de doenças infecciosas, tanto aquelas já existentes, quanto as infecções emergentes, que se colocam como verdadeiras ameaças à sobrevivência humana. A família dos agentes anti-infecciosos engloba os diferentes fármacos que possuem a capacidade de inibir, ou mesmo bloquear, a propagação de um determinado patógeno. Essa classe de fármacos pode também eliminar totalmente o agente etiológico presente no organismo hospedeiro. Dentro desta classe terapêutica encontramos os fármacos antivirais, os antiparasitários (antiprotozoários e anti-helmínticos), antibacterianos (incluindo os fármacos antituberculose), além dos fármacos antifúngicos.63 Atividade antiviral As infecções virais representam uma das principais causas de doenças infecciosas agudas e crônicas, sendo um dos principais contribuintes para o aumento global de doenças.64 Diversas pesquisas têm descrito estratégias virais com interferência nos mecanismos celulares que modulam os principais fatores da resposta imunitária e vias de sinalização da célula hospedeira.65 Vivemos, nesse momento, os impactos de uma pandemia causada pelo SARS-CoV-2, um vírus pertencente ao gênero Betacoronavírus, subfamília Orthocoronavirinae e família Coronaviridae (ICTV).66,67 Temos exemplos de outras infecções virais de grande impacto, como a causada pelo HIV, que surgiu na segunda metade do século XX e somente no ano de 2020 contribuiu para o óbito de cerca de 680.000 pessoas em todo o mundo.68 Na última década, várias doenças virais têm emergido ou reemergido, causando importantes impactos epidemiológicos em diferentes continentes, à exemplo dos recentes surtos associados aos vírus Nipah, Nilo Ocidental, febre do Vale do Rift, SARS, varíola dos macacos, gripe aviária e Chikungunya.69 As doenças virais são, em geral, extremamente infecciosas e podem ocorrer de modo imprevisível. Este cenário revela uma situação alarmante, com riscos constantes de epidemias iminentes.70 Para controlar as infecções virais, suas rápidas disseminações, bem como as mutações virais recorrentes, que são responsáveis pelo desenvolvimento de resistência, novas moléculas, em particular as oriundas de PNs que possuem potencial terapêutico, tem sido alvo de pesquisas em todo o mundo. Isto se deve, principalmente, por essas moléculas naturais possibilitarem a prevenção, intervenção na transmissão e a identificação de mecanismos antivirais, o que tem atraído grande interesse.71 Dentre os esses, os polifenóis, classe de PNs da qual a α-mangostina faz parte, tem merecido um destacado interesse.72 Atividade contra o vírus da hepatite C Os vírus causadores de hepatite crônica estão associados a doenças hepáticas inflamatórias como a cirrose hepática e o carcinoma hepatocelular.73 Estima-se que 354 milhões de pessoas em todo o mundo vivam com hepatite B ou C e, para a maioria, os métodos de diagnóstico e o tratamento estão fora de alcance. Segundo a Organização Mundial de Saúde (OMS), cerca de 4,5 milhões de mortes prematuras poderiam ser evitadas em países com baixos índices de desenvolvimento até 2030 por meio de vacinação, testes diagnósticos, medicamentos e campanhas educacionais. A estratégia global de combate às hepatites crônicas da visa reduzir as novas infecções em 90%, e as mortes em 65% até 2030.74 Embora tenha ocorrido avanços na eficácia e segurança dos medicamentos utilizados no tratamento terapêutico das hepatites crônicas B e C, como telaprevir, boceprevir, simeprevir e sofosbuvir, aprovados pelo FDA, o alto custo desses medicamentos pode limitar a inclusão de grande parte dos pacientes, principalmente nos países em desenvolvimento. Desse modo, uma nova classe de substâncias que desempenham mecanismos de ação contra o vírus das hepatites crônicas, necessita ser desenvolvida, para garantia do acesso universal.75 Sabendo das propriedades antioxidantes e antivirais do mangostão, Choi et al.,76 em 2014, avaliaram a potencial atividade do extrato etanólico do fruto em modelo in vitro de infecção com o vírus da hepatite C (HCV, genoma Rluc-J6/JFH1) em células de hepatoma humano Huh7.5. A fim de se avaliar a ação sobre a replicação viral, os autores estudaram tanto o efeito do extrato, quanto das substâncias isoladas. O extrato etanólico apresentou pronunciada atividade contra a replicação celular do vírus HCV, de modo que foi observada inibição da replicação viral com CE50 = 5,5 μg mL-1, enquanto a concentração citotóxica para 50% da população da célula hospedeira (CC50) foi de CC50 = 12,8 μg mL-1. Após o isolamento das substâncias majoritárias presentes no extrato, α-mangostina e g-mangostina, ambas tiveram seu efeito antiviral e citotóxico avaliado. Utilizando-se o mesmo modelo de infecção in vitro, observaram-se atividades antivirais com valores de CE50 de 6,3 μmol L-1 para α-mangostina e 2,7 μmol L-1 de g-mangostina e efeitos citotóxicos com valores de CC50 de 9,9 μmol L-1 para a α-mangostina e 8,2 μmol L-1 para g-mangostina, evidenciando-se um reduzido índice de seletividade (IS), que é calculado pela razão entre a concentração tóxica de uma dada amostra e sua concentração bioativa efetiva. No entanto, os autores chamaram atenção para o fato de que, em tratamento anterior com o extrato na concentração de 10 μmol L-1, a viabilidade celular permaneceu praticamente inalterada. Após análise por CLAE a proporção observada de α e g-mangostina, naturalmente encontradas no extrato, foi em torno de 5: 1. Logo, eles decidiram fixar a concentração de g-mangostina em 1 μmol L-1 e foram aumentando gradativamente a concentração de α-mangostina. Nessas condições, α-mangostina foi capaz de suprimir a replicação do vírus com um valor CE50 de 2,5 μmol L-1, não havendo citotoxicidade significativa até concentração de 8 μmol L-1. Esses resultados indicam que os principais constituintes do extrato etanólico do pericarpo do mangostão, as xantonas α- e g-mangostina, desempenham um papel crucial na supressão da replicação do vírus da hepatite C, quando eles coexistem em uma proporção natural.76 Atividade contra o HIV Apesar dos avanços significativos nos tratamentos para o HIV, as estratégias terapêuticas atuais ainda não garantem a cura do HIV.77 Com a atual terapia antirretroviral, permite-se que o nível de vírus seja mantido abaixo do nível de detecção. Porém, os efeitos adversos e a necessidade de administração diária dos medicamentos utilizados, mesmo que o paciente esteja relativamente bem, pode ocasionar a não adesão e interrupção do tratamento. A consequência de uma interrupção, ainda que breve, é um rápido aumento no nível viral, o que promove o aumento do potencial de mutações de escape da terapia atual, havendo a necessidade de ajustes na manutenção do regime dos fármacos aplicados no tratamento.78 O Vírus da Imunodeficiência Humana Tipo 1 (HIV-1), tem seu genoma constituído por duas cópias idênticas de RNA de fita simples, possuindo genes estruturais, reguladores e auxiliares, que estão envolvidos na codificação de proteínas virais que desempenham importante papel na expressão, transmissão e patogênese do vírus. Em meio ao processo de maturação do vírus, a poliproteína Gag-Pol é gerada, sendo a precursora do HIV-1.79 A protease do HIV-1 (aspartil protease) é fundamental durante o processo em que ocorre a catalise e a clivagem dos polipeptídeos precursores de Gag-Pol, sendo essa divisão uma etapa extremamente relevante para a geração de partículas infecciosas.80 No início das pesquisas do HIV muitos compostos naturais foram avaliados quanto à sua capacidade de supressão viral, várias substâncias à base de plantas foram estudadas e continuam sendo avaliadas. Essas novas substâncias com potencial inibitório podem dar origem a novos antirretrovirais, principalmente frente a mutações de escape, configurando-se como possíveis alternativas para terapia do HIV, com tratamentos mais econômicos.81 Chen e colaboradores, em 1996, avaliaram a atividade dos constituintes de G. mangostana frente à protease do vírus HIV. O efeito inibitório e os estudos cinéticos dos compostos isolados, α-mangostina e g-mangostina, foram realizados através da proteólise do substrato heptapeptídico.82 As duas xantonas avaliadas mostraram atividades inibitórias relevantes sobre a protease do vírus HIV, com valores de CE50, para α-mangostina e ɤ-mangostina, de 5,12 ± 0,41 μmol L-1 e 4,81 ± 0,32 μmol L-1, respectivamente. Para efeito comparativo, os pesquisadores usaram como controle positivo a Pepstatina A, um reconhecido inibidor de protease,83 que apresentou CE50 de 76 ± 5,4 nmol L-1. Esse estudo demonstrou que ambos os compostos, α-mangostina e g-mangostina, apresentaram um tipo de inibição não-competitivo. Os valores de constante de inibição, Ki, foram 10,7 ± 0,95 μmol L-1 e 7,8 ± 0,40 μmol L-1, para α-mangostina e g-mangostina, respectivamente. Os resultados dos valores de CE50 e valores de Ki de α-mangostina e g-mangostina mostram que a diferença estrutural entre as duas xantonas tem muito pouco efeito sobre suas atividades.82 Contudo, apesar de promissores e apresentarem potencial para a realização de estudos posteriores, os resultados do trabalho de Chen e colaboradores, até onde sabemos, não foram aprofundados. Atividade contra o vírus Chikungunya O vírus Chikungunya, transmitido pelo mosquito Aedes aegypti e Aedes albopictus, foi identificado pela primeira vez em 1952, durante um surto que ocorreu no planalto de Makonde, na região sul da Tanzânia.84 Atualmente a doença está distribuída globalmente, causando surtos esporádicos, dos quais os principais sintomas são febres e dores severas nas articulações.85 A dor nas articulações associada à Chikungunya é muitas vezes debilitante e pode variar em duração, de algumas semanas até anos. Trata-se de uma infecção recorrente em países tropicais da África e da Ásia, tendo, nos últimos anos, ocorrido também em regiões de clima temperado, como o Sul da Europa e as Américas Central e do Norte.86 Apesar de cerca de 1,3 bilhão de pessoas estarem em risco de contrair Chikungunya, ainda não há medicamentos ou vacinas especificas disponíveis para o tratamento ou mesmo a profilaxia da infecção.87 O ciclo replicativo do vírus no hospedeiro inicia-se via endocitose mediada por receptores, as principais proteínas do envelope viral, E1 e E2, são responsáveis por realizar a adsorção com a superfície das células.88 As proteínas não estruturais, nsP1-4, possuem diversas funções intracelulares, sendo reconhecidas por serem mediadoras primárias da replicação viral, comprometendo uma intervenção medicamentosa eficaz.89 Em 2021, Patil e colaboradores88 exploraram a atividade antiviral de α-mangostina, in vitro e in vivo, contra infecções por Chikungunya, bem como investigaram o possível mecanismo de ação envolvido na atividade antiviral. Em seus estudos de proliferação celular, as células Vero E6 foram infectadas com o vírus e submetidas a diferentes concentrações de α-mangostina (1 μmol L-1, 2 μmol L-1, 4 μmol L-1 e 8 μmol L-1). O efeito no vírus, conforme avaliado por ensaio de unidade formadora de foco (FFU), mostrou que na condição de pré-tratamento das células com α-mangostina, a 8 μmol L-1 e adicionada 4 h antes da infecção, houve redução da replicação viral, de 6,40 para 5,10 log10 médio FFU mL-1, o que significa uma redução de 95%. Quando ela foi adicionada na condição de co-tratamento, já com o vírus em cultura, a redução foi de 100%, na concentração de 8 μmol L-1. Na condição de pós-tratamento, que foi o tratamento das células com α-mangostina após 4 h de infecção ocorreu redução de 6,02 para 5,06 log10 FFU mL-1 médio, significando uma redução de 89%. No ensaio quantitativo de RT-PCR, observou-se uma redução significativa de 1log e 3log no número de cópias do RNA viral para as condições de pré e co-tratamento, na concentração de 8 μmol L-1 de α-mangostina, enquanto foi verificada uma redução < 1log no número de cópias de RNA do vírus, em condições pós-tratamento, evidenciando a ação antiviral.88 Os ensaios in vivo avaliaram tanto o efeito sobre a carga do RNA viral sérico, quanto sua presença no tecido muscular em camundongos C57BL/6 infectados por vírus Chikungunya por via intramuscular.90 O tratamento com a α-mangostina foi realizado por via intraperitoneal e a carga viral monitorada no 3º, 5º e 7º dias após a infecção (DAI). Foi observada redução significativa nos níveis de RNA viral dos camundongos tratados com 40 mg kg-1 de α-mangostina em relação aos animais sem tratamento. Para os níveis de RNA viral sérico a redução foi de 99,2% no 3º DAI, 99,4% no 5º DAI e 99,4% no 7º DAI. Já os níveis de RNA viral no tecido muscular foram reduzidos em 99,56%, 99,91% e 99,96% respectivamente para os 3º, 5º e 7º DAI.88 Além disso, os estudos histopatológicos mostraram que o tecido muscular infectado pelo vírus apresentou degeneração marcante, atrofia, infiltrações e edema no 3º, 5º e 7º DAI, em comparação aos tecidos normais. A presença de infiltração celular inflamatória mononuclear entre as fibras musculares, e alterações coagulativas e degenerativas com perda de continuidade no comprimento, foram observadas nos animais infectados. Contudo, quando tratados com a dose de 40 mg kg-1 de α-mangostina, verificou-se uma regeneração dos tecidos musculares. Por outro lado, nos animais com administração de dose de 20 mg kg-1 houve melhora nos sinais inflamatórios no 7º dia. Esses resultados indicam que α-mangostina, além de interagir suprimindo o vírus, também pode contribuir para a modulação do sistema imunológico do organismo infectado.91 Os autores ainda avaliaram os possíveis alvos de interação da α-mangostina com o vírus, através do uso de experimentos de docking molecular, o estudo indicou que a α-mangostina é capaz de se ancorar a proteínas do envelope viral. Foi detectada uma ligação potencial entre os domínios E1 II e E2 A, que se conecta às fitas ß-E2. O ligante, α-mangostina, liga-se no sítio intersticial aos domínios com afinidade de ligação da ordem de -8,6 kcal/mol, promovendo a estabilização de interações moleculares não-covalentes do complexo, ligando-se por meio de fortes interações de ligações de hidrogênio, interações p-alquil e alquil, além da interação do grupo prenila da α-mangostina. Essas interações, realizadas dentro de cada domínio, podem ser responsáveis pela atividade observada. A infecção da célula hospedeira está associada, principalmente, à fusão da membrana endossômica, dependente do pH, entre o vírus e a célula.92 Assim, a análise do potencial de interação local nesses domínios, verificado para a α-mangostina, é extremamente significante para estudos posteriores.88 Atividade contra o vírus da dengue A infecção pelo vírus da dengue é um grave problema de saúde pública. Estima-se uma incidência 100 milhões de infecções anualmente, sendo 500.000 casos graves de dengue, houve aumento no número de casos de mais de oito vezes nas últimas duas décadas, de 505.430 casos em 2000 para 5.2 milhões em 2019.93 O vírus da dengue é um membro da família Flaviviridae, com quatro sorotipos (DENV-1, DENV-2, DENV-3 e DENV-4) circulantes, transmitidos através da picada de mosquito vetor, as fêmeas de Aedes aegypti e Aedes albopictus. A infecção com qualquer um dos quatro sorotipos do vírus pode causar doenças que vão desde a febre da dengue leve até a forma mais grave, que é a febre hemorrágica da dengue, e a síndrome do choque da dengue.94 Não há vacinas ou medicamentos disponíveis para a prevenção ou tratamento da infecção. Há uma vacina licenciada (Dengvaxia®), porém, a imunopatologia única e a complexidade da infecção prejudicaram sua eficácia.95 Portanto, a busca por alternativas terapêuticas eficazes é atualmente alvo de grande interesse entre os pesquisadores envolvidos na área.96 A identificação de um fármaco que atue duplamente, agindo sobre os alvos iniciais do vírus da dengue, e module a resposta imune à infecção, é uma estratégia promissora para inibir a replicação viral, bem como para moderar a patogênese da doença. Foi demonstrado que a α-mangostina suprime a replicação do vírus da hepatite C, um vírus que pertencente à mesma família do vírus da dengue, Flaviviridae.74 Em 2021, Yongpitakwattana e colaboradores97 investigaram os efeitos de α-mangostina na infecção por dengue e na produção de citocinas/quimiocinas pró-inflamatórias. Durante a infecção, o principal alvo do sistema imunológico são as células dendríticas, ocorrendo nesse processo a produção e elevação dos níveis de citocinas e quimiocinas. Citocinas pró-inflamatórias, TNF-α e IFN-α, aumentam a ativação de células dendríticas e outras células do sistema imunológico, para com isso regular, de forma positiva, os genes estimulados por interferon, que possui atividade antiviral e induzem apoptose de células endoteliais.98 Então, eles observaram os efeitos antiviral e anti-inflamatório desenvolvido pela α-mangostina em células dendríticas, derivadas de monócitos primários, obtidos a partir de monócitos humanos. Após a infecção das células dendríticas primárias com o vírus (DENV2), os pesquisadores observaram, em experimentos de imunofluorescência, que nos tratamentos em concentrações de 20 e 25 μmol L-1 de α-mangostina houve redução significativa da carga viral, comparada ao controle.97 Para investigação do efeito sobre o ciclo replicativo do vírus, os autores realizaram um estudo cinético, no qual células dendríticas foram inoculadas com o vírus por 4 h. Seguindo-se o tratamento com a α-mangostina, o experimento foi, então, monitorado em 0, 3 e 6 h. Após 6 h, foi observada a redução na produção do vírus (DENV2). Esse resultado sugere que a inibição do vírus se dá na etapa de tradução de proteínas, ou na etapa de síntese de RNA. Para melhor compreensão, um estudo de RT-PCR foi realizado para quantificar o RNA viral e, com isso, descobriu-se que α-mangostina reduziu bastante o nível de RNA viral. Esse dado foi coerente com o estudo da ação da α-mangostina sobre o vírus da hepatite C, vírus de RNA de fita positiva como o DENV2, em que a xantona natural suprimiu a replicação viral, mediante a supressão da atividade da RNA polimerase, com uma redução subsequente na expressão da proteína do vírus.74 Diante desses fatos, os autores levantaram a hipótese de que α-mangostina inibe a síntese RNA, ao se ligar à polimerase viral e, assim, inibe sua capacidade de replicação do DENV2. Porém, esse mecanismo proposto precisa ainda ser melhor investigado.97 Na investigação sobre o efeito da α-mangostina na expressão de citocinas/quimiocinas para confirmar seu papel anti-inflamatório na infecção, verificou-se que a xantona natural foi capaz de reduzir o nível de citocinas/quimiocinas, TNF-α, CCL4, CCL5, CXCL10, IL6, IL1β, IL10, além de reduzir a transcrição de IFN-α em células dendríticas infectadas com DENV2. Esses dados evidenciaram que a α-mangostina possui ação anti-inflamatória, além de antiviral. A superexpressão de citocinas/quimiocinas, durante o processo de infecção, foi associada à elevação do estresse oxidativo in vitro e in vivo.99,100 Sob ação de agentes antioxidantes, o estresse oxidativo causado pelo vírus da dengue é reduzido, contribuindo para a prevenção de lesões hepáticas, devidas ao acúmulo de ROS, e isso foi verificado pela inibição da produção de citocinas pró-inflamatórias e apoptose.101 Descobriu-se ainda que, apesar do tratamento com α-mangostina na concentração de 25 μmol L-1 inibir de forma eficiente todos os sorotipos de DENV, o grau de inibição era distinto para cada um. Os quatro sorotipos DENV compartilham entre si 67 a 75% de identidade entre suas sequências de nucleotídeos. Com isso, variações na virulência e amplitude da infecção, que ocorre de forma distinta para cada cepa viral, podem contribuir para eficácia da α-mangostina.97 O potencial da α-mangostina e derivados contra o SARS-CoV-2 A emergência viral global atual causada pelo novo coronavírus (SARS-CoV-2), patógeno que atinge o sistema respiratório primário em humanos, surgiu em meados de dezembro de 2019 na cidade de Wuhan, China continental, sendo este o causador da doença denominada COVID-19. O SARS-CoV-2 se propagou mundialmente, atingindo todos os países, com mais de 430 milhões de casos confirmados de COVID-19, e 5,9 milhões de mortes associadas à doença em março de 2022.102 A transmissão do SARS-CoV-2 ocorre de pessoa à pessoa, através de gotículas das vias respiratórias, contato próximo com indivíduos infectados, por via oral e contato com o aerossol de pessoas portadoras do vírus, sendo a transmissão aérea a principal rota de disseminação.103 Em virtude da rápida propagação e natureza da transmissão, a COVID-19 foi declarada pela OMS como emergência de saúde pública de interesse internacional.104 As proteases virais, que desempenham papel fundamental durante o processo de produção das proteínas necessárias à replicação viral, fazem basicamente o corte, ou priming, na etapa final da síntese proteica. Dessa forma, essas proteases se apresentam como um alvo de estudos bastante promissor, uma vez que compostos ativos sobre estas enzimas seriam mais seletivos, pois possuiriam ação direta sobre o vírus.105 Jin e colaboradores, em 2020, conseguiram obter a estrutura cristalina da principal protease do vírus SARS-CoV-2, a Mpro, que foi depositada no Protein Data Bank (PDB ID: 6LU7). Essa é a única estrutura 3D de domínio público do vírus, estando organizada em forma de um dímero com duas subunidades idênticas, que juntas formam dois sítios ativos. Essa descoberta foi essencial, uma vez que essa protease se configura como um alvo altamente promissor na busca por moléculas com potencial clínico, que sejam capazes de inibir a clivagem de poliproteínas virais, impedindo a replicação do vírus, bloqueando assim a disseminação da infecção.106 A xantona natural α-mangostina foi descrita quanto à sua atividade contra protease do vírus HIV, que possui um nível de similaridade genômica bastante elevado em comparação com a Mpro do SARS-CoV-2.107 Assim, há a possibilidade de que α-mangostina possa ter atividade contra o vírus causador da COVID-19. Xantonas são substâncias polifenólicas e as características estruturais de compostos desta classe estão diretamente relacionadas à sua afinidade de ligação em termos de energia livre (ΔG) com as proteínas alvo, devido à presença de múltiplos grupos hidroxila. Atualmente, os estudos computacionais desempenham um papel fundamental na buscar por novas moléculas bioativas, representando uma importante ferramenta na área de química medicinal, sendo essencial para busca e desenvolvimento de múltiplos fármacos em potencial.108 Recentemente, Hidayat e colaboradores, em 2021,109 realizaram o estudo in sílico de α-mangostina, assim como de alguns de seus derivados, objetivando uma maior compreensão das suas atividades frente ao SARS-CoV-2. As modificações se concentram nas hidroxilas fenólicas e substituintes do anel aromático, átomos de carbono C1 e C6, para com isso, aumentar a afinidade para o sítio catalítico da protease Mpro.109 Parâmetros de teóricos de absorção, HIA e Caco-2, foram calculados utilizando o programa Pre-ADMET 2.0. O valor de Human Intestinal Absorption (HIA), que reflete o grau de absorção da substância no intestino humano varia de 0% -20% (baixo), 20% -70% (moderado) e 70% -100% (alto).110 Foram calculados para a α-mangostina e seus derivados valores de HIA na faixa de 90% a 99%, indicando um nível de absorção adequado pelo intestino. Já o modelo de predição de permeabilização de células Caco-2 in vitro é bastante empregado para estimativas da absorção de substâncias por via oral. Nesse modelo, os compostos são categorizados em três grupos de absorção <4 (baixa), 4-70 (moderada), > 70 (alta).111 Os valores de absorção da α-mangostina e seus derivados, estimadas para o modelo de células Caco-2, mostrou que a capacidade de penetrar a membrana celular está na categoria moderada (10,41 - 52,63). Os resultados de docking molecular à proteína Mpro de SARS-CoV-2 (PDB: 6LU7) da α-mangostina e seu derivado 3-(ciclopentiloxi)-6,8-diidroxy-2-metoxi-1,7-bis(3-metilbut-2-en-1-il)-9H-xanten-9-one (FKS9) foram comparados com o nelfinavir, um potencial inibidor de protease do coronavírus.112 Nesse trabalho, os quatro parâmetros ΔG, constante de inibição, ligação de hidrogênio e interações de Van der Waals, que determinam a afinidade das substâncias pelo sítio de interação na proteína, foram estudados. Valores de ΔG mais negativos, evidenciam que há maior estabilidade nas interações, aumentando a afinidade do conjugado ligante-proteína, consequentemente melhorando a atividade.113 O derivado FKS9 apresentou valor de ΔG de (−10,15 kcal/mol), inferior ao do nelfinavir (−9,74 kcal/mol) e da α-mangostina (−8,58 kcal/mol). Esse dado indica que as interações do derivado FKS9 com a Mpro são mais expressivas, em comparação com a α-mangostina e com o fármaco de referência, nelfinavir. Foi ainda avaliada a constante de inibição (Ki). Um menor valor de Ki indica uma menor quantidade, necessária para uma substância exercer a sua ação. O derivado FKS9 apresentou valor Ki de 36,45 µmol L-1, que foi bem menor do que o do nelfinavir (72,09 μmol L-1) e α-mangostina (511,49 μmol L-1).109 O estudo de docking molecular foi importante para investigar o potencial de interação do ligante da substância com o sítio ativo da proteína alvo. No caso da Mpro, as interações mais relevantes ocorrem com os resíduos Cys145 e His41, presentes no domínio de ligação desta proteína. Considerando a possibilidade destas substâncias poderem interagir com esses resíduos, bloqueando assim a atividade catalítica dessa protease, a replicação viral seria interrompida. O derivado FKS9 apresentou, no modelo estudado, uma interação com a cavidade catalítica da Mpro, se associando à His41 por meio de ligação de hidrogênio, o que evidencia seu potencial na inibição da replicação de SARS-CoV-2. Além disso, ao se considerar as regras de Lipinski, que estão associadas aos parâmetros de solubilidade e permeabilidade das substâncias no trato digestivo,114 as substâncias que detém valores de logP que não estão de acordo com as regras (logP < 5), provavelmente não apresentam o perfil de absorção e biodistribuição desejados in vivo. Assim, o derivado FKS9, apresentou valor calculado de logP = 6,04, mais adequado, quando comparado com a α-mangostina, que possui o valor calculado de logP = 3,71. Os dados obtidos demonstram que FKS9 pode ser investigado in vitro e, ainda, prevê-se que o mesmo possa ser administrado por via oral, tendo uma previsão de perfil de biodisponibilidade oral mais adequado. Nesse cenário, a α-mangostina, por ser uma molécula com alta versatilidade, acessível, e por apresentar diversas atividades descritas, inclusive antiviral, apresenta-se como uma molécula com grande potencial para a busca e desenvolvimento de novas substâncias ativas contra o coronavírus.109 Atividade antiparasitária Segundo a OMS existem hoje 20 tipos de doenças classificadas como Doenças Tropicais Negligenciadas (do inglês: Neglected Tropical Diseases - NTDs), das quais 12 são parasitoses. Estima-se que pelo menos 10% da população global esteja infectada com uma ou mais doenças negligenciadas, sendo a população dos países em desenvolvimento, que vivem abaixo da linha da pobreza, os mais afetados.115 Geralmente, essas doenças se configuram como crônicas e debilitantes, pois em razão de seus impactos sobre a produtividade, podem promover ainda mais o aumento da pobreza, prejudicar o desenvolvimento infantil, desqualificar socialmente seu portador e afetar a saúde das mulheres. Para o desenvolvimento e continuidade do progresso no combate às NTDs, há a necessidade de novas ferramentas, novos recursos e novas abordagens. Os produtos oriundos de fontes naturais detêm um alto potencial para aplicação como agentes antiparasitários, existindo diversos relatos na literatura sobre suas atividades em diferentes modelos de estudos, desde atividades antiprotozoários a anti-helmínticos, por exemplo.116 Como a disponibilidade de fármacos antiparasitários, é relativamente baixa117 e, com as evidências do aumento da resistência aos fármacos disponíveis para tratamento,118 a atividade em potencial de PNs, para esse tipo de aplicabilidade se torna cada vez mais interessante. Além disso, por existirem características comuns entre o câncer e parasitos, certos fármacos anticâncer possuem propriedades antiparasitárias e alguns antiparasitários apresentam atividade anticâncer. Esta ação mútua também deve ser considerada, por exemplo em abordagens de reposicionamento de fármacos.119 Atividade contra Plasmodium sp., agente etiológico da malária A malária é uma parasitose causada por protozoários do gênero Plasmodium, especialmente o P. falciparum. Esse parasita é responsável por mais de 80% dos casos de malária em todo o mundo, e causa a forma mais grave da doença, podendo ser fatal. O P. falciparum atinge, principalmente, populações mais pobres, que vivem em áreas rurais onde, na maioria das vezes não há o diagnóstico e tratamento adequado.120 O emprego de medicamentos comuns para tratamento da malária como aminoquinolinas, antifolatos, derivados de artemisinina e a hidroxinaftoquinona atovaquona, ocorre de modo que não se garante alta eficiência, isso devido ao alto custo e ao surgimento de resistência.121 Upegui et al., em 2015,122 avaliaram a ação antiparasitária de α-mangostina e δ-mangostina frente ao P. falciparum da cepa 3D7, sensível à cloroquina, e da cepa FCR3, resistente. Os resultados obtidos, demonstraram que a α-mangostina foi ativa contra as formas resistentes do parasita, P. falciparum FCR3, apresentando valor de CE50 = 0,2 μmol L-1, o que não se observou para a δ-mangostina que apresentou CE50 ≥ 121,2 μmol L-1. Para a cepa P. falciparum 3D7 sensível, α-mangostina e δ-mangostina também foram ativas, com valores de CE50 = 36,1 e 12,4 μmol L-1, respectivamente. Esses dados apontaram para uma ação diferenciada e seletiva, de modo que a atividade antiparasitária foi maior que a ação citotóxica. Dessa forma, o índice de seletividade relatado para a α-mangostina foi de 3,6, para cepa sensível, e 653,0, para a cepa resistente. A δ-mangostina apresentou valores de índice de seletividade de 21,1 para cepa sensível, e valor abaixo de 2,2 para cepa resistente.122 Para estudo da eficiência terapêutica, investigou-se o nível de supressão da parasitemia in vivo, adotando-se um modelo murino de infecção com P. berghei. A α-mangostina e δ-mangostina, foram administradas por via oral, em camundongos infectados, a uma dosagem de 100 mg kg-1 dia-1, durante 7 dias, havendo supressão da parasitemia da cepa P. berghei de 26,9% e 35,0%, respectivamente. Quando a administração de α-mangostina e δ-mangostina foi feita por via intraperitoneal, à dose diária de 50 mg kg-1 dia-1, por 7 dias, a parasitemia foi reduzida, respectivamente, em 45,8% e 54,3%. Quando os animais foram tratados duas vezes ao dia, com doses de 100 mg kg-1 dia-1 de α-mangostina ou δ-mangostina, por 7 dias, a diminuição foi de 80,7% e 79,9%, respectivamente. O alto nível de perfil de atividade averiguado para ambas as xantonas indicou que essas substâncias devem ser levadas em consideração como moléculas promissoras para o tratamento da malária.122 Atividade contra o Trypanosoma cruzi, agente etiológico da doença de Chagas A doença de Chagas (DC), ou tripanossomíase americana, é uma doença crônica, causada pelo protozoário Trypanosoma cruzi (Trypanosomatidae), que até o momento não conta com tratamento quimioterápico completamente eficaz. O protozoário apresenta um ciclo de vida bastante complexo, sendo capaz de infectar hospedeiros vertebrados e invertebrados.123 O parasito se encontra sob duas formas nos hospedeiros vertebrados, a forma tripomastigota, flagelada e infectante; e a forma amastigota, que não possui flagelo livre e se replica no interior das células.124 Os vetores de transmissão ao homem e a outros animais vertebrados são os insetos hematófagos triatomíneos, popularmente chamados de barbeiros. São conhecidas, no entanto, outras formas de transmissão que incluem a transfusional, que é a segunda via mais importante de propagação da doença em centros urbanos, a trans-placentária (congênita) e a transmissão pela via oral, que se dá pela ingestão de alimentos contaminados com formas viáveis do T. cruzi.125,126 Apesar de atingir principalmente populações de baixa renda em regiões rurais por toda a América Latina,127 os fluxos migratórios juntamente com as mudanças climáticas ocorridos nas últimas décadas, explicam relatos da ocorrência da DC nos Estados Unidos, Canadá e em vários países da Europa.128 A DC evolui no paciente, na maioria das vezes, de forma silenciosa, sendo que os sintomas mais debilitantes podem vir a se manifestar na fase crônica da doença, anos ou décadas após a infecção com o T. cruzi, caracterizada principalmente por um grave comprometimento das funções cardíacas.129 A disponibilidade de fármacos aplicáveis ao tratamento da DC é extremamente restrita, havendo somente os nitro-heterocíclos benznidazol e nifurtimox.130 Cabe ressaltar que estes fármacos já estão há quase meio século em uso, sem que alternativas tenham sido disponibilizadas. Na verdade, desde a descoberta de todo o ciclo evolutivo do parasita, descrito em 1909 por Carlos Chagas (Chagas, 1909), nenhum fármaco eficaz foi disponibilizado no mercado para a fase crônica da doença até o momento. A partir de 1980, o nifurtimox teve a sua comercialização interrompida no Brasil em razão de seus efeitos tóxicos,126 de modo que, atualmente, somente o benznidazol é destinado ao tratamento dessa doença no Brasil, mesmo não sendo eficiente em alguns estágios clínicos e apresentando sérios efeitos colaterais.131 Estima-se que 6 a 7 milhões de pessoas estejam infectadas em todo mundo, com cerca de 75 milhões de pessoas em risco de infecção.132 No Brasil, existem hoje aproximadamente dois milhões de pacientes crônicos, portadores da doença de Chagas. Destes, seiscentos mil desenvolvem complicações cardíacas ou digestivas que matam cerca de cinco mil pessoas a cada ano.133 Diferentes alvos moleculares já foram investigados, visando o desenvolvimento de novas alternativas terapêuticas para a DC.134 Neste sentido, a diversidade estrutural das moléculas de origem natural coloca-se como uma característica atraente e promissora na busca por novos anti-chagásicos. A ação tripanocida da α-mangostina foi avaliada em trabalho realizado, em 2013, por Al-Massarini e colaboradores. Os autores estudaram a atividade antitripanossômica in vitro de frações de diclorometano (DCM) e acetato de etila (EtOAc) obtidas do extrato etanólico do pericarpo seco do mangostão, bem como da α-mangostina isolada. Apesar da baixa seletividade in vitro, tanto as frações quanto o produto natural isolado foram ativos contra o T. cruzi (cepa Tulahuen CL2): DCM, CE50 = 7,6 μg mL-1; EtOAc, CE50 = 34,6 μg mL-1; α-mangostina, CE50 = 8,9 μmol L-1.135 A atividade tóxica da α-mangostina frente ao T. cruzi, pode ser complementada por sua atividade antioxidante, visto que a xantona natural pode agir mitigando os danos causados pelo estresse oxidativo, e pelo consequente processo inflamatório no qual ocorre destruição tecidual. Esses fenômenos são característicos da fase crônica da infecção, ocorrendo principalmente no miocárdio dos pacientes chagásicos.136 A literatura descreve a atividade protetora da α-mangostina sobre os danos causados ao miocárdio exposto a condições de estresse oxidativo, devido à sua ação antioxidante.137 Adicionalmente, a suplementação de antioxidantes tem sido sugerida como uma terapia adjuvante ao tratamento quimioterápico da DC, visto que compostos antioxidantes, como é o caso da α-mangostina, combatem as espécies reativas de oxigênio nocivas, diminuindo o dano oxidativo tecidual durante a progressão da DC em sua fase crônica.138 Apesar de não dispormos de dados específicos sobre a avaliação da α-mangostina como adjuvante, no modelo de infecção crônica, encontramos relatos de outros antioxidantes que têm demonstrado potenciais benefícios no controle do estresse oxidativo nos tecidos do hospedeiro. Resultados de estudos com melatonina, resveratrol, com a combinação das vitaminas C e E, além da associação de curcumina/benznidazol, e de outros antioxidantes direcionados às mitocôndrias, sugerem haver benefícios na redução dos níveis plasmáticos e cardíacos de produtos de peroxidação lipídica.139,140 Atividade antibacteriana A resistência bacteriana emergiu e espalhou-se rapidamente em escala global nos últimos anos. Não há dúvidas de que o uso excessivo de antibióticos durante os últimos 80 anos está associado ao aumento expressivo de resistência. Redes de monitoramento epidemiológico na Europa e na Ásia (EARS-Net), a Vigilância da Resistência aos Antimicrobianos da Ásia Central e do Leste Europeu (CAESAR) relataram que as bactérias resistentes se tornaram muito mais prevalentes durante a última década.141,142 Entre os patógenos que desenvolvem resistência a antibióticos, destacam-se a Pseudomonas aeruginosa e o Staphylococcus aureus, que estão amplamente disseminados em ambientes hospitalares.143 A formação de biofilme bacteriano aumenta a capacidade de resistência e dificulta o controle da infecção pelo uso de antibióticos. Observa-se, com frequência, que nas infecções relacionadas aos dispositivos e ao ambiente cirúrgico, a formação de biofilme em implantes e tecidos reduzem ainda mais o sucesso do tratamento.144,145 A terapia disponível causa somente a morte das células planctônicas, enquanto as células bacterianas crescem no interior dos biofilmes continuamente, mesmo após o término do tratamento, perpetuando a infecção.146 Encapsulamento de α-mangostina em nanopartículas para ação em biofilmes A classe das xantonas, principalmente aquelas isoladas de plantas superiores, constituem um repositório ainda muito pouco explorado, mas com enorme potencial para a descoberta de novos antibióticos de origem natural.147 Em 2021, Nguyen et al.148 investigaram a atividade de nanopartículas contendo α-mangostina sobre biofilmes de Staphylococcus aureus, incluindo a cepa resistente à meticilina, MRSA252. Os biofilmes bacterianos estão intimamente envolvidos no desenvolvimento de resistências, uma vez que formam uma barreira ao acesso de fármacos, de modo a acúmulo de antibióticos ocorre em concentrações sub-terapêuticas.149 Foi relatado a atividade antibiofilme da α-mangostina frente a S. mutans, através da ruptura do biofilme em concentrações de 150 μM.150 A aplicação direta da α-mangostina sobre biofilmes bacterianos é limitada, e isto se deve à sua solubilidade reduzida. Buscando solucionar esta limitação, os autores sintetizaram uma nanopartícula polimérica de polietilenoglicol (PEG) contendo α-mangostina, e sua atividade antibiofilme foi testada contra de S. aureus (cepa de referência NCTC6571 e a cepa multirresistente MRSA252). A escolha destas cepas ocorreu por apresentarem biofilmes com estruturas distintas, polissacarídicos e proteicos, respectivamente.148 Há relatos na literatura de que a associação de nanopartículas com diversos compostos, inclusive de fontes naturais, possibilita a melhora de parâmetros como solubilidade, estabilidade e biodisponibilidade, refletindo em uma maior eficácia,151 inclusive para a α-mangostina.152 As nanopartículas de PEG contendo α-mangostina apresentaram perfil de atividade melhorada tanto para a formação quanto para a erradicação do biofilme, particularmente no estágio inicial de formação. O tratamento com 24 μmol L-1 de nanopartícula de α-mangostina inibiu a formação de biofilme em 53-62%, em comparação com sua forma livre, que apresentou 40-44% de inibição. Na concentração de 48 μmol L-1, as nanopartículas de α-mangostina levaram à supressão no desenvolvimento dos biofilmes, para as duas cepas testadas, resultando na morte bacteriana, indicando que a disponibilidade de α-mangostina foi otimizada com o emprego da formulação nanoparticulada. Já em biofilmes pré-formados (24 h), as bactérias apresentaram nível mais elevado de resistência, tanto à nanopartícula de α-mangostina quanto à sua forma livre. Segundo os autores, a menor atividade seria causada pela difusão limitada da xantona natural no biofilme bacteriano.148 Sabe-se que há diferenças estruturais entre os biofilmes, dependendo da cepa bacteriana. A cepa MRSA252 produz substância extracelular polimérica (SEP), contendo principalmente proteína, enquanto na cepa NCTC6571 o EPS contém basicamente polissacarídeos. Tais diferenças refletem na sensibilidade dos respectivos biofilmes à α-mangostina. Com isso, os autores sugeriram a hipótese de que a matriz de biofilme proteico em MRSA252 fornece melhor proteção ao interagir com α-mangostina.148 Logo, eles analisaram a expressão dos principais genes relacionados ao crescimento do biofilme nas duas linhagens, após o tratamento com α-mangostina livre ou encapsulada em nanopartícula de PEG, tendo sido verificadas algumas diferenças interessantes. Para a cepa NCTC6571, a expressão de icaC foi suprimida em maior extensão, o que não se observou para MRSA252. Este gene é responsável pela codificação do transportador que está envolvido na produção de adesina do biofilme poli-beta-1,6-N-acetil-D-glucosamina (PNAG), sendo um dos principais constituintes da matriz polissacarídica de S. aureus NCTC6571,153 indicando que a composição da SEP é importante para a permeação do biofilme. Outro fator interessante foi que a expressão de fnbB foi claramente reduzida em NCTC6571, mas este gene teve sua expressão aumentada em MRSA252. Esse aumento está relacionado ao desenvolvimento de resistência, observada em subpopulações heterogêneas, altamente resistentes de MRSA, evidenciando que o gene fnbB está envolvido na resposta às condições de tratamento.148 Em contrapartida, a expressão do gene ebpS foi suprimida em MRSA252, mas intensificada em NCTC6571. O produto desse gene permite a ligação de S. aureus à elastina da célula hospedeira, contribuindo para a adesão, proliferação e invasão celular.154 Esses resultados indicam que a α-mangostina, quando associada a nanopartículas poliméricas, tem a eficácia da ação frente ao biofilme otimizada, particularmente nas etapas iniciais de formação do biofilme, inclusive contra a cepa MRSA252, multirresistente.148 Atividade anti-Mycobacterium tuberculosis O Mycobacterium tuberculosis, é o agente etiológico da tuberculose, doença infeciosa que afeta principalmente os pulmões, causando preocupações crescentes. A doença é uma das maiores causas de morte entre as doenças infecciosas, com um terço da população global infectada e 10,4 milhões de casos, com cerca de 1,74 milhões de mortes relatadas a cada ano.155 A terapia atual de regime prolongado envolve o uso, durante dois meses de tratamento de fase intensiva, com os antibióticos isoniazida, rifampicina, pirazinamida e etambutol; seguido por quatro meses de tratamento com isoniazida e rifampicina. Normalmente, necessita-se de um tempo maior para o tratamento da tuberculose multirresistente.156 Esse longo regime de tratamento, aliado ao uso de vários antibióticos de alto custo e de toxicidades consideráveis, são fatores que levam à interrupção precoce do tratamento, aumentando os riscos de surgimento de variantes de M. tuberculosis resistentes aos fármacos em uso.157 Em 2003, Suksamrarn et al. avaliaram o perfil de atividade antibacteriana das xantonas preniladas, isoladas do fruto mangostão, frente ao bacilo da tuberculose. Os resultados mostraram que o valor de concentração inibitória da α-mangostina foi de CIM de 6,25 µg mL-1, indicando o seu potente efeito inibitório contra M. tuberculosis.158 Posteriormente, Guzmán-Beltrán et al.159 avaliaram as atividades antibacterianas de ácido nordiidroguaiarético (NDGA) e α-mangostina no crescimento de M. tuberculosis H37Ra in vitro e em células THP-1, infectadas com H37Ra, e em macrófagos derivados de monócitos humanos. O NDGA inibiu o crescimento bacteriano de forma concentração-dependente. Os valores de CIM obtidos foram 250 µg mL-1 para NDGA e 62,5 µg mL-1 para α-mangostina, tendo como referência a rifampicina (0,4 μg mL-1). Além disso, o tratamento pós-infecção com NDGA ou α-mangostina foi capaz de diminuir a carga micobacteriana em células THP-1, em comparação com células não tratadas, após 3 e 5 dias de incubação, com redução significativa, de 75% e 50%, respectivamente.159 No processo de autofagocitose, as proteínas LC3 migram para as vesículas autofágicas. Com o aumento da concentração dessas proteínas no interior das vesículas, ocorre o aumento da fluorescência, indicando autofagia.160 Dessa forma, foi observado que, com a concentração de 7 μg mL-1 de NDGA, ocorreu aumento no percentual de células que expressaram LC3, em 80%. Por sua vez, a α-mangostina, a 6 μg mL-1, induziu autofagia em células THP-1, nas mesmas condições, e cerca de 84% das células apresentaram formação de autofagossomo, onde houve aumento visível no número e tamanho das vesículas autofágicas intracelulares. Os efeitos pós-tratamento na autofagia em macrófagos infectados com M. tuberculosis demonstrou que nessas células também houve aumento considerável no número de vesículas e na detecção de bactérias dentro das vesículas, sendo observadas 70% e 78% das células com vesículas, no ensaio com NDGA e α-mangostina, respectivamente.159 Devido às observações de que a α-mangostina exerce efeitos inibitórios sobre enzimas envolvidas na glicólise em Streptococcus mutans, como aldolase, gliceraldeído-3-fosfato desidrogenase e lactato desidrogenase,161 os autores sugerem que a α-mangostina pode promover a diluição de substâncias lipofílicas, como os constituintes da parede, bloqueando simultaneamente uma série de enzimas em M. tuberculosis,159 levando assim ao bloqueio do crescimento e da proliferação bacteriana.158 Atividade antifúngica O sistema respiratório humano está constantemente exposto a esporos de fungos, muitos estudos revelaram a presença de fungos viáveis, em altas taxas, em culturas de muco nasal e escarro brônquico, mesmo em pessoas saudáveis.162 Essa presença é comumente considerada como um processo normal de colonização, no entanto, pode se revelar como gatilho extrínseco para o surgimento de doenças alérgicas das vias aéreas superiores e inferiores. A exposição é inevitável, no entanto, ainda é desconhecido como os fungos transpõe o limite da colonização normal para os gatilhos de reações inflamatórias, levando ao surgimento de alergias, aspergilose broncopulmonar e rinossinusites.163 Atividade contra Candida albicans O fungo Candida albicans coexiste em harmonia com outros membros da microbiota humana. Porém, variações neste ambiente pode resultar em alterações neste equilíbrio, como mudanças de pH, alterações nutricionais, o uso de antibióticos, ou alterações do sistema imunológico, causadas por infecções ou terapia imunossupressora. Essas alterações podem promover a proliferação e desenvolvimento de infecções por C. albicans.164 Tais infecções podem variar desde superficiais da mucosa e da derme, como aftas, assaduras até infecções vaginais por fungos. Estima-se que 75% das mulheres terão algum tipo de infecção por fungos, até infecções mais graves, disseminadas por hematogênese.165 O fungo C. albicans é um dos principais causadores de infecções hospitalares, sendo responsável por cerca de 15% de todos os casos de sepse, com taxas de mortalidade na faixa de 40%.166 Narasimhan et al., em 2017, avaliaram o potencial antifúngico de α-mangostina e seus derivados. Seus análogos, tribenzil-α-mangostina e trietilmorfolina-α-mangostina, demonstraram, atividade antifúngica de inibição máxima contra Candida albicans, na concentração de 100 µg mL-1. Entre os derivados testados, os derivados triacetil-α-mangostina e tribenzenosulfonil-α-mangostina, na concentração de 100 µg mL-1, exibiram inibição contra Aspergillus niger. O derivado tribenzenosulfonil-α-mangostina mostrou inibição mais significativa contra as cepas de fungos avaliadas, usando o fármaco cetoconazol como medicamento de referência, a 50 e 100 µg mL-1.167 Atividade contra Colletotrichum gloeosporioides O fitopatógeno Colletotrichum gloeosporioides, causa impactos negativos na produção global de diversas espécies de cultivares, como frutas, vegetais, cereais, flores e gramíneas. Defensivos agrícolas têm sido usado para combate e controle, mas apesar dos antifúngicos serem eficientes, seu uso em larga escala gera graves consequências, como o surgimento de fungos mais resistentes, poluição ambiental e contaminação alimentar.168 Recentemente, em 2020, Ye et al.169 avaliaram a atividade da α-mangostina frente a vinte espécies de fungos fitopatogênicos. Em seus resultados, a α-mangostina a 100 µg mL-1 foi capaz de inibir o crescimento micelial in vitro dos fungos de formas distintas. A α-mangostina, exibiu a maior inibição contra C. gloeosporioides (90,38%) e Botryodiplodia theobromae (91,23%), e menor atividade foi contra Fusarium oxysporum (16,67%). Esse trabalho está entre os poucos que relata a ação antifúngica de α-mangostina contra fungos filamentosos, particularmente devido a atividade inibitória ocorrer sobre a germinação de esporos. Dentre os fitopatógenos testados, C. gloeosporioides mostrou-se altamente sensível, sendo observado que a germinação de esporos era bem mais sensível do que o crescimento micelial, em concentrações relativamente baixas de α-mangostina (10 µg mL-1). A ação diferenciada sobre a germinação de esporos e o crescimento de micélio pode tornar possível a compreensão preliminar sobre o seu provável mecanismo de ação.169 Inibidores de microtúbulos e inibidores da biossíntese de ergosterol, atuam como fungicidas na etapa inicial do desenvolvimento do fungo, principalmente durante o crescimento micelial, que é mais sensível. Porém, os inibidores mitocondriais são mais ativos na etapa de germinação de esporos.170 Similarmente aos inibidores mitocondriais, a α-mangostina exibiu maior atividade de inibição sobre esporos do que no crescimento micelial. A xantona natural provocou a desordem do plasma intracelular, mas não afetou a estrutura das hifas, diferindo dos efeitos dos inibidores que atuam nos processos de divisão nuclear e de biossíntese do ergosterol. Foram observadas alterações importantes sobre a mitocôndria, como o seu inchaço e números diminuídos da organela. Esses resultados indicam que α-mangostina exerce sua atividade inibitória direcionada às mitocôndrias fúngicas, destruindo o metabolismo energético.169
CONCLUSÕES Os estudos das propriedades farmacológicas e aplicações terapêuticas potenciais da xantona natural α-mangostina tem merecido uma atenção crescente e um esforço contínuo por parte dos químicos medicinais de produtos naturais nos últimos anos. Apesar de parecerem quimicamente simples, as xantonas podem exibir um perfil de atividade/reatividade muito rico. A α-mangostina pode ser considerada como uma estrutura privilegiada, visto sua capacidade de interação com múltiplos alvos biológicos, o que está relacionada às suas características moleculares, como a presença de um sistema de anel tricíclico heteroaromático, predominantemente planar e rígido; à presença de um grupo carbonila no anel central, capaz de realizar várias interações; um grupo éter biarílico, que contribui para as características eletrônicas do sistema; além dos substituintes presentes no núcleo xantônico, o qual acomoda três hidroxilas fenólicas, um éter aril-metílico e dois grupos prenila. Associada a essa capacidade de interação com diferentes tipos de receptores, a α-mangostina é um poderoso antioxidante, agindo através de mecanismos complementares (p.ex., transferência de átomos de hidrogênio e formação de adutos radicalares estáveis) na inativação das diferentes espécies reativas de oxigênio, como •OH e •OOH. Contudo, a aplicação clínica da xantona natural ainda é confrontada com as limitações farmacocinéticas da mesma. No entanto, essas restrições têm sido superadas através de uma quantidade extraordinária de trabalhos que estão voltados para a elaboração de sistemas de entrega controlados, além do planejamento adequado de modificações em sua estrutura, objetivando melhorar sua biodisponibilidade, seu perfil de atividade biológica e, principalmente, a segurança de sua administração em humanos. Os estudos citados nesta revisão demonstram claramente que a α-mangostina possui qualidades promissoras, que podem, rapidamente, subsidiar e estimular o desenvolvimento de estudos pré-clínicos, e mesmo clínicos. Além disso, o entendimento crescente das interações dessa substância sobre os mais diversos alvos moleculares, bem como a compreensão dos mecanismos de ação através dos quais ela demonstra suas ações frente a uma grande variedade de tipos celulares, tanto em modelos in vitro quanto in vivo, consolidam ainda mais o seu potencial terapêutico.
REFERÊNCIAS 1. Atanasov, A. G.; Waltenberger, B.; Pferschy-Wenzig, E. M.; Linder, T.; Wawrosch, C.; Uhrin, P.; Temml, V.; Wang, L.; Schwaiger, S.; Heiss, E. H.; Rollinger, J. M.; Schuster, D.; Breuss, J. M.; Bochkov, V.; Mihovilovic, M. D.; Kopp, B.; Bauer, R.; Dirsch, V. M.; Stuppner, H.; Biotechnol. Adv. 2015, 33, 1582 [Crossref]; Atanasov, A. G.; Zotchev, S. B.; Dirsch, V. M.; Supuran C. T.; Nat. Rev. Drug Discovery 2021, 20, 200. [Crossref] 2. Kinghorn, A. D.; Pan, L.; Fletcher, J. N.; Chai, H.; J. Nat. Prod. 2011, 74, 1539. [Crossref] 3. Newman, D. J.; Cragg, G. M.; J. Nat. Prod. 2016, 79, 629. [Crossref] 4. Pedraza-Chaverri, J.; Cárdenas-Rodríguez, N.; Orozco-Ibarra, M.; Pérez-Rojas, J. M.; Food Chem. Toxicol. 2008, 46, 3227 [Crossref]; Obolskiy, D.; Pischel, I.; Siriwatanametanon, N.; Heinrich, M.; Phytother. Res. 2009, 23, 1047 [Crossref]; Ovalle-Magallanes, B.; Eugenio-Pérez, D.; Pedraza-Chaverri, J.; Food Chem. Toxicol. 2017, 109, 102 [Crossref] 5. David, B.; Wolfender, J.-L.; Dias, D. A.; Phytochem. Rev. 2015, 14, 299. [Crossref] 6. Lawson, A. D. G.; MacCoss, M.; Heer, J. P.; J. Med. Chem. 2018, 61, 4283. [Crossref] 7. Nicolaou, K. C.; Proc. R. Soc. London, Ser. A 2014, 470, 20130690. [Crossref] 8. Masters, K.-S.; Bräse, S.; Chem. Rev. (Washington, DC, U. S.) 2012, 112, 3717. [Crossref] 9. Vieira, L. M. M.; Kijjoa. A.; Curr. Med. Chem. 2005, 12, 2413. [Crossref] 10. Pinto, M. M. M.; Palmeira, A.; Fernandes, C.; Resende, D. I. S. P.; Sousa, E.; Cidade, H.; Tiritan, M. E.; Correia-da-Silva, M.; Cravo, S.; Molecules 2021, 26, 431. [Crossref] 11. DeSimone, W. R.; Currie, K. S.; Mitchell, S. A.; Darrow, J. W.; Pippin, D. A.; Comb. Chem. High Throughput Screening 2004, 7, 473. [Crossref] 12. Bennett, G. J.; Lee, H. H.; Phytochemistry (Elsevier) 1989, 28, 967. [Crossref] 13. Bhattacharya, S. K.; Ghosal, S.; Chaudhuri, R. K.; Sanyal, A. K.; J. Pharm. Sci. (Philadelphia, PA, U. S.) 1972, 61, 1838. [Crossref] 14. Pastre, R.; Marinho, A. M. R.; Rodrigues-Filho, E.; Souza, A. Q. L.; Pereira, J. O.; Quim. Nova 2007, 30, 1867. [Crossref] 15. Peres, V.; Nagem, T. J.; de Oliveira, F. F.; Phytochemistry (Elsevier) 2000, 55, 683. [Crossref] 16. Iseda, S.; Bull. Chem. Soc. Jpn. 1957, 30, 629. [Crossref] 17. Bhatia, V. K.; Ramanathan, J. D.; Seshadri, T. R.; Tetrahedron 1967, 23, 1363. [Crossref] 18. Andreu, G. L. P.; Maurmann, N.; Reolon, G. K.; de Farias, C. B.; Schwartsmann, G.; Delgado, R.; Roesler, R.; Eur. J. Pharmacol. 2010, 635, 124. [Crossref] 19. Balunas, M. J.; Su, B.; Brueggemeier, R. W.; Kinghorn, A. D.; J. Nat. Prod. 2008, 71, 1161. [Crossref] 20. Nkengfack, A. E.; Mkounga, P.; Meyer, M.; Fomum, Z. T.; Bodo, B.; Phytochemistry (Elsevier) 2002, 61, 181. [Crossref] 21. Pinheiro, L.; Nakamura, C. V.; Dias Filho, B. P.; Ferreira, A. G.; Young, M. C. M.; Cortez, A. G.; Mem. Inst. Oswaldo Cruz 2003, 98, 549. [Crossref] 22. Kumagai, K.; Hosotani, N.; Kikuchi, K.; Kimura, T.; Saji, I.; J. Antibiot. 2003, 56, 610. [Crossref] 23. Pasterkamp, R. J.; Giger, R. J.; Ruitenberg, M.-J.; Holtmaat, A. J. G. D.; De Wit, J.; De Winter, F.; Verhaagen, J.; Mol. Cell. Neurosci. 1999, 13, 143. [Crossref] 24. Ren, Y.; Lantvit, D. D.; de Blanco, E. J. C.; Kardono, L. B. S.; Riswan, S.; Chai, H.; Cottrell, C. E.; Farnsworth, N. R.; Swanson, S. M.; Ding, Y.; Li, X.-C.; Marais, J. P. J.; Ferreira, D.; Kinghorn, A. D.; Tetrahedron 2010, 66, 5311. [Crossref] 25. Huang, G.-M.; Sun, Y.; Ge, X.; Wan, X.; Li, C.-B.; World J. Gastroenterol. 2015, 21, 6194. [Crossref] 26. Li, C.; Qi, Q.; Lu, N.; Dai, Q.; Li, F.; Wang, X.; You, Q.; Guo, Q.; Biochem. Cell Biol. 2012, 90, 718. [Crossref]. 27. Ke, H.; Morrisey, J. M.; Qu, S.; Chantarasriwong, O.; Mather, M. W.; Theodorakis, E. A.; Vaidya, A. B.; Antimicrob. Agents Chemother. 2017, 61, e01220-16 [Crossref]; Fernandes, C.; Carraro, M. L.; Ribeiro, J.; Araújo, J.; Tiritan, M. E.; Pinto, M. M. M.; Molecules 2019, 24, 791 [Crossref]; Li, M.; Su, F.; Zhu, M.; Zhang, H.; Wei, Y.; Zhao, Y.; Li, J.; Lv, S.; Molecules 2022, 27, 2937. [Crossref]. 28. Nayik, G. A.; Gull, A. In Antioxidants in Fruits: Properties and Health Benefits; Nayik, G. A., Gull, A., eds.; Springer: Singapore, 2020. 29. De Freitas, S. T.; Pareek, S. In Postharvest Physiological Disorders in Fruits and Vegetables; De Freitas, S. T., Pareek, S., eds.; 1st ed., CRC Press: Boca Raton, 2019; Schmid, W.; Eur. J. Org. Chem. 1855, 93, 83. [Crossref] 30. https://www.needpix.com/photo/887745/, acessada em setembro 2022. 31. De Mello, R. F. A.; de Souza Pinheiro, W. B.; Benjamim, J. K. F.; de Siqueira, F. C.; Chisté, R. C.; Santos, A. S.; Arabian J. Chem. 2021, 14, 103252. [Crossref] 32. Leyva-López, N.; Lizárraga-Velázquez, C. E.; Hernández, C.; Sánchez-Gutiérrez, E. Y.; Foods 2020, 9, 843 [Crossref]; FAO; The State of Food and Agriculture 2019. Moving forward on food loss and waste reduction, FAO: Rome, 2019. 33. Yang, A.; Liu, C.; Wu, J.; Kou, X.; Shen, R.; Eur. J. Pharmacol. 2021, 897, 173950. [Crossref] 34. https://www.tridge.com/intelligences/mangosteen/production, acessada em setembro 2022. 35. Do Sacramento, C. K.; Coelho Jr., E.; de Carvalho, J. E. U.; Müller, C. H.; do Nascimento, W. M. O.; Rev. Bras. Frutic. 2007, 29, 195. [Crossref] 36. Jung, H.-A.; Su, B.-N.; Keller, W. J.; Mehta, R. G.; Kinghorn, A. D.; J. Agric. Food Chem. 2006, 54, 2077. [Crossref] 37. Aizat, W. M.; Ahmad-Hashim, F. H.; Syed Jaafar, S. N.; J. Adv. Res. 2019, 20, 61. [Crossref] 38. Udani, J. K.; Singh, B. B.; Barrett, M. L.; Singh, V. J.; Nutr. J. 2009, 8. [Crossref] 39. WHO; General Guidelines for Methodologies on Research and Evaluation of Traditional Medicine World Health Organization, WHO: Geneva, 2000. 40. Mohamed, G. A.; Ibrahim, S. R. M.; Shaaban, M. I.; Ross, S. A.; J. Fitoterapia 2014, 98, 215. [Crossref] 41. https://clarivate.com/products/web-of-science/databases, acessada em setembro 2022. Palavras-chave utilizadas: alpha-mangostin or α-mangostin. Filtros utilizados no levantamento (Research Area): Pharmacology Pharmacy or Biochemistry Molecular Biology or Cell Biology. 42. Ibrahim, M. Y.; Hashim, N. M.; Mariod, A. A.; Mohan, S.; Abdulla, M. A.; Abdelwahab, S. I.; Arbab, I. A.; Arabian J. Chem. 2016, 9, 317. [Crossref] 43. Santos, C. M. M.; Freitas, M.; Fernandes, E.; Eur. J. Med. Chem. 2018, 157, 1460 [Crossref]; Nie, W.; Zan, X.; Yu, T.; Ran, M.; Hong, Z. He, Y.; Yang, T.; Ju, Y.; Gao, X.; Cell Death Dis. 2020, 11. [Crossref] 44. Aizat, W. M.; Jamil, I. N.; Ahmad-Hashim, F. H.; Noor, N. M.; PeerJ 2019, 7, e6324. [Crossref] 45. Fujita, M.; Inoue, T.; Chem. Pharm. Bull. 1980, 28, 2476. [Crossref] 46. Atkinson, J. E.; Gupta, P.; Lewis, J. R.; Chem. Commun. (London) 1968, 22, 1386. [Crossref] 47. Gupta, P.; Lewis, J. R.; J. Chem. Soc. C 1971, 629. [Crossref] 48. Peres, V.; Nagem, T. J.; Phytochemistry (Elsevier) 1997, 44, 191. [Crossref] 49. Beerhues L.; FEBS Lett. 1996, 383, 264. [Crossref] 50. Beerhues, L. In Biosynthesis of the active Hypericum perforatum constituents In Medicinal and Aromatic Plant Science and Biotechnology; Odabas, M. S., Çirak C., eds.; Global Science Books: Islework, 2011. 51. Klundt, T.; Bocola, M.; Lütge, M.; Beuerle, T.; Liu, B.; Beerhues, L.; J. Biol. Chem. 2009, 284, 30957. [Crossref] 52. Liu, B.; Falkenstein-Paul, H.; Schmidt, W.; Beerhues, L.; Plant J. 2003, 34, 847. [Crossref] 53. Austin, M. B.; Noel, J. P.; Nat. Prod. Rep. 2002, 20, 79. [Crossref] 54. Peters, S.; Schmidt, W.; Beerhues, L.; Planta 1997, 204, 64. [Crossref] 55. Parijadi, A. A. R.; Putri, S. P.; Ridwani, S.; Dwivany, F. M.; Fukusaki, E.; J. Biosci. Bioeng. 2018, 125, 238. [Crossref] 56. Sage, E. E.; Jailani, N.; Taib, A. Z. M.; Noor, N. M.; Said, M. I. M.; Bakar, M. A.; Mackeen, M. M.; PLoS One 2018, 13, e0205753. [Crossref] 57. Iikubo, K.; Ishikawa, Y.; Ando, N.; Umezawa, K.; Nishiyama, S.; Tetrahedron Lett. 2002, 43, 291. [Crossref] 58. Xu, D.; Nie, Y.; Liang, X.; Ji, L.; Hu, S.; You, Q.; Wang, F.; Ye, H.; Wang, J.; Nat. Prod. Commun. 2013, 8, 1101. [Crossref] 59. Atrahimovich, D.; Avni, D.; Khatib, S.; Antioxidants 2021, 10, 423. [Crossref]; Radi, R.; Proc. Natl. Acad. Sci. U. S. A. 2018, 115, 5839. [Crossref] 60. Grivennikova, V.G.; Vinogradov, A.D.; Biochem. Biophys. Acta 2006, 1757(5-6), 553. [Crossref]. 61. Martínez, A.; Galano, A.; Vargas, R. J. Phys. Chem. B 2011, 115, 12591. [Crossref] 62. Chavan T, Muth A. Future Med. Chem. 2021, 13, 1679. [Crossref] 63. Nogrady, T.; Weaver, D. F.; Medicinal Chemistry: A Molecular and Biochemical Approach, 3rd ed., Oxford Press: New York, 2005. 64. https://www.who.int/news-room/fact-sheets/detail/the-top-10-causes-of-death, acessada em setembro 2022. 65. Bösl, K.; Ianevski, A.; Than, T. T.; Andersen, P. I.; Kuivanen, S.; Teppor, M.; Zusinaite, E.; Dumpis, U.; Vitkauskiene, A.; Cox, R. J.; Kallio-Kokko, H.; Bergqvist, A.; Tenson, T.; Merits, A.; Oksenych, V.; Bjørås, M.; Anthonsen, M. W.; Shum, D.; Kaarbø, M.; Vapalahti, O.; Windisch, M. P.; Superti-Furga, G.; Snijder, B.; Kainov, D.; Kandasamy, R. K.; Front. Immunol. 2019, 10, 2186. [Crossref] 66. Platto, S.; Wang, Y.; Zhou, J.; Carafoli, E.; Biochem. Biophys. Res. Commun. 2021, 538, 14. [Crossref] 67. https://talk.ictvonline.org/taxonomy/, acessada em setembro 2022. 68. https://www.unaids.org/en/resources/fact-sheet, acessada em setembro 2022. 69. Chua, K. B.; Bellini, W. J.; Rota, P. A.; Harcourt, B. H.; Tamin, A.; Lam, S. K.; Ksiazek, T. G.; Rollin, P. E.; Zaki, S. R.; Shieh, W.-J.; Goldsmith, C. S.; Gubler, D. J.; Roehrig, J. T.; Eaton, B.; Gould, A. R.; Olson, J.; Field, H.; Daniels, P.; Ling, A. E.; Peters, C. J.; Anderson, L. J.; Mahy, B. W. J.; Science (Washington, DC, U. S.) 2000, 288, 1432 [Crossref]; Patil, P.; Agrawal, M.; Almelkar, S.; Jeengar, M. K.; More, A.; Alagarasu, K.; Kumar, N. V.; Mainkar, P. S.; Parashar, D.; Cherian, S.; Virol. J. 2021, 18, 47 [Crossref]. 70. Endy, T. P. In Hunter's Tropical Medicine and Emerging Infectious Diseases; Ryan, E. T.; Hill, D. R.; Solomon, T.; Aronson, N. E.; Endy, T. P., eds.; Elsevier: Edinburgh, 2020, Part 2: Viral diseases, cap. 36. [Crossref]; Schwartz, D. A.; Front. Virol. 2021. [Crossref] 71. Parvez, M. K.; Parveen, S.; Intervirology 2017, 60, 1. [Crossref]; Patel, B.; Sharma, S.; Nair, N.; Majeed, J.; Goyal, R. K.; Dhobi, M.; Mol. Cell. Biochem. 2021, 476, 2345. [Crossref]. 72. Montenegro-Landívar, M. F.; Tapia-Quirós, P.; Vecino, X.; Reig, M.; Valderrama, C.; Granados, M.; Cortina, J. L.; Saurina, J.; Sci. Total Environ. 2021, 801, 149719. [Crossref]. 73. Alter, M. J.; Kruszon-Moran, D.; Nainan, O. V.; McQuillan, G. M.; Gao, F.; Moyer, L. A.; Kaslow, R. A.; Margolis, H. S.; N. Engl. J. Med. 1999, 341, 556 [Crossref]; Di Bisceglie, A. M.; Hepatology (Hoboken, NJ, U. S.) 2000, 31, 1014 [Crossref]. 74. https://www.who.int/news-room/fact-sheets/detail/hepatitis-c, acessada em setembro 2022. 75. Denniston, M. M.; Jiles, R. B.; Drobeniuc, J.; Klevens, R. M.; Ward, J. W.; McQuillan, G. M.; Holmberg, S. D.; Ann. Intern. Med. 2014, 160, 293. [Crossref]; Seo, S.; Silverberg, M. J.; Hurley, L. B.; Ready, J.; Saxena, V.; Witt, D.; Hare, C. B.; Champsi, J. H.; Korn, D. G.; Pauly, M. P.; Chamberland, S.; Lai, J. B.; Marcus, J. L.; Clin. Gastroenterol. Hepatol. 2020, 18, 511. [Crossref] 76. Choi, M.; Kim, Y.-M.; Lee, S.; Chin, Y.-W.; Lee, C.; Virus Genes 2014, 49, 208. [Crossref] 77. https://www.unaids.org/en, acessada em setembro 2022. 78. Finzi, D.; Hermankova, M.; Pierson, T.; Carruth, L. M.; Buck, C.; Chaisson, R. E.; Quinn, T. C.; Chadwick, K.; Margolick, J.; Brookmeyer, R.; Gallant, J.; Markowitz, M.; Ho, D. D.; Richman, D. D.; Siliciano, R. F.; Science (Washington, DC, U. S.) 1997, 278, 1295. [Crossref]; Demeter, L. M.; Bosch, R. J.; Coombs, R. W.; Fiscus, S.; Bremer, J.; Johnson, V. A.; Erice, A.; Jackson, J. B.; Spector, S. A.; Squires, K. M.; Fischl, M. A.; Hughes, M. D.; Hammer, S. M.; J. Clin. Microbiol. 2002, 40, 2089. [Crossref]; Falcinelli, S. D.; Ceriani, C.; Margolis, D. M.; Archin, N. M.; Front. Microbiol. 2019, 10. [Crossref] 79. Mailler, E.; Bernacchi, S.; Marquet, R.; Paillart, J.-C.; Vivet-Boudou, V.; Smyth, R. P.; Viruses 2016, 8, 248 [Crossref]; Zhao, J.-C.; Deng, K.; Chin. Med. J. (Beijing, China, Engl. Ed.) 2020, 133, 2867 [Crossref]. 80. Bieniasz, P.; Telesnitsky, A.; Annu. Rev. Virol. 2018, 5, 165. [Crossref] 81. Cary, D. C.; Peterlin, B. M.; AIDS Res. Hum. Retroviruses 2018, 34, 31. [Crossref] 82. Chen, S.-X.; Wan, M.; Loh, B.-N.; Planta Med. 1996, 62, 381. [Crossref] 83. Matúz, K.; Mótyán, J.; Li, M.; Wlodawer, A.; Tőzsér, J.; FEBS J. 2012, 279, 3276. [Crossref] 84. Weinbren, M. P.; Haddow, A. J.; Williams, M. C.; Trans. R. Soc. Trop. Med. Hyg. 1958, 52, 253. [Crossref] 85. Thiberville, S.-D.; Moyen, N.; Dupuis-Maguiraga, L.; Nougairede, A.; Gould, E. A.; Roques, P.; de Lamballerie, X.; Antiviral Res. 2013, 99, 345. [Crossref] 86. Weaver, S. C.; Forrester, N. L.; Antiviral Res. 2015, 120, 32. [Crossref] 87. Nsoesie, E. O.; Kraemer, M. U.; Golding, N.; Pigott, D. M.; Brady, O. J.; Moyes, C. L.; Johansson, M. A.; Gething, P. W.; Velayudhan, R.; Khan, K.; Hay, S. I.; Brownstein, J. S.; Eurosurveillance 2016, 21, 30234. [Crossref] 88. Patil, P.; Agrawal, M.; Almelkar, S.; Jeengar, M. K.; More, A.; Alagarasu, K.; Kumar, N. V.; Mainkar, P. S.; Parashar, D.; Cherian, S.; Virol. J. 2021, 18, 47. [Crossref] 89. Rausalu, K.; Utt, A.; Quirin, T.; Varghese, F. S.; Zusinaite, E.; Das, P. K.; Ahola, T.; Merits, A.; Sci. Rep. 2016, 6, 37124. [Crossref] 90. Parashar, D.; Paingankar, M. S.; Kumar, S.; Gokhale, M. D.; Sudeep, A. B.; Shinde, S. B.; Arankalle, V. A.; PLoS Neglected Trop. Dis. 2013, 7, e2405. [Crossref] 91. Zhang, Y.; Sun, Z.; Pei, J.; Luo, Q.; Zeng, X.; Li, Q.; Yang, Z.; Quan, J.; ChemMedChem 2018, 13, 2057. [Crossref] 92. Li, L.; Jose, J.; Xiang, Y.; Kuhn, R. J.; Rossmann, M. G.; Nature (London, U. K.) 2010, 468, 705. [Crossref] 93. https://www.who.int/news-room/fact-sheets/detail/dengue-and-severe-dengue, acessada em setembro 2022. 94. Smartt, C. T.; Shin, D.; Alto, B. W.; Mem. Inst. Oswaldo Cruz 2017, 112, 829. [Crossref] 95. Ghosh, A.; Dar, L.; Indian J. Med. Microbiol. 2015, 33, 3. [Crossref] 96. Poddar, A.; Shukla, R.; Beesetti, H.; Arora, U.; Rajpoot, R. K.; Shanmugam, R. K.; Palla, S.; Nayyar, K.; Singh, D.; Singamaneni, V.; Gupta, P.; Gupta, A. P.; Gairola, S.; Bedi, Y. S.; Jain, T.; Vashishta, B.; Patil, R.; Madan, H.; Madan, S.; Kalra, R.; Sood, R.; Vishwakarma, R.; Lal, A. A.; Khanna. N.; bioRxiv, Microbiol. 2015. [Crossref] 97. Yongpitakwattana, P.; Morchang, A.; Panya, A.; Sawasdee, N.; Yenchitsomanus, P.-T.; Arch. Virol. 2021, 166, 1623. [Crossref] 98. Hopkins, R. A.; Connolly, J. E.; Immunol. Res. 2012, 53, 91. [Crossref]; Sugiyanto, Z.; Yohan, B.; Hadisaputro, S.; Dharmana, E.; Suharti, C.; Winarto; Djamiatun, K.; Rahmi, F. L.; Sasmono, R. T.; Nat. Prod. Bioprospect. 2019, 9, 345. [Crossref] 99. Soundravally, R.; Sankar, P.; Hoti, S. L.; Selvaraj, N.; Bobby, Z.; Sridhar, M. G.; Acta Trop. 2008, 106, 156. [Crossref] 100. Ferrari, M.; Zevini, A.; Palermo, E.; Muscolini, M.; Alexandridi, M.; Etna, M. P.; Coccia, E. M.; Fernandez-Sesma, A.; Coyne, C.; Zhang, D. D.; Marques, E. T. A.; Olagnier, D.; Hiscott, J.; J. Virol. 2020, 94, e01551. [Crossref] 101. Checconi, P.; De Angelis, M.; Marcocci, M. E.; Fraternale, A.; Magnani, M.; Palamara, A. T.; Nencioni, L.; Int. J. Mol. Sci. 2020, 21, 4084. [Crossref] 102. http://who.sprinklr.com, acessada em setembro 2022 103. Bogoch, I. I.; Brady, O. J.; Kraemer, M. U. G.; German, M.; Creatore, M. I.; Kulkarni, M. A.; Brownstein, J. S.; Mekaru, S. R.; Hay, S. I.; Groot, E.; Watts, A.; Khan, K.; Lancet 2016, 387, 335. [Crossref]; Dos Santos, W. G.; Biomed. Pharmacother. 2020, 129, 110493. [Crossref] 104. https://www.who.int/emergencies/diseases/novel-coronavirus-2019, acessada em setembro 2022. 105. Drag, M.; Salvesen, G. S.; Nat. Rev. Drug Discovery 2010, 9, 690. [Crossref] 106. Jin, Z.; Du, X.; Xu, Y.; Deng, Y.; Liu, M.; Zhao, Y.; Zhang, B.; Li, X.; Zhang, L.; Peng, C.; Duan, Y.; Yu, J.; Wang, L.; Yang, K.; Liu, F.; Jiang, R.; Yang, X.; You, T.; Liu, X.; Yang, X.; Bai, F.; Liu, H.; Liu, X.; Guddat, L. W.; Xu, W.; Xiao, G.; Qin, C.; Shi, Z.; Jiang, H.; Rao, Z.; Yang, H.; Nature (London, U. K.) 2020, 582, 289. [Crossref] 107. Eleftheriou, P.; Amanatidou, D.; Petrou, A.; Geronikaki, A.; Molecules 2020, 25, 2529. [Crossref] 108. Ortega, S. S.; Cara, L. C. L.; Salvador, M. K.; Drug Metab. Drug Interact. 2012, 27, 199 [Crossref]; Bender, B. J.; Gahbauer, S.; Luttens, A.; Lyu, J.; Webb, C. M.; Stein, R. M.; Fink, E. A.; Balius, T. E.; Carlsson, J.; Irwin, J. J.; Shoichet, B. K.; Nat. Protoc. 2021, 16, 4799 [Crossref]. 109. Hidayat, S.; Ibrahim, F. M.; Pratama, K. F.; Muchtaridi, M.; J. Adv. Pharm. Technol. Res. 2021, 12, 285. (PMID: 34345609) [Crossref] 110. Cheng, F.; Li, W.; Liu, G.; Tang, Y.; Curr. Top. Med. Chem. (Sharjah, United Arab Emirates) 2013, 13, 1273. [Crossref] 111. Yazdanian, M.; Glynn, S. L.; Wright, J. L.; Hawi, A.; Pharm. Res. 1998, 15, 1490. [Crossref] 112. Sargolzaei, M.; J. Mol. Graphics Modell. 2021, 103, 107803. [Crossref] 113. Lekhera, S.; Devlal, K.; Ghosh, A.; Chowdhury, P.; Rana, M.; Chem. Pap. 2022. [Crossref] 114. Lipinski, C. A.; Drug Discovery Today: Technol. 2004, 1, 337. [Crossref] 115. https://www.who.int/neglected_diseases/diseases/en/, acessada em setembro 2022. 116. Ismail, F. M.; Nahar, L.; Zhang, K. Y.; Sarker, S. D. Annu. Rep. Med. Chem. 2020, 55, 115 [Crossref] 117. Hu, Y.; Ellis, B. L.; Yiu, Y. Y.; Miller, M. M.; Urban, J. F.; Shi, L. Z.; Aroian, R. V.; PLoS One 2013, 8, e70702. [Crossref] 118. Geary, T. G.; Curr. Opin. Infect. Dis. 2012, 25, 709. [Crossref] 119. Dorosti, Z.; Yousefi, M.; Sharafi, S. M.; Darani, H. Y.; Future Oncol. 2014, 10, 2529. [Crossref] 120. Murray, C. J.; Rosenfeld, L. C.; Lim, S. S.; Andrews, K. G.; Foreman, K, J.; Haring, D.; Fullman, N.; Naghavi, M.; Lozano, R.; Lopez, A. D.; Lancet 2012, 379, 413. [Crossref] 121. Mita, T.; Tanabe, K.; Jpn. J. Infect. Dis. 2012, 65, 465 [Crossref]; Berzosa, P.; de la Fuente, I. M.; Ta-Tang, T.-H.; González, V.; García, L.; Rodríguez-Galet, A.; Díaz-Regañón, R.; Galán, R.; Cerrada-Gálvez, L.; Ncogo, P.; Riloha, M.; Benito, A.; Malar. J. 2021, 20, 463 [Crossref]. 122. Upegui, Y.; Robledo, S. M.; Romero, J. F. G.; Quiñones, W.; Archbold, R.; Torres, F.; Escobar, G.; Nariño, B.; Echeverri, F.; Phytother. Res. 2015, 29, 1195. [Crossref] 123. Paucar, R.; Moreno-Viguri, E.; Pérez-Silanes, S.; Curr. Med. Chem. 2016, 23, 3154. [Crossref] 124. Clayton, J.; Nature (London, U. K.) 2010, 465, S4. [Crossref] 125. Livingston, E, G.; Duggal, R.; Dotters-Katz, S.; Tropical Medicine and Infectious Disease 2021, 6, 202. [Crossref] 126. Coura, J. R.; de Castro, S. L.; Mem. Inst. Oswaldo Cruz 2002, 97, 3. [Crossref] 127. Houweling, T. A. J.; Karim-Kos, H. E.; Kulik, M. C.; Stolk, W. A.; Haagsma, J. A.; Lenk, E. J.; Richardus, J. H.; de Vlas, S. J.; PLoS Neglected Trop. Dis. 2016, 10, e0004546. [Crossref] 128. Lee, B. Y.; Bacon, K. M.; Botazzi, M. E.; Hotez, P. J.; Lancet Infect. Dis. 2013, 13, 342. [Crossref] 129. Stanaway J. D.; Roth, G.; Global Heart, 2015, 10, 139. [Crossref] 130. Bermudez, J.; Davies, C.; Simonazzi, A.; Real, J. P.; Palma, S.; Acta Trop. 2016, 156, 1. [Crossref] 131. Garcia, S.; Ramos, C. O.; Senra, J. F. V.; Vilas-Boas, F.; Rodrigues, M. M.; Campos-de-Carvalho, A. C.; Ribeiro-dos-Santos, R.; Soares, M. B.; Antimicrob. Agents Chemother. 2005, 49, 1521. [Crossref] 132. https://www.who.int/health-topics/neglected-tropical-diseases#tab=tab_1, acessada em setembro 2022. 133. Rassi Jr., A.; Rassi, A.; Marin-Neto, J. A.; Lancet, 2010, 375, 1388 [Crossref]; Santos, E. F.; Silva, Â. A. O.; Leony, L. M.; Freitas, N. E. M.; Daltro, R. T.; Regis-Silva, C. G.; Del-Rei, R. P.; Souza, W. V.; Ostermayer, A. L.; Costa, V. M.; Silva, R. A.; Ramos Jr, A. N.; Sousa, A. S.; Gomes, Y. M.; Santos, F. L. N.; PLoS Neglected Trop. Dis. 2020, 14, e0008445 [Crossref]. 134. Dias, L. C.; Dessoy, M. A.; Silva, J. J. N.; Thiemann, O. H.; Oliva, G.; Andricopulo, A. D.; Quim. Nova 2009, 32, 2444 [Crossref]; Sueth-Santiago, V.; Decote-Ricardo, D.; Morrot, A.; Freire-de-Lima, C. G.; Lima, M. E. F.; World Journal of Biological Chemistry 2017, 8, 57 [Crossref]. 135. Al-Massarani, S. M.; El Gamal, A. A.; Al-Musayeib, N. M.; Mothana, R. A.; Basudan, O. A.; Al-Rehaily, A. J.; Farag, M.; Assaf, M. H.; El Tahir, K. H.; Maes, L.; Molecules 2013, 18, 10599. [Crossref] 136. Paiva, C. N.; Medei, E.; Bozza, M. T.; PLoS Pathog. 2018, 14, e1006928. [Crossref] 137. Buelna-Chontal, M.; Correa, F.; Hernández-Reséndiz, S.; Zazueta, C.; Pedraza-Chaverri, J.; J. Med. Food 2011, 14, 1370. [Crossref] 138. Sánchez-Villamil. J. P.; Bautista-Niño, P. K.; Serrano, N. C.; Rincon, M. Y.; Garg, N. J.; Oxid. Med. Cell. Longevity, 2020, 2020. [Crossref] 139. Tieghi, T. M.; Manca, C. C.; Garcia, L. C. T.; Castanho, R. E. P.; Therezo, A. L. S.; Frei, F.; Taipeiro, E. F.; Martins, L. P. A.; Revista Da Sociedade Brasileira de Medicina Tropical 2017, 50, 184. [Crossref] 140. Maldonado, E.; Rojas, D. A.; Urbina, F.; Solari, A.; Antioxidants 2021, 10, 1022. [Crossref] 141. European Centre for Disease Prevention and Control. Surveillance of Antimicrobial Resistance in Europe. Annual Report of the European Antimicrobial Resistance Surveillance Network (EARS-Net) 2017, ECDC: Stockholm, 2018. 142. https://www.who.int/news/item/11-11-2021-more-countries-committing-to-tackling-antimicrobial-resistance, acessada em setembro 2022. 143. De Abreu, P. M.; Farias, P. G.; Paliva, G. S.; Almeida, A. M.; Morais, P. V.; BMC Microbiol. 2014, 14. [Crossref] 144. CDC. Antibiotic Resistance Threats in the United States, CDC: Atlanta, 2013. 145. Gomes, F.; Teixeira, P.; Oliveira, R.; Biofouling 2014, 30, 131. [Crossref] 146. Reiter, K. C.; Sant'Anna, F. H.; d'Azevedo, P. A.; Int. J. Antimicrob. Agents 2014, 43, 248. [Crossref] 147. Liu, X.; Shen, J.; Zhu, K.; RSC Med. Chem. 2022, 13, 107. [Crossref] 148. Nguyen, P. T. M.; Nguyen, M. T. H.; Bolhuis, A.; Saudi J. Biol. Sci. 2021, 28, 1615. [Crossref] 149. Lu, L.; Hu, W.; Tian, Z.; Yuan, D.; Yi, G.; Zhou, Y.; Cheng, Q.; Zhu, J.; Li, M.; Chin. Med. (London, U. K.) 2019, 14. [Crossref] 150. Nguyen, P. T. M.; Falsetta, M. L.; Hwang, G.; Gonzalez-Begne, M.; Koo, H.; PloS One 2014, 9, e111312. [Crossref] 151. Stan, D.; Enciu, A.-M.; Mateescu, A. L.; Ion, A. C.; Brezeanu, A. C.; Stan, D.; Tanase, C.; Front. Pharmacol. 2021, 12. [Crossref] 152. Sriyanti, I.; Edikresnha, D.; Rahma, A.; Munir, M. M.; Rachmawati, H.; Khairurrijal, K.; Int. J. Nanomed. 2018, 13, 4927. [Crossref] 153. Arciola, C. R.; Campoccia, D.; Ravaioli, S.; Montanaro, L.; Front. Cell. Infect. Microbiol. 2015, 5. [Crossref] 154. Park, P. W.; Broekelmann, T. J.; Mecham, B. R.; Mecham, R. P.; J. Biol. Chem. 1999, 274, 2845. [Crossref] 155. WHO; Global tuberculosis report 2017, WHO: Geneva, 2017. 156. Espinal, M. A.; Laszlo, A.; Simonsen, L.; Boulahbal, F.; Kim, S. J.; Reniero, A.; Hoffner, S.; Rieder, H. L.; Binkin, N.; Dye, C.; Williams, R.; Raviglione, M. C.; N. Engl. J. Med. 2001, 344, 1294 [Crossref]; Gazi, M. A.; Islam, M. R.; Kibria, M. G.; Mahmud, Z.; Eur. J. Clin. Microbiol. Infect. Dis. 2015, 34, 851 [Crossref]. 157. WHO; Anti-tuberculosis drug resistance in the world, WHO, Geneva, 2004. 158. Suksamrarn, S.; Suwannapoch, N.; Phakhodee, W.; Thanuhiranlert, J.; Ratananukul, P.; Chimnoi, N.; Suksamrarn, A.; Chem. Pharm. Bull. 2003, 51, 857. [Crossref] 159. Guzmán-Beltrán, S.; Rubio-Badillo, M. Á.; Juárez, E.; Hernández-Sánchez, F.; Torres, M.; Int. Immunopharmacol. 2016, 31, 149. [Crossref] 160. Sivangala Thandi, R.; Radhakrishnan, R. K.; Tripathi, D.; Paidipally, P.; Azad, A. K.; Schlesinger, L. S.; Samten, B.; Mulik, S.; Vankayalapati, R.; Nat. Commun. 2020, 11, 1. [Crossref] 161. Nguyen, P. T. M.; Marquis, R. E.; Can. J. Microbiol. 2011, 57, 217. [Crossref] 162. Brown, G. D.; Denning, D. W.; Gow, N. A. R.; Levitz, S. M.; Netea, M. G.; White, T. C.; Sci. Transl. Med. 2012, 4, 165rv13. [Crossref] 163. Iliev, I. D.; Leonardi, I.; Nat. Rev. Immunol. 2017, 17, 635. [Crossref] 164. Douglas, L. J.; Trends Microbiol. 2003, 11, 30. [Crossref]; Prieto, D.; Román, E.; Correia, I.; Pla, J.; PLoS One 2014, 9, e87128. [Crossref]. 165. Harriott, M. M.; Lilly, E. A.; Rodriguez, T. E.; Fidel, P. L.; Noverr, M. C.; Microbiology (London, U. K.) 2010, 156, 3635. [Crossref] 166. Nobile, C. J, Johnson, A. D.; Annu. Rev. Microbiol. 2015, 69, 71. [Crossref] 167. Narasimhan, S.; Maheshwaran, S.; Abu-Yousef, I. A.; Majdalawieh, A. F.; Rethavathi, J.; Das, P. E.; Poltronieri, P.; Molecules 2017, 22, 275. [Crossref] 168. Awang, Y.; Ghani, M. A. A.; Sijam, K.; Mohamad, R. B.; Afr. J. Microbiol. Res. 2011, 5, 5250 [Crossref]; Dean, R.; Van Kan, J. A.; Pretorius, Z. A.; Hammond-Kosack, K. E.; Di Pietro, A.; Spanu, P. D.; Rudd, J. J.; Dickman, M.; Kahmann, R.; Ellis, J.; Foster, G. D.; Mol. Plant Pathol. 2012, 13, 414 [Crossref] 169. Ye, H.; Wang, Q.; Zhu, F.; Feng, G.; Yan, C.; Zhang, J.; Molecules 2020, 25, 5335. [Crossref] 170. Karadimos, D. A.; Karaoglanidis, G. S.; Tzavella-Klonari, K. Crop Prot. 2005, 24, 23. [Crossref] |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access