Revisão
|
|
| Biomarcadores orgânicos e inorgânicos de aerossóis atmosféricos de regiões marinhas Organic and inorganic biomarkers of atmospheric aerosols from marine regions |
|
Sabrina Teixeira MartinezI,II; Jeancarlo Pereira dos AnjosI,II,III,#; Pedro Afonso de Paula PereiraI,II,III,IV; Lilian Lefol Nani GuarieiroI,II; Gisele Olímpio da RochaII,III,IV,*
I. Centro Universitário SENAI CIMATEC, 41650-010 Salvador - BA, Brasil Recebido em: 09/02/2023 *e-mail: giseleor@ufba.br; giseleolimpiorocha@gmail.com #Current address: Centro de Ciências Naturais e Humanas (CCNH), Universidade Federal do ABC, 09210-580 Santo André - SP, Brasil In this study, we overview the recent advancements in knowledge regarding organic and inorganic biomarkers of atmospheric aerosols from coastal zones and open marine areas. It deals with the interaction between the ocean and the atmosphere through their interface, the formation of a seawater microlayer (SML) and the exchange of a myriad of chemical compounds between those environmental compartments. We also discuss how marine aerosols (MAs) are intrinsically related to the global carbon cycle, influence the radiative budget of the Earth, and are related to global climate. At the end, we discuss the trends of new studies on the topic. INTRODUÇÃO Os aerossóis atmosféricos podem influenciar o balanço radiativo do planeta através da absorção e/ou da reflexão da radiação solar, influenciando os processos de formação de nuvens e neve, visto que podem agir como CCN (do inglês cloud condensation nuclei, ou núcleos de formação de nuvens) e IN (do inglês ice nuclei, ou núcleos de formação de gelo/neve).1 2 3 4 5 6 7 8 Fontes naturais de aerossóis atmosféricos globalmente relevantes incluem os oceanos, desertos e incêndios espontâneos, que juntos contribuem com 90% (relação massa-massa) para os aerossóis atmosféricos, sendo o spray marinho e a ressuspensão de poeira os contribuintes majoritários.1 Entretanto, considerando que os oceanos cobrem mais de 70% da superfície do planeta, o impacto do spray marinho no balanço radiativo do planeta é uma área crítica de investigações das ciências climáticas. Atualmente, as maiores incertezas dos modelos climáticos do planeta ainda estão associadas às contribuições relativas das interações dos aerossóis atmosféricos (principalmente os provenientes de regiões marinhas) e as nuvens.1,5,9 Os aerossóis atmosféricos de regiões costeiras e de mar aberto contribuem significativamente com aerossóis de origem natural em nível global. Através da interface oceano-atmosfera estima-se que sejam emitidos cerca de 3-30 Pg ano-1 (em termos de massa) de partículas para atmosfera, sendo que 98% deste total são atribuídas como partículas supermicrométricas (dp > 1 µm).10 Uma vez os aerossóis marinhos (do inglês marine aerosols, MAs) são promovidos para o ambiente atmosférico, eles circulam e se distribuem em todo planeta. Entretanto, os processos envolvidos na sua formação, emissão, modificação e/ou transporte ainda são muito pouco compreendidos pela comunidade científica.7,11 12 15 De uma maneira geral, os MAs podem ser constituídos tanto por componentes de origem biogênica quanto antrópicos, e que ambos provavelmente são formados e/ou modificados através de uma variedade complexa de processos biogeoquímicos.7,14 Se considerado apenas em termos de massa, os principais componentes químicos dos MAs provavelmente são os íons majoritários provenientes do spray marinho, que são gerados através da interação mecânica dos ventos com a superfície dos oceanos. Entretanto, nesse mesmo processo de geração de spray marinho, há a formação e arrebentação de bolhas de água do mar, e parte da matéria orgânica dissolvida nela também é exportada para a atmosfera na forma de aerossol.4,5,10,16,17 Ainda, compostos orgânicos voláteis (do inglês volatile organic compounds, VOCs) emitidos por bactérias, fitoplânctons, algas e outros organismos marinhos, bem como os produtos de oxidação desses VOCs, também são componentes importantes dos MAs.7,13,15 Contudo, observa-se que o conteúdo orgânico dos MAs de regiões oceânicas com alta produtividade biológica é maior do que os MAs de regiões de baixa produtividade.18 Adicionalmente, uma componente importante da formação e/ou composição dos MAs são partículas geradas nos continentes e então transportadas por centenas ou milhares de quilômetros até regiões costeiras e oceano aberto6,8,14,19 20 21 através do processo chamado de transporte atmosférico a longas distâncias. Por sua vez, durante o transporte atmosférico, as partículas sofrem transformações físicas (modificação de tamanho, de área superficial e volume, dentre outras), químicas (modificações da composição) e biológicas (crescimento de microrganismos). Portanto, a composição química e a heterogeneidade dos MAs são resultantes diretos das contribuições de diferentes fontes (naturais e antrópicas) bem como dos processos físicos, químicos e biológicos envolvidos. Desse modo, considerando a contribuição dos compostos orgânicos dos MAs, fica evidente sua importância direta na ciclagem do carbono orgânico e também sua participação central no ciclo global do carbono.22 Outro ponto interessante é que o aerossol proveniente de atmosferas marinhas possui matriz amostral com elevada complexidade e heterogeneidade. Os aerossóis são compostos por centenas e até milhares de substâncias orgânicas e inorgânicas. E quanto maior o número e variedade de substâncias que os compõem, mais complexa são as matrizes amostrais e mais processos físico-biogeoquímicos estão envolvidos na formação dos mesmos.7 Logo, estudar um determinado grupo de substâncias dos MAs significa necessariamente estudar apenas uma parcela muito pequena de seu histórico atmosférico. Ou seja, esse tipo de abordagem nos dá apenas uma visão restrita dos processos atmosféricos e, consequentemente, do clima do planeta. Desse modo, avaliar uma maior quantidade de espécies que compõem os MAs através de biomarcadores de diferentes fontes pode ser uma melhor alternativa para um melhor entendimento dos processos envolvidos na sua formação.19,23 A proposta desse artigo é apresentar um overview sobre o estado-da-arte dos aerossóis atmosféricos de regiões costeiras e marinhas, avaliando e discutindo criticamente o assunto de maneira abrangente. No final do texto são apresentadas as tendências de estudos futuros. Análise bibliométrica Com o objetivo de entender a tendência do estado-da-arte sobre marcadores biogênicos e antrópicos em aerossóis atmosféricos de zonas costeiras e marinhas, foi realizada a análise bibliométrica em 3 de janeiro de 2023 na plataforma ScienceDirect24 utilizando quatro estratégias de busca com os descritores: (i) aerosols AND coastal areas; (ii) polluting AND coastal zones; (iii) coastal AND zones AND biogenic AND markers e (iv) coastal AND zones AND anthropic AND markers. O período considerado nas buscas foi para os trabalhos publicados entre 1999 e 2023. O número de documentos recuperados foram: (i) 20.756; (ii) 20.785; (iii) 3.349 e (iv) 430, respectivamente. Foi observado que o número de publicações nos últimos 10 anos aumentou exponencialmente, o que indica o interesse e preocupações crescentes sobre o tema em questão (Figura 1).
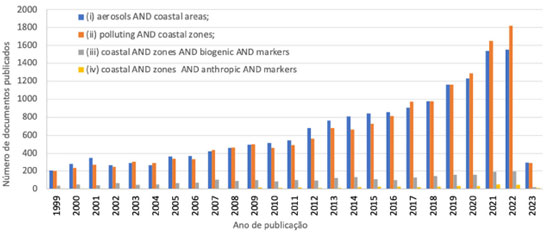 Figura 1. Número de publicações por ano sobre aerossóis e marcadores biogênicos e antrópicos em zonas costeiras (fonte: ScienceDirect, 2023)24
O conjunto de pesquisas desenvolvidas nos últimos 24 anos sobre (a) aerossóis, (b) poluição, (c) marcadores biogênicos e (d) marcadores antrópicos em zonas costeiras podem ser agrupados em 18, 18, 23 e 3 grandes clusters, respectivamente (Figura 2).25 As investigações desenvolvidas sobre os aerossóis emitidos em zonas costeiras destacam temas que podem influenciar no estudo destes, tais como: sensoriamento remoto, emissão de material particulado, elementos traço, bioaerossóis, entre outros (Figura 2a). Os temas em destaque para as pesquisas com foco na poluição em zonas costeiras já são direcionados para: mudanças climáticas, metais pesados, risco ecotoxicológico, material particulado, modificações no DNA, entre outros (Figura 2b). As pesquisas desenvolvidas sobre marcadores biogênicos focam em: biomarcadores, holoceno, bioestratigrafia, sedimentos, capacidade de absorção, e biodegradação, dentre outros (Figura 2c). Pesquisas sobre marcadores antrópicos em zonas costeiras não destacam os principais temas estudados, mas estão em sinergia com os demais descritores utilizados nas pesquisas (Figura 2d). Visando um melhor entendimento sobre tais pesquisas, a Figura 3 destaca com maior clareza os desenvolvimentos relacionados com os marcadores biogênicos e antrópicos existentes em zonas costeiras. A Figura 2d, apesar de trazer uma quantidade menor de publicações sobre o tema de estudo, quando comparado com as demais pesquisas, apresenta 3 grandes clusters que podem representar o tema de estudo. Um primeiro grupo de interesse que pode ser destacado são as fontes impactadas e possível origem de poluentes (cluster azul). Observa-se a existência de estudos de monitoramento, procedimentos analíticos sendo realizados em sedimentos, águas costeiras e estuários, relacionando biomarcadores com hidrocarbonetos e petróleo. O cluster verde traz indicadores sobre a preocupação com a poluição do ecossistema marinho. Outra preocupação observada nas publicações, destacada no cluster vermelho, são os impactos da poluição antrópica que refletem em variações genéticas, stress ambiental e aumento da toxicidade, gerados com a presença de metais pesados com destaque para os metais: cobre, cadmio, arsênio, cromo, cobalto, níquel, vanádio, manganês e zinco (Figura 2d).
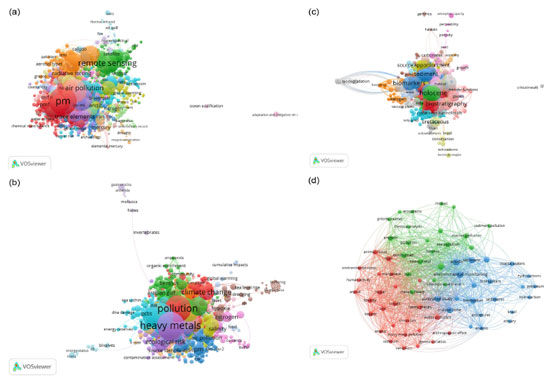 Figura 2. Clusters formados com grupo de palavras-chaves utilizadas nas publicações recuperadas na base de dados ScienceDirect24 e criado na plataforma VOSViewer:25 (a) aerosols AND coastal areas; (b) polluting AND coastal zones; (c) coastal AND zones AND biogenic AND markers; e (d) coastal AND zones AND anthropic AND markers25
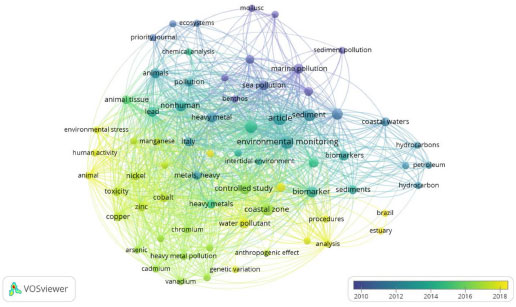 Figura 3. Clusters temporal formados com grupo de palavras-chaves utilizadas nas publicações recuperadas na base de dados ScienceDirect24 e criado na plataforma VOSViewer25
Desde o início dos registros das publicações nos anos 2000, já era possível observar as preocupações relacionadas com a poluição marinha, onde se observa na Figura 3 que os temas abordados nessa época estão em coloração próximas do azul. Uma vez identificados os impactos gerados pela poluição marinha, as investigações foram avançando para estudos de monitoramento e identificação de biomarcadores da poluição (palavras destacadas na coloração esverdeada na Figura 3). Atualmente, o estudo bibliométrico destaca (palavras na coloração amarela, Figura 3) uma tendência de desenvolvimentos de procedimentos analíticos visando avaliação do impacto da atividade antrópica no ecossistema marinho, caracterizando a presença de alguns elementos específicos em animais marinhos, estuários, sedimentos e água marinha. Tal presença vem sendo associada à toxicidade, variação genética e stress ambiental. Neste contexto, é de suma importância, não só o monitoramento das zonas costeiras visando a manutenção da qualidade de todo ecossistema e as contribuições das fontes biogênicas, mas também que existam políticas públicas ativas que mitiguem os danos causados pelo homem ao ambiente marinho.
COMPLEXIDADE DAS FRAÇÕES ORGÂNICAS E INORGÂNICAS DOS AEROSSÓIS MARINHOS Microcamada superficial oceânica Considerando que os oceanos cobrem 362 milhões de km2 ou 71% da superfície da Terra, a interface oceano-atmosfera é uma das maiores e mais importantes interfaces do planeta. Toda transferência de matéria do oceano para atmosfera, e vice-versa, passa necessariamente por essa interface, que apresenta características físicas, químicas e biológicas distintas tanto da parte da atmosfera que está imediatamente acima como da subsuperfície e camada de águas mais profundas dos oceanos. Uma porção importante dessa interface é a camada mais superficial dos oceanos de cerca 1-1000 µm de espessura e que está em contato direto com a atmosfera, sendo chamada de microcamada superficial oceânica (do inglês SML, sea surface microlayer).2,4,6,16,17,26,27 A SML provavelmente regula/contribui para as taxas de troca de energia e de matéria entre a atmosfera e o oceano, exercendo tanto impactos de curtos quanto de longos prazos em vários processos do "Sistema Terra", incluindo a formação de aerossóis marinhos, no ciclo biogeoquímico do carbono e outros elementos-chave, além de influenciar na regulação climática.27 Além disso, a composição química dos MAs está diretamente relacionada à composição química da SML. A SML é responsável pela transferência de substâncias orgânicas e inorgânicas para a atmosfera, contribuindo para a formação e a composição dos MAs, através de complexos processos físico-químicos. A SML, em relação às águas de subsuperfície e mais profundas, é enriquecida por uma grande diversidade de compostos orgânicos, tais como proteínas e outros materiais proteináceos, carboidratos, surfactantes, lipídios, terpenos, toxinas, poluentes e outros resíduos orgânicos derivados da matéria orgânica dissolvida (do inglês dissolved organic matter, DOM) e particulada (do inglês particulate organic matter, POM) do oceano. Por sua vez, os compostos presentes na DOM e na POM são derivados da atividade metabólica dos organismos (algas, fitoplânctons, bactérias, vírus, dentre outros organismos) e dos processos biogeoquímicos que ocorrem nos oceanos. Esses compostos orgânicos podem potencialmente mudar as propriedades da superfície da água do mar, conferindo algum grau de hidrofibicidade à SML e, consequentemente, aos aerossóis atmosféricos gerados a partir das transferências de massa derivadas da SML. A SML também tem um papel importante em regiões oceânicas eutróficas e em zonas costeiras devido à presença de maior quantidade de matéria orgânica com propriedades surfactantes nessas áreas. Esses surfactantes (e outros componentes orgânicos) podem ser tanto de origem natural quanto antrópica.28 29 30 31 32 Por outro lado, considerando a salinidade da água do mar (~ 35-37‰, dependendo do local, de uma mistura de sais inorgânicos majoritários, em uma proporção bem definida entre os cátions e ânions), seria de se esperar que a composição dos MAs quanto aos íons inorgânicos seguisse essa mesma proporção. Entretanto, há algumas importantes exceções. O enriquecimento de Ca2+ no spray marinho, relativo à água do mar já foi identificado em estudos do ambiente marinho e em câmaras de estudos de partículas marinhas nascentes (partículas primárias recentemente emitidas sob condições controladas). O mesmo já foi observado para os íons (Mg2+) e (K+)5,33 em partículas que também apresentaram déficits em íons Cl-.1,5,34 Por exemplo, partículas de spray marinho em tamanho submicrométrico (dp < 1 µm) foi observado um enriquecimento em até 500% de Ca2+ (em relação à água do mar), com alguns estudos mostrando um enriquecimento maior em partículas menores que 100 nm.5,35 Ainda não é bem compreendido se o Ca2+ apresenta-se de forma livre, ou complexado com matéria orgânica dissolvida na superfície do mar, ou se é o produto da precipitação de CaCO3 por certos grupos de fitoplânctons.5 Ainda, se por um lado, o conteúdo orgânico dos MAs (dependendo de sua composição), podem conferir características hidrofóbicas ou anfipáticas a estes, o conteúdo de íons majoritários presentes nos MAs pode conferir hidrofilicidade a essas partículas. A hidrofilicidade é uma característica física importante, já que confere boa capacidade de sorver água às partículas atmosféricas, conferindo aumento de seu diâmetro aerodinâmico e a dissolução de outros compostos orgânicos nesse filme líquido que envolve a superfície dos MAs. A capacidade de sorção de água das partículas ricas em íons majoritários, favorece a atuação dos MAs como CCN e IN. Por outro lado, o alto conteúdo de água nas partículas de MAs favorece a sorção de outras substâncias (gases traço, VOCs e outras substâncias volatilizáveis e/ou condensáveis) através de processos secundários (conversão gás-partícula).1,9,30 Acredita-se que componentes das frações inorgânica (por exemplo, íons majoritários, carbonatos e elementos traço, dentre outros) e orgânica apresentam-se associados entre si (internally mixed) nos MAs.5 Em observações feitas em laboratório através de experimentos de mesocosmos (câmaras de estudos que simulam em laboratório as condições ambientais sob condições controladas) sobre a formação de partículas atmosféricas primárias mostram que as espécies inorgânicas estão complexadas à matéria orgânica no spray marinho, sendo que a contribuição dos orgânicos pode variar entre 4-80% por volume, dependendo do procedimento utilizado para os experimentos e faixa de tamanho de partículas considerado. Esses estudos mostram que a fração orgânica aumenta com a diminuição do tamanho da partícula. Estimativas de partículas menores que 100 nm são da ordem de 5-37% em orgânicos.1,4,5,10,17,34 A fração orgânica dos MAs também está associada ao declínio de fitoplânctons através das atividades de bactérias e vírus, que liberam ácidos graxos e polissacarídeos que se acumulam na SML. A composição da fração orgânica do PM1 (partículas com diâmetro aerodinâmico menor ou igual a 1 µm) é caracterizada por uma grande fração (> 50%) de grupos hidroxilas, com menores contribuições de alcanos e de grupos aminos e de ácidos carboxílicos. As hidroxilas são geralmente consistentes com polissacarídeos solúveis em água, apesar de também serem observados polissacarídeos insolúveis em água nos MAs, o que pode suprimir a absorção de água e aumentar a tensão superficial dessas partículas atmosféricas.5 Biomarcadores de processos biogênicos Considerando as possíveis identidades químicas da matéria orgânica presente nos MAs, pode-se afirmar que estas sejam substâncias majoritariamente compostas por átomos de carbono, hidrogênio, oxigênio, nitrogênio e enxofre.6,8,14,19,22,23,36 37 38 39 40 Dentre as diferentes possibilidades de identificação e medidas de biomarcadores orgânicos ubíquos nos MAs, uma primeira abordagem seria a investigação do conteúdo de carbono orgânico (do inglês, organic carbon, OC) e carbono elementar (do inglês, elemental carbon, EC ou black carbon, BC), sendo que o conteúdo de carbono total (TC) é a soma entre OC e EC (Equação 1). Enquanto a medida de EC nos dá uma estimativa da emissão primária de combustão incompleta de matéria orgânica (queima de biomassa, queima de madeira, queima de combustíveis fósseis ou alternativos, dentre outros), com os níveis de OC é possível estimar a contribuição de uma ampla variedade de fontes primárias e secundárias de compostos orgânicos para atmosfera, seja de emissões biogênicas e/ou de emissões antrópicas.31,41 42 43 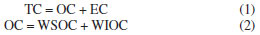 onde: TC = carbono total (do inglês total carbon); OC = carbono orgânico (do inglês organic carbon); EC = carbono elementar (do inglês elemental carbon); WSOC = carbono orgânico solúvel em água (do inglês water soluble organic carbon); WIOC = carbono orgânico insolúvel em água (do inglês water insoluble organic carbon). Carbono elementar (EC) é gerado durante a combustão incompleta de matéria orgânica (i.e., queima de biomassa e de combustíveis, dentre outros tipos) e emitido na forma de fuligem. As partículas ricas em EC geralmente apresentam-se na fração fina (PM2.5, dp < 2,5 µm), com importantes contribuições em partículas nanométricas (dp < 100 nm). Logo, além dos prováveis problemas ambientais que podem causar, tais como a de absorver radiação solar das regiões do visível e infravermelho (e.g., contribuindo para as alterações climáticas), podem também contribuir negativamente para saúde humana.4 No ambiente marinho, partículas atmosféricas ricas em EC podem ter sido geradas pela queima de combustível de embarcações, ou terem sido emitidas a grandes distâncias e então promovidas para as regiões marinhas através do transporte a longas distâncias e a circulação atmosférica.45,46 Por sua vez, o conteúdo de OC em aerossóis atmosféricos podem ser determinados os compostos orgânicos solúveis em água (do inglês, water soluble organic compounds, WSOC) e os compostos orgânicos insolúveis em água (do inglês, water insoluble organic compounds, WIOC), sendo OC, a soma entre WSOC e WIOC (Equação 2). Os WSOC são a fração majoritária dos orgânicos presentes nos aerossóis atmosféricos, e estima-se que a taxa de WSOC transferido para os oceanos por deposição seca seja entre 48-90 Tg ano-1.43 Dentre os WSOC, podem ser citados compostos com estruturas alifáticas e/ou anéis aromáticos que contenham grupamentos carboxila, hidroxila, carbonila, éster e metoxi, dentre outros. Atualmente, apenas cerca de 10-20% em massa dos WSOC de AMs foram elucidadas, e estes incluem ácidos mono-, di-, e tricarboxílicos, açúcares, aminoácidos e outros marcadores orgânicos polares (tais como 2-metiltetróis, ácido pínico, ácido pinóico, glioxal e metil-glioxal, dentre outros) que geralmente são provenientes da fotooxidação de compostos orgânicos voláteis biogênicos (do inglês, biogenic volatile organic compounds, BVOCs).12,14,19,39,40,47,48 Do ponto de vista analítico, considera-se que os compostos orgânicos representados como OC e/ou suas sub-frações (WSOC e/ou WIOC) sejam os responsáveis pelo aumento anormal da linha de base de cromatogramas principalmente obtidos por cromatografia a gás (GC), chamado de UCM (do inglês unresolved complex mixture, ou mistura complexa não resolvida). Apesar de, atualmente, com o emprego de cromatografia a gás bidimensional acoplada a espectrômetro de massas de alta resolução (GC × GC-HRMS) a resolução dos cromatogramas terem melhorado consideravelmente, ainda muito pouco é compreendido sobre essa fração orgânica dos MAs e outros métodos de identificação e qualificação de grupamentos químicos são empregados, tais como espectrômetro de massas para aerossóis atmosféricos (HR-ToF-AMS, high-resolution time-of-flight aerosol mass spectrometer), espectroscopia na região do infravermelho com transformada de Fourier (FTIR), ressonância magnética nuclear (RMN)29,49,50 combinados ou não com a determinação de isótopos estáveis (δ13C e δ15N).43 Considera-se atualmente que a maior parte dos WSOC compõem uma importante fração de compostos orgânicos solúveis em água classificadas como HUmic LIke Substances (HULIS), que são quimicamente similares aos ácidos fúlvico e húmico aquáticos e terrestres, que por sua vez, estão associados à fração chamada de brown carbon (BrC).14,43,51 Os compostos orgânicos que compõe o BrC conferem coloração em tons de marrom e, por isso são coletivamente chamados de brown carbon.52 O BrC é considerado como a fração do OC que absorve radiação solar, exibindo importante dependência de acordo com as faixas de comprimento de onda que é capaz de absorver, aumentando consideravelmente a absorção de radiações nas regiões do visível e ultravioleta. Apesar da capacidade de absorção de radiação solar do BrC ser menor do que a do BC (que absorve intensamente em praticamente todo o espectro solar), os impactos causados pelo BrC no balanço radiativo da atmosfera e as mudanças climáticas são consideráveis devido a sua grande abundância e ao fato de absorver eficientemente na região do espectro do UV próximo e os comprimentos de onda da região do azul.53 54 55 Estudos recentes têm demonstrado que o BrC é responsável por 20-50% do total de radiação absorvida pelos aerossóis na faixa entre 300-400 nm56 e também influenciam processos fotoquímicos atmosféricos, influenciando as taxas de fotólise de radicais atmosféricos e a formação de aerossóis orgânicos secundários (SOA, do inglês, secondary organic aerosols).14,38 39 40,43,51,55,57 O BrC pode ser formado pela queima incompleta de materiais carbonáceos, tais como combustíveis fósseis, biomassa e biocombustíveis. Além disso, o BrC pode também ser formado através de reações em fases gasosa e aquosa, ou através de reações heterogêneas de precursores biogênicos e antrópicos,55 dentre eles, os provenientes da atividade biológica de organismos marinhos, seus fragmentos ou sua excreção (e.g., vírus, bactérias, algas, fungos e esporos, dentre outros).52 Considerando as propriedades óticas e as químicas dos aerossóis ricos em BrC, os processos secundários, de reatividade e transformação química que participam, eles são capazes de contribuir/provocar modificações consideráveis nas características físicas e químicas, de crescimento higroscópico e de envelhecimento fotoquímico das partículas atmosféricas (do inglês particle aging).53 54 55,58,59 Logo, apesar dos recentes esforços da comunidade científica para melhor compreender os mecanismos de formação do BrC, principalmente no que se refere a melhor elucidação da composição química e de espécies que atuam como centros cromóforos e/ou fluóforos nos aerossóis atmosféricos,52,55,60,61 este tema ainda se apresenta como de grandes desafios para a química atmosférica. Adicionalmente, os HULIS presentes em aerossóis atmosféricos são uma classe de compostos orgânicos macromoleculares que podem ser facilmente isolados dos BrC, sendo considerados importantes componentes destes.62 Os HULIS atmosféricos são classificados como a porção hidrofóbica dos WSOC e compreendem estruturas com anéis policíclicos com cadeias de hidrocarbonetos laterais contendo hidroxilas, carbonilas e carboxilas.63 Eles podem ser emitidos diretamente através de processos de queima de biomassa. Nesse processo, biopolímeros naturais, tais como celulose e lignina podem ser termicamente decompostos, formando compostos (semi)voláteis de baixa massa molar que, por sua vez, podem se condensar entre si, formando espécies químicas de massas molares mais elevadas (HULIS) através de reações em fase gasosa. Adicionalmente, os HULIS podem também ser formados através de processos complexos que envolvem reações heterogêneas e fotossintetizadas entre compostos orgânicos voláteis (VOC) tanto de origem biogênica quanto antrópica.62 Ainda, no ambiente marinho, os HULIS podem ser emitidos através da atividade biológica de uma série de microrganismos e/ou organismos planctônicos.52 Não há ainda uma clara definição sobre a fração classificada como HULIS. Desse modo, os HULIS são determinados baseando-se em uma definição operacional, visto que um dos principais métodos de isolamento dos HULIS do restante da matriz amostral dos aerossóis é uma combinação entre a extração por solventes seguida por uma etapa de extração e clean up por cartuchos de SPE (extração em fase sólida), dentre outros métodos de extração, para separar os WSOC em frações hidrofílica e hidrofóbica.57,63 Os HULIS atmosféricos de regiões marinhas têm composição similar às substâncias húmicas (HS) aquáticas, mas com massas molares menores,57 com tendência a serem mais ativos em participar de reações de superfície das partículas, com menos acidez, e menor aromaticidade.57,63 Os WIOC são geralmente compostos orgânicos apolares, que podem conferir características hidrofóbicas aos MAs. Exemplos de WIOC podem ser os n-alcanos lineares ou ramificados, álcoois e ácidos graxos de cadeia longa e compostos policíclicos aromáticos (do inglês, polycyclic aromatic compounds, PACs), dentre outros. Enquanto os PACs são traçadores típicos de fontes antrópicas (e.g., processos de combustão incompleta), os n-alcanos lineares (n-C8-n-C40), os ácidos graxos e os álcoois de cadeia longa (C8-C40), dependendo da quantidade de carbonos que compõem a cadeia carbônica (relação entre números par e ímpar de carbonos), podem tanto indicar origem natural quanto antrópica,14,18,22,38,64 65 66 sendo úteis biomarcadores de fontes. A composição da fração orgânica dos MAs pode variar espacial e temporalmente devido à complexidade de suas fontes. Avaliar a fluorescência dos MAs pode ser útil para avaliar as propriedades ópticas dos mesmos, bem como as prováveis fontes.38 É sabido que moléculas orgânicas fluóforas que compõem o aerossol atmosférico marinho14 ou terrestre8,23,38,43,45,51,62 podem ser mapeadas através de diagramas de emissão-excitação (do inglês, emission-excitation diagram, EED). Após a obtenção dos EED, são avaliadas diferentes bandas de comprimento de onda que são consideradas como sendo representativas de determinados grupos de moléculas que são reconhecidas como biomarcadores de fontes. Exemplos são diferentes fluóforos que indicam espécies "protein-like", "HULIS-like", "terrestrial humic-like" e "marine humic-like", dentre outros (Figuras 4 e 5).14,23,31,38,43,45,51,60 Para aqueles leitores que se interessam em compreender melhor esses EED bem como as faixas de comprimentos de onda de excitação e emissão utilizadas para observar a relação entre composição química e as suas possíveis fontes, os autores gentilmente sugerem consultar os estudos de Pohlker et al.,39 Wu et al.,31,51,62 Afsana et al.57 e Jiang et al.67 pois são bem representativos do tema em questão. Contudo, ressalta-se que, como a fluorescência molecular não é uma técnica de caracterização inequívoca de compostos orgânicos, uma vez tendo sido identificados os centros fluorescentes, geralmente são utilizadas outras técnicas analíticas para aprofundar as investigações e também para a quantificação dos compostos de interesse (relacionando-os com as possíveis fontes).
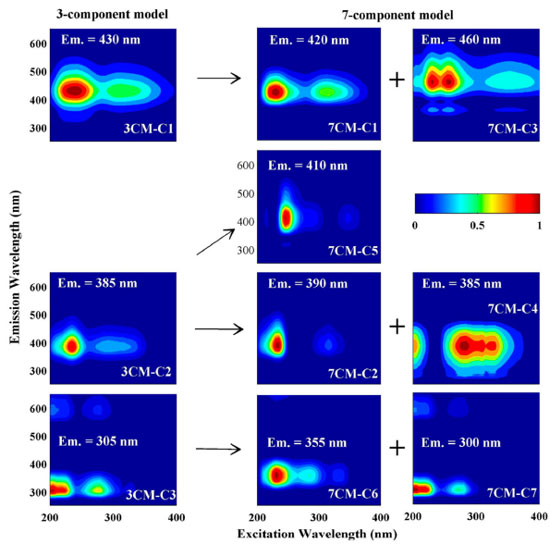 Figura 4. Perfis de diagrama de excitação-emissão (EED) de um conjunto de amostras de aerossóis coletados na Pensinsula Kii, Japão e a bordo do navio NOAA RV Ka'imimoana. Os componentes do EED foram identificados por 3 e 7 componentes através de soluções do modelo PARAFAC (do inglês, parallel fator analysis) para matéria orgânica solúvel em água (do inglês, water soluble organic matter, WSOM). A intensidade foi normalizada para que o máximo seja igual a 1. Os componentes químicos que correspondem as soluções PARAFAC de 3 componentes são 3CM-C1, -C2 e -C3, que são classificados como HULIS-1, HULIS-2 e PLOM (do inglês, protein-like organic matter), respectivamente. As setas representam combinações de soluções de 3 e 7 componentes com correlações positivas altas (r > 0,5; p < 0,01). O comprimento de onda de emissão (Em) na intensidade máxima de fluorescência para cada componente também é apresentada. Figura reproduzida com autorização de Chen et al.60 (direitos autorais (2016) da American Chemical Society)
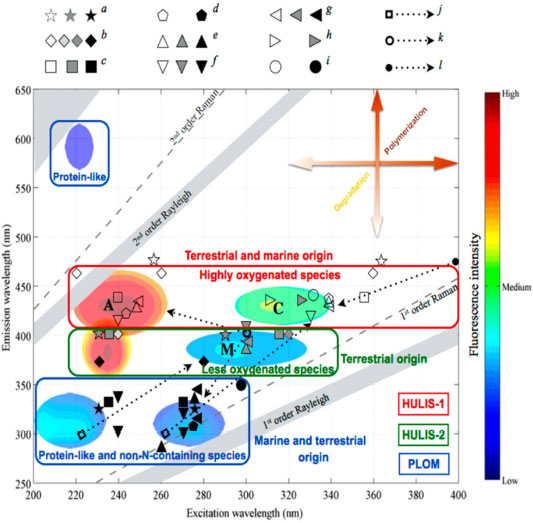 Figura 5. Diagrama da associação de perfis de emissão-excitação (EED) com possíveis estruturas químicas, fontes de emissão e processos químicos atmosféricos de compostos orgânicos solúveis em água (WSOC) presentes em aerossóis atmosféricos. Os retângulos em azul, verde e vermelho representam os intervalos de fluorescência de matéria orgânica com estruturas protein-like (PLOM), HULIS de origem terrestre e HULIS de origens terrestre e marinha, respectivamente. As cores dos círculos representam as intensidades relativas de fluorescência próximo aos picos dos componentes do EED. Os picos descritos por A, C e M representam os sinais de UVC excitados, UVA excitados e material húmico de origem marinha. Os marcadores rotulados com "a-i" representam o seguinte, da esquerda para a direita: a = componentes do WSOM de amostras de PM10 de Granada, Espanha classificados como quinone-like, HULIS terrestre e naphthalene-like; b = HULIS, aromáticos antrópicos, ácido fúlvico e substâncias de baixa massa molar em material solúvel em meio alcalino de poeira urbana de Ulsan, Coréia do Sul; c = dois componentes classificados como HULIS e PLOM em solução aquosa e em solução alcalina de PM2.5 de Aveiro, Portugal; d = HULIS e substâncias do tipo PLOM oceânica de material particulado total da atmosfera do Ártico; e = HULIS, HULIS marinho, e PLOM da água de chuva de Rameswaran, Índia; f = HULIS, HULIS marinho e PLOM da água de chuva de Aveiro, Portugal; g = HULIS, HULIS marinho e PLOM de água de neblina de Prairieville, Lousiana; h = aerossóis orgânicos secundários gerados em estudos de câmara derivados do naftaleno e do α-pineno; e i = BrC formado do glicol e sulfato de amônio em solução e os formados do metilglioxial e sulfato de amônio em solução. As setas "j-l" representam as mudanças das posições dos picos nos seguintes casos: j = dimerização do fenol na presença de 1-nitronaftaleno no estado triplete; k = foto-branqueamento dos cromóforos orgânicos pela exposição da água de chuva coletada em Wilmington, EUA à luz solar; e l = fotólise de aerossóis orgânicos secundários do limoneno gerados em estudos de câmara. Figura reproduzida com autorização de Chen et al.60 (direitos autorais (2016) da American Chemical Society)
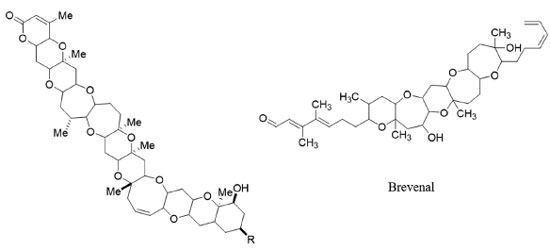
No que se refere aos compostos nitrogenados presentes em aerossóis atmosféricos, estes podem ser de origem tanto biogênica quanto antrópica e são também ubíquos na natureza. A fração em massa de nitrogênio total (do inglês total nitrogen, TN) em aerossóis atmosféricos varia de 1,2-17%.36 De maneira similar ao descrito em relação às espécies de carbono, o TN constitui-se como a soma do nitrogênio orgânico (do inglês organic nitrogen, ON) e do nitrogênio inorgânico (do inglês inorganic nitrogen, INit) (Equação 3). Por sua vez, a fração de ON também podem ser dividida entre os solúveis em água (do inglês water soluble organic nitrogen, WSON) e nitrogênio orgânico insolúvel em água (do inglês water insoluble organic nitrogen, WION) (Equação 4).19,36,48 Entretanto, menos ainda se sabe sobre esses compostos de nitrogênio. Uma fração importante de compostos nitrogenados presentes em aerossóis atmosféricos são o íon amônio (NH4+), seguido por uma série homóloga de aminas primárias, secundárias e terciárias.19,20,36,48 As aminas atmosféricas podem ser emissões primárias dos plânctons ou gerados na atmosfera através da degradação de aminoácidos emitidos por esses mesmos organismos. Aminas são compostos de caráter básico, e são responsáveis, juntamente com a amônia, pela neutralização dos aerossóis atmosféricos. As aminas em condições típicas atmosféricas são majoritariamente emitidas na fase gasosa, mas são rapidamente modificadas, seja pela oxidação com radicais hidroxila (•OH) seja pela reação com compostos de enxofre (tais como nss-SO42-, ou non-sea-salt sulfato, e ácido metanossulfônico), nucleando novas partículas ou se depositando em partículas pré-existentes.68 69 70 71 72 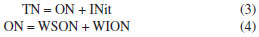 onde: TN = nitrogênio total (do inglês total nitrogen); ON = nitrogênio orgânico (do inglês organic nitrogen); INit = nitrogênio inorgânico (do inglês inorganic nitrogen); WSON = nitrogênio orgânico solúvel em água (do inglês water soluble organic nitrogen); WION = nitrogênio orgânico insolúvel em água (do inglês water insoluble organic nitrogen). O ácido metanossulfônico é o produto da oxidação do dimetilsulfeto (DMS) emitido por fitoplânctons, que posteriormente também se oxida formando nss-SO42-.69 70 71 72 O processo de nucleação de novas partículas, por meio das reações entre compostos de enxofre (ácido metanossulfônico e nss-SO42-) e compostos de nitrogênio (NH4+ e metilaminas) e posterior conversão gás-partícula é extremamente relevante para ambientes marinhos. E considerando-se que as aminas são bases mais fortes que a amônia e que clusters ternários de H2SO4+-H2O-amina são mais estáveis, a importância relativa das aminas na formação de novas partículas ainda precisa ser mais explorada e melhor investigada.19,20,36,48,68 Toxinas em aerossóis marinhos As brevetoxinas (PbTx) são neurotoxinas bloqueadoras dos canais de cálcio que possuem em sua estrutura química poliéter cíclicos. A presença destas toxinas em aerossóis de maré vermelha (reprodução desenfreada de algas vermelhas na superfície do oceano) está associada com o aumento de incidência de asma em humanos.73 Dentre as brevetoxinas produzidas pelo dinoflagelado Karenia brevis, o estudo sobre a composição do aerossol marinho ao longo da Praia da Flórida mostrou que a PbTx-2 foi a mais abundante na água, a PbTx-3 foi a mais abundante no ar, enquanto que a brevenal, uma brevetoxina antagonista, foi detectada tanto em amostras de água quanto em aerossóis74 (Figura 6). A Figura 7 apresenta as fórmulas estruturais para algumas brevetoxinas associadas ao aerossol marinho.
 Figura 6. Racional sobre o estudo de contaminação por toxinas provenientes de algas marinhas em aerossóis atmosféricos. Figura reproduzida de Perez-Medina et al.,75 sob autorização (direitos autorais (2021) reservados para a American Chemical Society)
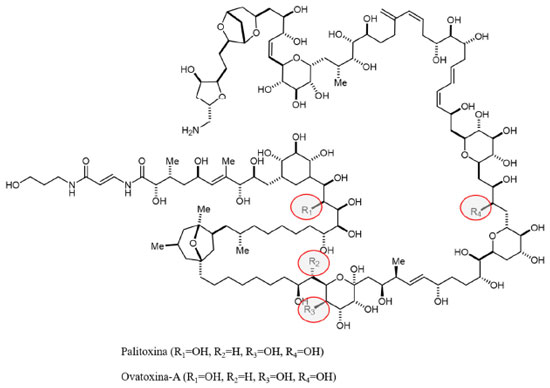
Em costas temperadas do Mar Mediterrâneo, Brasil e Nova Zelândia, eventos de blooms de dinoflagelados do gênero Ostreopsis têm sido relacionados com a mortalidade massiva de organismos bentônicos.75 Um dos eventos que pode estar envolvido, no ainda mal compreendido mecanismo de toxicidade, é a exposição a análogos da palitoxina (PLTX) produzidos pela Ostreopsis (O. cf. ovata), como ostreocinas e ovatoxinas (OVTX), transferidos para os aerossóis marinhos.76 A palitoxina é uma das toxinas marinhas não proteicas mais potentes conhecidas, sua estrutura química possui pequenas diferenças da ovatoxina-A77 (Figura 8).
Com o objetivo de compreender melhor o mecanismo envolvido na aerossolização das toxinas produzidas pelo gênero Ostreopsis, Medina-Perez et al.75 realizaram uma série de experimentos com geração de aerossóis em tanques e análise do perfil químico dos aerossóis por espectroscopia de ressonância magnética nuclear (RMN) de próton (Figura 9). Nos espectros de RMN 1H foi possível observar que o material particulado (POC, em azul) é dominado por peptídeos (rastreados por aminoácidos, como alanina, treonina, valina, isoleucina e leucina) e por açucares ou polióis (com sinais na região H−C−O com deslocamento químico entre 3,3 e 4,2 ppm, além de sinais referentes ao átomo de hidrogênio anomérico característico dos monossacarídeos mais comuns, com deslocamento químico entre 5,0 e 5,5 ppm). Os espectros de RMN 1H das bolhas aerossolizadas (bubble bursting, em vermelho na Figura 9) mostraram pouca sobreposição com os espectros do material particulado. Observa-se nos espectros das bolhas aerossolizadas sinais intensos para o ácido isobutírico e o glicerol. Em resumo, os resultados do perfil químico avaliados por RMN 1H mostraram que o processo de aerossolização no tanque enriquece aerossóis marinhos com lipídios e oligoaçúcares pequenos, enquanto os esgota de aminoácidos livres e peptídeos em geral, resultando em uma população de aerossóis na atmosfera com uma composição muito diferente da água.75 Os autores evidenciaram que o carbono orgânico particulado em água era drasticamente diferente dos aerossóis produzidos nos experimentos em tanques, o que sugere uma transferência seletiva de compostos orgânicos da água do mar para a atmosfera. Os resultados obtidos abriram novas oportunidades de pesquisa relacionadas a toxinas marinhas aerossolizadas e forneceram novos insights sobre a distribuição e transferência do material orgânico tóxico da água para a atmosfera.75
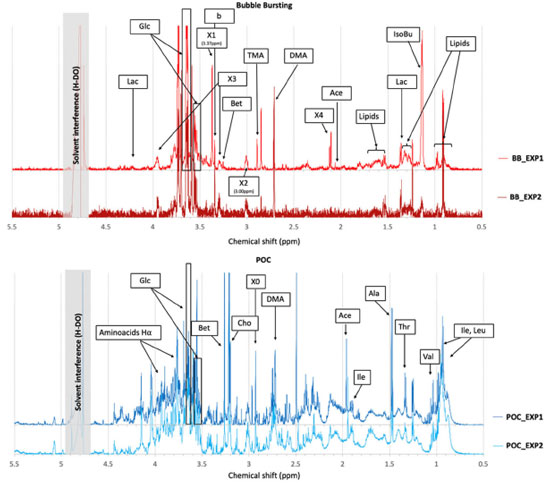 Figura 9. Região alifática dos espectros de NMR 1H obtidos em experimentos de aerossóis atmosféricos em bubble bursting (BB_EXP1 e BB_EXP2, espectros em vermelho) e de material particulado na água (POC_EXP1 e POC_EXP2, espectros em azul). Nas amostras de bubble bursting os sinais de ressonância de RMN 1H foram atribuídas ao ácido láctico (Lac), ácido acético (Ace), ácido isobutírico (IsoBu), di- e tri-metilaminas (DMA e TMA), glicerol (Glc), N-osmólitos (somente Bet: betaína). No espectro de material particulado, os sinais de NMR 1H foram atribuídas aos resíduos de aminoácidos (Ala, Thr, Val, Ile e Leu) e seus átomos de hidrogênio alfa, ácido isobutírico (IsoBu), ácido acético (Ace), DMA, N-osmólitos (Bet: betaína; Cho: colina) e glicerol (Glc). O pico em 2,92 ppm (rotulado como X0) assemelha-se ao metil do dimetilsulfoniopropionato (DMSP), não confirmado pela ausência dos sinais característicos em 2,8 e 3,49 ppm. Misturas não resolvidas de compostos alifáticos foram identificadas como lipídios. Picos ou estruturas indicadas como X# correspondem a ressonâncias ainda não atribuídas a traçadores específicos, mas já identificadas em estudos anteriores.75 Figura reproduzida de Perez-Medina et al.,75 sob autorização da American Chemical Society (direitos autorais (2021) reservados para a ACS)
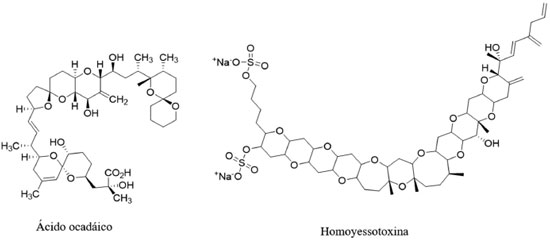
Van Acker et al.78 realizaram o primeiro estudo que evidenciou e caracterizou a aerossolização de ficotoxinas que (ainda) não foram associadas a efeitos no sistema respiratório humano. Para o desenvolvimento do método analítico os pesquisadores adicionaram cepas das microalgas tóxicas Prorocentrum lima e Protoceratium reticulatum, organismos capazes de produzir as fitotoxinas ácido ocadáico, homoyessotoxina e dinofisistoxina-1, para a produção controlada de aerossol de spray marinho em aquários (Figura 10). De acordo com os autores, o potencial de aerossolização dessas ficotoxinas foi destacado por seu enriquecimento de 78 a 1769 vezes em aerossol de spray marinho em relação à água. Com o método analítico estabelecido, os autores quantificaram de maneira indireta a concentração destas toxinas no ar costeiro da Bélgica, o que permitiu quantificar a magnitude (inofensiva) das concentrações do ácido ocadáico (0,6-51 pg m-3). Além disso, este estudo destaca que apesar dos efeitos adversos das toxinas, os aerossóis de spray marinho podem fornecer uma rota de exposição para todo um espectro de compostos marinhos com efeitos farmacológicos positivos.
Contribuições de compostos de combustão de matéria orgânica para o aerossol marinho Em geral, as fontes de compostos orgânicos nos aerossóis marinhos compreendem naturais e antrópicas, as quais as massas de ar terrestre podem transportar matéria orgânica abundante a longas distâncias.79,80 Diversos estudos têm demonstrado o transporte a longas distâncias de diferentes classes de poluentes orgânicos atmosféricos, podendo atingir e impactar em aerossóis marinhos.21,66,81,82 Assim, traçadores moleculares orgânicos desempenham um papel importante no rastreamento e identificação das fontes de emissões para os oceanos, tendo como ponto de atenção a avaliação do transporte dos produtos da queima de biomassa.83 A queima de biomassa é um fenômeno globalmente difundido, incluindo incêndios florestais, corte e queima de terras florestais para uso agrícola, queima de resíduos agrícolas no campo e a queima de madeira residencial para cozinhar e para fins de aquecimento. Consequentemente, os gases e partículas liberadas durante a queima da biomassa podem ser transportadas para longas distâncias das fontes de emissão. Com isso, a concentração de compostos provenientes da queima de biomassa nas regiões marinhas é controlada, principalmente, pelo transporte de poluentes a longas distâncias.84 Apesar da possibilidade de as atividades de queima de biomassa afetarem as mudanças climáticas, ainda existem muitos desafios na identificação e quantificação de aerossóis provenientes destas fontes, e seus impactos ao meio ambiente.85 Os aerossóis da queima de biomassa influenciam o sistema climático afetando o balanço radiativo da Terra, atuando como núcleos de condensação de nuvens.86 Fu et al.18 avaliaram as composições orgânicas de aerossóis marinhos coletados em diferentes oceanos, durante um cruzeiro ao redor do mundo. As concentrações de compostos orgânicos totais quantificados variaram de 0,94 a 111 ng m-3 (média de 34 ng m-3). Destacam-se os produtos da queima de biomassa (24%) como uma das principais fontes de compostos orgânicos marinhos no oeste do Pacífico Norte. De uma maneira geral, a biomassa é composta essencialmente por celulose, hemicelulose e lignina. A celulose é um polímero de glicose enquanto as hemiceluloses contêm, além da glicose, vários outros monômeros de açúcar (por exemplo, galactose e manose). A lignina é um polímero fenólico que une a celulose e a hemicelulose, formando a parede celular da planta. Quando ocorre a combustão de biomassa, grandes quantidades de numerosos compostos orgânicos são produzidos a partir da combustão de celulose e hemicelulose, incluindo anidroaçúcares, hidrocarbonetos policíclicos aromáticos (HPAs), metoxifenóis, ácidos resínicos, esteroides e terpenoides. Assim, o conteúdo de compostos orgânicos em aerossóis atmosféricos podem resultar da volatilização das moléculas orgânicas da biomassa, seguida de sua condensação, ou da pirólise de biopolímeros da biomassa.83,87 Algumas moléculas de açúcares são geralmente usadas para elucidar fontes e transporte de aerossóis orgânicos atmosféricos. Nesse sentido, anidroaçúcares (tais como levoglucosano, manosano e galactosano) (Figura 11) são reconhecidos como produtos de alteração térmica primária da pirólise de celulose e hemicelulose (importante fenômeno observado durante queimadas florestais, por exemplo) e vêm sendo considerados como principais traçadores primários, nos aerossóis atmosféricos oriundos da queima de biomassa. Estudos mostram que estas moléculas foram detectadas em alguns aerossóis marinhos e, com isso, estão sendo consideradas para a avaliação das contribuições de diferentes fontes de emissão de compostos orgânicos para a atmosfera.79,83,88,89 De acordo com Bhattarai et al., 90% das concentrações em massa do levoglucosano estão acumuladas em partículas com diâmetros aerodinâmicos inferiores a 2 µm.84
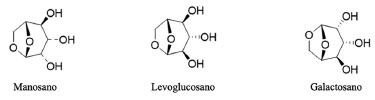 Figura 11. Estruturas químicas do manosano, levoglucosano e galactosano
Um método usando a cromatografia de troca aniônica de alto desempenho com detecção amperométrica pulsada (HPAEC-PAD) foi proposto para a determinação simultânea de açúcares neutros (fucose, ramnose, arabinose, galactose, glicose, manose, xilose, frutose e ribose), alditóis (xilitol, arabitol, sorbitol e manitol) e anidroaçúcares (levoglucosano, manosano e galactosano) e um dissacarídeo (sacarose) comumente encontrados em amostras atmosféricas e marinhas. Os resultados deste estudo mostraram que o levoglucosano (261 ng m-3) e sacarose (178 ng m-3) estavam entre os principais carboidratos neutros encontrados em amostras de material particulado total (do inglês total suspended particulate, TSP). A aplicação do método revelou que os açúcares anidros representaram 53% do total de açúcares neutros nas amostras coletadas. Os autores relatam que a presença de anidroaçúcares, como o levoglucosano e/ou manosano, nas amostras marinhas indicou claramente uma possível entrada terrestre destas substâncias, muito provavelmente via deposição atmosférica, pois esses compostos são considerados marcadores de queima de biomassa terrestres.90 Estudos na Antártida têm demonstrado a presença de levoglucosano em aerossóis marinhos, proveniente do transporte de aerossóis a longas distâncias, uma vez que esta região é cercada pelo oceano, contém pouca ou nenhuma fonte de queima de biomassa, carece de assentamentos humanos estáveis e, portanto, apresenta-se como um laboratório natural para investigar aerossóis de queima de biomassa após transporte a longas distâncias.86 Portanto, o levoglucosano é considerado um traçador ideal para queima de biomassa em aerossóis devido à sua alta taxa de emissão e especificidade com relação a fonte, sendo avaliada e monitorada em estudos de qualidade do ar.21 A abundância relativa de levoglucosano, galactosano e manosano no aerossol atmosférico é afetada significativamente pelo tipo de biomassa/biocombustível queimado e pelas condições de combustão, exibindo, dessa forma, grandes variações. Entretanto, a relação L/M (levoglucosano/manosano) varia significativamente nos produtos de queima de madeiras de lei (angiospermas), madeiras macias (gimnospermas) e resíduos agrícolas.87 Taxas mais baixas para a razão L/M (2-4) têm sido relatadas para combustão de madeiras macias, enquanto taxas mais altas (> 10) têm sido associadas a combustão de madeiras de lei.91 Compostos fenólicos derivados da pirólise de lignina e ácido de resina (por exemplo, ácido dehidroabiético) proveniente da queima de plantas coníferas também podem ser usados como biomarcadores da queima de biomassa em aerossóis atmosféricos.92 A lignina é o terceiro polímero natural ou biopolímero mais abundante depois da celulose e hemiceluloses, sendo a substância orgânica polimérica aromática mais abundante no reino vegetal. É composta de macromoléculas que constituem a principal estrutura vascular das plantas, sendo formada por três álcoois aromáticos diferentes (álcoois p-cumarílico, coniferílico e sinapílico), onde suas proporções diferem entre as principais classes de plantas (Figura 12).83,86,93
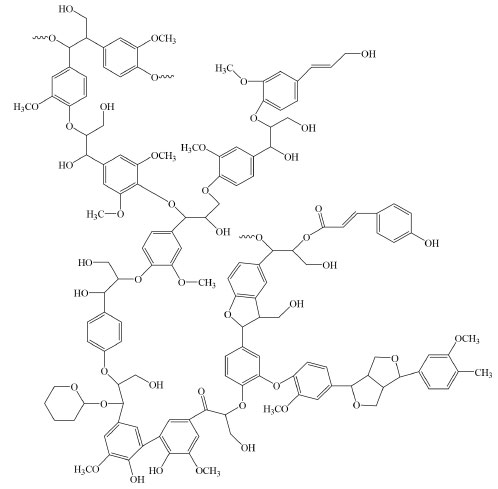 Figura 12. Estrutura química da lignina
A queima de lignina, em altas temperaturas, libera uma variedade de produtos metoxifenóis, como álcool homovanílico, vanilina, ácido vanílico, siringaldeído, ácido siríngico, p-hidroxibenzaldeído e ácido p-hidroxibenzóico (Figura 13). Portanto, além dos anidroaçúcares, compostos como ácido vanílico, ácido p-hidroxibenzoico, ácido siríngico são produtos abundantes da queima da lignina e também têm sido amplamente utilizados como marcadores moleculares orgânicos em aerossóis atmosféricos da queima de biomassa.83,84,92 Quando são transferidos para a atmosfera, durante a queima de biomassa, as proporções dos compostos fenólicos são indicativas do tipo de madeira queimada.94
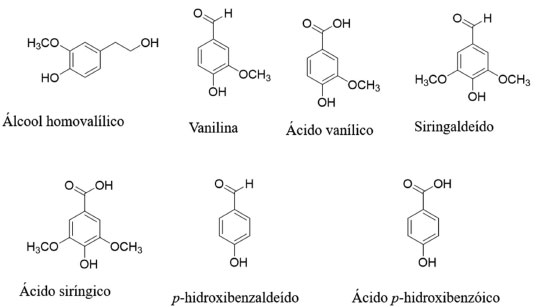 Figura 13. Estruturas químicas de compostos fenólicos provenientes da queima de biomassa, identificados em aerossóis atmosféricos
A lignina de madeira dura (angiosperma) é enriquecida em precursores de álcool sinapílico, de modo que a queima dessas plantas produz principalmente frações siringila e vanilila. Por sua vez, as madeiras macias (gimnospermas) contêm altas proporções de álcool coniferílico com componentes menores de álcool sinapílico e, com isso, a queima deste tipo de biomassa produz principalmente frações de vanilila.86 Zangrando et al. determinaram levoglucosano e compostos fenólicos (incluindo ácido vanílico, ácido isovanilico, ácido homovanílico, ácido siríngico, vanilina, siringaldeído, ácido ferúlico, ácido p-cumárico e coniferaldeído) no aerossol marinho de diversos locais da Antártida e observaram que a maior parte da massa de levoglucosano apresentou-se distribuída na fração grossa dos MAs (24,8 pg m-3), enquanto os compostos fenólicos estavam presentes em partículas finas dos MAs (34,0 pg m-3). Ao contrário do levoglucosano, que pode ser produzido apenas pela queima de biomassa, os compostos fenólicos podem ser provenientes tanto da queima de biomassa quanto de outras fontes. Os autores demonstraram, por meio de razões diagnóstico entre L/CF (levoglucosano/compostos fenólicos) que as fontes marinhas locais predominaram na determinação de compostos fenólicos na Antártida e as concentrações de levoglucosano estavam relacionadas a aerossóis de queima de biomassa advindos de fontes regionais, e não locais.86 As concentrações de um ácido aromático individual em aerossóis dependem da quantidade, condições de queima e tipo de biomassa. Estima-se que baixas concentrações de ácido siríngico sejam resultantes da baixa quantidade de emissões de combustão de madeira, enquanto altas concentrações de ácido p-hidroxibenzóico estejam relacionadas à queima de plantas herbáceas.95 Entretanto, a razão de concentração de ácido vanílico/ácido siríngico (VA/SyA) tem sido amplamente utilizada para identificar a fonte de queima de biomassa em AMs. As razões VA/SyA para madeira de lei variam de 0,12 a 4,00 e para madeira macia variam de 8,57 a 11,9, enquanto as razões associadas à queima de plantas herbáceas ou gramíneas situam-se entre os dois tipos de combustíveis (0,40 a 5,03). Contudo, a sobreposição das razões VA/SyA pode dificultar a contribuição das fontes, especialmente se houver mais de duas fontes de emissão.83,96 O ácido dehidroabiético (Figura 14) é produzido por desidratação pirolítica de ácido abiético da resina de coníferas, ou seja, sua produção ocorre durante o processo de queima de resina de coníferas, possibilitando que esta substância seja utilizada também como um marcador atmosférico específico de queima de biomassa para árvores coníferas e outras madeiras macias contendo resina.85 Estudos realizados por Chen et al.,97 mostraram que o ácido dehidroabiético foi a espécie predominante (40,6 ± 67,2 ng m-3) na determinação de ácidos aromáticos como biomarcadores de queima de biomassa, seguido pelo ácido p-hidroxibenzóico (24,8 ± 23,2 ng m-3), ácido vanílico (19,7 ± 16,6 ng m-3) e ácido siríngico (14,5 ± 9,6 ng m-3), em amostras de material particulado total (TPS) coletadas em Dushanbe (Tajiquistão). Os resultados comprovaram que a queima de biomassa contribuiu significativamente para a presença de compostos fenólicos e ácidos de resina em aerossóis atmosféricos da região estudada.97
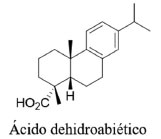 Figura 14. Estrutura química do ácido dehidroabiético, proveniente da queima de resina de coníferas
Os incêndios florestais são um grave problema em todo o mundo, afetando diretamente na formação de fumaça de biomassa e emitindo vários compostos oxigenados em aerossóis atmosféricos. Concentrações de até 4.320 ng m-3 de levoglucosano, 322,6 ng m-3 de galactosano e 262,2 ng m-3 de manosano foram encontradas na Floresta Amazônica em amostras de PM10 (material particulado com diâmetro aerodinâmico menor ou igual a 10 µm) coletadas durante a estação seca uma vez que, durante este período, são observados os maiores focos de incêndios florestais na região, principalmente proveniente da combustão de madeiras de lei.98 A ocorrência de incêndios florestais pode ser provocada intencional e/ou acidentalmente pelos seres humanos, embora fenômenos naturais como a atividade vulcânica e relâmpagos também levam a esta ocorrência.86 Conforme mencionado por Silveira et al., o fogo está entre os principais tipos de perturbação responsáveis pela degradação florestal na Amazônia. Nesta região, a maioria das fontes de ignição decorre do uso do fogo para renovar a vegetação de pastagens degradadas e limpar o excesso de biomassa após o desmatamento. Em termos de área queimada, Brasil e Bolívia contribuíram em média com 56% e 33%, respectivamente, da área anual queimada na Amazônia entre os anos de 2003 e 2020, destacando-se o agravamento do total de áreas atingidas por incêndios entre os anos de 2019 e 2020, quando houve um enfraquecimento das operações de controle ambiental na região em meio à pandemia de COVID-19.99,100 A Floresta Amazônica é um grande regulador do clima do planeta. A evapotranspiração da floresta alimenta os extensos "rios voadores" (massas de ar contendo elevada quantidade de vapor d'água que se formam na região equatorial do Oceano Atlântico) e que percorrem altas camadas da atmosfera (3-5 km de altura), a longas distâncias. A floresta retroalimenta essas massas de ar de vapor d'água que transportam a umidade da Amazônia para o centro-oeste, sudeste e sul do Brasil, incluindo as áreas costeiras do sul e sudeste, os quais podem conter grande proporção de produtos de queima de biomassa atingindo, principalmente, diferentes regiões do Oceano Atlântico Sul.101,102 Portanto, o transporte de aerossóis dos continentes para o ambiente marinho (incluindo produtos da queima de biomassa) representa uma importante fonte de contribuição para o aerossol marinho, uma vez que os aerossóis continentais são facilmente transportados para regiões marinhas pelas correntes de massas de ar que transitam no sentido da terra para o mar.7,103 Emissões por embarcações em ambiente marinho As emissões atmosféricas geradas em processos de combustão incompleta de combustíveis de origem fósseis são consideradas um grande problema ambiental. No ambiente marinho, uma fonte importante de poluentes atmosféricos é a emissão de embarcações proveniente da queima de diesel, apesar de existirem restrições cada vez maiores (decorrentes de regulamentações), o que leva a necessidade de busca por soluções, tais como a adoção de combustíveis alternativos para aplicação naval.104 105 106 Nos últimos anos, observou-se um aumento acentuado no tamanho da frota naval global, fomentado pela alta demanda do comércio marítimo mundial. Segundo Siriname et al.,107 80% de todas as mercadorias comercializadas no mundo são transportadas por navios. No entanto, apesar do transporte marítimo internacional ser considerado a forma mais eficiente em termos energéticos para deslocamentos a longas distâncias, a poluição promovida pela emissão de gases de efeitos danosos na combustão dos motores a diesel tem causado um grave impacto na saúde humana e no ecossistema marinho.108,109 Os combustíveis convencionais usados nos navios são formados por uma mistura de hidrocarbonetos, resultando em uma grande variedade de combustíveis a depender das fontes e do processamento a partir dos quais foram obtidos. Esses combustíveis podem ser classificados em residuais e destilados.110 Os combustíveis marítimos residuais, também conhecidos como óleo bunker, são misturas de frações residuais pesadas, provenientes do refino do petróleo, com diluentes, que são frações mais leves utilizadas para o ajuste da viscosidade e demais propriedades.111 Os combustíveis marítimos destilados são constituídos por correntes destiladas que podem conter traços de frações residuais dependendo da carga, sendo utilizados, principalmente, em embarcações de pequeno porte e motores auxiliares navais.111,112 Atualmente, o óleo combustível pesado é o mais utilizado para a alimentação do motor naval, enquanto o óleo diesel marítimo e gasóleo marítimo são normalmente usados para motores auxiliares e operação em portos. As cinco principais categorias de combustíveis navais, classificados de acordo com sua viscosidade e misturas são:113 (i) gasóleo marítimo (do inglês marine gas oil, MGO) que possui características próximas ao diesel utilizado em veículos terrestres; (ii) diesel marítimo (do inglês marine diesel oil, MDO) que se diferencia do MGO por conter uma mistura com óleos pesados; (iii) óleo combustível pesado (do inglês heavy fuel oil, HFO) que é constituído pelas frações residuais da destilação do petróleo; (iv) óleo combustível intermediário (do inglês intermediate fuel oil, IFO) que é similar ao diesel marinho, constituído por uma mistura residual de HVO e MGO; e óleo combustível marítimo (do inglês marine fuel oil, MFO) que apresenta características parecidas com o HFO e é constituído por uma mistura de HFO e MGO, contendo menor quantidade de IFO. O processo de combustão desses combustíveis marítimos citados anteriormente gera preocupações acerca das emissões atmosféricas (emissão de material particulado, NOx, SOx, compostos orgânicos voláteis e dióxido de carbono) devido as contribuições para aumento dos gases de efeito estufa (GEE) e outros impactos ambientais.114 Estima-se que as emissões de CO2 tenham aumentado de 31,4% entre 1970 e 2015, com cerca de 77% desse crescimento decorrente do setor marítimo.115 Em 2012, a indústria de transporte naval consumiu 300 milhões de toneladas de combustíveis derivados de fontes fósseis, emitindo 2-4% de dióxido de carbono, 10-13% de óxido de nitrogênio e 4-9% de dióxido de enxofre em todo o mundo. Em 2013, 77% do combustível marítimo utilizado foi óleo combustível pesado (HFO), produzido a partir do resíduo do refino de petróleo, que apresenta altos teores de enxofre e outras impurezas.109 É importante destacar que a emissão primária de aerossóis, oriunda da queima de combustíveis em ambiente marinho, pode contribuir de forma negativa para aumento da formação de aerossóis secundários atmosféricos. Assim, pode-se destacar as emissões primárias de material particulado neste processo de queima que compreende uma mistura complexa de matéria orgânica queimada e não queimada de combustível e óleo lubrificante, carbono elementar (CE), sulfato, nitrato, cinzas e outros. Assim, aerossóis secundários podem ser formados a partir de oxidação em fase gasosa, reações heterogêneas nas superfícies dos aerossóis primários e reações químicas multifásicas de compostos orgânicos em fase gasosa.116 Além disso, a emissão de compostos orgânicos na fase gasosa, como por exemplo compostos carboxílicos, podem também aumentar a formação de compostos secundários indesejáveis na atmosfera, como é o caso da formação de ozônio troposférico que se intensifica com as radiações solares e emissão de óxidos de nitrogênio.116 A demanda por combustível marinho vem crescendo diretamente com o desenvolvimento da economia mundial, tornando-se necessária a diminuição das emissões geradas por esse setor. Com isso, o International Marine Oil (IMO) está se voltando cada vez mais ao controle dos poluentes originados do setor marítimo.117 Desde 2020, o teor máximo de enxofre em combustíveis marítimos é estabelecido em 0,5% (ou 500 ppm), em massa. Em algumas áreas do globo, essas especificações são ainda mais restritivas, como no Mar Báltico, Mar do Norte, partes da América do Norte e a área caribenha dos Estados Unidos, onde, o limite de sulfurados é de 0,1% em massa. Além disso, em 2018, a IMO também se comprometeu com a redução da emissão de carbono no transporte marítimo em 40% (em relação aos níveis de 2008) até 2030 e em 70% até 2050.105,118 No Brasil foi estabelecido, através da Resolução ANP nº 903 de 18/11/2022,119 o teor máximo de enxofre em combustíveis marítimos de 0,5% (em massa). Além disso, no Artigo 3º estabelece que a adição obrigatória de biodiesel aos combustíveis aquaviários só será determinada quando as condições técnico-operacionais para o uso seguro da mistura estiverem estabelecidas, o que sugere que a demanda por pesquisas científicas e tecnológicas são altamente necessárias.119 Apesar do estabelecimento das restrições implementadas pela IMO, Bach e Hansen120 destacaram três desafios principais para uma regulamentação mais consistente, abrangente e rigorosa das emissões de GEE do transporte marítimo internacional: (i) falta de capacidade dentro da IMO para regular tecnologias múltiplas e emergentes; (ii) incerteza em torno do mandato regulatório da IMO; e (iii) falta de consenso político durante as negociações. Para que a IMO desempenhe um papel mais progressivo na mitigação das mudanças climáticas, esses fatores precisam ser considerados para garantir que a combinação de instrumentos políticos seja capaz de alcançar as metas de redução de emissões estabelecidas. Essas novas regulamentações têm provocado um impacto positivo no estudo e desenvolvimento de biocombustíveis alternativos e tecnologias, que possuam características promissoras à aplicação em motores náuticos e que possuam fontes renováveis e menores impactos ambientais. Na Tabela 1S (material suplementar) são destacados os estudos realizados com intuito de trazer respostas e apoio às políticas públicas, visando mitigar os impactos ambientais causados pelos motores marítimos. Os resultados das pesquisas apresentados na Tabela 1S destacam que a utilização de tecnologias com sistemas de pós-tratamento de gases de exaustão e uso de combustíveis alternativos aos combustíveis fósseis pode ser o caminho para a redução dos impactos ambientais gerados nos ambientes marinhos e costeiros.
OS AEROSSÓIS MARINHOS E AS IMPLICAÇÕES À DÉCADA DAS CIÊNCIAS OCEÂNICAS Os oceanos representam nesse início do século 21, desafios e oportunidades que, uma vez enfrentados de forma correta, poderão contribuir para a promoção de um ambiente global socialmente seguro, ambientalmente sustentável e economicamente próspero. A Década da Ciência dos Oceanos para o Desenvolvimento Sustentável, promovida para acontecer entre 2021 e 2030, é, conforme a Organização das Nações Unidas (ONU), uma oportunidade única das nações trabalharem juntas, em prol de gerar conhecimento científico global, necessário para a promoção do desenvolvimento sustentável de nossos oceanos compartilhados. Em um de seus lemas: "A Ciência que precisamos para o oceano que queremos", está explicitada a estratégia, projetada para alcançar os resultados visados, quais sejam: "estimular e coordenar esforços para pesquisa interdisciplinar em todos os níveis, de maneira a gerar e usar conhecimentos, para a ação transformadora necessária para se alcançar um oceano saudável, seguro e resiliente, para um desenvolvimento sustentável por volta de 2030 e além". Fica claro, assim, que para alcançar os objetivos desenhados acima, será fundamental um desenvolvimento científico integrado nas suas diferentes dimensões, que vise a compreensão dos problemas para o encontro das soluções mais adequadas. Entre os dezessete Objetivos de Desenvolvimento Sustentável (ODS) fixados pela ONU na Agenda 2030, o ODS 14 - Vida na Água, estabelece 10 metas que visam "Conservar e usar de forma sustentável os oceanos, mares e os recursos marinhos para o desenvolvimento sustentável."121 A capacidade dos oceanos em absorver o excesso de CO2 e o calor, produzidos por atividade humana, é imensa. Todavia, isso vem levando a uma situação de grande estresse global. A quantidade de calor extra absorvida, produzida a partir do aumento das concentrações atmosféricas de gases-estufa, principalmente CO2, já ocasionou um aumento médio da temperatura dos oceanos em cerca de 0,4 °C desde os anos 1950, observado especialmente em sua superfície, podendo levar à menor circulação das correntes marítimas e à diminuição da capacidade de mistura nas camadas verticais em lâminas d'água, afetando, por exemplo, a disponibilização de nutrientes. O aumento na temperatura dos oceanos já traz também sérias implicações para a regulação do clima, como, por exemplo, o aumento na frequência de eventos climáticos extremos (secas, inundações, dentre outros). Ele também reduz a quantidade de oxigênio dissolvido na água. Em seu conjunto, esses fatores tendem a acarretar a ameaça não somente à sobrevivência de diferentes espécies marinhas, mas também à segurança de populações que dependem desses recursos para sua subsistência.122 A absorção de CO2 pelos oceanos representa mais de 1 milhão de toneladas de CO2 fóssil por hora.123 Estima-se que isso represente cerca de 26% da emissão crescente desse gás-estufa. Como efeito direto, vem ocorrendo um decréscimo nos valores de pH da água do mar, refletindo em sua crescente acidificação. Ao longo de milhões de anos, o pH médio da água do mar oscilou regularmente entre 8,0 e 8,2, com ligeiras variações locais e sazonais. Na hipótese de que as emissões de CO2 permaneçam nos níveis atuais, modelos projetam que o seu valor atinja 7,8 por volta de 2100.124 Considerando a escala logarítmica do pH, isso representaria um aumento na concentração de íons H+ na água de quase duas vezes, em pouco mais de 100 anos! As maiores concentrações de íons H+ ocasionam decréscimo na disponibilidade de íons CO32-, vitais, por exemplo, para a formação da carapaça protetora de variedades de crustáceos e moluscos. Já foi observado em regiões do Pacífico Norte que, durante a emersão de águas com maior acidez, houve impactos sobre a formação e o crescimento em populações de conchas e mariscos.124 A poluição dos oceanos, derivada de atividades antrópicas em áreas costeiras ou próximas ao litoral, é também significativa e diversificada. De acordo com o Programa das Nações Unidas para o Meio Ambiente (UNEP), as cidades irão produzir globalmente cerca de 2,2 bilhões de toneladas de resíduos descartáveis, anualmente, até 2025, o que representa mais de três vezes a quantidade gerada em 2009.125 Além desses, outras importantes fontes de poluição para os oceanos compreendem esgotos domésticos não tratados; descargas de resíduos de pesticidas e fertilizantes, provenientes de atividade agrícola; descargas de efluentes de indústrias; descarte de plásticos; vazamentos ou descarga de tanques de navios, dentre outros. Deve-se considerar, igualmente, que uma parte considerável dos poluentes transportados na atmosfera, acaba sendo absorvida através de trocas atmosfera-oceano. Igualmente preocupante, a agricultura, praticada de forma intensiva em grandes extensões de áreas continentais, tem levado ao uso crescente de fertilizantes e pesticidas e à geração de grande quantidade de resíduos. Estes, quando carregados até os oceanos, através de rios ou por transporte pelo ar, seguido por processos de deposição, propiciam a formação de zonas mortas ou de hipóxia, reduzindo assim a extensão de áreas propícias à alimentação e reprodução de espécies de valor nutricional. Na indústria química, uma enorme quantidade de novos produtos e substâncias são criados e colocados no mercado a cada ano.126 Nesse grupo incluem-se, por exemplo, novos pesticidas, fármacos, produtos de cuidados pessoais, e outras substâncias usualmente classificadas como "Contaminantes Emergentes". Caso seu descarte não seja efetuado de maneira adequada, seu destino final poderá ser, uma vez mais, os oceanos. Diante do cenário descrito até aqui, observa-se que com a modificação antrópica do ambiente, leva-se a modificação da composição química das águas dos oceanos (tanto de regiões costeiras quanto de mar aberto) que pode levar a modificação das populações de organismos marinhos e seus metabolismos. Desse modo, altera-se também a biogeoquímica da SML, o padrão de transferência de massa e de energia da interface oceano-atmosfera, e, consequentemente, a biogeoquímica dos aerossóis atmosféricos de regiões marinhas, alterando sua complexidade, e possivelmente, seus efeitos potencialmente negativos à saúde humana e ao meio ambiente. Considerando-se que as diversas fontes de poluição acima mencionadas podem levar à formação de diferentes tipos de MAs de origem antrópica, e que os mesmos são provavelmente modificados através de uma variedade complexa de processos biogeoquímicos, sendo em muitos casos transportados por centenas ou milhares de quilômetros até regiões costeiras e oceano aberto, ao longo dos quais sofrem uma série de transformações físicas, químicas e biológicas, torna-se evidente, no escopo dos temas tratados na Década da Ciência dos Oceanos para o Desenvolvimento Sustentável, a necessidade de gerar conhecimentos que levem ao maior entendimento dos processos de formação e transformação de MAs, bem como os prováveis mecanismos para a sua remoção, para que, entre outros aspectos, possa-se atingir uma maior compreensão sobre como atingir a meta de um oceano saudável, seguro e resiliente, para um desenvolvimento sustentável.
CONCLUSÕES E TENDÊNCIAS DE ESTUDOS FUTUROS Através dos tópicos abordados no decorrer do texto, foram apresentadas a relevância das frações orgânicas e inorgânicas dos aerossóis atmosféricos de regiões marinhas bem como sua contribuição para a física e a biogeoquímica dos compostos de carbono, nitrogênio e enxofre da atmosfera e sua relação com os oceanos, para o balanço radiativo do planeta e suas implicações para a regulação do clima do sistema Terra. Os MAs podem ser constituídos tanto por componentes de origem biogênica quanto antrópica, e que ambos provavelmente são formados e/ou modificados através de uma variedade intrincada de processos biogeoquímicos. E que apesar de sua relevância, os MAs representam as maiores incertezas em modelos climáticos atuais. As frações orgânica e inorgânica de aerossóis atmosféricos de regiões marinhas e de zonas costeiras são formados tanto por processos naturais e antrópicos e através de processos primários e secundários, que aumentam consideravelmente a sua complexidade. Entretanto, ainda muito pouco é compreendido pela ciência como se dá a formação, transformação, modificação fotoquímica e degradação desses componentes. Logo, tornam-se extremamente necessários o desenvolvimento de novos estudos considerando os MAs. Para tanto, são apontadas algumas tendências de estudos em P&D&I associados aos MAs:
LISTA DE ABREVIAÇÕES MAs: aerossóis marinhos BC: black carbon BrC: brown carbon BVOC: biogenic volatile organic compounds CCN: cloud condensation nuclei DMS: dimetil sulfeto DOM: dissolved organic matter EC: elemental carbon EED: emission-excitation diagram GC: gas chromatography GEE: gases do efeito estufa HFO: heavy fuel oil HULIS: humic-like substances IFO: intermediate fuel oil IMO: International Marine Oil IN: ice nuclei INit: inorganic nitrogen MDO: marine diesel oil MFO: marine fuel oil MGO: marine gas oil nss-SO42-: non-sea sulfate OC: organic carbon ODS: Objetivos do Desenvolvimento Sustentável ON: organic nitrogen ONU: Organização das Nações Unidas PACs: polycyclic aromatic compounds PbTx: brevetoxinas POM: particulate organic matter PLOM: protein-like organic matter SML: sea surface marine layer SOA: secondary organic aerosols SPE: extração em fase sólida TC: total carbon TN: total nitrogen UCM: unresolved complex mixture UNEP: United Nations Environmental Program VOC: volatile organic compounds WIOC: water insoluble organic carbon WION: water insoluble organic nitrogen WSOC: water soluble organic carbon WSOM: water soluble organic matter WSON: water soluble organic nitrogen
MATERIAL SUPLEMENTAR Uma tabela (Tabela 1S) apresentando estudos de aplicação de novos biocombustíveis e tecnologias em motores marinhos está disponível em http://quimicanova.sbq.org.br, na forma de arquivo PDF, com acesso livre.
AGRADECIMENTOS Os autores gostariam de agradecer a Agência Nacional de Desenvolvimento Científico e Tecnológico (CNPq), Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES, código de financiamento 001), Serviço Nacional de Aprendizagem Industrial, Departamento Regional da Bahia (SENAI CIMATEC), ao Instituto Nacional de Ciência e Tecnologia em Energia & Ambiente (INCT E&A, projeto CNPq, nº 465497/2014-4) e o Centro Interdisciplinar em Energia e Ambiente (CIEnAm) da Universidade Federal da Bahia. Os autores também agradecem os suportes financeiros provenientes dos Projetos: MEPHYSTO (Biocomplexidade e Interações Físico-Químico-Biológicas em Múltiplas Escalas no Atlântico Sudoeste), integrante do Programa Antártico Brasileiro (CNPq nº 442695/2018-7), Projeto Pesquisando Kirimurê: Convergindo Educação, Ciência, Tecnologia e Inovação (CNPq nº 442187/2018-1) e Fundação de Amparo à Pesquisa do Estado da Bahia (FAPESB # 5545/2019). O presente estudo é uma contribuição para o Projeto AtlantECO do Edital Horizon 2020 da União Europeia, sob o grant nº 862923. O presente estudo reflete as opiniões apenas dos autores, e a União Europeia não poderá ser considerada responsável por quaisquer usos que poderão ser feitos a partir das informações contida nesse estudo. G. O. R. e L. L. N. G. agradecem pelas suas bolsas de pesquisa do CNPq.
REFERÊNCIAS 1. Prather, K. A.; Bertram, T. H.; Grassian, V. H.; Deane, G. B.; Stokes, M. D.; DeMott, P. J.; Aluwihare, L. I.; Palenik, B. P.; Azam, F.; Seinfeld, J. H.; Moffet, R. C.; Molina, M. J.; Cappa, C. D.; Geiger, F. M.; Roberts, G. C.; Russell, L. M.; Ault, A. P.; Baltrusaitis, J.; Collins, D. B.; Corrigan, C. E.; Cuadra-Rodriguez, L. A.; Ebben, C. J.; Forestieri, S. D.; Guasco, T. L.; Hersey, S. P.; Kim, M. J.; Lambert, W. F.; Modini, R. L.; Mui, W.; Pedler, B. E.; Ruppel, M. J.; Ryder, O. S.; Schoepp, N. G.; Sullivan, R. C.; Zhao, D.; Proc. Natl. Acad. Sci. U. S. A. 2013, 110, 7550. [Crossref] 2. Wagner, R.; Ickes, L.; Bertram, A. K.; Els, N.; Gorokhova, E.; Möhler, O.; Murray, B. J.; Umo, N. S.; Salter, M. E.; Atmos. Chem. Phys. 2021, 21, 13903. [Crossref] 3. Nandy, L.; Liu, S.; Gunsbury, C.; Wang, X.; Pendergraft, M. A.; Prather, K. A.; Dutcher, C. S.; ACS Earth Space Chem. 2019, 3, 1260. [Crossref] 4. Franklin, E. B.; Amiri, S.; Crocker, D.; Morris, C.; Mayer, K.; Sauer, J. S.; Weber, R. J.; Lee, C.; Malfatti, F.; Cappa, C. D.; Bertram, T. H.; Prather, K. A.; Goldstein, A. H.; Environ. Sci. Technol. 2022, 56, 16633. [Crossref] 5. Cravigan, L. T.; Mallet, M. D.; Vaattovaara, P.; Harvey, M. J.; Law, C. S.; Modini, R. L.; Russell, L. M.; Stelcer, E.; Cohen, D. D.; Olsen, G.; Safi, K.; Burrell, T. J.; Ristovski, Z.; Atmos. Chem. Phys. 2020, 20, 7955. [Crossref] 6. van Pinxteren, M.; Barthel, S.; Fomba, K. W.; Müller, K.; von Tümpling, W.; Herrmann, H.; Elementa 2017, 5, 1. [Crossref] 7. Flores, J. M.; Bourdin, G.; Altaratz, O.; Trainic, M.; Lang-Yona, N.; Dzimban, E.; Steinau, S.; Tettich, F.; Planes, S.; Allemand, D.; Agostini, S.; Banaigs, B.; Boissin, E.; Boss, E.; Douville, E.; Forcioli, D.; Furla, P.; Galand, P. E.; Sullivan, M. B.; Gilson, E.; Lombard, F.; Moulin, C.; Pesant, S.; Poulain, J.; Reynaud, S.; Romac, S.; Sunagawa, S.; Thomas, O. P.; Troublé, R.; de Vargas, C.; Thurber, R. V.; Voolstra, C. R.; Wincker, P.; Zoccola, D.; Bowler, C.; Gorsky, G.; Rudich, Y.; Vardi, A.; Koren, I.; Bull. Am. Meteorol. Soc. 2020, 101, E536. [Crossref] 8. Yue, S.; Bikkina, S.; Gao, M.; Barrie, L. A.; Kawamura, K.; Fu, P.; Geophys. Res. Lett. 2019, 46, 14881. [Crossref] 9. Prank, M.; Tonttila, J.; Ahola, J.; Kokkola, H.; Kühn, T.; Romakkaniemi, S.; Raatikainen, T.; Atmos. Chem. Phys. 2022, 22, 10971. [Crossref] 10. Sauer, J. S.; Mayer, K. J.; Lee, C.; Alves, M. R.; Amiri, S.; Bahaveolos, C. J.; Franklin, E. B.; Crocker, D. R.; Dang, D.; Dinasquet, J.; Garofalo, L. A.; Kaluarachchi, C. P.; Kilgour, D. B.; Mael, L. E.; Mitts, B. A.; Moon, D. R.; Moore, A. N.; Morris, C. K.; Mullenmeister, C. A.; Ni, C. M.; Pendergraft, M. A.; Petras, D.; Simpson, R. M. C.; Smith, S.; Tumminello, P. R.; Walker, J. L.; DeMott, P. J.; Farmer, D. K.; Goldstein, A. H.; Grassian, V. H.; Jaffe, J. S.; Malfatti, F.; Martz, T. R.; Slade, J. H.; Tivanski, A. V.; Bertram, T. H.; Cappa, C. D.; Prather, K. A.; Environ. Sci.: Processes Impacts 2022, 24, 290. [Crossref] 11. Jouffray, J. B.; Blasiak, R.; Norström, A. V.; Österblom, H.; Nyström, M.; One Earth 2020, 2, 43. [Crossref] 12. van Pinxteren, M.; Herrmann, H.; Atmos. Chem. Phys. 2013, 13, 11791. [Crossref] 13. Gorsky, G.; Bourdin, G.; Lombard, F.; Pedrotti, M. L.; Audrain, S.; Bin, N.; Boss, E.; Bowler, C.; Cassar, N.; Caudan, L.; Chabot, G.; Cohen, N. R.; Cron, D.; de Vargas, C.; Dolan, J. R.; Douville, E.; Elineau, A.; Flores, J. M.; Ghiglione, J. F.; Haëntjens, N.; Hertau, M.; John, S. G.; Kelly, R. L.; Koren, I.; Lin, Y.; Marie, D.; Moulin, C.; Moucherie, Y.; Pesant, S.; Picheral, M.; Poulain, J.; Pujo-Pay, M.; Reverdin, G.; Romac, S.; Sullivan, M. B.; Trainic, M.; Tressol, M.; Troublé, R.; Vardi, A.; Voolstra, C. R.; Wincker, P.; Agostini, S.; Banaigs, B.; Boissin, E.; Forcioli, D.; Furla, P.; Galand, P. E.; Gilson, E.; Reynaud, S.; Sunagawa, S.; Thomas, O. P.; Thurber, R. L. V.; Zoccola, D.; Planes, S.; Allemand, D.; Karsenti, E.; Frontiers in Marine Science 2019, 6, 1. [Crossref] 14. Fu, P.; Kawamura, K.; Chen, J.; Qin, M.; Ren, L.; Sun, Y.; Wang, Z.; Barrie, L. A.; Tachibana, E.; Ding, A.; Yamashita, Y.; Sci. Rep. 2015, 5, 1. [Crossref] 15. Hopkins, F. E.; Suntharalingam, P.; Gehlen, M.; Andrews, O.; Archer, S. D.; Bopp, L.; Buitenhuis, E.; Dadou, I.; Duce, R.; Goris, N.; Jickells, T.; Johnson, M.; Keng, F.; Law, C. S.; Lee, K.; Liss, P. S.; Lizotte, M.; Malin, G.; Murrell, J. C.; Naik, H.; Rees, A. P.; Schwinger, J.; Williamson, P.; Proc. R. Soc. A 2020, 476, 1. [Crossref] 16. Cunliffe, M.; Engel, A.; Frka, S.; Gasparović, B.; Guitart, C.; Murrell, J. C.; Salter, M.; Stolle, C.; Upstill-Goddard, R.; Wurl, O.; Prog. Oceanogr. 2013, 109, 104. [Crossref] 17. Quinn, P. K.; Bates, T. S.; Schulz, K. S.; Coffman, D. J.; Frossard, A. A.; Russell, L. M.; Keene, W. C.; Kieber, D. J.; Nat. Geosci. 2014, 7, 228. [Crossref] 18. Fu, P.; Kawamura, K.; Miura, K.; J. Geophys. Res.: Atmos. 2011, 116, 1. [Crossref] 19. Dall'Osto, M.; Ovadnevaite, J.; Paglione, M.; Beddows, D. C. S.; Ceburnis, D.; Cree, C.; Cortés, P.; Zamanillo, M.; Nunes, S. O.; Pérez, G. L.; Ortega-Retuerta, E.; Emelianov, M.; Vaqué, D.; Marrasé, C.; Estrada, M.; Sala, M. M.; Vidal, M.; Fitzsimons, M. F.; Beale, R.; Airs, R.; Rinaldi, M.; Decesari, S.; Facchini, M. C.; Harrison, R. M.; O'Dowd, C.; Simó, R.; Sci. Rep. 2017, 7, 6047. [Crossref] 20. Decesari, S.; Paglione, M.; Rinaldi, M.; Dall'osto, M.; Simó, R.; Zanca, N.; Volpi, F.; Facchini, M. C.; Hoffmann, T.; Götz, S.; Johannes Kampf, C.; O'Dowd, C.; Ceburnis, D.; Ovadnevaite, J.; Tagliavini, E.; Atmos. Chem. Phys. 2020, 20, 4193. [Crossref] 21. Schreuder, L. T.; Hopmans, E. C.; Stuut, J. B. W.; Sinninghe Damsté, J. S.; Schouten, S.; Geochim. Cosmochim. Acta 2018, 227, 171. [Crossref] 22. Gasparović, B.; Penezić, A.; Lampitt, R. S.; Sudasinghe, N.; Schaub, T.; Mar. Chem. 2016, 186, 101. [Crossref] 23. Yue, S.; Ren, L.; Song, T.; Li, L.; Xie, Q.; Li, W.; Kang, M.; Zhao, W.; Wei, L.; Ren, H.; Sun, Y.; Wang, Z.; Ellam, R. M.; Liu, C. Q.; Kawamura, K.; Fu, P.; J. Geophys. Res.: Atmos. 2019, 124, 4158. [Crossref] 24. https://www.sciencedirect.com/, acessada em maio 2023. 25. Eck, N. J.; Waltman, L.; VOSviewer Manual, 2019. [Link] acessado em maio 2023 26. Alves, C. A.; Quim. Nova 2014, 37, 1382. [Crossref] 27. Engel, A.; Bange, H. W.; Cunliffe, M.; Burrows, S. M.; Friedrichs, G.; Galgani, L.; Herrmann, H.; Hertkorn, N.; Johnson, M.; Liss, P. S.; Quinn, P. K.; Schartau, M.; Soloviev, A.; Stolle, C.; Upstill-Goddard, R. C.; van Pinxteren, M.; Zäncker, B.; Frontiers in Marine Science 2017, 4, 1. [Crossref] 28. Mustaffa, N. I. H.; Latif, M. T.; Ali, M. M.; AIP Conf. Proc. 2013, 1571, 625. [Crossref] 29. Lewis, S. L.; Russell, L. M.; Saliba, G.; Quinn, P. K.; Bates, T. S.; Carlson, C. A.; Baetge, N.; Aluwihare, L. I.; Boss, E.; Frossard, A. A.; Bell, T. G.; Behrenfeld, M. J.; ACS Earth Space Chem. 2022, 6, 1899. [Crossref] 30. Jaafar, S. A.; Latif, M. T.; Chian, C. W.; Han, W. S.; Wahid, N. B. A.; Razak, I. S.; Khan, M. F.; Tahir, N. M.; Mar. Pollut. Bull. 2014, 84, 35. [Crossref] 31. Wu, G.; Wan, X.; Ram, K.; Li, P.; Liu, B.; Yin, Y.; Fu, P.; Loewen, M.; Gao, S.; Kang, S.; Kawamura, K.; Wang, Y.; Cong, Z.; Environ. Pollut. 2020, 257, 113616. [Crossref] 32. Shaharom, S.; Latif, M. T.; Khan, M. F.; Yusof, S. N. M.; Sulong, N. A.; Wahid, N. B. A.; Uning, R.; Suratman, S.; Environ. Sci. Pollut. Res. 2018, 25, 27074. [Crossref] 33. Ault, A. P.; Moffet, R. C.; Baltrusaitis, J.; Collins, D. B.; Ruppel, M. J.; Cuadra-Rodriguez, L. A.; Zhao, D.; Guasco, T. L.; Ebben, C. J.; Geiger, F. M.; Bertram, T. H.; Prather, K. A.; Grassian, V. H.; Environ. Sci. Technol. 2013, 47, 5603. [Crossref] 34. Schwier, A. N.; Sellegri, K.; Mas, S.; Charrière, B.; Pey, J.; Rose, C.; Temime-Roussel, B.; Jaffrezo, J. L.; Parin, D.; Picard, D.; Ribeiro, M.; Roberts, G.; Sempéré, R.; Marchand, N.; D'Anna, B.; Atmos. Chem. Phys. 2017, 17, 14645. [Crossref] 35. Salter, M. E.; Hamacher-Barth, E.; Leck, C.; Werner, J.; Johnson, C. M.; Riipinen, I.; Nilsson, E. D.; Zieger, P.; Geophys. Res. Lett. 2016, 43, 8277. [Crossref] 36. Bhattarai, H.; Zhang, Y. L.; Pavuluri, C. M.; Wan, X.; Wu, G.; Li, P.; Cao, F.; Zhang, W.; Wang, Y.; Kang, S.; Ram, K.; Kawamura, K.; Ji, Z.; Widory, D.; Cong, Z.; Environ. Sci. Technol. 2019, 53, 12247. [Crossref] 37. Hu, Q. H.; Xie, Z. Q.; Wang, X. M.; Kang, H.; Zhang, P.; Sci. Rep. 2013, 3, 1. [Crossref] 38. Zhao, W.; Fu, P.; Yue, S.; Li, L.; Xie, Q.; Zhu, C.; Wei, L.; Ren, H.; Li, P.; Li, W.; Sun, Y.; Wang, Z.; Kawamura, K.; Chen, J.; Atmos. Environ. 2019, 213, 608. [Crossref] 39. Pöhlker, C.; Huffman, J. A.; Pöschl, U.; Atmos. Meas. Tech. 2012, 5, 37. [Crossref] 40. Crawford, I.; Gallagher, M. W.; Bower, K. N.; Choularton, T. W.; Flynn, M. J.; Ruske, S.; Listowski, C.; Brough, N.; Lachlan-Cope, T.; Fleming, Z. L.; Foot, V. E.; Stanley, W. R.; Atmos. Chem. Phys. 2017, 17, 14291. [Crossref] 41. Guo, L.; Ma, Y.; Tigabu, M.; Guo, X.; Zheng, W.; Guo, F.; Environ. Pollut. 2020, 264, 114709. [Crossref] 42. Chen, Q.; Heald, C. L.; Jimenez, J. L.; Canagaratna, M. R.; Zhang, Q.; He, L. Y.; Huang, X. F.; Campuzano-Jost, P.; Palm, B. B.; Poulain, L.; Kuwata, M.; Martin, S. T.; Abbatt, J. P. D.; Lee, A. K. Y.; Liggio, J.; Geophys. Res. Lett. 2015, 42, 4182. [Crossref] 43. Wu, Y.; Huang, X.; Jiang, Z.; Liu, S.; Cui, L.; Atmos. Res. 2020, 241, 104958. [Crossref] 44. Hu, Z.; Kang, S.; Xu, J.; Zhang, C.; Li, X.; Yan, F.; Zhang, Y.; Chen, P.; Li, C.; Atmos. Environ. 2023, 294, 119486. [Crossref] 45. Wu, C.; Trounce, H.; Dunne, E.; Griffith, D. W. T.; Chambers, S. D.; Williams, A. G.; Humphries, R. S.; Cravigan, L. T.; Miljevic, B.; Zhang, C.; Wang, H.; Wang, B.; Ristovski, Z.; Sci. Total Environ. 2023, 856, 159143. [Crossref] 46. Wu, D.; Niu, X.; Chen, Z.; Chen, Y.; Xing, Y.; Cao, X.; Liu, J.; Wang, X.; Pu, W.; Geophys. Res. Lett. 2022, 49, 1. [Crossref] 47. Wan, X.; Kawamura, K.; Ram, K.; Kang, S.; Loewen, M.; Gao, S.; Wu, G.; Fu, P.; Zhang, Y.; Bhattarai, H.; Cong, Z.; Environ. Pollut. 2019, 247, 216. [Crossref] 48. Dall'Osto, M.; Airs, R. L.; Beale, R.; Cree, C.; Fitzsimons, M. F.; Beddows, D.; Harrison, R. M.; Ceburnis, D.; O'Dowd, C.; Rinaldi, M.; Paglione, M.; Nenes, A.; Decesari, S.; Simó, R.; ACS Earth Space Chem. 2019, 3, 854. [Crossref] 49. Lewis, S. L.; Saliba, G.; Russell, L. M.; Quinn, P. K.; Bates, T. S.; Behrenfeld, M. J.; Frontiers in Marine Science 2021, 8, 1. [Crossref] 50. Lawler, M. J.; Lewis, S. L.; Russell, L. M.; Quinn, P. K.; Bates, T. S.; Coffman, D. J.; Upchurch, L. M.; Saltzman, E. S.; Atmos. Chem. Phys. 2020, 20, 16007. [Crossref] 51. Wu, Y.; Huang, X.; Jiang, Z.; Liu, S.; Cui, L.; Atmos. Res. 2020, 241, 104958. [Crossref] 52. Yan, G.; Kim, G.; Environ. Sci. Technol. 2017, 51, 11580. [Crossref] 53. Zhang, L.; Segal-Rozenhaimer, M.; Che, H.; Dang, C.; Sedlacek III, A. J.; Lewis, E. R.; Dobracki, A.; Wong, J. P. S.; Formenti, P.; Howell, S. G.; Nenes, A.; Atmos. Chem. Phys. 2022, 22, 9199. [Crossref] 54. Kang, H.; Shang, X.; Abdumutallip, M.; Chen, Y.; Li, L.; Wang, X.; Li, C.; Ouyang, H.; Tang, X.; Wang, L.; Rudich, Y.; Chen, J.; Sci. Total Environ. 2022, 837, 155817. [Crossref] 55. Deng, J.; Ma, H.; Wang, X.; Zhong, S.; Zhang, Z.; Zhu, J.; Fan, Y.; Hu, W.; Wu, L.; Li, X.; Ren, L.; Pavuluri, C. M.; Pan, X.; Sun, Y.; Wang, Z.; Kawamura, K.; Fu, P.; Atmos. Chem. Phys. 2022, 22, 6449. [Crossref] 56. Mukherjee, A.; Dey, S.; Rana, A.; Jia, S.; Banerjee, S.; Sarkar, S.; Environ. Pollut. 2020, 267, 115440. [Crossref] 57. Afsana, S.; Zhou, R.; Miyazaki, Y.; Tachibana, E.; Deshmukh, D. K.; Kawamura, K.; Mochida, M.; Sci. Rep. 2022, 12, 14379. [Crossref] 58. Frka, S.; Sala, M.; Brodnik, H.; Stefane, B.; Kroflič, A.; Grgić, I.; Chemosphere 2022, 299, 134381. [Crossref] 59. Mo, Y.; Zhong, G.; Li, J.; Liu, X.; Jiang, H.; Tang, J.; Jiang, B.; Liao, Y.; Cheng, Z.; Zhang, G.; J. Geophys. Res.: Atmos. 2022, 127, 1. [Crossref] 60. Chen, Q.; Miyazaki, Y.; Kawamura, K.; Matsumoto, K.; Coburn, S.; Volkamer, R.; Iwamoto, Y.; Kagami, S.; Deng, Y.; Ogawa, S.; Ramasamy, S.; Kato, S.; Ida, A.; Kajii, Y.; Mochida, M.; Environ. Sci. Technol. 2016, 50, 10351. [Crossref] 61. Jiang, X.; Liu, D.; Li, Q.; Tian, P.; Wu, Y.; Li, S.; Hu, K.; Ding, S.; Bi, K.; Li, R.; Huang, M.; Ding, D.; Chen, Q.; Kong, S.; Li, W.; Pang, Y.; He, D.; Environ. Sci. Technol. 2022, 56, 12873. [Crossref] 62. Wu, G.; Wan, X.; Gao, S.; Fu, P.; Yin, Y.; Li, G.; Zhang, G.; Kang, S.; Ram, K.; Cong, Z.; Environ. Sci. Technol. 2018, 52, 7203. [Crossref] 63. Fujii, Y.; Tohno, S.; Ikeda, K.; Mahmud, M.; Takenaka, N.; Sci. Total Environ. 2021, 753, 142009. [Crossref] 64. Zhang, J.; Yang, L.; Mellouki, A.; Chen, J.; Chen, X.; Gao, Y.; Jiang, P.; Li, Y.; Yu, H.; Wang, W.; Chemosphere 2018, 209, 147. [Crossref] 65. Na, G.; Gao, Y.; Li, R.; Gao, H.; Hou, C.; Ye, J.; Jin, S.; Zhang, Z.; Mar. Pollut. Bull. 2020, 156, 111173. [Crossref] 66. Kim, J. H.; Park, J.; Kim, S. B.; Shin, K. H.; Kim, S.; Gim, Y.; Atmosphere 2020, 11, 499. [Crossref] 67. Jiang, H.; Tang, J.; Li, J.; Zhao, S.; Mo, Y.; Tian, C.; Zhang, X.; Jiang, B.; Liao, Y.; Chen, Y.; Zhang, G.; Environ. Sci. Technol. Lett. 2022, 9, 913. [Crossref] 68. Yu, F.; Luo, G.; Atmos. Chem. Phys. 2014, 14, 12455. [Crossref] 69. Shen, Y.; Wang, J.; Gao, Y.; Chan, C. K.; Zhu, Y.; Gao, H.; Petäjä, T.; Yao, X.; Sci. Total Environ. 2020, 735, 139302. [Crossref] 70. Yan, J.; Zhang, M.; Jung, J.; Lin, Q.; Zhao, S.; Xu, S.; Chen, L.; Atmos. Environ. 2020, 233, 117611. [Crossref] 71. Yan, J.; Jung, J.; Zhang, M.; Bianchi, F.; Tham, Y. J.; Xu, S.; Lin, Q.; Zhao, S.; Li, L.; Chen, L.; Atmos. Chem. Phys. 2020, 20, 3259. [Crossref] 72. Ning, A.; Zhang, H.; Zhang, X.; Li, Z.; Zhang, Y.; Xu, Y.; Ge, M.; Atmos. Environ. 2020, 227, 117378. [Crossref] 73. Fleming, L. E.; Kirkpatrick, B.; Backer, L. C.; Bean, J. A.; Wanner, A.; Reich, A.; Zaias, J.; Cheng, Y. S.; Pierce, R.; Naar, J.; Abraham, W. M.; Baden, D. G.; Chest 2007, 131, 187. [Crossref] 74. Pierce, R. H.; Henry, M. S.; Blum, P. C.; Hamel, S. L.; Kirkpatrick, B.; Cheng, Y. S.; Zhou, Y.; Irvin, C. M.; Naar, J.; Weidner, A.; Fleming, L. E.; Backer, L. C.; Baden, D. G.; Harmful Algae 2005, 4, 965. [Crossref] 75. Medina-Pérez, N. I.; Dall'osto, M.; Decesari, S.; Paglione, M.; Moyano, E.; Berdalet, E.; Environ. Sci. Technol. 2021, 55, 468. [Crossref] 76. Ciminiello, P.; Dell'Aversano, C.; dello Iacovo, E.; Fattorusso, E.; Forino, M.; Tartaglione, L.; Benedettini, G.; Onorari, M.; Serena, F.; Battocchi, C.; Casabianca, S.; Penna, A.; Environ. Sci. Technol. 2014, 48, 3532. [Crossref] 77. Tartaglione, L.; Mazzeo, A.; Dell'Aversano, C.; Forino, M.; Giussani, V.; Capellacci, S.; Penna, A.; Asnaghi, V.; Faimali, M.; Chiantore, M.; Yasumoto, T.; Ciminiello, P.; Anal. Bioanal. Chem. 2016, 408, 915. [Crossref] 78. van Acker, E.; Huysman, S.; de Rijcke, M.; Asselman, J.; de Schamphelaere, K. A. C.; Vanhaecke, L.; Janssen, C. R.; Environ. Sci. Technol. 2021, 55, 6184. [Crossref] 79. Kang, M.; Fu, P.; Kawamura, K.; Yang, F.; Zhang, H.; Zang, Z.; Ren, H.; Ren, L.; Zhao, Y.; Sun, Y.; Wang, Z.; Atmos. Chem. Phys. 2018, 18, 13947. [Crossref] 80. Kumaravel, V.; Imam, M.; Badreldin, A.; Chava, R.; Do, J.; Kang, M.; Abdel-Wahab, A.; Catalysts 2019, 9, 276. [Crossref] 81. Giannarelli, S.; Onor, M.; Abete, C.; Termine, M.; Fuoco, R.; Microchem. J. 2019, 149, 103911. [Crossref] 82. Kang, M.; Guo, H.; Wang, P.; Fu, P.; Ying, Q.; Liu, H.; Zhao, Y.; Zhang, H.; Sci. Total Environ. 2019, 651, 2679. [Crossref] 83. Wan, X.; Kawamura, K.; Ram, K.; Kang, S.; Loewen, M.; Gao, S.; Wu, G.; Fu, P.; Zhang, Y.; Bhattarai, H.; Cong, Z.; Environ. Pollut. 2019, 247, 216. [Crossref] 84. Bhattarai, H.; Saikawa, E.; Wan, X.; Zhu, H.; Ram, K.; Gao, S.; Kang, S.; Zhang, Q.; Zhang, Y.; Wu, G.; Wang, X.; Kawamura, K.; Fu, P.; Cong, Z.; Atmos. Res. 2019, 220, 20. [Crossref] 85. Pokhrel, A.; Kawamura, K.; Kunwar, B.; Ono, K.; Tsushima, A.; Seki, O.; Matoba, S.; Shiraiwa, T.; Atmos. Chem. Phys. 2020, 20, 597. [Crossref] 86. Zangrando, R.; Barbaro, E.; Vecchiato, M.; Kehrwald, N. M.; Barbante, C.; Gambaro, A.; Sci. Total Environ. 2016, 544, 606. [Crossref] 87. Vicente, E. D.; Alves, C. A.; Atmos. Res. 2018, 199, 159. [Crossref] 88. Simoneit, B. R. T.; J. Geophys. Res. 2004, 109, D19S10. [Crossref] 89. Fu, P.; Kawamura, K.; Miura, K.; J. Geophys. Res. 2011, 116, D13302. [Crossref] 90. Nouara, A.; Panagiotopoulos, C.; Sempéré, R.; Mar. Chem. 2019, 213, 24. [Crossref] 91. Schmidl, C.; Luisser, M.; Padouvas, E.; Lasselsberger, L.; Rzaca, M.; Ramirez-Santa Cruz, C.; Handler, M.; Peng, G.; Bauer, H.; Puxbaum, H.; Atmos. Environ. 2011, 45, 7443. [Crossref] 92. Chen, P.; Kang, S.; Zhang, L.; Abdullaev, S. F.; Wan, X.; Zheng, H.; Maslov, V. A.; Abdyzhapar uulu, S.; Safarov, M. S.; Tripathee, L.; Li, C.; Environ. Pollut. 2022, 302, 119055. [Crossref] 93. McLaughlin, L. P.; Belmont, E. L.; J. Aerosol Sci. 2022, 166, 106067. [Crossref] 94. Zangrando, R.; Corami, F.; Barbaro, E.; Grosso, A.; Barbante, C.; Turetta, C.; Capodaglio, G.; Gambaro, A.; Sci. Total Environ. 2019, 650, 2117. [Crossref] 95. Myers-Pigg, A. N.; Griffin, R. J.; Louchouarn, P.; Norwood, M. J.; Sterne, A.; Cevik, B. K.; Environ. Sci. Technol. 2016, 50, 9308. [Crossref] 96. Wan, X.; Kang, S.; Li, Q.; Rupakheti, D.; Zhang, Q.; Guo, J.; Chen, P.; Tripathee, L.; Rupakheti, M.; Panday, A. K.; Wang, W.; Kawamura, K.; Gao, S.; Wu, G.; Cong, Z.; Atmos. Chem. Phys. 2017, 17, 8867. [Crossref] 97. Chen, P.; Kang, S.; Zhang, L.; Abdullaev, S. F.; Wan, X.; Zheng, H.; Maslov, V. A.; Abdyzhapar uulu, S.; Safarov, M. S.; Tripathee, L.; Li, C.; Environ. Pollut. 2022, 302, 119055. [Crossref] 98. Alves, N. O.; Brito, J.; Caumo, S.; Arana, A.; Hacon, S. S.; Artaxo, P.; Hillamo, R.; Teinilä, K.; Medeiros, S. R. B.; Vasconcellos, P. C.; Atmos. Environ. 2015, 120, 277. [Crossref] 99. Silveira, M. V. F.; Silva‐Junior, C. H. L.; Anderson, L. O.; Aragão, L. E. O. C.; Global Ecology and Biogeography 2022, 31, 2026. [Crossref] 100. Eufemia, L.; Turetta, A. P. D.; Bonatti, M.; Da Ponte, E.; Sieber, S.; Development Policy Review 2022, 40, 1. [Crossref] 101. Copertino, M.; Piedade, M. T. F.; Vieira, I. C. G.; Bustamante, M.; Cienc. Cult. (Campinas, Braz.) 2019, 71, 04. [Crossref] 102. Zhao, T.; Ye, J.; Ribeiro, I. O.; Ma, Y.; Hung, H. M.; Batista, C. E.; Stewart, M. P.; Guimarães, P. C.; de Arellano, J. V. G.; de Souza, R. A. F.; Guenther, A. B.; Martin, S. T.; Communications Earth & Environment 2021, 2, 205. [Crossref] 103. Yan, J.; Lin, Q.; Zhang, M.; Zhao, S.; Chen, L.; J. Environ. Sci. 2019, 83, 217. [Crossref] 104. Kesharwani, R.; Sun, Z.; Dagli, C.; Xiong, H.; Appl. Energy 2019, 242, 1467. [Crossref] 105. Bilgili, L.; Renewable Sustainable Energy Rev. 2021, 144, 110985. [Crossref] 106. Yang, Z.; Tan, Q.; Geng, P.; Polish Maritime Research 2019, 26, 153. [Crossref] 107. Siriname, S. N.; Hoffmann, J.; Asariotis, R.; Assaf, M.; Bacrot, C.; Benamara, H.; Crucelegui, J. L.; Hansen, P.; Kepesidi, A.; Kulaga, T.; Massenet, R.; Moreira, T.; Premti, A.; Rodríguez, L.; Tokuda, H.; Ugaz, P.; Youssef, F.; United Nations Conference on Trade and Development, New York, 2022. [Link] acessado em junho 2023 108. Yang, S.; Pan, X.; Han, Z.; Zhao, D.; Liu, B.; Zheng, D.; Yan, Z.; Chem. Eng. J. 2018, 331, 8. [Crossref] 109. Zhang, Z.; Zhao, C.; Wang, Y.; Sun, Y.; Zheng, Z.; J. Combust. Sci. Technol. 2017, 23, 436. [Link] acessado em maio 2023 110. Vedachalam, S.; Baquerizo, N.; Dalai, A. K.; Fuel 2022, 310, 122243. [Crossref] 111. Prucole, E. D. S.: Avaliação do Uso de Biodiesel na Formulação de Combustíveis Marítimos Residuais; Tese de Doutorado, Universidade Federal do Rio de Janeiro, Rio de Janeiro, Brasil, 2015. [Link] acessado em maio 2023 112. Sousa, C.; Delgado, F.; Maia, F.; Timerman, G.; Duarte, M.; Medeiros, S.; Distribuição de Combustíveis Marítimos no Brasil, em Conformidade com o IMO 2020: Oportunidades e Desafios para o Brasil, 2020. [Link] acessado em maio 2023 113. Mohd Noor, C. W.; Noor, M. M.; Mamat, R.; Renewable Sustainable Energy Rev. 2018, 94, 127. [Crossref] 114. Chiong, M. C.; Kang, H. S.; Shaharuddin, N. M. R.; Mat, S.; Quen, L. K.; Ten, K. H.; Ong, M. C.; Renewable Sustainable Energy Rev. 2021, 149, 111397. [Crossref] 115. Noor, M. C.; Mamat, R.; Ahmed, A. N.; International Journal of Innovative Computing, Information and Control (IJICIC) 2018, 14, 959. [Link] acessado em maio 2023 116. Zhou, H.; Zhao, H.; Hu, J.; Li, M.; Feng, Q.; Qi, J.; Zongbo, S.; Mao, H.; Jin, T.; Atmos. Enrviron. 2019, 218, 116987. [Crossref] 117. Müller-Casseres, E.; Carvalho, F.; Nogueira, T.; Fonte, C.; Império, M.; Poggio, M.; Wei, H. K.; Portugal-Pereira, J.; Rochedo, P. R. R.; Szklo, A.; Schaeffer, R.; Energy 2021, 219, 119444. [Crossref] 118. Tanzer, S. E.; Posada, J.; Geraedts, S.; Ramírez, A.; J. Cleaner Prod. 2019, 239, 117845. [Crossref] 119. Agência Nacional de Petróleo e Gás; Resolução ANP no 903, de 18 de novembro de 2022. [Link] acessado em maio 2023 120. Bach, H.; Hansen, T.; Marine Policy 2023, 147, 105379. [Crossref] 121. Stuchtey, M. R.; Vincent, A.; Merkl, A.; Bucher, M.; Lubchenco, J.; Pangestu, M. E.; The Ocean Panel, 2022. [Link] acessado em maio 2023 122. Ramírez, F.; Afán, I.; Davis, L. S.; Chiaradia, A.; Sci. Adv. 2017, 3, 1. [Crossref] 123. Gao, K.; Gao, G.; Wang, Y.; Dupont, S.; Mar. Life Sci. Technol. 2020, 2, 279. [Crossref] 124. United Nations; The Ocean and the Sustainable Development Goals under the 2030. Agenda for Sustainable Development. A Technical Abstract of the First Global Integrated Marine Assessment, New York, 2017. [Link] acessado em maio 2023 125. United Nations Environment Programme (UNEP); Global Chemicals Outlook II - From Legacies to Innovative Solutions: Implementing the 2030 Agenda for Sustainable Development, 2019. [Link] acessado em maio 2023 126. Kümmerer, K.; Clark, J. H.; Zuin, V. G.; Science 2020, 367, 369. [Crossref] |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access