Artigo
|
|
| Uso de coagulantes no tratamento de efluente de lavanderia hospitalar: a busca por processos físico-químicos sustentáveis visando remoção de poluentes e microrganismos patogênicos Use of coagulants in the treatment of hospital laundry effluent: the search for sustainable physical-chemical processes to removal pollutants and pathogenic microorganisms |
|
Eduarda V. S. GomesI I. Departamento de Engenharia Sanitária e Ambiental, Universidade Federal de Juiz de Fora, 36036-900 Juiz de Fora - MG, Brasil Recebido: 10/03/2024 *e-mail: fernanda.damasceno@ufjf.br Hospital laundry is an important source of environmental pollution because its effluent contains high loads of organic matter and microorganisms. Conventionally, the treatment is carried out using aluminum sulfate, a low-cost and highly efficient coagulant that is related to secondary contamination due to the generation of non-biodegradable sludge, its ability to accumulate metals and toxicity. Aiming for sustainable alternatives, the efficiency of tannin from the natural coagulant and Moringa oleifera seed was evaluated in relation to aluminum sulfate, seeking to adapt the color and turbidity parameters and determine the antimicrobial activity of the seed. Using a concentration of 100 mg L-1 of aluminum sulfate, 97.4 and 93.95% of color and turbidity removals in the effluent were obtained, respectively. With 50 mg L-1 tannin showed an efficiency of 84.96% for color removal and 89.75% for turbidity. Tests were also carried out with Moringa oleifera seeds using saline seed extract, crushed seeds and aqueous seed extract, with a reduction in conductivity by more than 99%, removing pollutant ions for the saline extract. Of the methodologies used, the best result was obtained with the aqueous extract, achieving removals of 89.63% of color, 78.33% of turbidity, and inhibition of more than 98.1% of microorganism growth. INTRODUÇÃO Em centros urbanos são gerados efluentes domésticos e não domésticos, sendo os últimos resultantes de atividades industriais, comerciais ou de prestação de serviços. Caso sejam despejados no corpo hídrico receptor ou na rede coletora de efluente doméstico sem o tratamento prévio, diversos problemas ambientais e sanitários podem ocorrer.1 Os efluentes não domésticos podem apresentar diferentes características devido as diversas atividades geradoras, o que inviabiliza uma padronização de suas características físico-químicas e biológicas.2 Entre estes efluentes, podemos destacar aqueles oriundos de lavanderias hospitalares, já que os municípios apresentam pelo menos uma unidade de saúde a fim de garantir o bem-estar da população.3 Patógenos, sanitizantes, desinfetantes, antibióticos e detergentes são substâncias frequentemente encontradas em efluentes de lavanderia hospitalar.4 Quando seu despejo é realizado sem tratamento prévio, diversos problemas ambientais, à saúde humana e ao ecossistema aquático podem ser observados a jusante do lançamento.5 Por isso, sua adequação às legislações vigentes é de extrema importância.6 No Brasil, o tratamento usual para efluentes de lavanderias hospitalares é o físico-químico via coagulação/floculação utilizando reagentes sintéticos, com destaque para o sulfato de alumínio (SA), uma vez que apresenta eficiente remoção de cor e turbidez a baixo custo.7 Entretanto, coagulantes inorgânicos à base de sais de alumínio podem gerar uma contaminação secundária ao meio ambiente e prejuízos à saúde em razão da geração de lodo químico recalcitrante, capacidade de bioacumulação e toxicidade capaz de provocar o desenvolvimento de câncer, doenças renais, motoras, neurodegenerativas.8-11 Buscando minimizar a problemática citada, a busca por coagulantes/floculantes naturais, biodegradáveis e de baixa toxicidade torna-se necessária, indo ao encontro das recomendações da Organização das Nações Unidas (ONU), no que diz respeito ao cuidado com a poluição das fontes de água disponíveis.5,12-14 Dentre os coagulantes naturais destacam-se os taninos (TSG). A aplicação destes em efluentes de lavanderia se mostra eficiente em razão da sua capacidade de remoção de surfactantes aniônicos.15-18 Os taninos são compostos que pertencem ao grupo de substâncias denominadas de glicosídeos polifenólicos, podendo estar presentes no meio como ésteres ou heterosídeos com alta massa molecular (500 a 3000 Da) e estrutura complexa. Eles são produtos naturais que podem ser obtidos através de extratos da casca e da madeira de plantas como acácia (Acacia mearnsii), quebracho (Schinopsis lorentzii), castanheiro (Castanea sativa), tara (Caesalpinia spinosa) e mirabolano (Terminalia chebula).11,19,20 A unidade básica estrutural de um tanino pode ser observada na Figura 1a. A presença de grupos hidroxila no tanino indica sua natureza aniônica, já que anéis fenólicos são bons doadores de hidrogênio. Na Figura 1b podemos observar as possíveis interações estabelecidas por um tanino hipotético quando presente em uma solução aquosa contendo partículas carregadas. Estas interações moleculares podem induzir a coagulação e acredita-se que quanto mais grupos fenólicos estiverem disponíveis numa estrutura de tanino, mais eficaz será a sua capacidade de coagulação.21
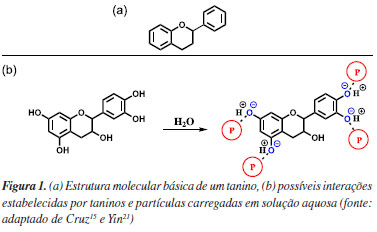
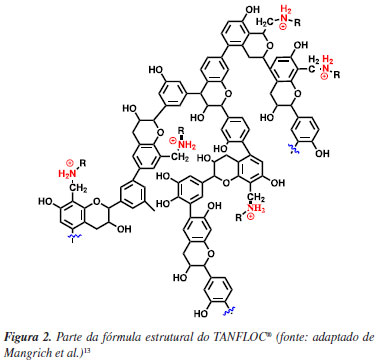
A estrutura dos taninos nos permite dizer que estes compostos exibem características como hidrofobicidade, devido à presença dos anéis aromáticos; hidrofilicidade, devido aos grupos -OH; presença de heterociclos que permitem reações de hidrólise e condensações; e sítios nucleofílicos que podem reagir com compostos orgânicos e metais presentes no meio.22 Entre os taninos mais utilizados para tratamento de água e de efluentes, podemos destacar o TANFLOC®, produzido pela empresa TANAC (Figura 2).8,13,23 O fabricante disponibiliza uma série de diferentes taninos de acordo com o tipo de efluente a ser tratado, sendo o TANFLOC SG considerado o apropriado para o tratamento de efluentes de lavanderias industriais.24
Outro produto natural bastante estudado é a semente de Moringa oleifera (MO), popularmente conhecida como Acácia branca, são utilizadas para o tratamento de efluentes da indústria têxtil.25-28 Neste coagulante, a literatura21,29-36 sugere que os componentes ativos são peptídeos catiônicos de massa molecular variando entre 6 e 16 kDa, porém ainda há grandes esforços para elucidar qual realmente seria o princípio ativo coagulante presente nessas sementes. Sugere-se que, em relação ao mecanismo de coagulação relacionado às proteínas, ocorre através de adsorção, neutralização de cargas e ponte interpartículas. Outro fator importante no que diz respeito à utilização da Moringa oleifera consiste no fato dela ser capaz de controlar o aumento da população de microrganismos. Pode-se encontrar na literatura28,37-39 relatos de remoção de até 99% de bactérias do efluente. Por isso, evidencia-se seu grande potencial no tratamento de efluentes de lavanderias hospitalares. Considerando o que foi discutido, o presente trabalho teve como objetivo realizar o tratamento do efluente da lavanderia de um hospital de uma cidade do Estado do Rio de Janeiro, utilizando dois coagulantes naturais e um sintético e avaliar a adequação do efluente perante a legislação vigente quanto a parâmetros físico-químicos e microbiológicos.
PARTE EXPERIMENTAL Para o desenvolvimento deste trabalho foram coletados 3 lotes, em datas distintas, do efluente da lavanderia de um hospital de pequeno porte em Conservatória, Distrito de Valença, RJ, e foram realizados 24 ensaios em um equipamento Jar Test modelo Q305FT3 da marca Quimis. O hospital atende as necessidades básicas do distrito. Realiza cirurgias de catarata e atendimentos de emergências, segundo informações do local. A lavanderia hospitalar atende aos requisitos da Agência Nacional de Vigilância Sanitária quanto aos procedimentos operacionais necessários para a realização da atividade como, por exemplo, a segregação da área suja e área limpa (Figura 1S, Material Suplementar). Destaca-se que o efluente da lavanderia é segregado do efluente sanitário e mantido em reservatório fechado, sem interferências de outros efluentes ou ações climáticas na caracterização do mesmo. Além disso, a lavanderia apresenta porte industrial, conforme os equipamentos utilizados para atender as demandas de limpeza de roupas de cama e vestimentas do hospital (Figuras 2S e 3S, Material Suplementar). O tanino foi fornecido pela empresa TANAC e as sementes de Moringa oleifera foram adquiridas através do comércio varejista da região de Juiz de Fora, MG. Caracterização dos lotes de efluente bruto e do efluente tratado Cada lote de efluente foi caracterizado a fim de garantir a reprodutibilidade dos testes. As análises foram conduzidas de acordo com os métodos estabelecidos pelo Standard Methods for the Examination of Water and Wastewater.40 Os seguintes parâmetros foram analisados, tanto para o efluente bruto quanto para o efluente tratado: turbidez (NTU), cor aparente (uC), cor verdadeira (uC), condutividade (µS cm-1), potencial hidrogeniônico (pH), alcalinidade (mg L-1 CaCO3), série de sólidos (mg L-1), demanda química de oxigênio (mg L-1 O2) e demanda bioquímica de oxigênio (mg L-1 O2). Turbidez Foi realizada a leitura do "branco" com água deionizada e, em seguida, a cubeta foi preenchida com o efluente até o nível indicado na vidraria para a leitura de turbidez (NTU). Para essa análise, um turbidímetro de bancada da marca Del Lab modelo DLI 2500 foi utilizado. Cor aparente e cor verdadeira As análises de cor foram conduzidas em um espectrofotômetro modelo DR 6000 da marca Hach utilizando uma cubeta de vidro com 1 cm de caminho óptico. Todas as leituras foram feitas utilizando o comprimento de onda 456 nm, conforme indicado pelo Standard Methods for the Examination of Water and Wastewater.40 Através de uma curva de calibração preparada a partir de concentrações que variaram entre 5 e 500 uC foi possível obter o valor de cor correspondente para cada leitura de absorbância. Para determinação da cor aparente foram utilizadas alíquotas da amostra sem filtragem, enquanto para a cor verdadeira as amostras foram filtradas em papel de filtro. De modo semelhante ao realizado para a análise de turbidez, leituras de "branco" com água deionizada também foram realizadas de modo a zerar o equipamento. Condutividade e potencial hidrogeniônico As medidas de condutividade (µS cm-1) e potencial hidrogeniônico (pH) foram realizadas de maneira semelhante: as amostras foram transferidas para um béquer onde o volume adicionado foi o suficiente para cobrir os eletrodos dos equipamentos. Cada análise foi realizada em um recipiente diferente para minimizar contaminação e os sensores do condutivímetro e pHmetro foram higienizados com água deionizada antes de realizar as leituras das amostras. O condutivímetro modelo CG 1800 da marca Gehaka e o pHmetro modelo mPA 210 da marca MS Tecnopon foram utilizados para essas análises. Alcalinidade A alcalinidade (mg L-1 CaCO3) foi realizada a partir da titulação com ácido sulfúrico 0,02 N (H2SO4) da amostra filtrada, utilizando fenolftaleína e verde de bromocresol como indicadores. O valor da alcalinidade foi obtido a partir do volume total de ácido gasto na titulação, aplicado na Equação 1, onde T é o volume total gasto na titulação, N indica a normalidade e FC o fator de correção para a solução de ácido sulfúrico utilizada. 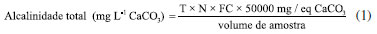 Série de sólidos A análise da série de sólidos do efluente foi dividida em sólidos suspensos e dissolvidos, fixos e voláteis. As amostras foram filtradas em membrana de fibra de vidro. O permeado foi então transferido para cápsulas de porcelanas previamente secas e taradas para determinação da série de sólidos dissolvidos. Já para a série de sólidos suspensos, foram utilizados os filtros de membrana de vidro em conjunto com capsulas de porcelana. Após secagem em estufa a 105 ºC, as amostras foram levadas a mufla a 550 ºC, para determinação dos sólidos fixos e voláteis. Demanda química de oxigênio (DQO) A DQO foi determinada pelo método de digestão em tubos fechados, a 150 ºC, durante 2 h, utilizando dicromato de potássio como oxidante forte e sulfato de prata como catalisador. Após digestão e resfriamento a temperatura ambiente, foram lidas as absorbâncias, em espectrofotômetro Hach DR 6000, com comprimento de onda igual a 600 nm. O bloco digestor modelo Thermo Digest da marca PoliControl foi utilizado para essa análise. Demanda bioquímica de oxigênio (DBO) Para a avaliação da DBO foi utilizado o método Winkler. As amostras diluídas foram armazenadas em estufa incubadora modelo T-130X da marca Thelga, por 5 dias, a 20 ºC. O consumo de oxigênio dissolvido (OD) foi determinado pelo método titulométrico com tiossulfato de sódio (Na2S2O3) 0,0125 N, utilizando amido como indicador. Como a razão DQO/DBO5 encontrada é maior que 4, destaca-se que o efluente utilizado no trabalho não é biodegradável, ou seja, a fração inerte é elevada e por isso é indicado o tratamento físico-químico.2 Tratamento do efluente de lavanderia hospitalar com sulfato de alumínio (SA) Em todos os ensaios de coagulação e floculação realizados, o tempo de mistura rápida (TMR) foi de 2 min a 500 rotações por min (rpm), o tempo de mistura lenta (TML) igual a 20 min a 40 rpm e a sedimentação ocorreu por 1 h. Preparou-se uma solução padrão a 2% (peso/volume) de Al2(SO4)3 e, a partir dela, calculou-se o volume necessário para a concentração desejada em cada jarro do ensaio. Na primeira corrida de testes, o pH do efluente foi mantido, variando as concentrações entre 150 e 600 mg L-1. A concentração que mostrou os melhores resultados foi então selecionada para a segunda corrida de testes, dessa vez mantendo a concentração de alumínio e variando o pH entre 5 e 9. O ajuste foi realizado utilizando solução de H2SO4 na proporção 1:1. Ao término desses, uma nova variação na concentração foi realizada (terceira corrida de testes) de modo a otimizar o processo de tratamento visando o melhor custo-benefício utilizando sulfato de alumínio como coagulante. Tratamento do efluente de lavanderia hospitalar com tanino (TSG) As concentrações iniciais do tanino foram escolhidas a partir dos resultados obtidos na literatura.41 De modo semelhante ao coagulante químico, também foi preparada uma solução padrão a 2% (peso/volume) do TANFLOC SG com o auxílio de agitador magnético, modelo C-MAG HS 7 da marca IKA, a fim de garantir a homogeneidade da solução. A preparação foi feita dessa forma em virtude da propriedade higroscópica do tanino. Foram realizados testes nas concentrações de 50, 100 e 150 mg L-1 de tanino, com ajuste de pH para valores 8, 6 e 4,5, objetivando encontrar o pH e concentração ótima para esse coagulante. Tratamento do efluente de lavanderia hospitalar com semente de moringa (MO) As sementes de Moringa oleifera foram descascadas, secas em estufa a 110 ºC por 1 h, trituradas com o auxílio de almofariz e pistilo resultando em um pó fino e secas novamente a 110 ºC por 20 min para remoção da umidade e, então, armazenadas em geladeira. Para o procedimento de secagem das sementes, foi realizada uma adaptação nas metodologias aplicadas nos trabalhos realizados pelos grupos de pesquisa de Ströher et al.26 e Cardoso et al.42 A Figura 3 apresenta a semente em sua forma íntegra, já descascada e triturada.
Três metodologias para a aplicação da semente foram testadas: em solução de cloreto de sódio, em pó e em solução em água. (i) Solução em cloreto de sódio: a massa necessária do pó triturado foi agitada em solução de cloreto de sódio (NaCl) 1,0 mol L-1, sendo agitado por 30 min em agitação rápida. Após agitação, o extrato salino de Moringa oleifera foi filtrado em coador de tecido e seu pH mensurado. Nos testes de coagulação-floculação utilizando esse extrato, as concentrações variaram de 50 a 950 mg L-1. Para a realização dos ensaios, verificou-se a necessidade de ajuste de pH para 10 no lote 3 de efluente bruto, com hidróxido de sódio 6 N (NaOH), garantindo uma padronização dos experimentos. (ii) Pó da semente aplicado diretamente como agente coagulante: diferentes massas de pó foram adicionadas diretamente nos frascos do Jar Test. As concentrações de semente de Moringa oleifera variaram de 150 a 950 mg L-1. (iii) Solução em água deionizada: a massa necessária do pó triturado de semente de Moringa em água deionizada (extrato aquoso de Moringa oleifera), agitados por 30 min em agitação rápida e, posteriormente, a solução foi filtrada em filtro de tecido. As concentrações testadas variaram entre 150 e 950 mg L-1. Após o processo de agitação e filtragem da solução das sementes trituradas, observou-se a formação de uma solução branca (Figura 4S, Material Suplementar), indicando a dissolução de parte das sementes na água e na solução de NaCl 1,0 mol L-1, isso permite facilitar o contato dos agentes coagulantes com a sujidade presente no efluente. Conforme relatado em um estudo realizado por Ndabigengesere e Narasiah,43 cerca de 25% do pó triturado da semente é solubilizado durante a agitação. Ao utilizar o extrato a 5% (peso/volume), salino ou aquoso, das sementes de Moringa oleifera como agente coagulante, optou-se pelo preparo de uma nova solução padrão antes de cada ensaio, uma vez que é possível encontrar na literatura relatos indicando que o armazenamento do extrato pode tornar o processo de coagulação/floculação ineficiente, isso pode ser corroborado por um trabalho de Cardoso et al.44 O mesmo procedimento também foi realizado por Ndabigengesere e Narasiah,43 durante um estudo de 1998, visando prevenir o envelhecimento da solução padrão e consequente mudança na atividade de coagulação e decomposição dos compostos orgânicos. Ensaio microbiológico Para o ensaio microbiológico, foram utilizados o efluente bruto e após o tratamento com os três coagulantes (sulfato de alumínio, tanino e moringa) em meio ágar de contagem de placas (PCA), conforme sugerido pelo Standard Methods.40 As placas de Petri foram preparadas utilizando a técnica de semeadura em pour plate: adicionou-se 0,1 mL e 1 mL de amostra, de modo a realizar culturas com dois volumes distintos, depois foram adicionados aproximadamente 20 mL de meio de cultura líquido. Para a completa homogeneização, foram realizados movimentos em forma de "8", após a solidificação, as placas foram levadas para estufa bacteriológica da marca Solab à 35 ºC pelo período de 48 ± 3 h, sendo realizado o registro fotográfico após o primeiro e segundo dia de incubação. Uma autoclave modelo Q190-22 da marca Quimis foi utilizada para a esterilização do meio de cultura e das placas. E o processo de montagem das placas foi realizado em uma cabine de fluxo laminar. A contagem das colônias nas placas foi realizada após 48 h de incubação e representada em unidades formadoras de colônias (UFC) por mL, a fim de observar a evolução no desenvolvimento de colônias para as placas dos efluentes bruto e tratados com diferentes coagulantes. Calculou-se a média de cada duplicada. Para o efluente bruto, foi considerado que o valor encontrado é respectivo a 100% da capacidade de microrganismos se desenvolverem pelo período de 48 h. Enquanto, para as demais placas, calculou-se a porcentagem de inibição do crescimento em relação ao valor máximo encontrado para as culturas com o efluente bruto, dessa forma foi possível verificar o potencial de cada um dos coagulantes testados em relação a capacidade de inibir a proliferação de microrganismos após o tratamento.
RESULTADOS E DISCUSSÃO Antes de iniciar os testes em cada novo lote de efluente, foi realizada a caracterização deste de modo a garantir a reprodutibilidade dos tratamentos. A Tabela 1 permite comparar as características iniciais de cada um dos lotes trabalhados.
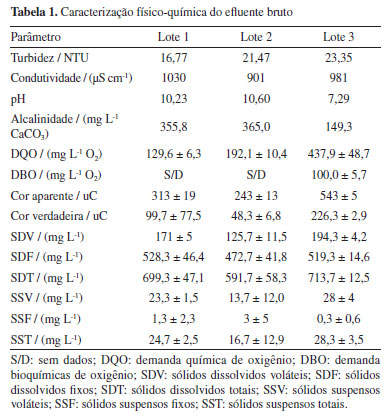
A partir dos resultados apresentados na Tabela 1, foi possível delinear o melhor tratamento aplicável aos 3 lotes. Primeiramente, o sulfato de alumínio foi testado como tratamento para o efluente de lavanderia hospitalar. Durante os ensaios sem ajuste de pH, foram observadas altas remoções turbidez (acima de 90%) para as concentrações de 250 e 400 mg L-1. Escolheu-se 250 mg L-1 como a melhor dosagem (menor custo) para continuidade dos testes. Dentre os valores de pH avaliados, os resultados obtidos com pH 5 e pH 7 não foram satisfatórios quanto os resultados em pH 9, em termos de remoção de turbidez, cuja remoção foi de 92%. Portanto, os últimos ensaios tendo como coagulante o sulfato de alumínio, foram realizados com pH 9. Pode-se verificar os resultados após cada ensaio nas Tabelas 1S e 2S do Material Suplementar. A Tabela 2 apresenta o melhor resultado obtido (100 mg L-1) com o coagulante químico.
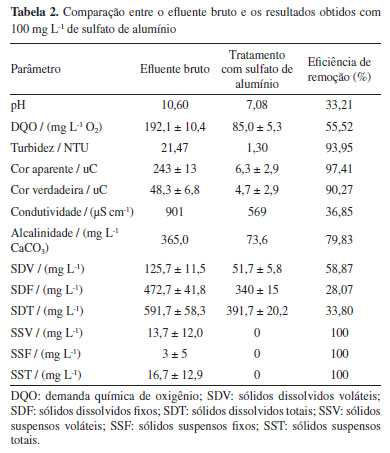
Embora a literatura relate que o sulfato de alumínio atua de modo satisfatório na faixa de pH 5 e 7, optou-se por avaliar, também, o desempenho desse agente químico no pH com valores próximos de 9 devido à natureza alcalina do efluente. Dessa forma, foi possível realizar o tratamento utilizando o menor volume de ácido sulfúrico possível, conforme também realizado por Zotesso et al.10 Após a realização de 7 ensaios utilizando o Al2(SO4)3 como coagulante, observou-se que, neste trabalho, a concentração ideal de Al2(SO4)3 encontrada para esse efluente foi igual à encontrada por Zotesso et al.,10 em 2015, onde 100 mg L-1 também foram suficientes para o tratamento do efluente de uma lavanderia hospitalar no processo de coagulação/floculação. A concentração ideal obtida para o Al2(SO4)3 permitiu observar uma remoção de cor e turbidez igual a 97,41 e 93,95%, respectivamente. Foi observada uma redução de 36,85% da condutividade, indicando a remoção de contaminantes químicos do efluente tratado e a remoção de 35,62% dos sólidos totais, sendo que 100% dos sólidos suspensos foram removidos após o período de sedimentação. Esse tratamento reduziu em mais da metade o teor de matéria orgânica, uma remoção de 55,52% de DQO foi encontrada para o efluente tratado. O sulfato de alumínio, durante o tratamento, consome naturalmente os constituintes da alcalinidade como os bicarbonatos, carbonatos e hidróxidos, o que promove a redução desse parâmetro e, consequentemente, a redução do pH do meio, segundo Coral et al.45 Para o presente trabalho, houve uma redução significativa de pH e a remoção de alcalinidade foi de 79,83%. O efluente após o tratamento com 100 mg L-1 de Al2(SO4)3 pode ser visualizado através da Figura 4.

Após finalizados os testes com sulfato de alumínio, iniciou-se os testes utilizando o coagulante tipo tanino. De acordo com recomendações do fabricante, o coagulante utilizado (TANFLOC SG) é efetivo na faixa de pH variando entre 4,5 e 8.24 Sendo assim, os testes ocorreram com ajustes de pH dentro da faixa recomendada em três concentrações distintas (50, 100 e 150 mg L-1). Foi observado que, na concentração de 50 mg L-1, em pH 6, a remoção de turbidez foi de 90%, semelhante as concentrações de 100 mg L-1 e 150 mg L-1, que foram 92 e 93%, respectivamente. Devido ao custo/benefício, optou-se pela menor concentração. Pode-se verificar os resultados após cada ensaio nas Tabelas 3S e 4S do Material Suplementar. Os valores dos parâmetros antes e após o tratamento da melhor condição estão expostos na Tabela 3.
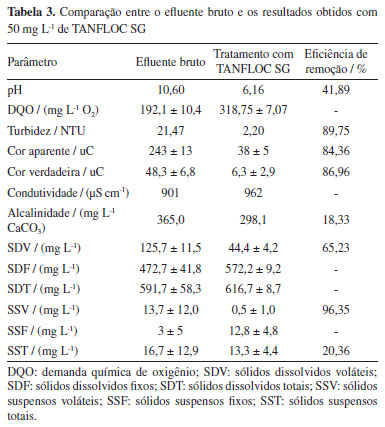
Como resultado, o pH 6 e concentração de 50 mg L-1 de tanino foi a condição de maior eficiência na remoção da cor aparente (84,36%) e da turbidez (89,75%). Essa dosagem foi semelhante à encontrada por Trevisan41 que concluiu através de seu estudo que 45 mg L-1 de TANFLOC SG foi a melhor concentração para tratar água com valores de cor aparente e turbidez elevados, atendendo ao padrão organoléptico da Portaria No. 2.914/201146 do Ministério da Saúde. Foi verificado um aumento da DQO no efluente pós-tratamento, o que nos leva a inferir que parte da matéria orgânica presente nesse coagulante não foi removida junto aos flocos, contribuindo para a carga de matéria orgânica solúvel do efluente. Para esse coagulante, a condutividade do efluente tratado aumentou ligeiramente em comparação ao efluente bruto. Vale ressaltar que, após tratamento, não foram observadas mudanças no pH, e que, diferente do sulfato de alumínio, foi observada a flotação dos flocos quando aplicadas concentrações superiores a 50 mg L-1. A Figura 5, referente ao primeiro ensaio com esse coagulante, evidencia essa característica.

Visando minimizar os custos com ajuste de pH do efluente, realizou-se também teste sem ajuste de pH, que se encontrava em torno de 10 antes do ensaio. Entretanto não foi observada a formação de flocos, conforme pode ser observado na Figura 6.

Esse resultado corrobora com a recomendação do fabricante no que se refere a faixa ótima de pH. O efluente tratado com 50 mg L-1 de TANFLOC SG, em pH 6 pode ser observado por meio da Figura 7.

Por fim, as sementes de moringa foram testadas como coagulante. Após consulta em literatura, decidiu-se testar três metodologias para aplicação da semente de moringa no tratamento físico-químico do efluente de lavanderia hospitalar: extraída em solução salina, semente pura e extraída em água. Partindo de uma concentração de 50 mg L-1 do extrato salino, foi observado o aumento dos parâmetros de turbidez e cor aparente do efluente tratado. Com esses resultados, foi necessário verificar maiores concentrações do extrato, chegando a 950 mg L-1. A dosagem que resultou na melhor remoção de turbidez (63%) foi de 850 mg L-1, sem ajuste de pH. Ao aplicar diretamente como coagulante as sementes trituradas, a melhor concentração foi de 350 mg L-1, resultando numa remoção de 68% de turbidez, sem ajuste de pH. Os resultados de todos os ensaios podem ser verificados nas Tabelas 5S a 8S do Material Suplementar. Como última metodologia empregada para utilização da semente de moringa como agente coagulante, aplicou-se o extrato aquoso. A concentração de 950 mg L-1, foi a que apresentou o melhor resultado dos parâmetros analisados, sobretudo na remoção da turbidez do efluente (78%). A Tabela 4 apresenta os melhores resultados obtidos para remoção de cor e turbidez para cada metodologia aplicada para o preparo das sementes de Moringa oleifera utilizadas no tratamento do terceiro lote de efluente bruto.
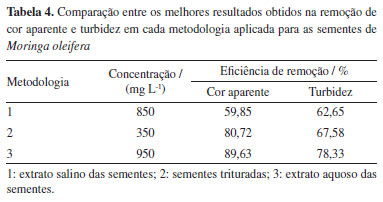
De acordo com a Tabela 4, é possível verificar que a metodologia 2 (semente triturada) foi a que demandou menor concentração de coagulante, entretanto, resultou em remoção menor que 70% de turbidez. Nesse sentido, o melhor resultado foi atingido ao se utilizar a metodologia 3, onde o extrato aquoso foi empregado, na concentração de 950 mg L-1, que resultou em remoção de turbidez próxima a 80%. Para comparar os resultados entre a mesma concentração para diferentes metodologias, pode-se consultar o Quadro 1S do Material Suplementar. Embora as concentrações requeridas para o tratamento com a moringa serem consideravelmente maiores que as dos demais coagulantes, ressalta-se a sua grande atividade antimicrobiana, o que é um fator positivo para um efluente de origem hospitalar. Dentre as metodologias avaliadas, o uso da semente de moringa em solução de NaCl 1,0 mol L-1 apresentou alta taxa de remoção de condutividade, ao avaliar o valor da condutividade do efluente bruto e tratado. Diversos resultados apresentaram uma eficiência maior que 99% na remoção de condutividade, essa relação pode ser verificada na Tabela 5.
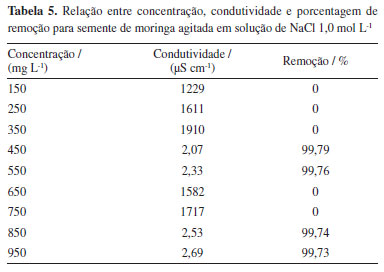
Essa eficiência na remoção da condutividade pode ser explicada pela presença de proteínas catiônicas e polieletrólitos presentes na semente de Moringa oleifera. Ambos atuam neutralizando as cargas das partículas presentes no efluente.32,33,36,47,48 Para os resultados supracitados, nota-se que não é possível obter uma linearidade entre a concentração e remoção de condutividade. Entretanto, esse resultado pode ser corroborado pelo trabalho de Olabimtan et al.,49 onde 30 mg L-1 conferiram uma redução de 86,28% desse parâmetro em um efluente de lavanderia comercial. Araújo etal.27 também obtiveram resultados satisfatórios ao utilizar o extrato da semente de Moringa oleifera em água destilada, conferindo uma remoção de 57,50% de condutividade ao final do tratamento. Com isso, o resultado apresentado na literatura vem de encontro com o presente trabalho. Entretanto, destaca-se que os dados referentes a essa queda brusca de condutividade ainda devem ser investigados, posto que na literatura ainda não há registros acerca do mecanismo de ação das sementes. A diminuição da condutividade presente em um efluente é considerada importante porque esse parâmetro é considerado um indicativo da presença de contaminantes iônicos no meio.50 Esse parâmetro é utilizado no controle de poluição de rios e lagoas para avaliação de possíveis impactos ambientais provocados pelo lançamento indevido de efluentes industriais.47 Logo, uma condutividade baixa pode nos permitir dizer que o efluente tratado possui uma baixa carga de contaminantes químicos. Para o efluente de lavanderia hospitalar, espera-se como poluentes químicos os íons oriundos da dissociação dos produtos químicos utilizados no processo de lavagem de roupas como, por exemplo, alvejantes, detergentes e amaciantes.5 Além disso, também existe a possibilidade da contaminação por fármacos, presentes em virtude do material excretado pelos pacientes nas roupas ou através da manipulação profissional. Para as três metodologias, é possível observar os resultados completos após cada ensaio no Material Suplementar, Tabelas 5S a 10S. Os resultados obtidos com o extrato aquoso de Moringa oleifera podem ser observados na Tabela 6.
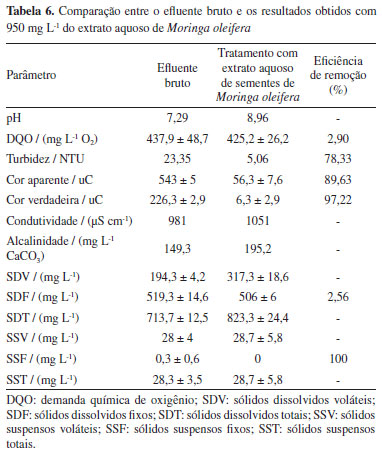
Pode-se observar, um aumento de 63,3% de sólidos dissolvidos voláteis (SDV), o que indica uma elevação no teor de matéria orgânica do efluente. Contudo, devido à origem natural das sementes, pode-se esperar um aumento do teor de matéria orgânica no efluente, provocado pela própria adição do coagulante durante o tratamento, conforme resultados encontrados por Ströher et al.51 A DQO não diferiu de modo significativo após o tratamento, levando a uma discreta redução de 2,9%. Por meio do teste F, comparou-se o valor de F calculado e o valor de F crítico em um nível de confiança de 95%. Desse modo, como Fcalculado < Fcrítico, tem-se que os resultados de DQO para o efluente bruto e tratado não diferem significativamente. A Tabela 7 apresenta os dados utilizados para a aplicação do teste F.
O pH do efluente foi ajustado para 10 para que houvesse um padrão de comparação com as demais metodologias aplicadas na utilização da semente de Moringa oleifera. Após o tratamento do efluente, foi possível observar que a semente de moringa também não causou alterações significativas no valor do pH em cada ensaio. O melhor resultado, concentração 950 mg L-1, foi obtido através da terceira metodologia, onde o extrato aquoso das sementes foi utilizado como coagulante. O valor encontrado é próximo ao obtido por Ndabigengesere e Narasiah,43 em 1998, que encontraram as dosagens ótimas entre 500 e 1000 mg L-1 para o tratamento de efluentes domésticos e industriais realizados em seu trabalho. Os autores também utilizaram o extrato aquoso a 5% de sementes de Moringa oleifera. O efluente tratado com 950 mg L-1 do extrato aquoso da semente de Moringa oleifera pode ser observado através da Figura 8.

Observou-se um aumento na alcalinidade do efluente tratado, o que pode ser explicado em razão da utilização de NaOH 6 N para o ajuste de pH durante os ensaios, uma vez que foi necessário elevar o pH do efluente bruto. Para fins de comparação entre os três coagulantes utilizados, pode-se observar no Material Suplementar as Tabelas 1S-10S, que permitem verificar os resultados de todos os parâmetros analisados ao final de cada um dos 24 ensaios realizados com os três coagulantes. As atuais legislações vigentes, seja a nível federal, estadual ou municipal, carecem de informações detalhadas sobre os parâmetros de cor e turbidez, bem como condutividade. Por isso, utilizamos legislações auxiliares para guiar nossos esforços para o tratamento mais adequado do efluente de lavanderia hospitalar, a fim de garantir a qualidade da água de um possível corpo hídrico receptor. De modo a verificar a eficiência do tratamento perante as legislações auxiliares utilizadas, primeiramente, a Tabela 8 permite a comparação de certos parâmetros do efluente com o valor máximo permitido (VMP) dispostos pela Portaria GM/MS No. 888, de 4 de maio de 2021,52 que dispõe de padrões organolépticos de potabilidade da água.
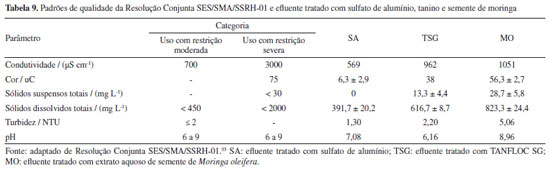
Pode-se verificar que o tratamento com sulfato de alumínio foi eficiente para atender aos limites estabelecidos pela Portaria GM/MS No. 888.52 Observa-se que o valor de turbidez para o efluente tratado com o extrato aquoso de semente de moringa é próximo ao VMP, entretanto sua cor aparente e sólidos dissolvidos totais encontram-se fora do limite permitido. O mesmo vale para o tratamento realizado com TANFLOC SG. Para os valores de pH, a resolução CONAMA No. 3576 estabelece que devem situar-se entre a faixa de 6 a 9, todos os tratamentos se enquadram na legislação, visto que estão entre valores de 7 a 8. Visando o reuso da água pode-se comparar a adequação de certos parâmetros por meio da Resolução Conjunta SES/SMA/SSRH-01,53 através da Tabela 9, onde há duas categorias: uso com restrição moderada e uso com restrição severa. A primeira diz respeito a atividades como irrigação paisagística, lavagem de logradouros e outros espaços públicos privados, construção civil, desobstrução de galerias de águas pluviais e rede de esgotos, lavagem de veículos e combate a incêndio. Enquanto que "uso com restrição severa" são para todos os usos mencionados anteriormente, excluindo combate a incêndio e lavagem interna de veículos.53
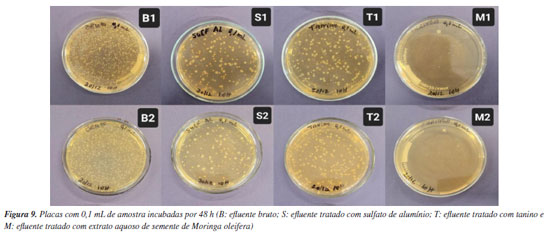
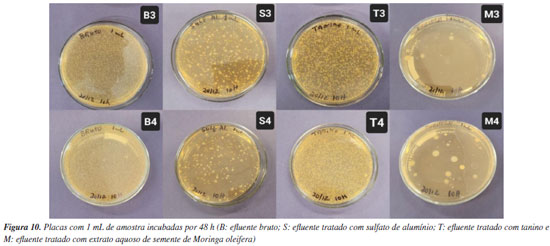
Por meio da análise entre o VPM e a caracterização dos efluentes tratados com os três coagulantes testados, tem-se que todos podem se enquadrar em "uso com restrição severa" e o sulfato de alumínio encontra-se dentro do esperado para "uso com restrição moderada". Contudo, ainda é necessário que o efluente passe por tratamento secundário, desinfecção e filtração. Analisando os resultados obtidos por Nonfodji et al.,37 Andrade,28 Vieira et al.38 e Lo Monaco et al.39 que constataram a eficácia da semente de moringa como agente antibacteriano, optou-se por comparar o crescimento de microrganismos do efluente bruto e tratado com os três coagulantes testados, de modo a verificar a capacidade de inibição de crescimento de microrganismos de cada um. Embora não tenha sido possível caracterizar o tipo de microrganismo presente nas amostras, foi possível verificar a capacidade de inibição provocada por cada um dos tratamentos nas placas cultivadas (Figuras 9 e 10). Sendo assim, os resultados são de natureza quantitativa.
Por meio da Tabela 10 é possível verificar a relação entre placas e unidades formadoras de colônias (UFC) por mL de amostra após 48 h de incubação.

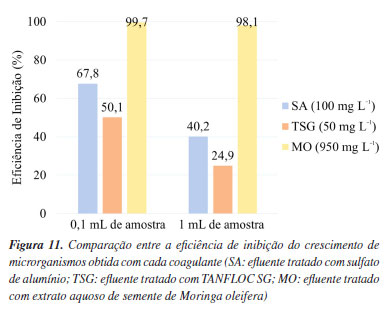
Conforme observado na Figura 11, tem-se que ao final das 48 h de incubação, o efluente tratado com as sementes de Moringa oleifera agitadas em água garantiu uma inibição de 99,7 e 98,1% no crescimento de microrganismos para as placas cultivadas com 0,1 mL e 1 mL de amostra, respectivamente. Já para os tratamentos realizados com sulfato de alumínio e tanino, os resultados não foram satisfatórios.
Considerando que o efluente alvo deste trabalho é oriundo de uma lavanderia hospitalar, espera-se a presença de bactérias e outros microrganismos patogênicos. Portanto, é importante que antes do lançamento no corpo hídrico, o tratamento não só o adeque aos parâmetros físico-químicos de interesse da legislação vigente, mas que também seja capaz de remover microrganismos responsáveis por doenças de veiculação hídrica, visando garantir a segurança da saúde pública. Então, a partir deste estudo, pode-se considerar o tratamento de efluentes não domésticos, como o de uma lavanderia hospitalar, com semente de moringa como uma alternativa, já que observamos que ela apresentou forte capacidade de reduzir a população de microrganismos no meio. Além de ser um coagulante proveniente de fonte natural e, portanto, não apresentar riscos ambientais consideráveis, a semente de moringa apresenta baixo custo e, também, é de fácil aquisição.
CONCLUSÕES A partir da realização de 24 ensaios, encontrou-se que as concentrações ótimas de coagulação/floculação para o sulfato de alumínio, tanino e extrato aquoso da semente de Moringa oleifera foram 100, 50 e 950 mg L-1, respectivamente. Para o sulfato de alumínio, foi possível alcançar remoções significativas de cor, turbidez e alcalinidade. Além da redução dos parâmetros DQO e sólidos totais. Os resultados obtidos com o tanino mostraram-se eficientes na remoção de cor e turbidez mesmo com a elevação desses parâmetros durante o último lote de efluente bruto trabalhado. Ademais, ele apresenta a menor concentração requerida para o tratamento. Já para a semente de Moringa oleifera, destaca-se seu desempenho na remoção de mais de 99% de condutividade quando empregado o extrato salino, reduzindo a carga de contaminantes químicos do efluente. E, para o extrato aquoso, mais de 98% de inibição do crescimento de microrganismos. Além disso, ela também apresentou resultados satisfatórios para redução de cor e turbidez. Após a mudança para o lote 3 de efluente, foi verificada a reprodutibilidade dos resultados encontrados anteriormente para o sulfato de alumínio e tanino. Assim, mesmo com cor e turbidez superiores ao primeiro e ao segundo lotes de efluente bruto, os resultados ainda se mostraram satisfatórios. Para o ensaio com o terceiro lote de efluente, o sulfato de alumínio conferiu remoções de cor e turbidez de 93,92 e 88,01%, respectivamente. Já para o tanino, encontrou-se remoções de 94,84 e 89,34% para os mesmos parâmetros. No caso da semente de moringa, esta foi avaliada diretamente no terceiro lote de efluente. Ao final do tratamento físico-químico, todos os efluentes tratados encontraram-se dentro da faixa de pH permitida pela legislação no que diz respeito ao padrão para lançamento de efluentes líquidos. A escolha do coagulante para o emprego no dia a dia da lavanderia dependerá da avaliação criteriosa dos gestores do hospital em relação ao custo-benefício de cada um deles em relação ao investimento disponível para realizar o tratamento. A avaliação da viabilidade técnica e econômica deve levar em consideração, além da eficiência na remoção dos poluentes, a facilidade ou não da compra dos reagentes e insumos necessários.
MATERIAL SUPLEMENTAR O material suplementar desse trabalho está disponível em http://quimicanova.sbq.org.br/, na forma de arquivo PDF, com acesso livre.
REFERÊNCIAS 1. Archela, E.; Carraro, A.; Fernandes, F.; Barros, O. N. F.; Archela, R. S.; Geografia 2010, 12, 517. [Link] acessado em Setembro 2024 2. Von Sperling, M.; Introdução à Qualidade das Águas e ao Tratamento de Esgotos, 4ª ed.; Editora UFMG: Belo Horizonte, 2014. 3. Ministério da Saúde, Brasil possui 1.915 Municípios sem Serviços Médicos Privados que Dependem Exclusivamente do SUS, https://www.gov.br/saude/pt-br/assuntos/noticias/2023/marco/brasil-possui-1-915-municipios-sem-servicos-medicos-privados-que-dependem-exclusivamente-do-sus#:~:text=O%20Sistema%20Único%20de%20Saúde,oferecem%20serviços%20particulares%20de%20saúde, acessado em Setembro 2024. 4. Souza, R. C.: Tratamento de Efluentes de Lavanderia Hospitalar para Fins de Reuso; Dissertação de Mestrado, Universidade Estadual de Maringá, Maringá, Brasil, 2012. [Link] acessado em Setembro 2024 5. Abreu, M. J. S.: Uso de Coagulantes e Floculantes Naturais no Tratamento de Efluentes de Lavanderia Hospitalar; Dissertação de Mestrado, Universidade Federal do Tocantins, Palmas, Brasil, 2020. [Link] acessado em Setembro 2024 6. Conselho Nacional do Meio Ambiente (CONAMA); Resolução No. 357, de 14 de março de 2005, Dispõe sobre a Classificação dos Corpos de Água e Diretrizes Ambientais para o seu Enquadramento; Diário Oficial da União (DOU), Brasília, de 18/03/2005. [Link] acessado em Setembro 2024 7. Fiorentini, V.: Uso do Tanino no Processo de Tratamento de Água como Melhoria em Sistema de Gestão Ambiental; Dissertação de Mestrado, Universidade Federal de Santa Maria, Santa Maria, Brasil, 2005. [Link] acessado em Setembro 2024 8. Silva, T. S. S.: Estudo da Tratabilidade Físico-Química com Uso de Taninos Vegetais em Água de Abastecimento e de Esgoto; Dissertação de Mestrado, Fundação Oswaldo Cruz, Rio de Janeiro, Brasil, 1999. [Link] acessado em Setembro 2024 9. Lo Monaco, P. A. V.; Matos, A. T.; Eustáquio Júnior, V.; Nascimento, F. S.; Paiva, E. C. R.; Revista Engenharia na Agricultura 2012, 20, 453. [Crossref] 10. Zotesso, J.; Honorio, J.; Cossich, E.; Tavares, C.; Anais do 37º Congresso Brasileiro de Sistemas Particulados; São Carlos, Brasil, 2015. [Crossref] 11. Sulaiman, M.; Zhigila, D. A.; Mohammed, K.; Umar, D. M.; Aliyu, B.; Manan, F. A.; Journal of Advanced Review on Scientific Research 2017, 30, 1. [Link] acessado em Setembro 2024 12. Thakur, S. S.; Choubey, S.; Int. J. ChemTech Res. 2014, 6, 3628. [Link] acessado em Setembro 2024 13. Mangrich, A.; Doumer, M.; Mallmannn, A.; Wolf, C.; Rev. Virtual Quim. 2014, 6, 2. [Crossref] 14. Ibrahim, A.; Yaser, A. Z.; Lamaming, J.; J.Environ. Chem. Eng. 2021, 9, 105007. [Crossref] 15. Cruz, J. G. H.: Alternativas para a Aplicação de Coagulante Vegetal à Base de Tanino no Tratamento do Efluente de uma Lavanderia Industrial; Dissertação de Mestrado, Universidade Federal do Rio Grande do Sul, Porto Alegre, Brasil, 2004. [Link] acessado em Setembro 2024 16. Beltrán-Heredia, J.; Sánchez-Mártin, J.; Solera-Hernández, C.; Ind. Eng. Chem. Res. 2009, 48, 5085. [Crossref] 17. Zotesso, J. P.; Cossich, E. S.; Janeiro, V.; Tavares, C. R. G.; Environ. Sci. Pollut. Res. 2017, 24, 6278. [Crossref] 18. Zotesso, J. P.; Cossich, E. S.; Tavares, C. R. G.; Anais do 11o Encontro Nacional de Produção Científica; Maringá, Brasil, 2019. [Link] acessado em Setembro 2024 19. Steinmetz, R. L. R.: Aplicação de Polieletrólitos para a Separação de Metais de Efluentes da Suinocultura; Dissertação de Mestrado, Universidade Federal de Santa Maria, Santa Maria Brasil, 2007. [Link] acessado em Setembro 2024 20. Auad, P.: Composição Química de Taninos Vegetais, Curtimento e Propriedades nos Couros; Dissertação de Mestrado, Universidade Federal do Rio Grande do Sul, Porto Alegre Brasil, 2018. [Link] acessado em Setembro 2024 21. Yin, C. Y.; Process Biochem. 2010, 45, 1437. [Crossref] 22. Koopmann, A. K.; Schuster, C.; Torres-Rodríguez, J.; Kain, S.; Pertl-Obermeyer, H.; Petutschnigg, A.; Hüsing, N.; Molecules 2020, 25, 4910. [Crossref] 23. Skoronksi, E.; Niero, B.; Fernandes, M.; Alves, M.; Trevesian, V.; Rev. Ambiente Agua 2014, 9, 680. [Crossref] 24. TANAC, TANFLOC SG, https://www.tanac.com.br/novo/wp-content/uploads/2021/06/CT_TANFLOC_SG_PT_0-1.pdf, acessado em Setembro 2024. 25. Santana, G. B.; Nóbrega, D. C.; Oliveira, J. T.; Martins, I. A.; Nascimento, R. F.; Vidal, C. B.; Revista Tecnologia 2020, 41, 1. [Crossref] 26. Ströher, A. P.; Couto Junior, O. M.; Menezes, M. L.; Bergamasco, R.; Pereira, N. C.; Revista E-xacta 2012, 5, 66. [Crossref] 27. Araújo, G. S.; Santos, Y. P.; de Oliveira, A. G.; Brazilian Journal of Development 2020, 6, 32822. [Crossref] 28. Andrade, P. V.: Uso da Semente de Moringa oleifera como Coagulante no Tratamento Terciário de Efluente Sanitário; Dissertação de Mestrado, Universidade Estadual Paulista Júlio de Mesquita Filho, São Paulo, Brasil, 2021. [Link] acessado em Setembro 2024 29. Ndabigengesere, A.; Narasiah, K. S.; Talbot, B. G.; Water Res. 1995, 29, 703. [Crossref] 30. Gassenschmidt, U.; Jany, K. D.; Bernhard, T.; Niebergall, H.; Biochim. Biophys. Acta, Gen. Subj. 1995, 1243, 477. [Crossref] 31. Ghebremichael, K. A.; Gunaratna, K. R.; Henriksson, H.; Brumer, H.; Dalhammar, G.; Water Res. 2005, 39, 2338. [Crossref] 32. Okuda, T.; Baes, A. U.; Nishijima, W.; Okada, M.; Water Res. 2001, 35, 405. [Crossref] 33. Broin, M.; Santaella, S.; Cuine, S.; Kokou, K.; Peltier, G.; Joet, T.; Appl. Microbiol. Biotechnol. 2002, 60, 115. [Crossref] 34. Sousa, A. M. P.; Salles, H. O.; Oliveira, H. D; Souza, B. B. P.; Cardozo Filho, J. L.; Sifuentes, D. N.; Prates, M. V.; Bloch Junior, C.; Bemquerer, M. P.; Egito, A. S.; J. Proteomics 2020, 217, 103692. [Crossref] 35. Muyibi, S. A.; Evison, L. M.; Water Res. 1995, 29, 1099. [Crossref] 36. Ghebremichael, K. A., Moringa Seed and Pumice as Alternative Natural Materials for Drinking Water Treatment, https://fr.ircwash.org/sites/default/files/Ghebremichael-2004-Moringa.pdf, acessado em Setembro 2024. 37. Nonfodji, O. M.; Fatombi J. K.; Ahoyo, T. A.; Osseni, S. A.; Aminou, T.; Journal of Water Process Engineering 2020, 33, 101103. [Crossref] 38. Vieira, G. H. F.; Mourão, J. A.; Ângelo, A. M.; Costa, R. A.; Vieira, R. H. S. F.; Rev. Inst. Med. Trop. Sao Paulo 2010, 52, 129. [Crossref] 39. Lo Monaco, P. A. V.; Matos, A. T.; Ribeiro, I. C. A.; Nascimento, F. S.; Sarmento, A. P.; Rev. Ambiente Agua 2010, 5, 222. [Crossref] 40. APHA; Standard Methods for the Examination of Water and Wastewaer, 23rd ed.; Baird, R. B.; Eaton, A. D.; Rice, E. W., eds.; Amer Public Health Assn: Washington, 2017. 41. Trevisan, T. S.: Coagulante Tanfloc SG como Alternativa ao Uso de Coagulantes Químicos no Tratamento de Água na ETA Cafezal; Trabalho de Conclusão de Curso, Universidade Tecnológica Federal do Paraná, Curitiba, Brasil, 2014. [Link] acessado em Setembro 2024 42. Cardoso, E. S.; Santana, F. N. R. P.; Santos, T. M.; Santana, S. F.; Silva, G. F.; Faria, L. J. G. Em Engenharia de Produtos Naturais: Planejamento, Experimentação, Obtenção de Produtos e Purificação; Faria, L. J. G.; Andrade, E. L., orgs.; Editora Científica Digital: Guarujá, 2021, p. 51. [Crossref] 43. Ndabigengesere, A.; Narasiah, K. S.; Environ. Technol. 1998, 19, 789. [Crossref] 44. Cardoso, K. C.; Bergamasco, R.; Cossich, E. S.; Moraes, C. K.; Acta Sci., Technol. 2008, 30, 193. [Crossref] 45. Coral, L. A.; Bergamasco, R.; Bassetti, F. J.; 2nd International Workshop Advances in Cleaner Production; São Paulo, Brasil, 2009. [Link] acessado em Setembro 2024 46. Ministério da Saúde; Portaria No. 2.914, de 12 de dezembro de 2011, Dispõe sobre os Procedimentos de Controle e de Vigilância da Qualidade da Água para Consumo Humano e seu Padrão de Potabilidade, Brasil, 2011. [Link] acessado em Setembro 2024 47. Almada, R. B.: Processos Físico-Químicos Acoplados para Tratamento de Efluente Industrial para Fins de Reuso; Dissertação de Mestrado, Universidade Federal do Rio de Janeiro, Rio de Janeiro, Brasil, 2008. [Link] acessado em Setembro 2024 48. Franco, C. S.; Batista, M. D. A.; Oliveira, L. F. C.; Kohn, G. P.; Fia, R.; Eng. Sanit. Ambiental 2017, 22, 781. [Crossref] 49. Olabimtan O. H; Batari M. L.; Suleman, S. M.; Esew, O.; Abubakar Z.; International Journal of Creative and Innovative Research in All Studies 2019, 2, 59. [Link] acessado em Setembro 2024 50. Companhia Ambiental do Estado de São Paulo (CETESB); Apêndice C - Significado Ambiental e Sanitário das Variáveis de Qualidade das Águas e dos Sedimentos e Metodologias Analíticas e de Amostragem 2022; CETESB: São Paulo, 2022. [Link] acessado em Setembro 2024 51. Ströher, A. P.; Menezes, M. L.; Bergamasco, R.; Pereira, N. C.; Engevista 2013, 15, 255. [Crossref] 52. Ministério da Saúde; Portaria GM/MS No. 888, de 04 de maio de 2021, Altera o Anexo XX da Portaria de Consolidação GM/MS No. 5, de 28de setembro de 2017, para Dispor sobre os Procedimentos de Controle e de Vigilância da Qualidade da Água para Consumo Humano e seu Padrão de Potabilidade; Diário Oficial da União (DOU), Brasília, No. 85, de 07/05/2021, p. 127. [Link] acessado em Setembro 2024 53. Governo do Estado de São Paulo; Resolução Conjunta SES/SMA/SSRH No. 01, de 28 de junho de 2017, Disciplina o Reuso Direto não Potável de Água, para Fins Urbanos, Proveniente de Estações de Tratamento de Esgoto Sanitário e dá Providências Correlatas; Diário Oficial do Estado de São Paulo (DOE), São Paulo, de 29/06/2017, seção I, p. 41-42. [Link] acessado em Setembro 2024
Editor Associado responsável pelo artigo: Cassiana C. Montagner |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access