Educação
|
|
| Reutilização do ácido acetilsalicílico preparado nas aulas de química orgânica experimental como revelador de impressões digitais: uma aplicação no ensino de química Reuse of acetylsalicylic acid synthesized in organic chemistry lab classes as a fingerprint developer: an application in chemistry education |
|
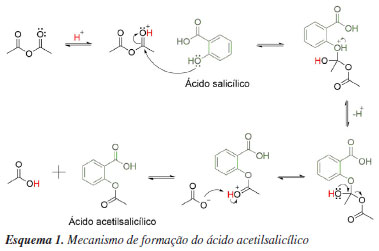
Caroline I. SilveiraI,II; Samuel A. PereiraI,II; Victoria B. V. de LeonI; Jeanifer T. CamachoI; Amanda F. LeitzkeI; Rogério A. FreitagI; Claudio M. P. de PereiraI I. Laboratório de Inovação em Química (InnovasChem), Centro de Ciências Químicas, Farmacêuticas e de Alimentos (CCQFA), Universidade Federal de Pelotas, 96010-900 Pelotas - RS, Brasil Recebido: 22/03/2024 *e-mail: brunondrosa@gmail.com Acetylsalicylic acid (ASA) synthesized in the practical classes of experimental organic chemistry is generally discarded after the classes. Thus, the objective of this work is to find an alternative application for ASA and to promote awareness about the recycling of chemicals in educational and research environments. In addition, it explores the subsequent application of this synthesized ASA in the creation of powdered developers for latent fingerprints. The adopted methodology included the recrystallization of the previously synthesized ASA, followed by the development of three distinct formulations of powdered developers, which include ASA, lignin, and methylene blue. Subsequently, these powders were used to identify latent fingerprints, demonstrating that they are promising substances for such applications. INTRODUÇÃO O ácido acetilsalicílico, popularmente conhecido como Aspirina®, é um dos primeiros medicamentos sintéticos documentados na história e amplamente utilizado ainda nos dias atuais. Inicialmente empregado como anti-inflamatório, atualmente é aplicado em novas terapias devido aos progressos na pesquisa.1 A sua origem iniciou através da casca de salgueiro contendo salicina como analgésico. A síntese do ácido salicílico (AS) em 1859 por Hermann Kolbe foi um marco, embora seu uso farmacológico fosse limitado devido a efeitos colaterais. Felix Hoffmann alcançou a primeira síntese estável e pura de ácido acetilsalicílico em 1897, na qual foi patenteada pela Bayer em 1900 se tornando o analgésico mais popular do mundo. Seu potencial anticoagulante foi descoberto em 1953, e seu mecanismo de ação em 1971, rendendo aos pesquisadores o Prêmio Nobel.1 A síntese de ácido acetilsalicílico (AAS) é uma atividade comum em aulas de química orgânica experimental. Nessas aulas os alunos são expostos ao mecanismo reacional subjacente à formação do composto e também adquirem conhecimentos sobre técnicas de laboratório essenciais, incluindo o processo de refluxo e os princípios da filtração.2,3 A síntese do AAS envolve a reação de acetilação do ácido salicílico, na qual um grupo acetila é adicionado à molécula. O mecanismo da formação do ácido acetilsalicílico está representado no Esquema 1. Primeiramente, o anidrido acético é protonado, formando um carbocátion que aumenta a sua reatividade. Em seguida, acontece a adição da hidroxila fenólica a carbonila ativada. Então, a remoção do hidrogênio estabiliza o oxigênio positivamente carregado. Posteriormente, há a deslocalização do par de elétrons da hidroxila, formando uma dupla ligação com o carbono e rompendo a ligação C-O, gerando o ânion acetato. Por fim, este ânion acetato retira o hidrogênio ligado ao oxigênio positivamente carregado, formando o produto ácido acetilsalicílico.4 Essa reação é geralmente realizada em um sistema de refluxo, que permite a elevação da temperatura e a manutenção das condições reacionais por um período prolongado. Após a síntese, o produto é isolado e purificado através de técnicas de filtração, como a filtração a vácuo ou a filtração por gravidade. Essas técnicas permitem a separação do sólido desejado (AAS) dos resíduos ou impurezas presentes na mistura reacional. Além de aprender sobre o mecanismo de síntese do AAS, os alunos também desenvolvem habilidades práticas, como o manuseio adequado de equipamentos de laboratório, controle de temperatura, manipulação de reagentes e produtos químicos, e segurança no laboratório.5-7
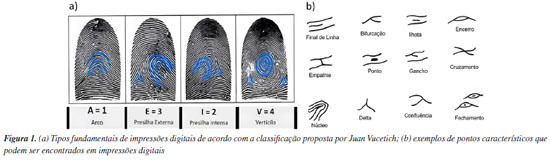
No entanto, é comum que o produto sintetizado seja descartado após o término da aula, o que levanta questões sobre a otimização do uso de recursos e a minimização de resíduos químicos. Este trabalho surge do princípio de prevenção da química verde que consiste em evitar a produção de um resíduo químico, ressignificando assim um produto químico puro e transformando-o em um material multidisciplinar, purificando-o por recristalização e investigando seu potencial uso em uma aplicação prática e forense: a formulação de pós reveladores de impressões digitais.8 As impressões digitais desempenham um papel importante na perícia forense e podem ser usadas para identificar indivíduos com uma alta probabilidade de precisão.9 Juan Vucetich foi um pioneiro na ciência das impressões digitais e é conhecido por ter desenvolvido um sistema de classificação de impressões digitais em seu livro “Dactiloscopia Comparada”.10 Em 1892, Juan Vucetich utilizou suas habilidades e conhecimentos para resolver um caso criminal importante na Argentina, uma vez que as impressões digitais foram fundamentais para identificar o culpado. Em seu sistema de classificação de impressões digitais Vucetich subdividiu as impressões digitais de acordo com a posição e direção de conjuntos de cristas assim como a presença ou ausência de delta obtendo quatro tipos fundamentais de impressões digitais sendo eles o arco, a presilha interna, a presilha externa e o verticilo (Figura 1a).9,10
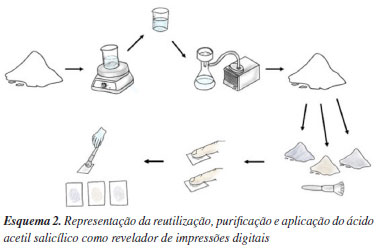
Além dos quatro tipos fundamentais de desenhos papilares nas impressões digitais (arco, presilha, verticilo e composto), os detalhes específicos das cristas das impressões digitais são compostos por uma série de minúcias ou pontos característicos como pode ser observado na Figura 1b. Essas minúcias são perturbações fisiológicas naturais nas cristas que são usadas para a identificação e comparação de impressões digitais.10 As impressões digitais, quando detectadas em locais de crime, são consideradas como evidências circunstanciais e incontestáveis em investigações forenses e para a justiça criminal, pois as impressões digitais possuem características como unicidade, perenidade e imutabilidade.11 As impressões digitais latentes são amplamente encontradas em locais de crime, porém para sua identificação é necessária a utilização de alguma técnica de visualização. Existem diversas técnicas para revelação de impressões digitais latentes e a mais amplamente empregada é a técnica de revelação por pó revelador devido à sua simplicidade e eficácia, essa técnica se baseia na aderência mecânica ou física dos pós aos componentes úmidos e oleosos dos resíduos das impressões digitais.12-14 Nesse sentido, o trabalho tem como objetivo usar AAS purificado para formulação de pós reveladores juntamente com a lignina e o azul de metileno. A lignina foi escolhida por ser um corante renovável, derivado de matrizes que são descartadas na indústria como a casca de arroz. Além disso, sua eficácia na revelação de impressões latentes foi previamente comprovada em estudos científicos já existentes.15 A escolha do azul de metileno como componente se deu ao seu baixo custo e à necessidade de disponibilizar pós reveladores de diversas tonalidades, visando assegurar a eficácia na revelação de impressões digitais em uma ampla variedade de superfícies coloridas.15-17 Além disso, existem graduações e pós-graduações que dispõem do ensino de papiloscopia, que é a ciência que estuda as impressões digitais para fins de identificação humana. O ácido acetilsalicílico é uma substância amplamente utilizada na medicina devido às suas propriedades analgésicas e anti-inflamatórias. No entanto, o seu potencial para revelação de impressões digitas não havia sido relatado. Nesse sentido, o trabalho visa avaliar a viabilidade desta aplicação alternativa como ilustrado no Esquema 2 e, ao mesmo tempo, promover a conscientização sobre a importância da reciclagem de produtos químicos em ambientes educacionais e de pesquisa.
PROCESSOS METODOLÓGICOS Recristalização e caracterização A recristalização do AAS sintetizado em aula prática de química orgânica experimental foi realizada com álcool etílico, de modo que 3 g do sólido obtido foi transferido para um béquer, foi adicionado 10 mL de álcool etílico e a mistura foi aquecida entre 56 e 60 ºC até completa dissolução. Após resfriamento, foram lentamente adicionados 50 mL de água destilada gelada e o sistema foi então deixado em repouso durante 15 min. Após a formação dos cristais, os mesmos foram separados por filtração a vácuo. Para avaliação do produto após recristalização, foi realizada uma cromatografia em camada delgada (CCD) utilizando placas de alumínio (20 cm × 20 cm) revestidas com sílica gel 60 F254 como fase estacionária e, como fase móvel, hexano e acetato de etila na proporção de 7:3. A revelação da CCD foi por meio de uma câmara escura de luz ultravioleta. A molécula foi caracterizada por espectrofotômetro de infravermelho com transformada de Fourier modelo IRSpirit, Shimadzu, utilizando pastilhas de KBr e leituras de 400 a 4000 cm-1 com 45 varreduras. A análise cromatográfica foi realizada utilizando cromatógrafo gasoso acoplado a espectrometria de massas modelo GCMS-QP2020, Shidmazu, equipado com coluna capilar RTX-5MS (30 m × 0,25 mm × 0,25 μm). A temperatura do forno foi fixada em 40 ºC, aumentando de 15 ºC min-1 para 280 ºC, mantendo-se durante 10 min. O hélio foi utilizado como gás de transporte (66 kPa) a um fluxo de 1,23 mL min-1. O injetor foi mantido a 280 ºC e funcionou durante 1 min no modo split (tempo de amostragem). A temperatura da interface e da fonte iônica foi de 300 e 200 ºC, respectivamente. O sistema MS foi operado em modo de ionização de impacto eletrônico a 70 eV e em monitorização de íons selecionadas (SIM). Os compostos encontrados nas amostras foram identificados utilizando bases de dados informatizadas de espectro de massa (NIST17) e dados provenientes da literatura para confirmar a pureza do AAS após a recristalização.18,19 Formulação A partir do AAS purificado foram realizadas três formulações distintas. Na primeira formulação (A), foi utilizado 0,5 g de AAS e 0,5 g de azul de metileno. Para a segunda formulação (B), foi utilizado 0,5 g de AAS e 0,5 g de lignina. Na terceira formulação (C), foi utilizado 0,5 g de AAS, 0,25 g de azul de metileno e 0,25 g de lignina. Todas as composições foram maceradas até a obtenção de um pó homogêneo.20,21 Deposição e revelação das impressões digitais latentes As impressões digitais latentes (naturais e sebáceas) foram obtidas através de três doadores e depositadas em placas de vidro. Para as impressões digitais latentes naturais, os doadores lavaram previamente as mãos com sabão neutro e, após 30 min, depositaram nas placas. Para as impressões digitais latentes sebáceas, os doadores friccionaram suavemente o polegar nas áreas oleosas do rosto (nariz e testa) para coletar as secreções sebáceas e, posteriormente, depositaram nas superfícies. Após 24 h de deposição, as revelações foram feitas utilizando as três formulações de pós mencionadas anteriormente e as mesmas foram registradas utilizando uma câmera fotográfica profissional (Canon EOS Rebel T6).22
RESULTADOS E DISCUSSÃO A partir do ácido acetilsalicílico proveniente das aulas de orgânica experimental foi realizada uma purificação por meio de recristalização. Após o processo de recristalização observou-se a formação de cristais na solução (Figura 2a), os mesmos foram separados por filtração a vácuo como ilustrado na Figura 2.

Primeiramente, após a purificação foi realizada a CCD em comparação entre o ácido salicílico que é utilizado como precursor na síntese do AAS, e o produto purificado. A Figura 3 representa a CCD obtida, na qual é possível observar o fator de retenção do AAS de 0,2 e para o AS de 0,55 no solvente utilizado (hexano e acetato de etila 7:3). Ambos compostos apresentam caráter polar, interagindo predominantemente com o acetato de etila da fase móvel. O hexano tem a função de reduzir esta interação, fazendo com que ocorra uma melhor separação dos compostos. Nota-se que a mancha do ácido acetilsalicílico possui uma menor interação com a fase móvel quando comparado à mancha do ácido salicílico. Isso ocorre porque o grupo fenólico presente no AS possui maior polaridade que o grupo éster do AAS.23,24 Dessa forma, podemos aferir que todo o reagente foi consumido e consequentemente o produto foi formado. Além disso, é possível observar apenas uma mancha no AAS, o que também indica que o produto está puro, sendo essa informação confirmada pela cromatografia gasosa.

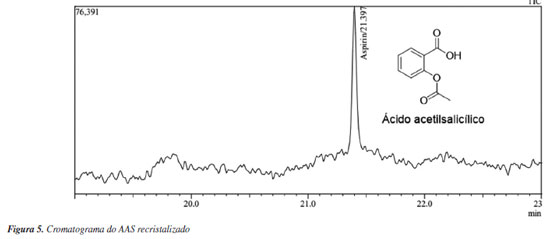
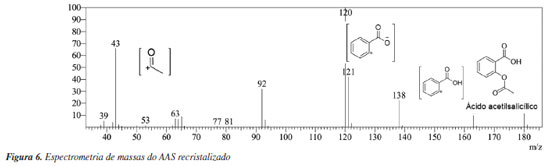
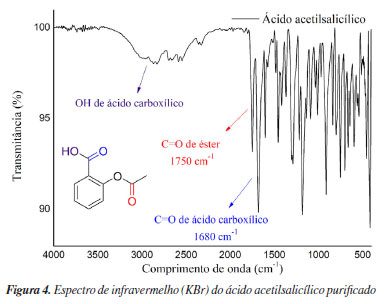
A caracterização do AAS foi realizada por espectrometria de infravermelho e cromatografia acoplada a espectrometria de massas como ilustrado nas Figuras 4, 5 e 6 respectivamente. No espectro de infravermelho (Figura 4) é possível observar bandas características do AAS, bem como a banda de hidroxila (OH) de ácidos carboxílicos em 3100 cm-1, e as bandas de carbonila (C=O) de éster e ácido carboxílico respectivamente em 1750 e 1680 cm-1. Cabe salientar que se não houvesse ocorrido a formação do produto, não seria possível a visualização da banda referente a C=O de éster. Além disso, o cromatograma (Figura 5) apresenta um único pico no tempo de retenção 21,397 min, o que indica que o composto em questão está puro. Na Figura 6, é possível observar o espectro de massas que apresenta o padrão de fragmentação da estrutura química, de modo que a razão massa carga 180 m/z refere-se ao íon molecular do AAS. As fragmentações em 121 e 120 m/z ([C7H5O2]+ e [C7H4O2]+), correspondem à perda característica do grupamento acetila, já a fragmentação em 43 m/z ([C2H3O]+), à perda e o aparecimento da carbonila.25
Após a confirmação da pureza do AAS, foram realizadas três formulações distintas contendo AAS, lignina e azul de metileno como representado na Figura 7. Por meio da adição desses pigmentos, é possível observar que a coloração final das formulações A-C apresentou cor azul claro, laranja e marrom respectivamente. Essas diferentes colorações são importantes, pois as impressões digitais podem ser encontradas em diferentes objetos que vão apresentar diferentes cores.26 Com isso, é indicada a utilização do pó que apresenta o melhor contraste de acordo com o substrato.
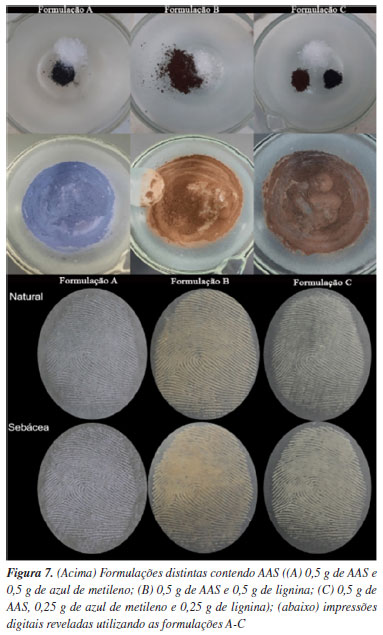
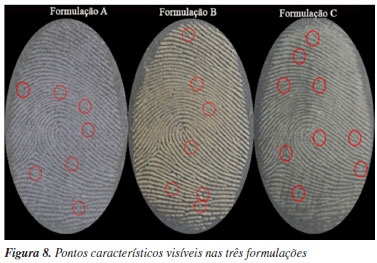
Feitas as formulações, os pós foram aplicados em impressões digitais latentes naturais e sebáceas de 3 doadores. A Figura 7 também apresenta as imagens das impressões digitais reveladas utilizando as formulações A-C. A partir das imagens é possível observar que todas as formulações foram promissoras na revelação das impressões digitais demonstrando imagens das papilas dérmicas dos doadores de forma clara, o que permitiria que fossem utilizadas para fins de identificação humana. Cabe ressaltar que a formulação B com lignina foi mais eficiente e isso pode se dar pela lignina utilizada ter alta concentração de SiO2, o que permite uma boa capacidade de interação do material com as secreções deixadas pelas impressões digitais e não ao substrato.15 Vale ressaltar que os pós utilizados atualmente tanto para perícia, pela polícia científica, como para ensino em cursos de graduação e pós-graduação em áreas relacionadas à química forense, são adquiridos via importação, o que acaba elevando o custo destes materiais, uma vez que não existe um produto nacional. Dessa forma, a reutilização desses compostos obtidos das aulas práticas de orgânica experimental e que seriam descartados, constituem uma solução sustentável e de menor custo para a universidade proporcionar ensino nessa área. A Figura 8 demonstra impressões digitais reveladas com as três formulações, onde é possível observar o tipo fundamental de presilha externa e alguns pontos característicos. Esses detalhes das cristas e as minúcias são o que provavelmente identificaria um suposto indivíduo em uma cena de crime.11
Finalmente, é importante destacar que, por meio deste experimento, é viável introduzir aos estudantes conceitos relacionados à síntese orgânica, cromatografia, interpretação de resultados analíticos e ciências forenses, com foco na papiloscopia. A utilização dessas substâncias como agentes reveladores de impressões digitais latentes com propósitos educacionais tem como principal objetivo a ampliação da aprendizagem, estabelecendo conexões claras entre a teoria e a prática. Isso promove a compreensão da química aplicada e desperta o interesse dos alunos nas aulas, especialmente porque a química forense é uma área em crescimento.27,28 Além disso, esses compostos são facilmente obtidos, possuem custos reduzidos em comparação com os produtos recomendados para revelação de impressões digitais latentes e são caracterizados por sua baixa toxicidade, tornando seu uso seguro em laboratórios para os estudantes. O Quadro 1 resume as questões abordadas sobre o tema.

CONCLUSÃO E PERSPECTIVAS Primeiramente, a recristalização do AAS se mostrou eficaz na obtenção de cristais puros demonstrando a viabilidade de aproveitar o AAS sintetizado nas aulas. As formulações dos pós reveladores com AAS recristalizado, lignina e azul de metileno apresentaram eficiência quanto ao potencial de ser aplicado no ensino de química forense ampliando seu alcance e utilidade em ambientes educacionais e de pesquisa. O experimento proposto neste estudo pode ser implementado no ensino de Química em cursos de graduação e técnicos em Química, Farmácia e Toxicologia. Essa abordagem oferece conteúdos teóricos e práticos para explorar a síntese de compostos orgânicos, o reaproveitamento de resíduos, interpretação de resultados analíticos como infravermelho, cromatografia gasosa e espectrometria de massas, em um contexto de aplicação em ciências forenses, com ênfase na papiloscopia. Isso naturalmente desperta o interesse dos alunos devido à relevância prática do assunto. Vale ressaltar que o AAS e suas respectivas formulações demonstraram eficácia como reveladores de impressões digitais, tanto para impressões digitais naturais quanto sebáceas, em superfícies de vidro. Além disso, os compostos são facilmente obtidos, têm baixo custo e não apresentam toxicidade, o que permite sua utilização segura em ambiente de sala de aula. O trabalho não apenas abordou a otimização de recursos e a minimização de resíduos químicos, mas também ofereceu uma solução sustentável e eficaz.
AGRADECIMENTOS Agradecemos a CAPES (001), FAPERGS (22/2551-0001050-4) e INCT Forense (465450/2014-8).
REFERÊNCIAS 1. Fijałkowski, Ł.; Skubiszewska, M.; Grześk, G.; Koech, F. K.; Nowaczyk, A.; Molecules 2022, 27, 8412. [Crossref] 2. Solomons, T. W. G.; Fryhle, C. E.; Snyder, S. A.; Química Orgânica, 12ª ed.; LTC: Rio de Janeiro, 2018. 3. da Luz, L. T. S.; Gomes, S. I. A. A.; Sandri, M. C. M.; de Mello, F.; Bolzan, J. A.; Educ. Quim. 2019, 30, 54. [Crossref] 4. Anbu, N.; Nagarjun, N.; Jacob, M.; Kalaiarasi, J. M. V. K.; Dhakshinamoorthy, A.; Chemistry 2019, 1, 69. [Crossref] 5. Pimenta, S. F.; Gomes, S. I. A. A.; Sandri, M. C. M.; Revista Debates em Ensino de Química 2023, 10, 180. [Link] acessado em Outubro 2024 6. Domingues, L. A.; Magalhães, C. G.; Sandri, M. C. M.; Quim. Nova Esc. 2022, 44, 105. [Crossref] 7. da Luz, L. T. S.; Gomes, S. I. A. A.; Sandri, M. C. M.; de Mello, F.; Bolzan, J. A.; Educ. Quim. 2019, 30, 54. [Crossref] 8. Lenardão, E. J.; Freitag, R. A.; Dabdoub, M. J.; Batista, A. C. F.; Silveira, C. C.; Quim. Nova 2003, 26, 123. [Crossref] 9. Figini, A. R.; Datiloscopia e Revelação de Impressões Digitais, 1a ed.; Millennium: Campinas, 2012. 10. Caballero, S. A. D.; Papiloscopia. Certeza ou Dúvida? Apologia à Micropapiloscopia, 2ª ed.; Millennium: Campinas, 2012. 11. Velho, J. A.; Geiser, G. C.; Espindula, A.; Ciências Forenses: Uma Introdução às Principais Áreas da Criminalística Moderna, 3ª ed.; Millenium: Campinas, 2017. 12. Leitzke, A. F.; Berneira, L. M.; da Rosa, B. N.; Moreira, B. C.; Mariotti, K. C.; Venzke, D.; Pereira, C. M. P.; Quim. Nova 2022, 45, 424. [Crossref] 13. Frick, A. A.; Chidlow, G.; Lewis, S. W.; van Bronswijk, W.; For. Sci. Int. 2015, 254, 133. [Crossref] 14. Carvalho, D. S.; da Cunha, W. F.; Lobo, B. J. M.; de Oliveira Neto, P. H.; Revista Brasileira de Ciências Policiais 2021, 12, 323. [Link] acessado em Outubro 2024 15. da Rosa, B. N.; da Rosa, M. P.; Poletti, T.; de Lima, N. P. K.; Maron, G. K.; Lopes, B. V.; Mariotti, K. C.; Beck, P. H.; Carreno, N. L. V.; de Pereira, C. M. P.; Surfaces 2022, 5, 481. [Crossref] 16. Arshad, A.; Farrukh, M. A.; Ali, S.; Khaleeq-Ur-Rahman, M.; Tahir, M. A.; J. For. Sci. 2015, 60, 1182. [Crossref] 17. Scotti, R.; Lima, E. C.; Benvenutti, E. V.; Piatnicki, C. M. S.; Dias, S. L. P.; Gushikem, Y.; Kubota, L. T.; Quim. Nova 2006, 29, 208. [Crossref] 18. Menegatti, R.; Fraga, C. A. M.; Barreiro, E. J.; Quim. Nova Esc. 2001, 16. [Link] acessado em Outubro 2024 19. dos Reis, C.; da Silva, R. M.; Braga, I. C.: Síntese do Ácido Acetilsalicílico e Recristalização com Diferentes Solventes Orgânicos; Trabalho de Conclusão de Curso, Centro Universitário UNIFACIMED, Cacoal, Brasil, 2022. [Link] acessado em Outubro 2024 20. Barbara, I. F. S.; Almeida, J. V. M.; Lopes, B. V.; Berneira, L. M.; Bueno, D. T.; Pereira, C. M. P.; XXXI Congresso de Iniciação Científica; Pelotas, Brasil, 2022. [Link] acessado em Outubro 2024 21. Leitzke, A. F.; Bueno, D. T.; Poletti, T.; Maron, G. K.; Lopes, B. V.; Morais, E. V.; Inacio, A. P. O. L.; Silveira, C. I.; da Silva, J. P.; Dias, D.; Carreño, N. L. V.; de Pereira, C. M. P.; Egyptian Journal of Forensic Sciences 2024, 14, 19. [Crossref] 22. Balsan, J. D.; Rosa, B. N.; Pereira, C. M. P.; Santos, C. M. M.; Quim. Nova 2019, 42, 845. [Crossref] 23. Dołowy, M.; Pyka-Pająk, A.; J. Planar Chromatogr.--Mod. TLC 2017, 30, 363. [Crossref] 24. Amorim, A. F. V.; Métodos Cromatográficos, 1ª ed.; Editora da Universidade Estadual do Ceará: Fortaleza, 2019. 25. Pavia, D. L.; Lampman, G. M.; Kriz, G. S.; Vyvyan, R. J.; Introdução à Espectroscopia, 5a ed.; Cengage: São Paulo, 2021. 26. da Rosa, B. N.; Maron, G. K.; Lopes, B. V.; Rocha, A. C. S.; Gatti, F. M.; Machado, J. O. A.; Barichello, J. M.; Mariotti, K. C.; Trossini, G. H. G.; Carreno, N. L. V.; Pereira, C. M. P.; Mater. Chem. Phys. 2023, 295, 127033. [Crossref] 27. Yamashita, B.; French, M.; Bleay, S.; Cantu, A.; Inlow, V.; Ramotowski, R.; Sears, V.; Wakefield, M. Em Latent Fingerprint Examination: Elements, Human Factors and Recommendations; Accursio, E., ed.; Nova Science Pubishers, Inc.: Nova York, 2014, p. 225. 28. Nicolodi, C.; da Rosa, B. N.; da Silva, C. C.; Berneira, L. M.; Pacheco, B. S.; Poletti, T.; Venzke, D.; Mariotti, K. C.; Pereira, C. M. P.; Quim. Nova 2019, 42, 962. [Crossref]
Editor Associado responsável pelo artigo: Giovanni W. Amarante |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access