Revisão
|
|
| Da amostragem à purificação: metodologias e técnicas para avaliação de siloxanos no biogás From sampling to purification: methodologies and techniques for evaluation of siloxanes in biogas |
|
Carla M. B. GomesI; Cleuciane T. do NascimentoI; Rodolfo A. SchaffnerI; Guilherme E. Q. SouzaI; Alessandra FreddoII; Daiana G. MartinezII; Helton J. AlvesI,* I. Departamento de Engenharia e Exatas, Universidade Federal do Paraná (UFPR, Setor Palotina), 85950-000 Palotina- PR, Brasil *e-mail: helton.alves@ufpr.br RESUMOBiogas has emerged as an important source of clean and renewable energy, with its energy viability dependent on purity grade. Primarily composed by methane and carbon dioxide, biogas can also contain nitrogen, water vapor, oxygen, hydrogen sulfide, ammonia, hydrocarbons and siloxanes. Regarding methane, all other components are considered contaminants, with volatile methylsiloxanes (VMSs) being the major challenge in terms of control and removal. VMSs are commonly found in personal care products and industrial applications, and their presence is highly detrimental to biogas energy generation equipment by forming silica deposits that cause fouling and damage, reducing operational efficiency and system longevity. In this context, three topics are crucial: (i) sampling techniques (bags, gas cylinders, canisters, adsorbent tubes, and impingers); (ii) detection and quantification methods for VMSs, highlighting gas chromatography coupled with mass spectrometry; and (iii) biogas purification/removal strategies (adsorption, absorption, refrigeration/condensation, biological degradation, and membrane separation). This review explores the methodologies involved in these topics, presenting literature research approaches and their effectiveness regarding siloxanes, contributing to biogas applications. Palavras-chave: siloxanes; biogas; sampling; analysis; purification.INTRODUÇÃO A busca por fontes de energias limpas e sustentáveis é considerada uma emergência mundial, devido ao constante desenvolvimento dos países junto com o alto consumo de combustíveis fósseis e não renováveis. Neste contexto, o biogás, um gás resultante de um processo fermentativo de biodigestão anaeróbica de diferentes biomassas, pode ser considerado uma importante alternativa de combustível limpo para a produção de energia renovável.1-6 A biodigestão anaeróbica é um processo biológico que, além de produzir biogás, também gera um biofertilizante. Esse processo ocorre por meio da decomposição de resíduos orgânicos, realizada por diferentes bactérias em condições de ausência ou restrição de oxigênio. As principais rotas metabólicas envolvidas são: hidrólise, acidogênese, acetogênese e metanogênese.7 O biogás produzido é majoritariamente composto por metano (CH4) em uma proporção entre 45 e 75%, e por dióxido de carbono (CO2) com teor variando entre 25 e 65%, e minoritariamente por outros gases, tais como nitrogênio (N2) (0-3%), vapor de água (H2O) (< 10%), oxigênio (O2) (0-1%), sulfeto de hidrogênio (H2S) (50-20.000 ppmv), amônia (NH3) (< 10.000 ppmv), hidrocarbonetos (0-200 mg m-3) e siloxanos (< 40 mg m-3). As proporções dos gases estão relacionadas com a matéria orgânica utilizada como substrato no processo de biodigestão anaeróbica.1-3 Outros fatores, tais como demanda biológica de oxigênio (DBO), demanda química de oxigênio (DQO), relação inóculo-substrato (RIS), relação carbono-nitrogênio (C/N), taxa de carga orgânica (TCO), tempo de retenção hidráulica (TRH), temperatura e pH, também afetam o rendimento da biodigestão.8 Com exceção do CH4, os demais constituintes mencionados são considerados contaminantes, sendo o CH4 o principal responsável pelo poder calorífico do biogás.1,4,6 Em geral, as técnicas de purificação do biogás estão relacionadas a remoção do H2S, devido aos problemas de corrosão de tubulações, motores e outros equipamentos metálicos provocados pela presença deste composto, enquanto os siloxanos são responsáveis pela formação de depósitos de sílica, causando incrustações.1,2,6,9 A purificação do biogás para o biometano (cerca de 90% de CH4) ou a reforma do biogás para hidrogênio, são processos que aumentam seu valor agregado.1 Entre as técnicas de purificação do biogás para o biometano têm-se por exemplo métodos físicos, químicos e biológicos. No Brasil, a Agência Nacional do Petróleo (ANP) por meio das Resoluções ANP No. 886/202210 e No. 906/202211 estabelece os parâmetros para o controle de qualidade do biometano, com teor mínimo de 90% de metano. O biometano possui uma composição similar ao gás natural, podendo substituí-lo em todas suas aplicações. Porém, a utilização do biometano para diferentes aplicações deve seguir altos padrões de qualidade.1,12 Neste cenário, além das técnicas direcionadas para purificação do biogás, outros aspectos também são relevantes no tema, sendo inclusive realizadas previamente às etapas de purificação. Dentre estas, têm-se metodologias para amostragem, detecção e quantificação dos compostos considerados indesejáveis no biogás. A realização destas etapas é capaz de direcionar quanto a necessidade da purificação do biogás e qual técnica é mais apropriada, a depender dos compostos detectados. Além disso, as técnicas de amostragem e detecção são fundamentais para indicar se a remoção de contaminantes do biogás está sendo eficiente e se pode ser aplicado para o uso desejado. Com base na amostragem, detecção e quantificação de siloxanos presentes no biogás, têm-se técnicas de coleta com e sem pré-concentração. A análise desses compostos por cromatografia gasosa é amplamente aplicada, utilizando-se diversos detectores.13 A quantificação é principalmente feita por cromatografia a gás acoplada à espectrometria de massas (CG-EM).14-16 Neste contexto, nos últimos anos, diversos estudos13,14 vêm sendo desenvolvidos com objetivo de indicar as principais vantagens e desvantagens de cada técnica de amostragem, de detecção e de remoção de siloxanos, com o intuito de garantir confiabilidade as análises envolvendo biogás e biometano. Esta revisão tem como objetivo apresentar os principais tópicos relacionados ao tema siloxanos no biogás, tais como amostragem, detecção e quantificação e remoção/purificação.
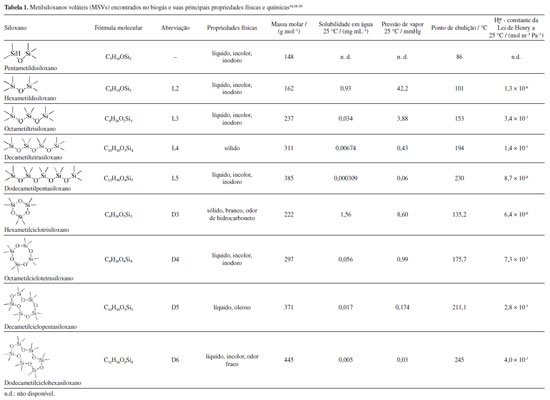
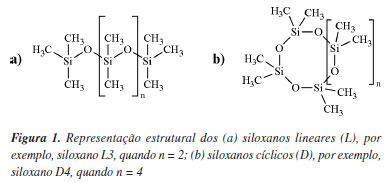
PRINCIPAIS CARACTERÍSTICAS DOS SILOXANOS Dentre as impurezas descritas como VOCs (do inglês, volatile organic compounds) estão os siloxanos, e entre estes, os metilsiloxanos voláteis (MSVs), que são encontrados no biogás. Os MSVs são considerados os compostos traços presentes no biogás mais difíceis de serem controlados e são altamente prejudiciais aos equipamentos.3,14,17 Os metilsiloxanos lineares possuem uma ligação do tipo (CH3)3SiO(Si(CH3)2O)nSi(CH3)3, no qual n varia de 0 a 4. E os cíclicos possuem uma ligação- (Si(CH3)2O)n-, no qual n varia de 3 a 6. Os MSVs encontrados no biogás são divididos em duas categorias, pela classificação da IUPAC, os cíclicos, denominados de configuração "D", e as estruturas lineares "L" conforme apresentado na Figura 1.12,14,18
A presença das ramificações metílicas nestes compostos confere à molécula algumas propriedades interessantes como hidrofobicidade, baixa solubilidade em água e estabilidade térmica, que aliada a baixa constante da Lei de Henry, auxiliam na alta volatilidade destes compostos, conforme apresentado na Tabela 1.12,14,17,19 Outro composto de silício e contaminante presente no biogás é o trimetilsilanol, comumente abreviado como TMSOH. Como este possui um grupamento OH diretamente ligado ao átomo de silício apresenta uma alta solubilidade do composto em água, diferente do observado para os MSVs.14
Os MSVs são encontrados principalmente em produtos de higiene pessoal e cosméticos, sendo assim descartados ao meio ambiente por meio do tratamento de esgoto e em aterros sanitários. Além disso, estão presentes em aplicações industriais, como aditivos em produtos de limpeza, desengordurantes, lubrificantes, solventes, tintas, vernizes e dispositivos médicos.3,4,6,12,21 Como não são decompostos durante o processo de biodigestão, os siloxanos acabam incorporados na biomassa, sendo que os mais voláteis acabam sendo volatilizados durante o processo de biodigestão e passam a compor o biogás. Por isto, os MSVs são encontrados majoritariamente em biogás originário de estações de tratamento de esgoto e aterro sanitário.4,6 Em geral, os siloxanos designados como D4 e D5 são os mais encontrados no biogás, representando mais de 90% da concentração total.9,22 Os MSVs podem trazer diversos impactos durante as aplicações do biogás, caso não sejam removidos ou não estejam presentes em baixas concentrações. No Brasil, as Resoluções ANP No. 886/202210 e No. 906/202211 estabelecem a concentração máxima de 0,3 mg de silício por m3 de biometano proveniente de estações de tratamento de esgoto e de aterro sanitário, para o uso veicular ou para a distribuição em instalações residenciais, comerciais e industriais. As normativas são baseadas nos padrões estabelecidos pela Sociedade Americana de Testes e Materiais (ASTM, do inglês American Society for Testing and Materials), e a Organização Internacional de Padronização (ISO, do inglês International Organization for Standardization) e Associação Brasileira de Normas Técnicas (ABNT).23 O Comitê Europeu de Normalização (ECS, do inglês European Committee for Standardization) estabelece o limite de 0,3 mg de silício por m3 de biometano, mesmo valor adotado pela ANP no Brasil.24,25 A Associação Canadense de Gás (CGA, do inglês Canadian Gas Association) estabelece o limite máximo de 1 ppmv, equivalente à 2,5 mg m-3 de L2 ou 6,2 mg m-3 de D5.26 Já a Comissão de Serviços Públicos da Califórnia (CPUC, do inglês California Public Utilities Commission) estabelece o limite de 0,1 mg m-3.26 A aplicação do biogás contaminado com MSVs em motores a combustão e trocadores de calor pode levar a formação de depósitos de sílica dentro do motor, danificando-o e reduzindo sua vida útil, bem como a redução da energia gerada na combustão, e aumento no custo operacional. A oxidação dos MSVs leva a formação de dióxido de silício (SiO2) (Equação 1). Durante a combustão, o SiO2 possui uma característica de vidro amorfo líquido, e após o resfriamento a fase amorfa cristaliza-se acumulando-se na forma de depósitos de micro-vidro.4,6,14,27-29 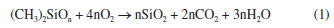 Desta forma, é de fundamental importância a identificação e quantificação destes compostos no biogás, para direcionar sua aplicação, bem como a avaliação se os sistemas de purificação utilizados estão sendo eficientes. O desenvolvimento de métodos de amostragem e quantificação requerem equipamentos modernos e por isso é vantajoso a análise de qual técnica é mais apropriada e mais confiável para este objetivo.
METODOLOGIAS DE AMOSTRAGEM A identificação e quantificação dos MSVs presentes no biogás dependem da coleta do gás e da análise realizada em laboratório. Um dos pré-requisitos para determinar a qualidade do biogás é referente ao método de coleta, que deve garantir que a composição encontrada seja um reflexo preciso do gás coletado, sem sofrer alterações ao longo do tempo de coleta e de acordo com o método de detecção utilizado. Ao escolher uma metodologia de coleta, é importante considerar os seguintes fatores:
Na literatura, as metodologias de coleta de siloxanos são divididas em dois grupos principais: coleta sem pré-concentração e coleta com pré-concentração. No método de coleta sem pré-concentração, todo o gás é coletado diretamente em recipientes, como cilindros de gás, canisters ou sacos de coleta. As vantagens incluem a facilidade no manuseio, a possibilidade de obter múltiplas amostras a partir de uma única coleta, além de sua versatilidade, já que o gás coletado pode ser dividido para diferentes análises. No entanto, algumas desvantagens devem ser consideradas, como a limitação do volume dos recipientes, que pode ser insuficiente para detectar compostos em níveis traço, além do risco de perdas de concentração durante o transporte, causadas por vazamentos, decomposição ou conversão dos compostos.13,30 Na coleta com pré-concentração, os compostos de interesse são concentrados em um meio específico, sem que o gás seja armazenado. Existem três abordagens principais: (i) coleta em meio sólido, por adsorção física ou química; (ii) coleta em meio líquido, por absorção e borbulhamento; e (iii) coleta criogênica, por condensação dos compostos.13,30 As técnicas de pré-concentração oferecem vantagens como maior eficiência na detecção de compostos traço, já que permitem a coleta de volumes maiores de gás sem necessidade de armazená-lo. Além disso, garantem maior segurança ao eliminar o risco de armazenar gases inflamáveis, como biogás e biometano. Por outro lado, essas técnicas apresentam desvantagens, como a possibilidade de saturação do material adsorvente, conhecida como volume de ruptura. Esse parâmetro corresponde ao volume de gás que atravessa o adsorvente até o momento em que os compostos adsorvidos começam a ser liberados na extremidade oposta. Quando esse volume é excedido, a eficiência da adsorção diminui, podendo superestimar a concentração dos compostos de interesse.13,30 Outro desafio é o efeito da umidade, que pode comprometer a eficiência, já que a água compete com os compostos de interesse pela adsorção. Esse problema pode ser mitigado com o uso de adsorventes hidrofóbicos ou pela realização de uma etapa prévia de secagem do gás. Além disso, há a necessidade de replicatas, já que cada coleta representa uma amostra única, ao contrário da coleta sem pré-concentração, onde uma única amostra pode ser dividida para várias análises.13,30 Sacos de amostragem Os sacos de amostragem para coleta de siloxanos são vedados e podem ser fabricados a partir de materiais como fluoreto de polivinila (PVF, Tedlar®), polietileno tereftalato (PET, Nalophan®) e politetrafluoretileno (PTFE, Teflon®). Embora esses materiais sejam amplamente utilizados, podem adsorver compostos orgânicos voláteis (VOCs) nas paredes internas dos sacos, afetando as taxas de recuperação. As principais vantagens do uso de sacos de amostragem incluem a facilidade e agilidade na amostragem, com pouco ou nenhum equipamento adicional, além de não requerer treinamento específico para o manuseio. Os sacos podem ser preenchidos sob baixa pressão ou com o auxílio de uma bomba diretamente da linha de gás. No entanto, é necessário cautela no transporte e armazenamento, pois o material do saco pode influenciar a adsorção de VOCs, comprometendo a recuperação. Além disso, a presença de metano, principal componente do biogás e inflamável, exige cuidados extras durante o transporte e o cumprimento de normas regulatórias.30,31 Pode-se considerar que, além da adsorção dos VOCs nas paredes dos sacos de amostragem, também pode ocorrer o mesmo efeito nos materiais componentes das válvulas de conexão, bem como fenômenos relacionados à permeabilidade do gás nas paredes do saco de amostragem, vazamento por meio do septo e de válvulas. O efeito contrário, ou seja, a permeabilidade do gás ambiente para dentro do saco de amostragem também pode ocorrer, alterando significativamente os valores de concentração dos analitos. Este movimento é afetado principalmente pela umidade e temperatura relativa dentro e fora do saco de amostragem. Fenômenos relativos à degradação fotoquímica também podem ocorrer, pela exposição do saco de amostragem à luz solar.30 Beghi e Guillot32 conduziram uma análise comparativa entre os sacos de amostragem Tedlar® e Nalophan® para a coleta de VOCs, tióis e siloxanos. Os resultados indicaram que os sacos Nalophan® resultaram em um cromatograma de fundo (background) mais limpo em comparação aos sacos Tedlar®, que apresentaram sinais referentes a compostos resultantes da degradação dos próprios sacos. Estes sinais interferiram na detecção dos sinais referentes aos VOCs, quando esses estão presentes em baixa concentração. O impacto resultante da diferença no material componente do encaixe dos sacos de coleta Tedlar® também já foi avaliado, por meio de ensaios de recuperação de siloxanos. Um modelo com um único encaixe de polipropileno foi comparado ao com encaixe de aço inoxidável de porta dupla. O mesmo procedimento foi realizado para os dois modelos, adicionando-se soluções de siloxanos em hexano, e posterior preenchimento com CH4 e CO2. Assim, foi possível indicar que após 8 dias, o primeiro modelo com encaixe de polipropileno apresentou recuperação de 85% enquanto o saco de coleta com encaixe em aço inoxidável apresentou apenas 30% de recuperação.33 Similarmente, o estudo desenvolvido por Mariné et al.34 também indicou uma menor porcentagem de recuperação de VOCs utilizando sacos de amostragem Tedlar® com encaixe de aço inoxidável. Conforme apresentado nos estudos citados, a perda dos VOCs ocorre entre a amostragem e a análise, no período de estocagem. Pode ocorrer a retenção na parede dos sacos de coleta utilizados e/ou nos materiais componentes do encaixe da válvula do saco de coleta. Algumas alterações também estão relacionadas as características de cada siloxano armazenado. Por exemplo, no estudo desenvolvido por Arnold e Kajolinna,28 a concentração do siloxano D5 caiu para 65% após um dia de armazenamento em um saco de coleta Tedlar®, enquanto a concentração dos siloxanos D4 e L4, com menor massa molar, foi de 87 e 88%, respectivamente, para o mesmo período. Este comportamento indica que houve uma rápida adsorção de D5 nas paredes do saco de coleta. Ajhar et al.33 e Arrhenius et al.35 também identificaram este comportamento, de rápida adsorção dos siloxanos mais pesados na parede do saco de coleta, quando comparado a siloxanos mais leves. Cilindros de gás Cilindros de gás também podem ser utilizados para a coleta de siloxanos. Ao contrário dos sacos de amostragem, os cilindros são utilizados para a coleta de gás sob alta pressão, podendo atingir valores acima de 5000 psi (345 bar). Esses cilindros estão disponíveis em alumínio e em aço inoxidável, sendo largamente utilizados na indústria de gás para a coleta de gás natural, e gás natural liquefeito para avaliação de sua composição gasosa, conforme a ISO 10715.36 Pela produção do biogás e do biometano serem predominantemente próximas à pressão atmosférica, os cilindros não são muito utilizados para amostragem destes gases, quando comparado a outras metodologias.13 Conforme observado para os sacos de amostragem, também pode ocorrer a perda de compostos traço por meio de fenômenos de adsorção na parede interna do cilindro.30 No estudo desenvolvido por Arrhenius et al.,35 foi observada uma maior estabilidade na concentração de siloxanos e compostos contendo enxofre quando estes foram armazenados em cilindros de gás passivados sob alta pressão (> 6 MPa) do que quando armazenados sob baixa pressão (0.8 MPa). Este comportamento está associado a fenômenos de adsorção, uma vez que sob baixa pressão, há uma maior proporção do número total de moléculas que irá ocupar os sítios ativos da superfície interna do cilindro. Em contraste, sob alta pressão, essa proporção diminui, resultando em um menor número de moléculas disponíveis para ocupar estes sítios ativos. De modo geral, encontrar o tratamento ideal para os cilindros destinados para o armazenamento de todas as espécies químicas encontradas no biogás e biometano é considerado desafiador.35 Canisters Os canisters também podem ser utilizados para a coleta de siloxanos. Estes são recipientes feitos de aço inoxidável no qual a amostragem é realizada evacuando-se o ar presente neles sob vácuo com controle de pressão, entre 0,3 e 1 bar. A coleta do gás é realizada pela conexão de uma válvula, até que o canister atinja o equilíbrio com a pressão atmosférica. Dentre as vantagens desta forma de coleta têm-se a facilidade no manuseio, no qual não é necessário nenhum equipamento adicional quando se opta pela coleta passiva, sem utilização de uma bomba. Na coleta denominada como ativa, uma bomba é utilizada para realizar o bombeamento do gás para o canister.13,30 Porém, como desvantagens, têm-se o alto custo do canister bem como o custo envolvido para a limpeza deste. Além disso, Brymer et al.37 concluíram que 168 de 194 VOCs foram recuperados utilizando esta metodologia de coleta, ou seja, apenas 86%. A perda observada pode ser devida a mecanismos de adsorção física, ou dissolução de compostos solúveis em água condensada e/ou reação química com outros compostos gasosos. A estabilidade de um VOC em um canister está relacionada a pressão de vapor, polaridade, solubilidade, e reatividade do composto em meio aquoso, bem como características da superfície do canister, pressão e temperatura durante a coleta e estocagem.38 Outra desvantagem desta técnica de coleta está atrelada à preparação dos padrões, uma vez que é necessária a introdução dos siloxanos no canister. Segundo Saeed et al.,39 esta pode ser feita pela adição dos siloxanos dissolvidos em um solvente orgânico, no estudo conduzido foi utilizado hexano. Porém, foi possível indicar que esta forma de introdução da amostra não é factível para os siloxanos de alto ponto de ebulição, como D4, D5 e D6, uma vez que estes necessitam de mais tempo para sua completa vaporização, indicando uma baixa porcentagem de recuperação. No estudo desenvolvido por Schweighkofler e Niessner,40 foi observada uma baixa porcentagem de recuperação para o siloxano L5, de 35%, enquanto D6 não pode ser recuperado, concluindo assim que a concentração de D6 no biogás não pode ser determinada por este método de coleta. Observações semelhantes foram relatadas no estudo desenvolvido por Hayes et al.,41 no qual foi realizada a comparação da coleta de siloxanos do biogás utilizando 3 metodologias, SummaTM canister, impingers preenchidos com metanol e tubos adsorventes com carvão ativo. Os autores concluíram pelos ensaios de recuperação realizados que SummaTM canister foi considerado com desempenho superior aos impingers com metanol quando se trata dos siloxanos mais leves, tais como pentametildisiloxano e D3. Porém, foi inferior nos resultados dos ensaios com os MSVs cíclicos D4, D5 e D6, no qual os impingers apresentaram melhor desempenho. Tubos adsorventes A utilização de tubos adsorventes é uma das metodologias classificadas como de pré-concentração. Estes são feitos de vidro de borossilicato ou de aço inoxidável com superfície passivada, e então são preenchidos com diversos materiais adsorventes sólidos, tais como carvão ativado, sílica gel, polímeros orgânicos porosos, como o Tenax®, e resinas como a XAD.15 Durante a coleta, o gás flui pelo tubo e os analitos ficam adsorvidos na superfície do material adsorvente. A dessorção pode ser realizada pela utilização de solventes e/ou aquecimento do material.30,31 Dentre as vantagens deste método está a facilidade na operação, manuseio, transporte e estocagem. Além disso, os adsorventes utilizados são selecionados de acordo com o composto desejado para a coleta, excluindo o efeito de matriz. A escolha do adsorvente é dependente de suas características físico-químicas e texturais. Uma das formas de avaliação da força adsorvente do material é por meio do volume de ruptura. Nesse sentido, quanto maior este volume, mais apropriado é o material adsorvente para aquele analito.30 Lamma et al.42 avaliaram este parâmetro, volume de ruptura, para MSVs nos seguintes adsorventes: Tenax® TA, Carbotrap®, Carbotrap® C, Chromosorb® 106, CarbosieveTM III e Caboxen® 1000. Neste estudo não foi indicado o melhor adsorvente para os compostos avaliados, uma vez que para todos foi encontrado, em geral, um baixo volume de ruptura. Adicionalmente, para os MVSs mais pesados não foi possível determinar este parâmetro, possivelmente devido à adsorção irreversível destes componentes nos adsorventes. Os autores indicaram que para este tipo de analito, deve ser avaliada a utilização de múltiplos tubos com materiais distintos para garantir total adsorção dos compostos em análise. Raich-Montiu et al.43 realizaram um estudo comparativo entre as técnicas de amostragem de pré-concentração de siloxanos e TMSOH. Foram utilizados tubos adsorventes ORBOTM 32 e impingers. Também foi realizada a amostragem sem pré-concentração, utilizando sacos de coleta Tedlar® de 200 L, seguida da concentração nas técnicas citadas. Não foi observada diferença significativa entre os resultados de amostragem de pré-concentração direta ou indireta, coleta em sacos Tedlar® e transferência para tubos adsorventes ou impingers. Porém, foi observada uma melhor resposta para a quantificação das coletas feitas diretamente em tubos adsorventes, principalmente para amostras provenientes de estações de tratamento de águas residuais com baixas concentrações dos siloxanos. Kim et al.44 também compararam os resultados da amostragem de biogás de aterro sanitário com tubos adsorventes e impingers. Porém, neste estudo, foram utilizados três materiais adsorventes, sendo estes, carvão ativado de coco, carvão ativado e sílica gel. Para a dessorção dos compostos, foi utilizado metanol. Dentre os materiais adsorventes, a sílica gel apresentou os piores resultados de concentração de siloxanos, enquanto os carvões avaliados apresentaram resultados próximos ao método tido como convencional, com impingers. Segundo os autores, é sugerida a utilização do carvão ativado de coco, em vez do uso de impingers, devido principalmente a facilidade de manuseio dos tubos adsorventes e do menor tempo de amostragem. Tansel e Surita45 também realizaram um estudo para avaliar se a utilização de carvão ativado seria adequada para a amostragem de siloxanos presentes em amostras de biogás coletadas da digestão anaeróbica proveniente de aterro sanitário e de estações de tratamento de água. A quantificação foi realizada a partir da dessorção térmica e por cromatografia gasosa acoplada à espectrometria de massas. Foi possível concluir que 700 mg de carvão ativado foram suficientes para a adsorção do TMSOH e do siloxano L2. Porém, para os siloxanos de massa molar mais altas, L3, D3, D4, D5 e D6, a utilização de apenas 1 tubo adsorvente não foi suficiente para a adsorção total, sendo estes encontrados nos tubos sequenciais (segundo, terceiro e quarto). Os autores indicaram que, a não adsorção dos siloxanos mais pesados não está necessariamente ligada à sua alta concentração no biogás, mas sim na baixa afinidade de adsorção do carvão ativado para com os siloxanos descritos. Sendo assim, para uma análise quantitativa confiável utilizando-se carvão ativado, seria indicado um aumento da quantidade de tubos e também da massa de carvão colocado em cada tubo, bem como a utilização de carvões funcionalizados. Gallego et al.46 desenvolveram e validaram um método para a quantificação de VOCs, incluindo MSVs utilizando duas das metodologias de amostragem já citadas. Inicialmente as amostras de biogás foram coletadas em sacos de amostragem de folha multilaminada inerte SupelTM, seguida pela transferência para tubos adsorventes Carbotrap®, CarbopackTM e Carboxen® 569. A dessorção térmica seguida de CG-EM, foi utilizada para a identificação e quantificação dos VOCs presentes nas amostras de biogás. Também foi avaliada a estabilidade dos compostos ao armazenamento em sacos de amostragem, em até 3 dias, comparando com os resultados obtidos pela transferência imediata do biogás para os tubos adsorventes citados. No estudo realizado por Mariné et al.34 já mencionado, também foi realizada a comparação entre dois métodos de amostragem de biogás, utilizando sacos de amostragem Tedlar® e cartuchos de tubos adsorventes, com três metodologias de detecção por CG-EM. Dentre os objetivos do estudo, foi realizada a comparação da estabilidade dos VOCs entre os dois métodos, em uma janela de estocagem de 4 dias. Em relação aos siloxanos avaliados, D3, D4 e D5, não foi recomendada a quantificação destes compostos com estocagem de longo período em sacos de coleta Tedlar®. Além disso, não foi recomendada a reutilização dos sacos, uma vez que os compostos foram detectados mesmo após a realização dos protocolos de limpeza implementados. A estabilidade dos siloxanos pelo mesmo período de 4 dias também foi avaliada utilizando-se tubos adsorventes preenchidos com Tenax® TA e Unicarb. As análises realizadas demostraram que apenas houve perda significativa após 4 dias de estocagem para alguns compostos, tais como nonano, nonadecano e etanotiol, demonstrando ser efetiva e confiável a utilização destes adsorventes para a coleta e quantificação de siloxanos. Impingers A utilização dos denominados impingers, tubos coletores por borbulhamento, também é uma técnica de coleta com pré-concentração. Nesses dispositivos, comumente feitos de vidro, é adicionado um solvente ou uma solução, no qual o gás irá ser borbulhado. Assim, neste processo ocorre a dissolução e absorção dos compostos voláteis no meio selecionado. Nesta técnica, as características do solvente selecionado possuem grande influência, principalmente o ponto de ebulição, que pode resultar em perdas significativas de concentração. Desta forma, em geral, recomenda-se que a coleta seja feita sob banho a baixa temperatura e que as amostras sejam armazenadas sob refrigeração. O volume de solvente, a temperatura de coleta, o fluxo de gás e o volume de gás amostrado são geralmente determinados a partir da composição do gás e dos compostos a serem coletados. Comparada com as técnicas sem pré-concentração, esta técnica é considerada a mais complexa em questão de manuseio e instalação, bem como requer mais tempo para a realização da amostragem, incluindo a utilização de tubos adsorventes. Após a coleta, as amostras são direcionadas para a análise em laboratório, podendo-se utilizar diversas técnicas para detecção e quantificação, que serão discutidas a diante.13,16,30 O solvente orgânico mais adequado para a coleta tem sido estudado em diversos artigos sobre o tema na literatura, bem como a porcentagem de recuperação e a estabilidade dos siloxanos durante o armazenamento, tanto das amostras coletadas quanto das soluções padrões. Além disso, estudos comparativos entre as metodologias de amostragem já citadas, sacos de amostragem, canisters e tubos adsorventes, também são frequentes na literatura, na sua utilização para a coleta de biogás, biometano e gás natural. Por exemplo, além da investigação feita em relação ao encaixe dos sacos de amostragem, Ajhar et al.33 também avaliaram a decomposição de soluções estoque de siloxanos preparadas em metanol após 23 dias de estocagem a 4 ºC. Observou-se uma perda de 16% para D3, 57% para L2 e de 76% para D3. No estudo também já mencionado, realizado por Saeed et al.39 em 2002, foi realizada a comparação entre a amostragem utilizando-se canisters e , ou seja, uma metodologia sem pré-concentração em relação a uma com pré-concentração em meio líquido. Em relação ao uso de impingers, foi verificada a estabilidade dos siloxanos lineares pentametildisiloxano, L2, L3, e os cíclicos D4, D5 e D6 em metanol. Com exceção do pentametildisiloxano e do D3, os demais apresentaram taxas de recuperação aceitáveis por um período máximo de 21 dias, mantendo-se as amostras armazenadas sob refrigeração de aproximadamente 4 ºC. No caso, o siloxano pentametildisiloxano teve uma recuperação ruim, caindo para 60% com 7 dias de estocagem, enquanto o composto D3 não foi estável suficiente durante a análise cromatográfica. Comparando com os resultados de recuperação dos mesmos compostos, com exceção dos cíclicos de maior massa molecular, D4, D5 e D6, menos voláteis, quando armazenados em canisters tiveram taxas de recuperação aceitáveis por um período de 7 dias. Já em um estudo mais recente desenvolvido por Wang et al.47 em 2020, foi observado que a coleta em impingers preenchidos com metanol e a análise por Purga e Armadilha acoplada a cromatografia a gás e espectrometria de massas (P&T-CG-EM), possibilitou a análise de oito siloxanos. Dentre os compostos avaliados, têm-se os siloxanos lineares L2, L3, L4 e L5 e cíclicos D3, D4, D5 e D6, sendo que no estudo desenvolvido, em contrapartida com o apresentado por Saeed et al.,39 foi possível realizar a detecção do siloxano D3, devido à alta sensibilidade da técnica de análise utilizada. Nos estudos desenvolvidos por Piechota et al.,12,14,27,48 dentre as investigações realizadas, destaca-se a avaliação do melhor solvente orgânico para a absorção, comparando os resultados obtidos com a utilização de acetona, metanol e n-hexano. Em 2013, foram realizadas coletas de biogás provenientes de diferentes fontes, de aterro sanitário, de plantas de tratamento de águas residuais e também de biorreator de agricultura, utilizando a coleta em impingers com os solventes mencionados. A partir das análises das amostras coletadas e análise por CG-EM, foi possível indicar que as coletas realizadas em acetona apresentaram os melhores resultados, indicando uma maior capacidade de absorção dos compostos voláteis. Com esse experimento, foi observada a ausência de MSVs no biogás proveniente da agricultura, sendo os compostos D4 e D5, representantes de mais de 70% do total de MSVs encontrados no biogás de aterro sanitário.27 Em 2014, Piechota e Buczkowski12 avaliaram a eficiência de absorção dos MSVs nos 3 solventes citados, n-hexano, metanol e acetona. Para isto, foram utilizados 3 impingers em série, variando a ordem dos solventes utilizados, sendo que a melhor absorção de siloxanos foi observada na sequência: acetona, metanol e n-hexano e na sequência de metanol, acetona e n-hexano. Com isso, foi possível indicar que os solventes polares utilizados no primeiro impinger demonstraram os melhores resultados. Além disso, os dois detectores, DIC (detector de ionização em chama) e EM (espectrometria de massas), apresentaram boas respostas de detecção. Em sequência, a partir dos estudos realizados, Piechota et al.48 em 2015, validaram a utilização de 3 impingers preenchidos com acetona para a coleta dos MSVs e de TMSOH, presentes no biogás proveniente de aterro sanitário, com detecção por CG-EM. Em 2021, Piechota14 expandiu seus estudos de comparação de metodologias de coleta de biogás provenientes de agricultura, de aterro sanitário e de estações de tratamento de águas residuais. Foram comparados os resultados das amostras coletadas em sacos de amostragem Tedlar®, tubos adsorventes com carvão ativado, micro-impinger e impingers. Dentre as metodologias avaliadas, a utilização dos micro-impingers e impingers foram consideradas superiores as demais, sendo que dentre os solventes avaliados, acetona, metanol e dodecano, os melhores resultados de absorção foram novamente observados para as amostras coletadas em acetona. Novamente, a detecção e quantificação dos siloxanos lineares e cíclicos foi realizada utilizando CG-EM, sendo que o estudo desenvolvido contribuiu para a demonstração de uma metodologia prática, rápida e eficiente para as análises de MSVs.14
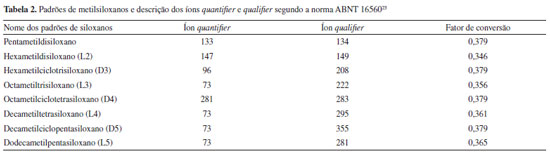
METODOLOGIAS DE ANÁLISE QUALITATIVA E QUANTITATIVA Dentre as técnicas já descritas na literatura22,41,47,48 para a análise de siloxanos têm-se a cromatografia gasosa (CG) acoplada a diversos detectores tais como espectrometria de massas (EM), detector por ionização de chama (DIC) e detector por emissão atômica (DEA). Além disso, a técnica de dessorção térmica acoplada à cromatografia gasosa com detecção por espectrometria de massas (DT-CG/EM), comumente utilizada para análise de amostras de ar, também vêm sendo utilizada para a análise de siloxanos presentes no biogás.46 A ionização química a pressão atmosférica/espectrometria de massas tandem (APCI-MS/MS) também já foi utilizada para a análise de siloxanos.49 No campo já foi utilizado um analisador gasoso por espectroscopia na região do infra-vermelho (IV) fornecendo o teor total de silício por m3 do biogás.50,51 Também podem ser utilizadas as técnicas de espectrometria de absorção atômica (EAA) ou espectrometria de emissão atômica (EEA) para a determinação da concentração total de silício, que engloba a classe dos MSVs.22 Assim como para a seleção da metodologia de amostragem, deve-se considerar alguns fatores para seleção do método analítico para a detecção dos siloxanos. Dentre esses fatores têm-se: seletividade e sensibilidade do detector, disponibilidade e custo da análise. Em relação a seletividade, o DIC é considerado o menos seletivo para a detecção e quantificação de siloxanos. Considerando a complexidade de uma amostra de biogás, uma vez que os compostos orgânicos são ionizáveis e produzem um sinal proporcional ao número de carbonos do composto, qualquer molécula que possua uma ligação C-H, tal como siloxanos, irá gerar um sinal no cromatograma. Desta forma, pode haver dificuldade na identificação do pico referente ao siloxano, atrapalhando sua quantificação de forma confiável, devido a sobreposição de picos provenientes de outros compostos.41,50 Este comportamento, por exemplo, foi observado no estudo realizado por Calbry-Muzyka et al.,50 no qual diversos métodos de coleta e detecção de siloxanos foram comparados. Como parte dos resultados atingidos, observou-se uma dificuldade para a quantificação dos siloxanos L5 e D6 por CG-DIC, devido à co-eluição com outros compostos, mesmo com um tempo de análise longo. A utilização do DEA permite uma melhora na seletividade ao identificar compostos que possuam o átomo de silício, reduzindo os sinais observados em comparação com o DIC. Porém, em termos de seletividade, a EM supera essas limitações, colocando-se superior aos demais detectores, uma vez que são observados íons m/z relativos ao composto de interesse, mesmo em casos de co-eluição. Assim, é possível realizar a quantificação por meio da relação de intensidade de um ou mais íons m/z específicos do siloxano em análise e sua respectiva concentração. Além disso, a utilização deste detector permite a identificação de outros compostos presentes na amostra analisada, por meio da comparação do espectro de massa obtido com a biblioteca disponível no programa utilizado.41 Em relação aos custos envolvidos das análises, o DIC é consideravelmente mais barato quando comparado ao DEA e a EM, mas em geral, é mais comum a existência dos detectores DIC e EM nos laboratórios voltados para análises ambientais, indicando novamente uma preferência para a utilização de CG-EM.41 Com bases nestes pontos, ainda não há um método padrão que seja aceito universalmente para esta análise, porém no Brasil têm-se a recomendação da norma ABNT NBR 16560- Biogás e Biometano- Determinação de Siloxanos por Cromatografia em Fase Gasosa e Amostragem com Impingers.23 Segundo a norma, a coleta é realizada utilizando-se impingers com metanol e a identificação e quantificação dos MSVs é realizada por meio da técnica cromatográfica em fase gasosa acoplada a detecção por espectrometria de massas (CG-EM). Ao optar pelo seguimento da norma ABNT NBR 16560,23 alguns itens são necessários para compor o kit coleta/amostragem, tais como: uma bomba de amostragem com regulador de fluxo; impingers de vidro de 25 mL; mangueiras de PTFE Teflon® e metanol grau HPLC. Além disso, deve-se atentar para a utilização de um recipiente capaz de manter os impingers resfriados a 0 ºC durante a realização da coleta. Para a quantificação dos MSVs, faz-se necessária a aquisição dos padrões de siloxanos, individuais ou em mistura de todos os descritos, para a construção das curvas de calibração analíticas. A norma indica as condições cromatográficas para a separação de todos os MVSs que constam na norma, como coluna, temperaturas e tempo de análises, também apresenta os íons m/z designados como quantifier (íon de quantificação) e qualifier (íon de qualificação) a serem utilizados no modo SIM (do inglês, single ion monitoring) (Tabela 2).23 O padrão de fragmentação dos MSVs é caraterizado principalmente pela perda de íons metila [M- 15]+, podendo ser assim selecionados outros íons para monitoramento, além dos sugeridos pela norma ABNT 16560.23
Com base nos valores calculados de concentração de cada siloxano, é possível indicar o teor total de silício presente no volume da amostra coletada.23 A amostragem e quantificação adequada dos metilsiloxanos presentes no biogás, indica quanto a necessidade e a escolha apropriada de um método de remoção, que serão apresentados a seguir.
METODOLOGIAS DE PURIFICAÇÃO Com o contínuo e aumento do consumo de produtos que possuem siloxanos em sua formulação, faz-se necessário, além da coleta e quantificação, o desenvolvimento de tecnologias para a remoção destes compostos do biogás, para seguir com suas aplicações comerciais e industriais.6 Diversas metodologias podem ser empregadas para a remoção dos siloxanos presentes no biogás podendo ser físicas, químicas e/ou biológicas. Por exemplo, métodos como adsorção, absorção, refrigeração/condensação, degradação biológica e separação por membranas são algumas das opções disponíveis. As técnicas de remoção empregadas são selecionadas a partir de quais siloxanos estão presentes no biogás, pois, devido a diferença das propriedades físicas e químicas de cada MSV, uma técnica pode ser mais eficiente que a outra. Muitas vezes, é necessário utilizar um conjunto de técnicas para atingir a remoção total destes compostos.4 Adsorção A técnica de adsorção é a mais utilizada para a remoção dos MSVs presentes no biogás, tanto em laboratório como na indústria. A eficiência na purificação está relacionada diretamente com as propriedades do material adsorvente.3,6 Por exemplo, os siloxanos (adsorbato) são atraídos para os sítios ativos da superfície do material adsorvente. Sendo assim, é desejável que o adsorvente possua alta área superficial e grandes diâmetros de poros, aumentando a acessibilidade das moléculas serem adsorvidas no material. Além disso, a quantidade do material adsorvente utilizado e a dimensão da coluna são dependentes da concentração de siloxanos presentes no gás a serem removidos com a capacidade de adsorção do material.4 Esta técnica de remoção é considerada simples, barata e eficiente. Porém, têm-se como desvantagem a dificuldade de dessorção dos MSVs a depender do material adsorvente. Este fator pode resultar na necessidade de trocas frequentes do material, ou perda de capacidade de remoção com o processo de regeneração. Embora seja realizado procedimentos de dessorção para a recuperação do material, após regenerado, a capacidade de adsorção será sempre menor quando comparado ao seu primeiro uso. Dentre os materiais comumente utilizados, têm-se os a base de sílica tais como sílica-gel, peneiras moleculares, zeólitas e argila e outros a base de carbono, tais como carvão ativado.4,6 O carvão ativado é comumente utilizado para a remoção de MSVs do biogás. No entanto, também é observada a adsorção de metano, reduzindo assim a proporção de metano na composição gasosa. Esse fenômeno também é responsável por reduzir a capacidade de adsorção do carvão para as demais impurezas.6 Dentre os fatores que afetam a capacidade de adsorção do carvão ativado em relação aos siloxanos está a umidade relativa do biogás. Uma umidade entre 50 e 70% ocasionam uma perda significativa na capacidade de adsorção de 10 vezes ou mais.19 Com a alta concentração de VOCs presentes no biogás, especialmente o H2S, o carvão ativado torna-se rapidamente saturado. A saturação do carvão ativado diminui a adsorção de siloxanos e acelera a necessidade de remoção do leito para a regeneração do carvão, que por consequência, eleva os custos operacionais.6,52 Diferentemente do carvão ativado, as peneiras moleculares não adsorvem o metano, sendo utilizadas para a remoção dos compostos mais polares presentes no biogás, como água, H2S, CO2 e os siloxanos.6 Diversos estudos descritos na literatura indicam que a sílica gel apresenta uma melhor capacidade de adsorção de metilsiloxanos quando comparado com a utilização de outros materiais adsorventes. Por exemplo, no estudo realizado por Schweigkofler e Niessner40 já apresentado, foi avaliado a capacidade de adsorção de diversos materiais, tais como carvão ativado, Carbopack B®, Tenax TA®, resinas XAD II, peneira molecular 13X e sílica gel. Dentre os adsorventes sólidos mencionados, a sílica gel foi considerada o material com o melhor custo-benefício, uma vez que além de apresentar a melhor adsorção dos siloxanos, com capacidade de 100 mg g-1, atuou também como agente secante para o biogás. Jung e Jurng53 investigaram a aplicação de uma sílica modificada no processo de adsorção e dessorção de siloxanos. Foram utilizadas diferentes concentrações de NaOH para a modificação da superfície da sílica em pó e então avaliado o volume de ruptura dos materiais sintetizados. O siloxano D5 foi selecionado como representante da classe de MSVs para os ensaios de adsorção. Foi observado um aumento na eficiência de remoção de 95% (por um período de 300 min) com o uso da sílica original para 97% (por um período de 1.400 min) com o uso da sílica modificada pela adição de solução de NaOH (3 mol L-1). Constatou-se um aumento no volume de ruptura de 350 para 1500 min, indicando um incremento de quatro vezes na capacidade de remoção da sílica modificada. Silva et al.54 desenvolveram um estudo envolvendo a síntese de um material poroso à base de sílica proveniente de areia residual de estações de tratamento de águas residuais. Este foi aplicado para a remoção de siloxanos por adsorção do biogás. O estudo da eficiência de adsorção da sílica sintetizada foi realizado, em comparação com outras duas sílicas comerciais. Assim, foi testada a adsorção dos siloxanos D4 e D5 em octano, em diferentes concentrações, nos materiais selecionados, com análise da concentração por CG-EM e pelo balanço de massa do material utilizado. A sílica sintetizada apresentou os melhores resultados de adsorção, provavelmente vinculado as suas características, tais como menores tamanhos de partícula e maiores poros, em comparação com as sílicas comerciais. Absorção O método de absorção física usando sistema de lavagem com água está entre as técnicas mais comumente usadas para a purificação do biogás. Esse mesmo processo também pode ser usado com sistema de lavagem com solventes e com óleo mineral.4 Considerando as características físicas e químicas dos siloxanos, o tetradecano e selexol são solventes compatíveis para uma remoção efetiva dos MSVs, enquanto a lavagem com água é eficiente para a remoção do TMSOH.4,6 Para o método de absorção química, têm-se comumente a utilização de ácidos e/ou bases concentradas, para a quebra das ligações Si-O e então absorção dos compostos. Em geral, os ácidos sulfúrico, nítrico e fosfórico são utilizados para a purificação gás-líquido. Contudo, como desvantagem desta técnica têm-se problemas de corrosão, potencialmente prejudicial ao ambiente, além do aumento nos custos de produção.6 Pascual et al.55 compararam a remoção dos MSVs L2, L3, D4 e D5; pela utilização de um biofiltro convencional em relação ao mesmo biofiltro mas com a adição de 30% de óleo de silicone. Foi observada uma eficiência de 20% na remoção dos MSVs com a utilização do biofiltro, observando-se a produção de CO2 durante os experimentos realizados. Porém, com a adição do óleo de silicone, a eficiência de remoção foi elevada para 70%, demonstrando uma capacidade de eliminação cinco vezes maior. Os resultados mais expressivos foram observados para os siloxanos D4 e D5, no qual foi observado um aumento de 13 para 85% e de 18 para 90%, respectivamente, na eficiência de remoção. Refrigeração/condensação O processo de resfriamento sob baixa pressão do biogás pode resultar na condensação de compostos, possibilitando assim sua remoção. No entanto, a utilização desta técnica para a remoção de siloxanos não é considerada amplamente eficaz, devido às baixas taxas de eliminação alcançadas. Além disso, o custo operacional desta técnica é elevado, uma vez que uma alta taxa de energia é necessária para o resfriamento do gás.4 A principal vantagem desta tecnologia está relacionada com a não geração de resíduos, ao contrário do que ocorre com as técnicas de adsorção e absorção. Desta forma, é importante avaliar as vantagens e desvantagens desta metodologia, uma vez que, comumente se faz necessária a combinação com outros mecanismos de remoção para garantir uma eliminação significativa dos MSVs.4 No estudo realizado por Schweigkofler e Niessner56 foi avaliado o efeito da utilização da refrigeração do biogás a 5 ºC para a remoção de siloxanos no biogás. Foi observado uma redução de VOCs entre 20 e 25%, de 11% para os siloxanos, quando comparado as concentrações iniciais nos testes realizados. Degradação biológica Os MSVs não são compostos facilmente biodegradados, porém recentemente alguns métodos biológicos vêm sendo desenvolvidos com os microorganismos dos gêneros Pseudomonas, Zooglea, Xanthomonadacea, Rhodanobacter e Mesorhizobium.4,56 Para a remoção biológica dos siloxanos utiliza-se de biopurificadores (BS), biofiltros (BF) e filtros de biotrickling (BTF). No entanto, o processo é considerado lento e com baixa eficiência para os sistemas tanto anaeróbicos bem como aeróbicos, uma vez que os microorganismos precisam se adaptar com os siloxanos como fonte de carbono para o metabolismo.6 Dentre os estudos envolvendo o gênero Pseudomonas, Li et al.57 desenvolveram um filtro biológico aeróbio de leito fixo contendo Pseudomonas aeruginosa S240. A degradação do siloxano D4 foi avaliada. A detecção dos compostos L3, trimetilmetoxisilano, ácido silícico, metanol e CO2 foram observados como produtos provenientes da degradação de D4, uma vez que este foi a única fonte de material orgânico utilizado no estudo. Foi possível observar a degradação de 74% de D4, 50 mg m-3 por um tempo de residência de 13,2 min, por meio da utilização de um gás sintético aeróbico. Yang e Corsolini58 conduziram um estudo para a avaliação da eficácia da adição de um biofiltro, composto por lodo ativado proveniente de estação de tratamento de águas residuais, ao processo de remoção de siloxanos do biogás. Este biofiltro é considerado uma opção de baixo custo, sendo amplamente utilizado como dispositivo de controle de poluentes do ar. Assim, este foi integrado antes do filtro de carvão ativado já utilizado como método de purificação do biogás, visando avaliar o seu impacto na capacidade de remoção de siloxanos. A partir dos experimentos realizados, foi possível observar uma melhoria nas porcentagens de remoção dos siloxanos avaliados D3, D4 e D5 com a utilização do conjunto biofiltro mais carvão ativado, comparado com a utilização apenas do carvão ativado. Foram observadas as respectivas taxas de remoção, de 91,39 para 98,13% (D3), de 81,54 para 96,61% (D4), 69,43 para 78,58% (D5). Dentre as explicações para esta melhoria, os autores expuseram algumas possibilidades, tais como a remoção direta dos siloxanos pelo biofiltro por meio de mecanismos de adsorção e absorção. Acredita-se que o mecanismo predominante não seja o de absorção, uma vez que a área superficial do material utilizado foi considerada pequena (3,7 m2 g-1) quando comparada à área superficial do carvão ativado (< 300 m2 g-1). Além disso, a absorção pode ter sido limitada devido à baixa solubilidade em água dos MSVs avaliados. Caso tenham sido dissolvidos em água, estes podem ter sido degradados pelos micro-organismos presentes no lodo utilizado. Outra possibilidade envolve a remoção de vapor de água pelo biofiltro, deixando os sítios ativos do carvão ativado disponíveis para a adsorção dos siloxanos.58 Membranas A utilização de membranas para a purificação do biogás trata-se da colocação de uma barreira física com o intuito de reter alguns compostos. Essas membranas são camadas finas de aproximadamente 0,22 mm feitas de um material específico para a remoção de certos compostos. Os materiais componentes das membranas são comumente poliméricos ou inorgânicos. As vantagens envolvendo o uso desta metodologia estão relacionadas com o baixo custo energético e a obtenção de um biometano com alto teor de pureza. Têm-se também a operação contínua da membrana, sem etapas de regeneração, conforme observado para materiais adsorventes.6 Até o momento, poucos estudos foram descritos envolvendo a utilização de membranas para a remoção seletiva de siloxanos, com observações de valores de remoção próximos a 80%. Dentre estes, Ajhar et al.59 investigaram a utilização de membranas comerciais de polidimetilsiloxano (PDMS) para a purificação de um biogás sintético contaminado com os siloxanos L2, L3, L4 e D3, D4 e D5, em dois sistemas operacionais. A eficiência de remoção foi superior ao utilizar o sistema com operação de 3 terminais comparada à 4 terminais, no qual foram observadas as seguintes porcentagens de remoção, 30, 70, 90, 60, 75 e 90% para os MSVs L2, L3, L4, D3, D4 e D5, respectivamente.
CONCLUSÕES Com o destaque global do biogás como uma fonte de energia limpa e renovável, e considerando os impactos causados por contaminantes, especialmente os siloxanos, esta revisão abordou as metodologias para amostragem, análise e remoção destes compostos, proporcionando um panorama claro das opções disponíveis para pesquisadores e empresas do setor energético. Com as metodologias disponíveis e apresentadas é possível avaliar em um contexto experimental e econômico qual técnica é mais apropriada e factível dentro do objetivo estabelecido, seja em um ambiente laboratorial e/ou industrial. No Brasil, a norma NBR 16560 apresentada nesta revisão recomenda o uso de impingers para a amostragem e a utilização de cromatografia gasosa acoplada à espectrometria de massas como técnica de detecção e quantificação, alinhando-se as metodologias mais eficazes e confiáveis, dentre as descritas na literatura. Quanto as técnicas para a remoção dos siloxanos, destacam-se as técnicas de adsorção, com o uso de carvão ativado e sílica gel, amplamente utilizadas para a purificação do biogás em relação a outros contaminantes. Além disso, ao considerar o desenvolvimento de modelos de energia renovável torna-se crucial também contemplar a geração de resíduos nos processos citados, sustentando assim o conceito renovável e minimizando os potenciais impactos ambientais associados ao uso dessas tecnologias. Portanto, essa revisão destacou a importância de escolher e aplicar as técnicas mais apropriadas com base na estrutura disponível e nos objetivos específicos, garantindo eficácia na análise e purificação do biogás.
AGRADECIMENTOS Os autores agradecem o apoio do Centro Internacional de Energias Renováveis (CIBiogás/ITAIPU) e da Gesellschaft für Internationale Zusammenarbeit (GIZ), bem como o financiamento concedido pelo projeto PD&I 002/2021 da Fundação Araucária - consolidação do novo arranjo de pesquisa e inovação em hidrocarbonetos renováveis do Estado do Paraná (NAPI HCR).
REFERÊNCIAS 1. Oliveira, L. G.; Cremonez, P. A.; Machado, B.; da Silva, E. S.; Silva, F. E. B.; Corrêa, G. C. G.; Lopez, T. F. M.; Alves, H. J.; Can. J. Chem. Eng. 2023, 101, 2361. [Crossref] 2. Angelidaki, I.; Treu, L.; Tsapekos, P.; Luo, G.; Campanaro, S.; Wenzel, H.; Kougias, P. G.; Biotechnol. Adv. 2018, 36, 452. [Crossref] 3. Alves, C. M. A. C.; Abreu, F. O. M. S.; Araújo, R. S.; Oliveira, M. L. M.; Chem. Pap. 2023, 77, 1. [Crossref] 4. Nyamukamba, P.; Mukumba, P.; Chikukwa, E. S.; Makaka, G.; Energies 2020, 13, 6088. [Crossref] 5. Pramanik, S. K.; Suja, F. B.; Zain, S. M.; Pramanik, B. K.; Bioresour. Technol. Rep. 2019, 8, 100310. [Crossref] 6. Shen, M.; Zhang, Y.; Hu, D.; Fan, J.; Zeng, G.; Environ. Sci. Pollut. Res. 2018, 25, 30847. [Crossref] 7. Aguilar-Aguilar, F. A.; Nelson, D. L.; Pantoja, L. A.; Santos, A. S.; Rev. Virtual Quim. 2017, 9, 2383. [Crossref] 8. Ibro, M. K.; Ancha, V. R.; Lemma, D. B.; J.Chem. 2024, 2024, 4599371. [Crossref] 9. Dewil, R.; Appels, L.; Baeyens, J.; Energy Convers. Manage. 2006, 47, 1711. [Crossref] 10. Agência Nacional do Petróleo, Gás Natural e Biocombustíveis (ANP); Resolução ANP No. 886, de 29 de setembro de 2022, Estabelece a Especificação e as Regras para Aprovação do Controle da Qualidade do Biometano Oriundo de Aterros Sanitários e de Estações de Tratamento de Esgoto Destinado ao Uso Veicular e às Instalações Residenciais, Industriais e Comerciais, a ser Comercializado no Território Nacional; Diário Oficial da União (DOU), Brasília, ed. 186, de 29/09/2022, p. 47. [Link] acessado em Dezembro 2024 11. Agência Nacional do Petróleo, Gás Natural e Biocombustíveis (ANP), Resolução ANP No. 906, de 18 de novembro de 2022, Dispõe sobre as Especificações do Biometano Oriundo de Produtos e Resíduos Orgânicos Agrossilvopastoris e Comerciais Destinado ao Uso Veicular e às Instalações Residenciais e Comerciais a ser Comercializado em Todo o Território Nacional; Diário Oficial da União (DOU), Brasília, de 24/11/2022. [Link] acessado em Dezembro 2024 12. Piechota, G.; Buczkowski, R.; Int. J. Environ. Anal. Chem. 2014, 94, 837. [Crossref] 13. Arrhenius, K.; Brown, A. S.; van der Veen, A. M. H.; Anal. Chim. Acta 2016, 902, 22. [Crossref] 14. Piechota, G.; Molecules 2021, 26, 1953. [Crossref] 15. Woolfenden, E.; J. Chromatogr. A 2010, 1217, 2685. [Crossref] 16. Eichler, C. M. A.; Wu, Y.; Cox, S. S.; Klaus, S.; Boardman, G. D.; Biomass Bioenergy 2018, 108, 1. [Crossref] 17. Gaj, K.; Energies 2020, 13, 2605. [Crossref] 18. Hobson, J. F.; Atkinson, R.; Carter, W. P. L. Em Organosilicon Materials. The Handbook of Environmental Chemistry, vol. 3; Chandra, G., ed.; Springer: Berlin, Heidelberg, 1997, cap. 3. 19. de Arespacochaga, N.; Valderrama, C.; Raich-Montiu, J.; Crest, M.; Mehta, S.; Cortina, J. L.; Renewable Sustainable Energy Rev. 2015, 52, 366. [Crossref] 20. Sander, R.; Atmos. Chem. Phys. 2023, 23, 10901. [Crossref] 21. Companioni-Damas, E. Y.; Quim. Nova 2017, 40, 192. [Crossref] 22. Wang, J.; Liao, L.; Wang, L.; Wang, L.; Biomass Bioenergy 2022, 158, 106347. [Crossref] 23. Associação Brasileira de Normas Técnicas (ABNT); NBR 16560: Biogás e Biometano- Determinação de Siloxanos por Cromatografia em Fase Gasosa e Amostragem com Impingers; ABNT, Brasil, 2017. [Link] acessado em Dezembro 2024 24. Paolini, V.; Petracchini, F.; Carnevale, M.; Gallucci, F.; Perilli, M.; Esposito, G.; Segreto, M.; Occulti, L. G.; Scaglione, D.; Ianniello, A.; Frattoni, M.; J. Environ. Manage. 2018, 217, 288. [Crossref] 25. European Committee for Standardization (CEN); Standard EN 16723-2:2017 Natural Gas and Biomethane for Use in Transport and Biomethane for Injection in the Natural Gas Network - Part 2: Automotive Fuels Specification; CEN, 2017. [Link] acessado em Dezembro 2024 26. 2018 AGA-EPA Renewable Natural Gas Workshop, https://19january2021snapshot.epa.gov/sites/static/files/2018-11/documents/15._jim_tweedie_-_508.pdf, acessado em Janeiro 2025; Von Wald, G.; Brandt, A.; Rajagopal, D.; Stanion, A.; Sweeney, J. L.; Mace, A. J.; Brady, S. E.; Biomethane in California Common Carrier Pipelines: Assessing Heating Value and Maximum Siloxane Specifications; California Council on Science & Technology: Sacramento, 2018. [Link] acessado em Dezembro 2024 27. Piechota, G.; Igliński, B.; Buczkowski, R.; Energy Convers. Manage. 2013, 68, 219. [Crossref] 28. Arnold, M.; Kajolinna, T.; Waste Manage. 2010, 30, 1011. [Crossref] 29. Gersen, S.; Visser, P.; van Essen, M.; Brown, M.; Lewis, A.; Levinsky, H.; Renewable Energy 2019, 132, 575. [Crossref] 30. Lecharlier, A.; Carrier, H.; Le Hécho, I.; Anal. Chim. Acta 2022, 1229, 340174. [Crossref] 31. Arrhenius, K.; Fischer, A.; Büker, O.; Appl. Sci. 2019, 9, 1171. [Crossref] 32. Beghi, S.; Guillot, J.-M.; J. Chromatogr. A 2008, 1183, 1. [Crossref] 33. Ajhar, M.; Wens, B.; Stollenwerk, K. H.; Spalding, G.; Yüce, S.; Melin, T.; Talanta 2010, 82, 92. [Crossref] 34. Mariné, S.; Pedrouzo, M.; Marcé, R. M.; Fonseca, I.; Borrull, F.; Talanta 2012, 100, 145. [Crossref] 35. Arrhenius, K.; Yaghooby, H.; Rosell, L.; Büker, O.; Culleton, L.; Bartlett, S.; Murugan, A.; Brewer, P.; Li, J.; van der Veen, A. M. H.; Krom, I.; Lestremau, F.; Beranek, J.; Biomass Bioenergy 2017, 105, 127. [Crossref] 36. ISO 10715:1997 (E): Natural Gas- Sampling Guidelines, ISO: Geneva, 1997. [Link] acessado em Dezembro 2024 37. Brymer, D. A.; Ogle, L. D.; Jones, C. J.; Lewis, D. L.; Environ. Sci. Technol. 1995, 30, 188. [Crossref] 38. Kelly, T. J.; Holdren, M. W.; Atmos. Environ. 1995, 29, 2595. [Crossref] 39. Saeed, S.; Kao, S.; Graening, G.; AWMA Symposium on Air Quality Measurement Methods and Technology; San Francisco, United States, 2002. [Link] acessado em Dezembro 2024 40. Schweigkofler, M.; Niessner, R.; Environ. Sci. Technol. 1999, 33, 3680. [Crossref] 41. Hayes, H.; Graening, G. J.; Saeed, S.; Kao, S.; SWANA LFG Symposium; Tampa, United States, 2003. [Link] acessado em Dezembro 2024 42. Lamaa, L.; Ferronato, C.; Fine, L.; Jaber, F.; Chovelon, J. M.; Talanta 2013, 115, 881. [Crossref] 43. Raich-Montiu, J.; Ribas-Font, C.; de Arespacochaga, N.; Roig-Torres, E.; Broto-Puig, F.; Crest, M.; Bouchy, L.; Cortina, J. L.; Anal. Chim. Acta 2014, 812, 83. [Crossref] 44. Kim, N.-J.; Chun, S.-K.; Cha, D. K.; Kim, C.; Bull. Korean Chem. Soc. 2013, 34, 2353. [Crossref] 45. Tansel, B.; Surita, S. C.; Waste Manage. 2016, 52, 122. [Crossref] 46. Gallego, E.; Roca, F. J.; Perales, J. F.; Guardino, X.; Gadea, E.; Int. J. Environ. Anal. Chem. 2015, 95, 291. [Crossref] 47. Wang, N.; Tan, L.; Xie, L.; Wang, Y.; Ellis, T.; J. Environ. Sci. 2020, 91, 54. [Crossref] 48. Piechota, G.; Igliński, B.; Buczkowski, R.; Int. J. Environ. Anal. Chem. 2015, 95, 867. [Crossref] 49. Badjagbo, K.; Héroux, M.; Alaee, M.; Moore, S.; Sauvé, S.; Environ. Sci. Technol. 2010, 44, 600. [Crossref] 50. Calbry-Muzyka, A.; Tarik, M.; Gandiglio, M.; Li, J.; Foppiano, D.; de Krom, I.; Heikens, D.; Ludwig, C.; Biollaz, S.; Renewable Energy 2021, 177, 61. [Crossref] 51. Hepburn, C. A.; Vale, P.; Brown, A. S.; Simms, N. J.; McAdam, E. J.; Talanta 2015, 141, 128. [Crossref] 52. Kuhn, J. N.; Elwell, A. C.; Elsayed, N. H.; Joseph, B.; Waste Manage. 2017, 63, 246. [Crossref] 53. Jung, H.; Jurng, J.; Renewable Energy 2020, 156, 459. [Crossref] 54. Silva, E. N.; Cantillo-Castrillon, M.; Dantas, T. M.; Mesquita, Y. M.; Maia, D. A. S.; Bastos-Neto, M.; Barcellos, W. M.; Azevedo, D. C. S.; J. Environ. Chem. Eng. 2021, 9, 104805. [Crossref] 55. Pascual, C.; Cantera, S.; Muñoz, R.; Lebrero, R.; Chemosphere 2020, 251, 126359. [Crossref] 56. Schweigkofler, M.; Niessner, R.; J. Hazard. Mater. 2001, 83, 183. [Crossref] 57. Li, Y.; Zhang, W.; Xu, J.; J. Hazard. Mater. 2014, 275, 175. [Crossref] 58. Yang, L.; Corsolini, S. I.; J. Environ. Chem. Eng. 2019, 7, 103284. [Crossref] 59. Ajhar, M.; Bannwarth, S.; Stollenwerk, K.-H.; Spalding, G.; Yüce, S.; Wessling, M.; Melin, T.; Sep. Purif. Technol. 2012, 89, 234. [Crossref]
Editor Associado responsável pelo artigo: Boniek G. Vaz |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access