Artigo
|
|
| Clarificación de vinazas provenientes de la industria de la "raicilla", mediante el uso de hidrogeles Clarification of vinasses from the "raicilla" industry, through the use of hydrogels |
|
Maribel Arrizón FregozoI; Nestor García RamírezI; Jorge Alberto Cortes OrtegaII; Juan Carlos Sánchez DíazI,* I. Departamento de Ingeneiría Química, Universidad de Guadalajara, 44430 Jalisco, México Recibido: 05/11/2024 *e-mail: sanchezdiaz@gmail.com In this work, the clarification process of vinasse from the "raicilla" industry produced in the municipality of Mascota, Jalisco, Mexico is presented. Acrylamide and acrylamide/methacrylic acid hydrogels were synthesized, with a water/monomer ratio of 90:10 by mass. Subsequently, each xerogel sample was loaded with cobalt, copper or nickel ions. The hydrogels loaded with each metal were placed in NaOH 0.1 M solution, so the OH- ions penetrated the hydrogel and reacted with the metal ions, forming the corresponding hydroxide. Then the hydrogels loaded and swollen in the NaOH solution were placed in the vinasse for two days. After this time, a new hydrogel was placed and left for two more days, with which the intensity of the color of the vinasse decreased, as the process was repeated. In all cases, the treated vinasse was clarified, without significant changes in volume, indicative that the hydrogel no longer absorbs solution. This opens up the possibility of using this method for the clarification of vinasse from "raicilla" industry, through prior feasibility studies in efficiency, reuse of hydrogel, costs and technological development. INTRODUCCIÓN La raicilla es una bebida alcohólica destilada hecha de diferentes variedades de agave originarias de Jalisco, México. La raicilla es similar al tequila, pero se elabora con una planta diferente y tiene un sabor único.1 Las vinazas son las aguas residuales producto de la destilación del tequila; tienen un alto contenido de materia orgánica, con una demanda química de oxígeno (DQO) superior a 38,215 mg L-1 y sólidos totales (ST) superiores a 21,883 mg L-1, y poseen pH bajo, de 3.5-3.9.2 Se descargan a una temperatura de 90 ºC, lo que las convierte en un contaminante térmico. Su color se debe al pigmento café oscuro de las melanoidinas, la presencia de fenoles, caramelo y melanina, propios del licor de destilerías de melazas,3-7 que se pueden formar por las reacciones amino-carbonil8 de Maillar, al hidrolizar por calentamiento los azúcares de las pencas de agave. En el estudio del tratamiento de "vinazas" provenientes de diferentes industrias, como lo son las tequileras, de bioetanol y otros productos de consumo humano o con otras aplicaciones tecnológicas, se han utilizado microorganismos, tanto aeróbicos como anaeróbicos,9,10 lográndose diferentes grados de purificación, entre uno de los parámetros utilizados para determinar el éxito de esta purificación, se encuentra la clarificación de la vinaza; para este fin se han utilizado resinas de absorción en la remoción de compuestos fenólicos, parte de los compuestos que proporcionan el color.11 Se han utilizado algunos procesos mas complejos como lo son la filtración por membranas que son precedidos por tratamientos fisicoquímicos previos.12,13 Así mismo se utilizan métodos fotocatalíticos, utilizando un proceso homogéneo con fotofentona unas concentraciones de [H2O2]/[Fe+2] de 15 mol L-1.9 Existen docenas de estudios más que se han publicado, pero se tienen gastos energéticos considerables, debido a todos los procesos que se deben de aplicar. La formación de complejos entre metales y compuestos orgánicos a sido un área de investigación estudiada durante un largo tiempo, diversos estudios14-16 han tratado el tema, por lo que en este trabajo se lleva a cabo el uso de hidrogeles conteniendo iones metálicos y dar paso a la reacción de formación de hidróxidos metálicos in situ (Cu, Co y Ni), mediante la adición de solución de NaOH 0.1 M, para proveer a los hidrogeles de compuestos que puedan incrementar las interacciones con compuestos orgánicos y así poder utilizarlos en la clarificación de vinazas, mediante un proceso en lotes, sin agitación mecánica, para de esta manera disminuir los costes en este proceso de clarificación. El primer paso para mostrar la eficacia de estos sistemas es analizar la capacidad de los hidrogeles de remover las sustancias que le proporcionan el color a las vinazas y determinar si existe una diferencia entre el tipo de metal y de hidrogel utilizado durante el proceso.
PARTE EXPERIMENTAL Métodos y materiales Los monómeros a utilizados fueron acrilamida (AM) y ácido metacrílico (MAA), con una pureza del 99% obtenidos de Sigma. Las sales de cloruro de cobalto (CoCl2.6H2O), cloruro de cobre (CuCl2.2H2O) y cloruro de níquel (NiCl2.6H2O) fueron obtenidos de Sigma con 99% de pureza. El iniciador de la reacción de polimerización persulfato de potasio (KPS) con 99% de pureza fue obtenido de Aldrich. El agente entrecruzante N',N'-metilenebisacrilamida (NMBA) con 99% de pureza fue obtenido de TCI. El agua bidestilada y deionizada para todos los experimentos fue obtenida de productos Selecropura. Se utilizó el espectrofotómetro Unico s-250 con celdas de cuarzo. Síntesis de hidrogeles En trabajos previos17-22 se han sintetizado y estudiado ampliamente hidrogeles de acrilamida y acrilatos. Por lo que se siguió el procedimiento de dichos estúdios para este trabajo; preparar hidrogeles de acrilamida y acrilamida/ácido metacrílico (90:10), en soluciones al 10% de monómeros totales (en masa), con 1% de agente entrecruzante y 3% de iniciador, llevándose la reacción a 55 ºC durante 2 h. Una vez sintetizados los hidrogeles se cortaron en cilindros de 1 cm de espesor, se colocaron en agua destilada por una semana, al final de este tiempo se colocaron a secar en una estufa de vació hasta peso constante, al polímero seco se le conoce como xerogel. Carga del metal Se colocaron los xerogeles de acrilamida y acrilamida/ácido metacrílico en soluciones de cloruro de cobre (3000 ppm), cloruro de cobalto (2000 ppm) y cloruro de níquel (1975 ppm), en una proporción de solución metálica/xerogel de 40:1 en masa por un tiempo de dos días. Al termino de este tiempo los hidrogeles, son retirados del medio y se colocan a secar, en una estufa de vació a 50 ºC, una vez que las muestras están totalmente secas, se reincorporan en la solución del metal, esta nueva solución esta constituida de la solución residual y se completa con solución fresca de los iones metálicos correspondientes, hasta completar una proporción de solución/hidrogel de 40:1. Se repite el proceso anterior por 4 ocasiones mas. Este proceso se realiza para provocar que los iones metálicos penetren lo mas posible en la matriz polimérica. Transformación del metal en hidróxidos y limpieza de los hidrogeles Una vez terminado el proceso de carga del metal, los hidrogeles conteniendo los iones metálicos e hinchados del ultimo proceso de carga, se sumergieron en soluciones acuosas de NaOH 0.1 M, en una proporción de solución de NaOH/hidrogel de 5:1, con la finalidad de que los iones OH-, penetren al hidrogel y en el interior del mismo se lleve a cabo la reacción con el metal correspondiente. Los hidrogeles permanecen sumergidos en estas soluciones metálicas por un tiempo de dos días. Los hidrogeles son removidos del medio, y se colocan en solución fresca de NaOH 0.1 M, por dos días mas. La solución residual de NaOH es analizada mediante espectroscopia ultravioleta-visible (UV-Vis), para determinar la presencia de iones metálicos o partículas de estos metales. El procedimiento anterior se repite hasta que no se detecte por medio del UV-Vis la presencia de partículas, en la solucion residual, con lo que se establece que los compuestos metálicos formados permanecen en el interior del hidrogel. Hinchamiento en la ¨vinazas¨ Los hidrogeles cargados y almacenados en solución de NaOH, son colocados en la solución madre de vinaza en una proporción de 1:1 en masa (esto equivale a 1 g de vinaza por cada 0.02 g de polímero seco) sin agitación durante dos días. Al termino de este tiempo son removidos del medio. La solución residual resultante es analizada por espectrometría de UV-Vis. A la solución de vinaza residual se le agrego un nuevo hidrogel y se repitió el procedimiento anterior. En total fueron agregados en 5 ocasiones hidrogeles para cada muestra de vinaza estudiada. Curva de calibración La vinaza fue obtenida de la fermentación de "raicilla" de la compañía de Raicilla Hermanos Arrizón, Rancho La Vieja, Mexico, el único tratamiento que se le dio a la vinaza, fue un proceso de filtración en una rejilla de 0.5 µm de longitud. La solución madre (vinaza obtenida) fue utilizada para preparar diluciones de la misma mediante agua destilada para la preparación de la curva de calibración y realizar la medición de absorbancia mediante espectrometría de UV-Vis en una longitud de onda de 250 nm. El análisis se realizo en celdas de cuarzo, con el espectrofotómetro UV-Vis marca UNICO modelo 250. Se eligió la longitud de onda de 270 nm, ya que en los espectros obtenidos en este punto se presentaba una curva característica que iba disminuyendo de forma gradual con la dilución de la vinaza. La ecuación de la curva de calibración fue [vinaza] = 1.7809 × Abs - 0.1419, la cual tiene un coeficiente de correlación de 0.99, y fue utilizada al medir la absorbancia de diferentes concentraciones de vinazas preparadas y, de esta forma, calcular la concetración con dicha ecuación, obteniendose mediciones con una desviación estandar menor al 3%. Las muestras recolectadas de cada prueba, para su evaluación, fueron diluidas de tal forma que la concetración de la vinaza tenga un valor cercano al 5%, despues del tratamiento, ya que esta concentración se encuentra en un punto medio de la curva de calibración, donde la relación de la absorbancia vs. concentración tiene comportamiento lineal.
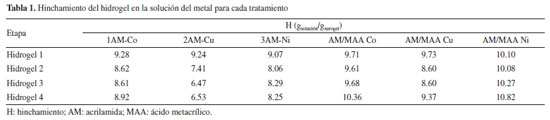
RESULTADOS Y DISCUSIONES Carga y reacción del metal La capacidad de absorber agua o solución del hidrogel, es conocida como hinchamiento (H), el cual se mide por los gramos de solución absorbida por cada gramo de xerogel, en la Tabla 1 se presenta el hinchamiento obtenido por cada tipo de hidrogel con el metal correspondiente por cada tratamiento realizado. Se observa que el hinchamiento disminuye gradualmente en cada etapa realizada para los hidrogeles de AM, mientras que para los hidrogeles de AM/MAA, el hinchamiento se mantiene constante.
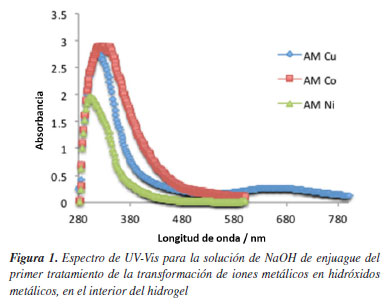
Se analizaron las soluciones residuales mediante UV-Vis y en todos los casos las soluciones residuales contenían concentraciones similares a la solución madre correspondiente. Con lo cual se puede establecer que el proceso de hinchamiento y secado de las muestras, permite una mayor carga de metal dentro de la matriz polimérica. En la Figura 1 se observa que las curvas obtenidas en el análisis del espectro de UV-Vis para la primera solución residual de NaOH de los hidrogeles de acrilamida estudiados, para cada metal cargado alrededor de 300 nm, que se presenta una fuerte señal en el espectro mostrado. Cuando se sintetizan partículas metálicas, una forma de identificar la presencia de estas partículas es mediante la aparición de esta señal.9 De estas curvas se puede obtener la banda prohibida, así como los eV de las partículas metálicas. En tanto que el tamaño y la forma de la partícula se obtiene mediante el microscopio electrónico. Por lo que la aparición de estas curvas en la solución NaOH del primer tratamiento, nos permite establecer que el metal adherido a la superficie del hidrogel o en la cercanía de la superficie, sufre una transformación hacia el hidróxido y su posterior migración a la solución. En tanto que el metal que penetro en el hidrogel, sufre la transformación dentro de él.
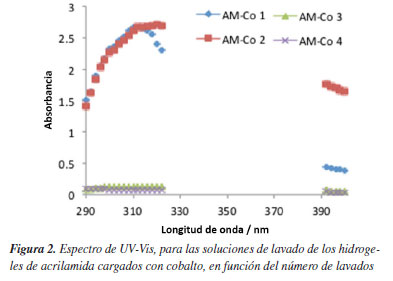
En la Figura 2 se presentan los espectros de UV-Vis, para las soluciones de lavado de los hidrogeles de acrilamida cargados con cobalto, donde se observa que la señal alrededor de 300 nm, va disminuyendo al aumentar el numero de lavado hasta casi desaparecer en el tercer y cuarto lavado. Con esto, podemos establecer que las partículas del metal que se han formado en el interior del hidrogel, ya no han emigrado a la solución. Resultados semejantes se obtuvieron para el resto de los hidrogeles.
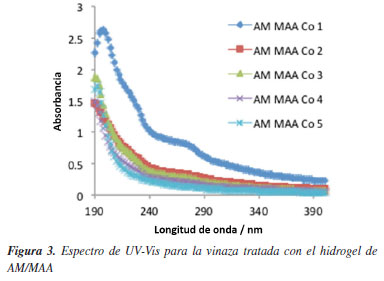
Experimentos de la clarificación de la vinaza Los hidrogeles cargados con el metal e hinchados en solución NaOH 0.1 M, se pusieron en contacto con la vinaza en una proporción 1:1 en masa. Se tomaron muestras a las 24, 48, 72 h y a los 7 días. Se realizo una dilución a todas las muestras recolectadas con agua destilada, para obtener una concentración de 1.2% y de esta forma poder realizar la comparación entre las soluciones de vinazas tratadas con la solución madre original. Cuando se analizaron los espectros de UV-Vis a los tiempos estudiados, se observa que, a las 48 h, se alcanzan los valores mínimos en la intensidad de las curvas, por lo que el proceso de absorción de los compuestos orgánicos por el hidrogel llegaba al punto de equilibrio, por lo que se estableció que el tiempo de experimentación de todas las muestras sería de 2 días. En la Figura 3 se presentan los espectros de UV-Vis para las diferentes etapas de tratamiento de la vinaza con el hidrogel de AA/MAA cargado con cobalto, los cuales se comparan con el espectro que tiene la composición de 1.22% de vinaza (que es la composición de todas las muestras diluidas que se tomaron después de cada tratamiento de la vinaza), donde se observa la disminución en la intensidad del espectro de las muestras tratadas. La disminución en la intensidad de los espectros se correlaciona de forma visual al cambio en la intensidad de la coloración de la vinaza tratada, que se presenta en la Figura 4. En esta figura se presentan las fotografías de las vinazas después de cada tratamiento realizado, donde se observa la disminución en la intensidad de la coloración, desde un café intenso hasta un amarillo descolorido.

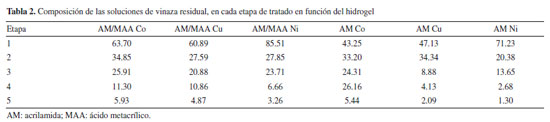
La composcion calculada mediante la ecuación obtenida con el análisis de UV-Vis, (Tabla 2) se observa la disminución de la concentración de las vinazas tratadas y se puede apreciar que los hidrogeles que contienen níquel tienen una mejor eficiencia, pudiéndose apreciar también de forma visual en la Figura 5, donde se presentan las vinazas tratadas en la etapa 5. Se obsrva que la tonalidad de las vinazas tratadas con los hidrogeles que dontienen níquel, presentan un color amarillo menos intenso, con respecto al resto de las muestras y se corrobora en la Tabla 2. Mientras que la concentración de las soluciones residuales de las vinazas al utilizar níquel alcanzó el valor de 1.30% con el hidrogle da AM, las concentraciones de las soluciones residulaes fueron de 2.09 y 5.44% para los hidroglees de Cu y Co respectivamente. Cuando se compara el tipo de hidrogel utilizado, se observa que los hidrogles de AM disminuyen la concentración de las soluciones residuales con mayor eficiencia que cuando se compara con el hidrogel de AM/MAA, cuando se utiliza níquel.

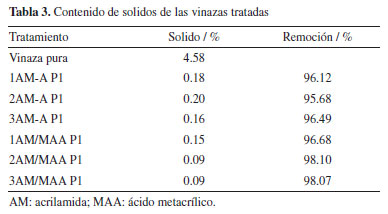
En la Tabla 3 se presenta la determinación de los solidos totales de las vinazas tratadas después de la etapa 5, donde se observa que se ha removido alrededor del 98% de los solidos totales para todas las muestras.
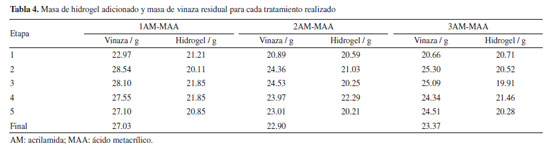
Al colocar la vinaza en contacto con los hidrogeles, no se observo un cambio significativo en el volumen de la vinaza tratada, con lo que se puede establecer que la clarificación de las vinazas es debido a la absorción por parte de los hidrogeles, de los compuestos que les proporcionan color a las vinazas y no por la dilución de la vinaza con la solución que contienen los hidrogeles. Esto se observa en la Tabla 4, donde se presentan las masas residuales de las soluciones de vinaza y de los hidrogeles en cada etapa de tratamiento y existe un ligero incremento en el volumen de la vinaza tratada, solo en la etapa 1, manteniéndose constante en el resto de las etapas. Esto se observa para todas las muestras de hidrogeles utilizados.
CONCLUSIONES Se sinterizaron hidróxidos metálicos en el interior de hidrogeles de acrilamida y acrilamida-acido metacrílico. La presencia de hidróxidos metálicos en el interior de la matriz polimérica, incremento la capacidad de los hidrogeles de absorber los compuestos orgánicos, que constituyen a la vinaza, ya que al colocarse en contacto los hidrogeles cargados con los hidróxidos formados en su interior y con solución de NaOH 0.1 M con las vinazas, se realizo un proceso de absorción de los compuestos orgánicos constituyentes de las vinazas. El desalojo de compuestos orgánicos y otros más, dio como resultado la clarificación de las vinazas de hasta un 98%. Mediante UV-Vis se comprobó que, en las soluciones residuales de las vinazas tratadas, desaparecen las señales características de las vinazas estudiadas, así como la aparición de nuevas señales, lo que puede ser un indicio de la existencia de un fenómeno de degradación o transformación de los compuestos que forman las vinazas. Quedaría por determinar que tipo de nuevos compuestos fueron creados y su nivel de toxicidad respecto a los existentes inicialmente, lo que abre toda una línea de investigación sobre esta posibilidad, que desencadenaría en el posible diseño de un proceso, no solo para clarificar las vinazas, si no en la transformación de estos compuestos y así disminuir su daño ambiental o la formación de subproductos que puedan ser aplicados a nivel industrial.
MATERIAL SUPLEMENTARIO El material complementario de este trabajo (figuras de los espectros UV-Vis para las soluciones de vinazas diluidas, para la vinaza residual del proceso de clarificación en función del tiempo de contacto con el hidrogel y para las vinazas residuales de todos los hidrogeles vs. 5.8% de vinaza diluida) está disponible en http://quimicanova.sbq.org.br/ como archivo PDF, de libre acceso.
DECLARACIÓN DE DISPONIBILIDAD DE DATOS Todos los datos están disponibles en el texto.
REFERENCIAS 1. Vid Mexicana, Conoce la Raicilla, https://www.vidmexicana.com/blogs/hablemos-de-vinos/conoce-la-raicilla, accedido en junio 2025. 2. Íñiguez, G.; Hernández, R.; Rev. Int. Contam. Ambiental 2010, 26, 299. [Link] accedido en junio 2025 3. Sirianuntapiboon S.; Somchai P.; Ohmomo, S.; Atthasampunna, P.; Agric. Biol. Chem. 1988, 52, 387. [Link] accedido en junio 2025 4. Zelaya-Benavidez, E. Z.; Martínez-Gutiérrez, G. A.; Escamirosa-Tinoco, C.; Morales, I.; Ecosistemas y Recursos Agropecuarios 2021, 8, e3159. [Crossref] 5. Martínez-Castillo, L. M.; Bustos-Vázquez, M. G.; Trujillo-Ramírez, D.; Rodríguez Castillejos, G. C.; Castillo-Ruiz, O.; Investigación y Desarrollo en Ciencia y Tecnología 2023, 8, 795. [Crossref] 6. de la Peña-Arellano, L. A.; Alférez-Ibarra, J. A.; Valle-Cervantes, S.; Rodríguez-Rosales, M. D.; Ordaz-Díaz, L. A.; Tecnociencia Chihuahua 2024, 18, 3. [Crossref] 7. Díaz-Barajas, S.; Moreno-Andrade, I.; Garzón-Zúñiga, M. A.; Tecnología y Ciencias del Agua 2022, 15, 1. [Crossref] 8. Wedzicha, B. L.; Kaputo, M. T.; Food Chem. 1992, 43, 359. [Crossref] 9. Houbron, E.; Sandoval, M.; Hernández, A.; Rev. Int. Contam. Ambiental 2016, 32, 255. [Crossref] 10. Lopez Velarde, M.; Ventura, E.; Rodriguez, J. A.; Oliver, H.; Rev. Int. Contam. Ambiental 2020, 36, 81. [Crossref] 11. Sanchez-Ureña, S.; Valadez-Rosales, M.; Correa-Camacho, J.; Marino-Marmolejo, E.; Revista de Energía Química y Física 2019, 6, 1. [Crossref] 12. Becerra-Ospina N.: Clarificación de Vinazas de Caña de Azúcar Por Tratamiento Fisicoquímico Y Filtración Con Membranas; Tesis Maestría, Universidad Nacional de Colombia, Bogota, Colombia, 2014. [Link] accedido en junio 2025 13. Barba H.; Luz, E.; García, L.; Ingeniería de Recursos Naturales y del Ambiente 2012, 11, 63. [Link] accedido en junio 2025 14. González-Guadarrama, M. J.; Castillo-Blum, S.; Armienta-Hernández, M.; Geofis. Int. 2022, 61, 1. [Crossref] 15. Alguacil, F.; Rev. Metal. 1999, 35, 53. [Crossref] 16. González-Martín, R.; Pacheco-Fernández, I.; Ayala, J. H.; Afonso, A. M.; Pino, V.; Talanta 2019, 203, 35. [Crossref] 17. Aydinoglu, D.; e-Polimers 2015, 15, 81. [Crossref] 18. Gharekhani, H.; Olad, A.; Mirmohseni, A.; Bybordi, A.; Carbohydr. Polym. 2017, 168, 1. [Crossref] 19. García Sánchez, L. G. J.; Cortés Ortega, J. A.; Polímeros 2014, 24, 752. [Crossref] 20. Cortés-Ortega, J. A.; Quim. Nova 2013, 36, 757. [Crossref] 21. Gómez-Vázquez, D.; Cajero-Zul, L. R.; Torres-Ávalos, J. A.; Sandoval-García, K.; Cortés-Ortega, J. A.; López-Dellamary, F. A.; Soltero-Martínez, J. F. A.; Martínez-Richa, A.; Nuño-Donlucas, S. M.; J. Macromol. Sci., Part A: Pure Appl. Chem. 2019, 56, 417. [Crossref] 22. Muñoz-García, R. O.; Hernández, M. E.; Ortiz, G. C.; Fernández, V.; Arellano, M. R.; Sánchez-Díaz, J. C.; Quim. Nova 2015, 38, 1031. [Crossref]
Editor responsable del artículo: Giovanna Machado |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access